9-10高二下·黑龙江·期末
1 . 在xR2++yH++O2=mR3++nH2O的离子方程式中,对系数m和R3+的判断正确的是
| A.m=4,R2+体现氧化性 |
| B.m=y,R3+是氧化产物 |
| C.m=2,R2+是氧化剂 |
| D.m=y,R3+是还原产物 |
您最近一年使用:0次
11-12高二下·黑龙江鹤岗·期中
名校
2 . 1994年度诺贝尔化学奖授予为研究臭氧做出贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3的分子结构如图,呈V型,两个O----O键的夹角为116.5o。三个原子以一个O原子为中心,另外两个O原子分别构成一个共价键;中间O原子提供2个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学键——三个O原子均等地享有这个电子。请回答:
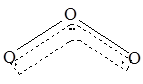
(1)臭氧与氧气的关系是_____________ 。
(2)写出下列分子与O3分子的结构最相似的是_______________ 。
(3)分子中某原子有一对或几对没有跟其他原子共用的价电子叫孤对电子,那么O3分子有________ 对孤对电子。
(4)O3分子是否为极性分子____________ (填是或否)。
(5)O3具有强氧化性,它能氧化PbS为PbSO4而O2不能,试配平:
_____ PbS +___ O3=________ PbSO4+_______ O2
生成1mol O2的转移电子物质的量为___________ mol。
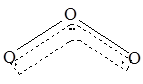
(1)臭氧与氧气的关系是
(2)写出下列分子与O3分子的结构最相似的是
| A.H2O | B.CO2 | C.SO2 | D.BeCl2 |
(3)分子中某原子有一对或几对没有跟其他原子共用的价电子叫孤对电子,那么O3分子有
(4)O3分子是否为极性分子
(5)O3具有强氧化性,它能氧化PbS为PbSO4而O2不能,试配平:
生成1mol O2的转移电子物质的量为
您最近一年使用:0次
3 . 草酸溶液能使酸性KMnO4溶液褪色,其离子方程式为:MnO4-+H2C2O4+H+→CO2↑+Mn2++__(未配平)。关于此反应的叙述正确的是
| A.该反应的还原产物是CO2 |
| B.该反应右框内的产物是OH- |
| C.配平该反应后,H+计量数是6 |
| D.1molMnO4-在反应中失去5mol电子 |
您最近一年使用:0次
2016-07-27更新
|
582次组卷
|
9卷引用:2015-2016学年黑龙江牡丹江一中高二下期末化学试卷
4 . 由于易被氧化而不宜长期存放的药品是
①KMnO4溶液 ②H2S溶液 ③FeSO4溶液 ④Cu(NO3)2溶液 ⑤Na2SO3溶液
①KMnO4溶液 ②H2S溶液 ③FeSO4溶液 ④Cu(NO3)2溶液 ⑤Na2SO3溶液
| A.①和③ | B.①②③ | C.②③⑤ | D.②③④⑤ |
您最近一年使用:0次
9-10高二下·黑龙江·期末
5 . 储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯。其反应,式为:
C + K2Cr2O7+ H2SO4→ CO2+ Cr2(SO4)3+ K2SO4+ H2O
(1)完成并配平上述反应的化学方程式并标出电子转移方向与数目;_________
(2)此反应的氧化剂是_________ ,氧化产物是_________ ;
(3)H2SO4在上述反应中表现出来的性质是______ (填选项编号)
(4)上述反应中若产生0.1mol CO2气体,则转移电子的物质的量是______ mol。
C + K2Cr2O7+ H2SO4→ CO2+ Cr2(SO4)3+ K2SO4+ H2O
(1)完成并配平上述反应的化学方程式并标出电子转移方向与数目;
(2)此反应的氧化剂是
(3)H2SO4在上述反应中表现出来的性质是
| A.酸性 | B.氧化性 | C.吸水性 | D.脱水性 |
(4)上述反应中若产生0.1mol CO2气体,则转移电子的物质的量是
您最近一年使用:0次



