名校
1 . 稀土在电子、激光、核工业、超导等诸多高科技领域有广泛的应用。钪(Sc)是一种稀土金属,利用钛尾矿回收金属轨的工艺流程如图所示。回答下列问题: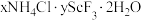 是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。
是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。
②“脱水除铵”是复盐沉淀的热分解过程。
(1)“焙烧”过程生成Sc2O3的化学方程式为_________ ,为“焙烧”过程中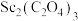 充分反应可采取的措施有
充分反应可采取的措施有__________ 。
(2)“置换”过程需要在氩气做保护气、高温条件下进行,发生反应的化学方程式为_______ 。
(3)“脱水除铵”过程中固体质量与温度的关系如图1所示,其中在380℃到400℃会有白烟冒出,保温至无烟气产生,即得到ScF3,由图象中数据计算复盐中x:z=___________ 。__________ (填“正”或“负”极),d电极上的电极反应式为__________ 。

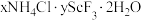 是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。
是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。②“脱水除铵”是复盐沉淀的热分解过程。
(1)“焙烧”过程生成Sc2O3的化学方程式为
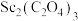 充分反应可采取的措施有
充分反应可采取的措施有(2)“置换”过程需要在氩气做保护气、高温条件下进行,发生反应的化学方程式为
(3)“脱水除铵”过程中固体质量与温度的关系如图1所示,其中在380℃到400℃会有白烟冒出,保温至无烟气产生,即得到ScF3,由图象中数据计算复盐中x:z=

您最近半年使用:0次
名校
解题方法
2 . 铬(Cr)广泛应用于冶金、化工、航天等领域。工业上以络铁矿(主要成分为FeCr2O4,含有少量Al2O3)为原料制备金属铬的工艺流程如图所示:
(1)FeCr2O4中Fe为+2价,Cr的化合价为______ ,“焙烧”中FeCr2O4反应的化学方程式为__________ 。
(2)“沉铝”中所得滤渣的成分为________ ,需控制pH=6~10的原因为_______________ 。
(3)“酸化”中反应的离子方程式为____________ ;若该反应的平衡常数K=4×1014,已知:“酸化”后溶液中c( )=1.6×10-3mol/L,则溶液中c(
)=1.6×10-3mol/L,则溶液中c( )=
)=_______ mol/L。
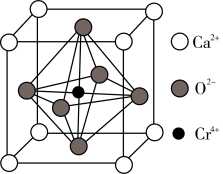
(4)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中Ca2+、O2-采用面心立方最密堆积方式(处于面对角线上的钙离子与氧离子紧密相邻)。________ pm。

(1)FeCr2O4中Fe为+2价,Cr的化合价为
(2)“沉铝”中所得滤渣的成分为
(3)“酸化”中反应的离子方程式为
 )=1.6×10-3mol/L,则溶液中c(
)=1.6×10-3mol/L,则溶液中c( )=
)=(4)Ca、O、Cr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中Ca2+、O2-采用面心立方最密堆积方式(处于面对角线上的钙离子与氧离子紧密相邻)。
您最近半年使用:0次
2024-04-11更新
|
133次组卷
|
2卷引用:重庆市万州第二高级中学2023-2024学年高二下学期3月月考化学试题
3 . 某小组用硫铜矿煅烧废渣(主要含Fe2O3、CuO、FeO)为原料制取Cu2O,流程如图:
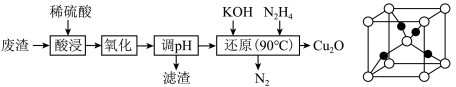
下列说法错误的是

下列说法错误的是
| A.“调节pH”时可以选择CuO或Cu(OH)2 |
| B.“还原”过程中消耗的CuSO4、N2H4的物质的量之比为4:1 |
| C.用N2H4还原制取Cu2O的优点是产生N2氛围,可防止产品被氧化 |
| D.Cu2O的晶胞结构如上图所示,1个Cu2O晶胞中含1个氧原子 |
您最近半年使用:0次
名校
4 . 下列反应的离子方程式表述正确的是
A.金属钠投入 溶液中: 溶液中: |
B.氯化铝溶液与过量浓氨水混合: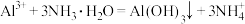 |
C.向NaHSO3溶液中滴 溶液: 溶液: |
D.向酸性高锰酸钾溶液中滴加过氧化氢: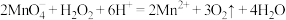 |
您最近半年使用:0次
名校
解题方法
5 . 砷化镓是一种半导体化合物,可用于太阳能电池。一种砷化镓废料(主要成分为GaAs,含 、
、 、
、 等杂质)中回收单质镓和砷的化合物的工艺流程如图所示。
等杂质)中回收单质镓和砷的化合物的工艺流程如图所示。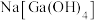 的形式进入溶液。
的形式进入溶液。
②离子完全沉淀时的pH: 为8,
为8, 为5.6。
为5.6。
(1)第一电离能比较:As________ Ga(填“<”“>”或“=”,下同),原子半径比较:As________ Ga。
(2)下图为砷化镓晶胞,白球所代表原子的配位数是________ 。已知:晶胞参数为apm,密度为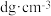 ,则阿伏加德罗常数
,则阿伏加德罗常数 可表示为
可表示为________ (用含a、d的式子表示)。________ 。
(4)“调pH①”时,pH=________ 最合适;滤液②的溶质成分为________ (写化学式)。
(5)写出用惰性电极电解制备镓单质的电极反应方程式:________ 。
 、
、 、
、 等杂质)中回收单质镓和砷的化合物的工艺流程如图所示。
等杂质)中回收单质镓和砷的化合物的工艺流程如图所示。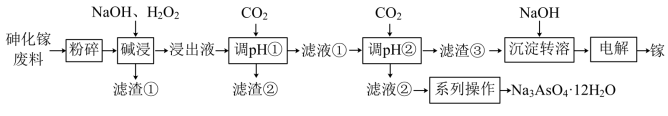
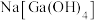 的形式进入溶液。
的形式进入溶液。②离子完全沉淀时的pH:
 为8,
为8, 为5.6。
为5.6。(1)第一电离能比较:As
(2)下图为砷化镓晶胞,白球所代表原子的配位数是
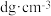 ,则阿伏加德罗常数
,则阿伏加德罗常数 可表示为
可表示为
(4)“调pH①”时,pH=
(5)写出用惰性电极电解制备镓单质的电极反应方程式:
您最近半年使用:0次
2024-03-25更新
|
93次组卷
|
2卷引用:重庆市渝西中学2023-2024学年高二下学期4月月考化学试题
名校
6 . 锰酸锂离子电池是第二代锂离子动力电池,性能优良。工业上以软锰矿浆(主要成分为 ,还有少量铁、铝、及硅的氧化物)为原料制备锰酸锂
,还有少量铁、铝、及硅的氧化物)为原料制备锰酸锂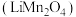 ,工业流程如下图所示:
,工业流程如下图所示:
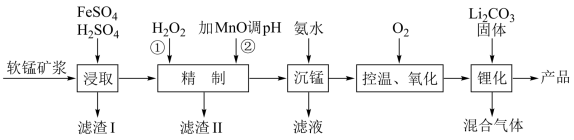
(1)基态 原子的价电子排布式为
原子的价电子排布式为______ 。
(2)“精制”过程中,实际加入 的量比理论用量多,主要原因是
的量比理论用量多,主要原因是______ ; 是含有
是含有______ 键(填“极性”或“非极性”,下同)和______ 键的______ 分子: 能与水混溶,却不能溶于
能与水混溶,却不能溶于 ,请予以解释
,请予以解释______ 。
(3)“沉锰”过程得到的是 和
和 ,二者均可以被氧化为
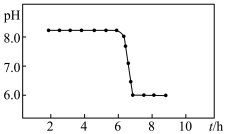
,二者均可以被氧化为 ,若“控温、氧化”过程中溶液的
,若“控温、氧化”过程中溶液的 随时间变化关系如下图所示,其中溶液的
随时间变化关系如下图所示,其中溶液的 明显下降的原因是
明显下降的原因是______ (用化学方程式表示)。
(4)“锂化”过程是将 和
和 按
按 的物质的量之比配料,反应3-5小时,然后升温至600-750℃,保温24小时,自然冷却至室温得到产品。该过程所得混合气体的成分是
的物质的量之比配料,反应3-5小时,然后升温至600-750℃,保温24小时,自然冷却至室温得到产品。该过程所得混合气体的成分是______ 。
 ,还有少量铁、铝、及硅的氧化物)为原料制备锰酸锂
,还有少量铁、铝、及硅的氧化物)为原料制备锰酸锂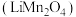 ,工业流程如下图所示:
,工业流程如下图所示:
(1)基态
 原子的价电子排布式为
原子的价电子排布式为(2)“精制”过程中,实际加入
 的量比理论用量多,主要原因是
的量比理论用量多,主要原因是 是含有
是含有 能与水混溶,却不能溶于
能与水混溶,却不能溶于 ,请予以解释
,请予以解释(3)“沉锰”过程得到的是
 和
和 ,二者均可以被氧化为
,二者均可以被氧化为 ,若“控温、氧化”过程中溶液的
,若“控温、氧化”过程中溶液的 随时间变化关系如下图所示,其中溶液的
随时间变化关系如下图所示,其中溶液的 明显下降的原因是
明显下降的原因是
(4)“锂化”过程是将
 和
和 按
按 的物质的量之比配料,反应3-5小时,然后升温至600-750℃,保温24小时,自然冷却至室温得到产品。该过程所得混合气体的成分是
的物质的量之比配料,反应3-5小时,然后升温至600-750℃,保温24小时,自然冷却至室温得到产品。该过程所得混合气体的成分是
您最近半年使用:0次
名校
7 . X、Y、Z、W、P、Q是元素周期表前四周期的六种常见元素,原子序数依次增大。X在自然界中有多种同素异形体,其中一种是自然界中最硬的单质;Z是地壳中含量最多的元素;W基态原子核外的9个原子轨道上填充了电子,且有1个未成对电子;P是常见的金属元素,其单质能与盐酸反应,不与碱反应,它的某种氧化物可用作红色颜料;Q基态原子的M层全充满,N层没有成对电子,只有一个未成对电子。回答以下问题:
(1)P、Q中位于周期表的d区的是__________ (填元素符号,下同),基态Q原子的价层电子排布式为__________ ;元素X、Y、Z中,电负性最大的是__________ 。
(2)烃 的1个分子中含有
的1个分子中含有__________ 个σ键;X和Y的简单氢化物中沸点更高的是__________ (填化学式),理由是__________ (答2点)。
(3)化合物 可用作杀菌消毒剂和漂白剂,
可用作杀菌消毒剂和漂白剂, 分子的中心原子杂化类型是
分子的中心原子杂化类型是__________ ;工业上可用W的单质与潮湿的碳酸钠反应制取 ,并生成另外两种含钠的化合物,反应中无其它气体生成,写出该反应的化学方程式
,并生成另外两种含钠的化合物,反应中无其它气体生成,写出该反应的化学方程式__________ 。
(1)P、Q中位于周期表的d区的是
(2)烃
 的1个分子中含有
的1个分子中含有(3)化合物
 可用作杀菌消毒剂和漂白剂,
可用作杀菌消毒剂和漂白剂, 分子的中心原子杂化类型是
分子的中心原子杂化类型是 ,并生成另外两种含钠的化合物,反应中无其它气体生成,写出该反应的化学方程式
,并生成另外两种含钠的化合物,反应中无其它气体生成,写出该反应的化学方程式
您最近半年使用:0次
2024-02-22更新
|
139次组卷
|
3卷引用:重庆市铜梁一中等重点中学2023-2024学年高二下学期3月月考化学试题
8 . 碱式碳酸铜可用作有机催化剂。工业上以辉铜矿(主要成分为 ,含
,含 及少量
及少量 )为原料制备碱式碳酸铜,工业流程如下:
)为原料制备碱式碳酸铜,工业流程如下:
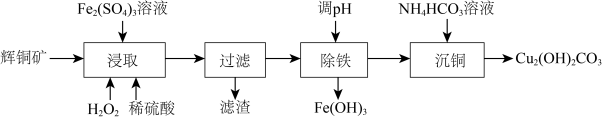
(1)滤渣可能含S、______ (填化学式)。
(2)①“浸取”时能提高辉铜矿Cu浸取率的措施有______ (填2条)。
②某小组测得Cu浸取率随 浓度及温度影响的变化曲线如下:
浓度及温度影响的变化曲线如下:

由图一可知 适宜的浓度范围为
适宜的浓度范围为______ :由图一中的a点分析,浸取时 也起到了氧化辉铜矿的作用,该反应的离子方程式为
也起到了氧化辉铜矿的作用,该反应的离子方程式为______ :图二中高于85℃时Cu浸取率下降的原因是______ 。
(3)“除铁”步骤调pH可加入试剂______ (填选项字母);
a.NaOH b.HCl c.CuO d.
(4)常温下,“过滤”后的滤液中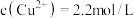 ,则“除铁”步骤调pH应小于
,则“除铁”步骤调pH应小于______ [常温下, ]。
]。
 ,含
,含 及少量
及少量 )为原料制备碱式碳酸铜,工业流程如下:
)为原料制备碱式碳酸铜,工业流程如下:
(1)滤渣可能含S、
(2)①“浸取”时能提高辉铜矿Cu浸取率的措施有
②某小组测得Cu浸取率随
 浓度及温度影响的变化曲线如下:
浓度及温度影响的变化曲线如下:
由图一可知
 适宜的浓度范围为
适宜的浓度范围为 也起到了氧化辉铜矿的作用,该反应的离子方程式为
也起到了氧化辉铜矿的作用,该反应的离子方程式为(3)“除铁”步骤调pH可加入试剂
a.NaOH b.HCl c.CuO d.

(4)常温下,“过滤”后的滤液中
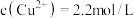 ,则“除铁”步骤调pH应小于
,则“除铁”步骤调pH应小于 ]。
]。
您最近半年使用:0次
名校
9 . 氧化还原滴定实验与中和滴定原理相似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之),也是分析化学中常用的分析手段。
Ⅰ.用 溶液滴定20.00mL浓度约为
溶液滴定20.00mL浓度约为 溶液。
溶液。
(1)该酸碱中和滴定实验最好选用______ (填标号)作指示剂。
A.酚酞 B.石蕊 C.甲基橙
(2)实验所用仪器如图所示仪器甲盛装______ (填“NaOH”或“ ”溶液。若滴定开始和结束时,盛装
”溶液。若滴定开始和结束时,盛装 溶液的滴定管中的液面如图所示,终点读数为
溶液的滴定管中的液面如图所示,终点读数为______ mL
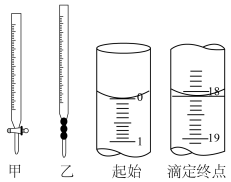
(3)在上述实验过程中,出现下列操作(其他操作正确)会造成测定结果(待测液浓度值)偏低的有______ (填序号)。
a.量取标准液的碱式滴定管未用标准液润洗
b.取醋酸的酸式滴定管,滴定前滴定管尖端有气泡,滴定后气泡消失
c.锥形瓶用蒸馏水洗涤后,水未倒尽,仍残留一定量水
d.当滴定结束时,俯视碱式滴定管读数
Ⅱ.用氧化还原滴定方法测定粗品中 的质量分数。
的质量分数。
实验步骤:称取6g粗品配制250mL的溶液待用.用酸式滴定管取 溶液于锥形瓶中,然后加入过量的KI溶液并酸化,加几滴淀粉溶液,立即用配制的
溶液于锥形瓶中,然后加入过量的KI溶液并酸化,加几滴淀粉溶液,立即用配制的 溶液滴定至终点(反应为
溶液滴定至终点(反应为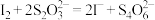 ),消耗
),消耗 溶液25.00mL。
溶液25.00mL。
回答下列问题:
(4)向 溶液中加入过量的KI溶液并酸化,
溶液中加入过量的KI溶液并酸化, 被还原成
被还原成 ,写出该反应的离子方程式:
,写出该反应的离子方程式:____________ 。
(5)用 溶液滴定至终点的现象为
溶液滴定至终点的现象为______ 。
(6)粗品中 的质量分数为
的质量分数为______ 。
(7)若在取 溶液时有部分溶液滴到了锥形瓶外。则测定结果
溶液时有部分溶液滴到了锥形瓶外。则测定结果______ (填“偏高”“偏氐”或“不变”)。
Ⅰ.用
 溶液滴定20.00mL浓度约为
溶液滴定20.00mL浓度约为 溶液。
溶液。(1)该酸碱中和滴定实验最好选用
A.酚酞 B.石蕊 C.甲基橙
(2)实验所用仪器如图所示仪器甲盛装
 ”溶液。若滴定开始和结束时,盛装
”溶液。若滴定开始和结束时,盛装 溶液的滴定管中的液面如图所示,终点读数为
溶液的滴定管中的液面如图所示,终点读数为
(3)在上述实验过程中,出现下列操作(其他操作正确)会造成测定结果(待测液浓度值)偏低的有
a.量取标准液的碱式滴定管未用标准液润洗
b.取醋酸的酸式滴定管,滴定前滴定管尖端有气泡,滴定后气泡消失
c.锥形瓶用蒸馏水洗涤后,水未倒尽,仍残留一定量水
d.当滴定结束时,俯视碱式滴定管读数
Ⅱ.用氧化还原滴定方法测定粗品中
 的质量分数。
的质量分数。实验步骤:称取6g粗品配制250mL的溶液待用.用酸式滴定管取
 溶液于锥形瓶中,然后加入过量的KI溶液并酸化,加几滴淀粉溶液,立即用配制的
溶液于锥形瓶中,然后加入过量的KI溶液并酸化,加几滴淀粉溶液,立即用配制的 溶液滴定至终点(反应为
溶液滴定至终点(反应为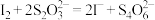 ),消耗
),消耗 溶液25.00mL。
溶液25.00mL。回答下列问题:
(4)向
 溶液中加入过量的KI溶液并酸化,
溶液中加入过量的KI溶液并酸化, 被还原成
被还原成 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(5)用
 溶液滴定至终点的现象为
溶液滴定至终点的现象为(6)粗品中
 的质量分数为
的质量分数为(7)若在取
 溶液时有部分溶液滴到了锥形瓶外。则测定结果
溶液时有部分溶液滴到了锥形瓶外。则测定结果
您最近半年使用:0次
名校
解题方法
10 . 亚硝酸钙 是白色粉末、易潮解、易溶于水,在钢筋混凝土工程中,常用作水泥硬化促进剂和防冻阻锈剂。实验用
是白色粉末、易潮解、易溶于水,在钢筋混凝土工程中,常用作水泥硬化促进剂和防冻阻锈剂。实验用 与
与 制备亚硝酸钙装置如图所示(夹持装置已略去)。
制备亚硝酸钙装置如图所示(夹持装置已略去)。
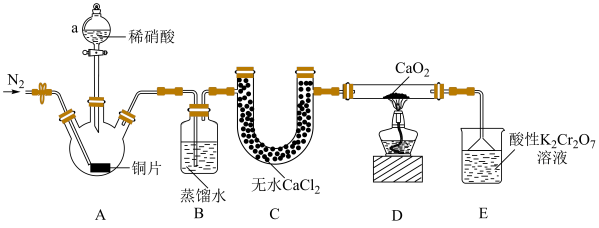
回答下列问题:
(1)盛装稀硝酸的仪器 名称为
名称为________ 。
(2)加入稀硝酸之前需通入一段时间 ,其目的是
,其目的是________ 。
(3)装置A中反应的化学方程式为________ 。
(4)上述装置有一处明显不足,会导致亚硝酸钙产率降低,改进的方法是________ 。
(5)此法制得的亚硝酸钙中常含有硝酸钙杂质,现用如下方法测定产品中硝酸钙的含量。
实验原理:



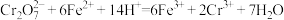
实验步骤:
Ⅰ.称量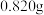 产品溶于水,加入足量的硫酸钠固体,充分搅拌后过滤;
产品溶于水,加入足量的硫酸钠固体,充分搅拌后过滤;
Ⅱ.将滤液配制成 溶液,取
溶液,取 溶液于锥形瓶中,加入足量
溶液于锥形瓶中,加入足量 饱和溶液,煮沸
饱和溶液,煮沸 ,冷却;
,冷却;
Ⅲ.再向锥形瓶中加入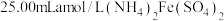 溶液和适量硫酸;
溶液和适量硫酸;
Ⅳ.加入4滴指示剂,用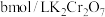 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液 。
。
①步骤Ⅳ中盛装 标准溶液的仪器名称是
标准溶液的仪器名称是________ 。
②所得产品中硝酸钙的质量分数为________
③下列操作会导致硝酸钙的质量分数测定结果偏高的是________ 。
A.盛装 标准液前未用
标准液前未用 标准液润洗滴定管
标准液润洗滴定管
B.滴定时振荡太剧烈,使锥形瓶中液体溅出
C.达到滴定终点时,仰视读数
 是白色粉末、易潮解、易溶于水,在钢筋混凝土工程中,常用作水泥硬化促进剂和防冻阻锈剂。实验用
是白色粉末、易潮解、易溶于水,在钢筋混凝土工程中,常用作水泥硬化促进剂和防冻阻锈剂。实验用 与
与 制备亚硝酸钙装置如图所示(夹持装置已略去)。
制备亚硝酸钙装置如图所示(夹持装置已略去)。
回答下列问题:
(1)盛装稀硝酸的仪器
 名称为
名称为(2)加入稀硝酸之前需通入一段时间
 ,其目的是
,其目的是(3)装置A中反应的化学方程式为
(4)上述装置有一处明显不足,会导致亚硝酸钙产率降低,改进的方法是
(5)此法制得的亚硝酸钙中常含有硝酸钙杂质,现用如下方法测定产品中硝酸钙的含量。
实验原理:



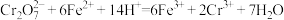
实验步骤:
Ⅰ.称量
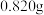 产品溶于水,加入足量的硫酸钠固体,充分搅拌后过滤;
产品溶于水,加入足量的硫酸钠固体,充分搅拌后过滤;Ⅱ.将滤液配制成
 溶液,取
溶液,取 溶液于锥形瓶中,加入足量
溶液于锥形瓶中,加入足量 饱和溶液,煮沸
饱和溶液,煮沸 ,冷却;
,冷却;Ⅲ.再向锥形瓶中加入
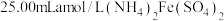 溶液和适量硫酸;
溶液和适量硫酸;Ⅳ.加入4滴指示剂,用
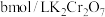 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液 。
。①步骤Ⅳ中盛装
 标准溶液的仪器名称是
标准溶液的仪器名称是②所得产品中硝酸钙的质量分数为
③下列操作会导致硝酸钙的质量分数测定结果偏高的是
A.盛装
 标准液前未用
标准液前未用 标准液润洗滴定管
标准液润洗滴定管B.滴定时振荡太剧烈,使锥形瓶中液体溅出
C.达到滴定终点时,仰视读数
您最近半年使用:0次



