名校
1 . 从冶炼金属产生的某酸泥(含 单质,
单质, 及锌、铜的化合物等)中回收汞和硒的一种工艺如下:
及锌、铜的化合物等)中回收汞和硒的一种工艺如下: 、
、 、
、 、
、 形式进入溶液。
形式进入溶液。 固体的晶体类型与石墨的晶体类型
固体的晶体类型与石墨的晶体类型___________ 相同(填“是”或者“不”);分离氧化浸出液和浸出渣的操作是___________ 。
2.还原沉汞时加入的 属于正盐,则
属于正盐,则 属于
属于___________ 元酸:沉汞后溶液中磷以最高价形式存在,“还原沉汞”的主要反应中氧化剂和还原剂的物质的量之比为___________ 。
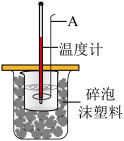
3.实验室测定中和反应热效应的装置如图所示,该装置有利于减少实验误差的设计措施有___________ (至少写一条)。
i.取 粗硒于锥形瓶中,加入
粗硒于锥形瓶中,加入 浓盐酸和
浓盐酸和 浓硝酸,沸水浴加热,使
浓硝酸,沸水浴加热,使 全部转化为
全部转化为 ;
;
ii.除去过量的 和溶解的
和溶解的 ;
;
iii. 加入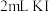 溶液、
溶液、 淀粉溶液,然后用
淀粉溶液,然后用 标准溶液进行滴定,到达滴定终点时,消耗
标准溶液进行滴定,到达滴定终点时,消耗 标准溶液
标准溶液 。
。
已知:
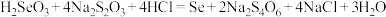

4.滴定时使用的定量仪器为___________ ,到达滴定终点时的现象为___________ 。
5.根据实验数据计算粗硒中硒的纯度为___________ 。
 单质,
单质, 及锌、铜的化合物等)中回收汞和硒的一种工艺如下:
及锌、铜的化合物等)中回收汞和硒的一种工艺如下: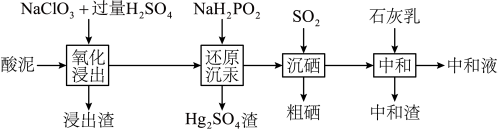
 、
、 、
、 、
、 形式进入溶液。
形式进入溶液。 固体的晶体类型与石墨的晶体类型
固体的晶体类型与石墨的晶体类型2.还原沉汞时加入的
 属于正盐,则
属于正盐,则 属于
属于3.实验室测定中和反应热效应的装置如图所示,该装置有利于减少实验误差的设计措施有
i.取
 粗硒于锥形瓶中,加入
粗硒于锥形瓶中,加入 浓盐酸和
浓盐酸和 浓硝酸,沸水浴加热,使
浓硝酸,沸水浴加热,使 全部转化为
全部转化为 ;
;ii.除去过量的
 和溶解的
和溶解的 ;
;iii. 加入
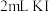 溶液、
溶液、 淀粉溶液,然后用
淀粉溶液,然后用 标准溶液进行滴定,到达滴定终点时,消耗
标准溶液进行滴定,到达滴定终点时,消耗 标准溶液
标准溶液 。
。已知:

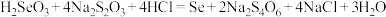

4.滴定时使用的定量仪器为
5.根据实验数据计算粗硒中硒的纯度为
您最近半年使用:0次
名校
2 . 已知:① (绿色)(强碱性条件)
(绿色)(强碱性条件)
② (强酸性条件)
(强酸性条件)
(1)在KOH溶液中, 与
与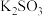 溶液发生反应,还原剂为
溶液发生反应,还原剂为___________ ,还原产物为___________ 。
(2)将 溶液滴入NaOH溶液微热,得到透明的绿色溶液,写出反应的离子方程式
溶液滴入NaOH溶液微热,得到透明的绿色溶液,写出反应的离子方程式___________ 。
(3)向20mL浓度为0.02mol/L的 溶液中滴加
溶液中滴加 溶液,使
溶液,使 全部转化为
全部转化为 ,则反应前需向
,则反应前需向 溶液加入
溶液加入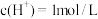 的酸不少于
的酸不少于___________ mL。
 (绿色)(强碱性条件)
(绿色)(强碱性条件)②
 (强酸性条件)
(强酸性条件)(1)在KOH溶液中,
 与
与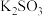 溶液发生反应,还原剂为
溶液发生反应,还原剂为(2)将
 溶液滴入NaOH溶液微热,得到透明的绿色溶液,写出反应的离子方程式
溶液滴入NaOH溶液微热,得到透明的绿色溶液,写出反应的离子方程式(3)向20mL浓度为0.02mol/L的
 溶液中滴加
溶液中滴加 溶液,使
溶液,使 全部转化为
全部转化为 ,则反应前需向
,则反应前需向 溶液加入
溶液加入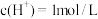 的酸不少于
的酸不少于
您最近半年使用:0次
名校
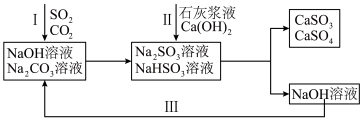
3 . 双碱法是一种用于燃煤尾气脱硫的工艺,其具有脱硫效率高、成本低等优点,以下是一种脱硫工艺简要流程。 时,
时, 和
和 的电离常数如下表所示。
的电离常数如下表所示。
1.等浓度的 和
和 溶液,
溶液,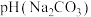
___________ 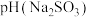 (填“>”、“<”或“=”),请依据电离平衡常数分析原因:
(填“>”、“<”或“=”),请依据电离平衡常数分析原因:___________ 。
2.过程I中, 溶液吸收
溶液吸收 时,随着
时,随着 的通入,会得到不同溶质组成的溶液。
的通入,会得到不同溶质组成的溶液。 时,
时, 的物质的量分数
的物质的量分数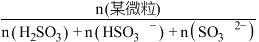 与pH的关系如图所示。
与pH的关系如图所示。___________ 。
②等浓度 和
和 的混合溶液中,下列关系正确的是
的混合溶液中,下列关系正确的是___________ 。
A.
B.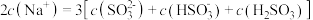
C.
D.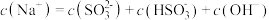
3.生成的 沉淀会被空气中氧气氧化,写出
沉淀会被空气中氧气氧化,写出 被氧化过程的化学方程式为:
被氧化过程的化学方程式为:___________ 。
4.工业上也可以用氨水吸收尾气中的 。氨水吸收
。氨水吸收 后,氨水全部转化为铵盐的溶液。为测定铵盐溶液的成分,设计如下实验。
后,氨水全部转化为铵盐的溶液。为测定铵盐溶液的成分,设计如下实验。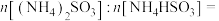
___________ 。
 时,
时, 和
和 的电离常数如下表所示。
的电离常数如下表所示。 |  |
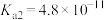 | |
 |  |
 |
1.等浓度的
 和
和 溶液,
溶液,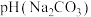
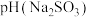 (填“>”、“<”或“=”),请依据电离平衡常数分析原因:
(填“>”、“<”或“=”),请依据电离平衡常数分析原因:2.过程I中,
 溶液吸收
溶液吸收 时,随着
时,随着 的通入,会得到不同溶质组成的溶液。
的通入,会得到不同溶质组成的溶液。 时,
时, 的物质的量分数
的物质的量分数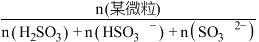 与pH的关系如图所示。
与pH的关系如图所示。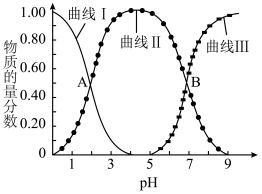
②等浓度
 和
和 的混合溶液中,下列关系正确的是
的混合溶液中,下列关系正确的是A.

B.
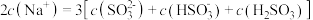
C.

D.
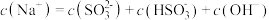
3.生成的
 沉淀会被空气中氧气氧化,写出
沉淀会被空气中氧气氧化,写出 被氧化过程的化学方程式为:
被氧化过程的化学方程式为:4.工业上也可以用氨水吸收尾气中的
 。氨水吸收
。氨水吸收 后,氨水全部转化为铵盐的溶液。为测定铵盐溶液的成分,设计如下实验。
后,氨水全部转化为铵盐的溶液。为测定铵盐溶液的成分,设计如下实验。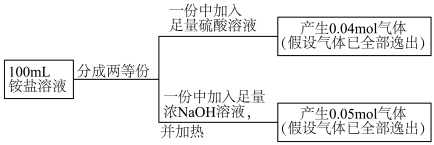
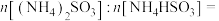
您最近半年使用:0次
名校
4 . 化学社团的学生们查阅相关资料并设计了如下装置制备亚硝酰氯(NOCl)。 。
。
②亚硝酰氯熔点为-64.5℃、沸点为-5.5℃,气态呈黄色,液态时呈红褐色,遇水易反应。
1.装置的连接顺序为a→b→c→___________ →h,实验时先打开分液漏斗活塞滴入稀硝酸,当观察到F中___________ 时,开始向装置中通入 。
。
2.写出A中发生的化学方程式___________ 。
3.装置B的作用是___________ ,装置D中长颈漏斗的作用是___________ 。
制得的亚硝酰氯(NOCl)中可能含有少量杂质,化学社团的同学们设计了如下实验测定NOCl的纯度。
①取5.000g,三颈烧瓶中所得产物溶于适量氢氧化钠溶液中,然后加入一定量稀硫酸和KI溶液,并通入足量 ,将NO全部赶出,最后将溶液稀释至500.00mL;
,将NO全部赶出,最后将溶液稀释至500.00mL;
②取25.00mL上述所得溶液,用淀粉作指示剂,用0.15
 标准溶液滴定至终点,最终消耗标准溶液的体积为20.00mL。
标准溶液滴定至终点,最终消耗标准溶液的体积为20.00mL。
已知:
①
②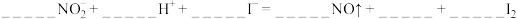
③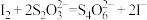
4.补充并配平反应②并标出电子转移的方向和数目___________ 。
5.滴定终点的现象___________ ,结合相关数据,计算实验测得产品中NOCl的纯度为___________ (保留三位小数)。
6.下列操作将导致NOCl纯度测量偏低的是___________。

 。
。②亚硝酰氯熔点为-64.5℃、沸点为-5.5℃,气态呈黄色,液态时呈红褐色,遇水易反应。
1.装置的连接顺序为a→b→c→
 。
。2.写出A中发生的化学方程式
3.装置B的作用是
制得的亚硝酰氯(NOCl)中可能含有少量杂质,化学社团的同学们设计了如下实验测定NOCl的纯度。
①取5.000g,三颈烧瓶中所得产物溶于适量氢氧化钠溶液中,然后加入一定量稀硫酸和KI溶液,并通入足量
 ,将NO全部赶出,最后将溶液稀释至500.00mL;
,将NO全部赶出,最后将溶液稀释至500.00mL;②取25.00mL上述所得溶液,用淀粉作指示剂,用0.15

 标准溶液滴定至终点,最终消耗标准溶液的体积为20.00mL。
标准溶液滴定至终点,最终消耗标准溶液的体积为20.00mL。已知:
①

②
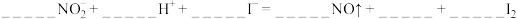
③
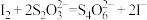
4.补充并配平反应②并标出电子转移的方向和数目
5.滴定终点的现象
6.下列操作将导致NOCl纯度测量偏低的是___________。
A.滴定过程中剧烈振荡导致 挥发 挥发 |
| B.滴定前滴定管有气泡,滴定后气泡消失 |
| C.锥形瓶用待测液润洗 |
D.滴定管用蒸馏水润洗后,直接加入 标准溶液进行滴定 标准溶液进行滴定 |
您最近半年使用:0次
名校
解题方法
5 . 卤素互化物、拟卤素与卤素单质的结构,性质相似。常见的卤素互化物有ICl、IBr等,拟卤素有(CN)2、(SCN)2等。
(1)卤族元素位于元素周期表的_______ 。
(2)79Br和81Br这两种核素的中子数之差的绝对值为_______ 。
(3)①Cl2;②ICl;③IBr三种物质熔点由高到低的顺序为_______ 。
(4)①已知CN-与N2结构相似,CN-的电子式为______ 。
②推算HCN分子中σ键与π键数目之比为_______ 。
③关于氨基氰(N≡C-NH2)分子的说法中正确的是_______ 。
A.C原子采用sp3杂化
B.N原子的杂化形式有sp与sp3杂化
C.C≡N键的键长大于C-N键
D.所有原子满足8电子稳定结构
开采的金矿可用氰化法提取,步骤如下:
i.将金矿砂溶于pH为10.5~11的KCN溶液,并鼓入空气,过滤除去矿渣,得含K[Au(CN)2]的滤液;
ii.向滤液中加入足量金属锌,得单质金。Zn+2K[Au(CN)2]=2Au+K2[Zn(CN)4]
(5)K[Au(CN)2]中Au+的配体为______ 。
(6)K2[Zn(CN)4]中Au+的配位数为______ 。
(7)i中反应的离子方程式为:_______ 。
 Au+
Au+ CN-+
CN-+ _______+
_______+ _______=
_______= [Au(CN)2]-+
[Au(CN)2]-+ _______
_______
(8)已知Ka(HCN)=4.0×10-10。i中,pH<10.5会导致相同时间内Au的浸取率下降,原因_______ 。
(1)卤族元素位于元素周期表的
| A.s区 | B.p区 | C.d区 | D.f区 |
(3)①Cl2;②ICl;③IBr三种物质熔点由高到低的顺序为
| A.①>②>③ | B.③>②>① | C.②>①>③ | D.③>①>② |
②推算HCN分子中σ键与π键数目之比为
③关于氨基氰(N≡C-NH2)分子的说法中正确的是
A.C原子采用sp3杂化
B.N原子的杂化形式有sp与sp3杂化
C.C≡N键的键长大于C-N键
D.所有原子满足8电子稳定结构
开采的金矿可用氰化法提取,步骤如下:
i.将金矿砂溶于pH为10.5~11的KCN溶液,并鼓入空气,过滤除去矿渣,得含K[Au(CN)2]的滤液;
ii.向滤液中加入足量金属锌,得单质金。Zn+2K[Au(CN)2]=2Au+K2[Zn(CN)4]
(5)K[Au(CN)2]中Au+的配体为
(6)K2[Zn(CN)4]中Au+的配位数为
(7)i中反应的离子方程式为:
 Au+
Au+ CN-+
CN-+ _______+
_______+ _______=
_______= [Au(CN)2]-+
[Au(CN)2]-+ _______
_______(8)已知Ka(HCN)=4.0×10-10。i中,pH<10.5会导致相同时间内Au的浸取率下降,原因
您最近半年使用:0次
名校
6 . Ⅰ.有钠、氢、氧、硫四种元素,用其中的一种或几种元素可以组成多种物质,写出符合下列要求的化学式(各写一个):
(1)酸式盐___________ ;
(2)非电解质___________ ;
(3)强电解质___________ ;
(4)弱电解质___________ 。
Ⅱ.完成下列问题
(5)配平下列反应________ ;
___________ ___________
___________ (浓)
(浓) ___________
___________ ___________
___________ ___________
___________ ___________
___________ 。
。
(6)该反应中还原产物为___________ ,若有 参加反应,则参加反应的
参加反应,则参加反应的 为
为___________  ,其中被氧化的
,其中被氧化的 为
为___________  ,转移电子的物质的量为
,转移电子的物质的量为___________  。
。
(1)酸式盐
(2)非电解质
(3)强电解质
(4)弱电解质
Ⅱ.完成下列问题
(5)配平下列反应
___________
 ___________
___________ (浓)
(浓) ___________
___________ ___________
___________ ___________
___________ ___________
___________ 。
。(6)该反应中还原产物为
 参加反应,则参加反应的
参加反应,则参加反应的 为
为 ,其中被氧化的
,其中被氧化的 为
为 ,转移电子的物质的量为
,转移电子的物质的量为 。
。
您最近半年使用:0次
名校
7 . I.人类活动中的碳排放无可避免。
(1)配平下列反应,并标出电子转移的方向和数目。___________
___________CH4+___________NO2 ___________NO+___________CO2+___________H2O
___________NO+___________CO2+___________H2O
(2)有一种处理废水中的HCOOH的微型原电池。电池含有Fe-C,使用时通入空气,便可以在___________ 生成H2O2。
A.阴极 B.负极 C.阳极 D.正极
写出H2O2与HCOOH反应生成CO2的化学方程式:___________ 。
Ⅱ.一种富集CO2的原电池模拟装置如下图。
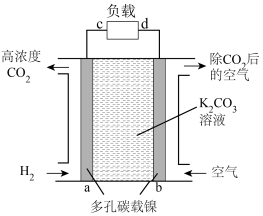
(3)b极为___________ 极(填“正”或“负”),a电极上发生的电极反应为___________ 。
(4)上述电极材料采用多孔碳载镍,“多孔”的优点是___________ 。
(5)该装置若消耗2 mol H2,则理论上在b极除去CO2的体积约为___________ L(标准状况下)。
(1)配平下列反应,并标出电子转移的方向和数目。
___________CH4+___________NO2
 ___________NO+___________CO2+___________H2O
___________NO+___________CO2+___________H2O(2)有一种处理废水中的HCOOH的微型原电池。电池含有Fe-C,使用时通入空气,便可以在
A.阴极 B.负极 C.阳极 D.正极
写出H2O2与HCOOH反应生成CO2的化学方程式:
Ⅱ.一种富集CO2的原电池模拟装置如下图。

(3)b极为
(4)上述电极材料采用多孔碳载镍,“多孔”的优点是
(5)该装置若消耗2 mol H2,则理论上在b极除去CO2的体积约为
您最近半年使用:0次
名校
8 . 氨气是重要的化工原料,氨水、硝酸盐、铵盐等均可作化肥产品。
(1)在VL浓度为 的氨水中滴加等体积
的氨水中滴加等体积 的盐酸,使pH=7,则产物中一水合氨浓度为
的盐酸,使pH=7,则产物中一水合氨浓度为___________  。
。
(2)在自然界的氮循环过程中,硝化细菌将土壤中的 转化为
转化为 后,土壤中的O2进一步将
后,土壤中的O2进一步将 氧化为
氧化为 ,在氧气较少的环境下,
,在氧气较少的环境下, 又可以在反硝化细菌的作用下与
又可以在反硝化细菌的作用下与 反应,使氮以N2形式放出。氧气与
反应,使氮以N2形式放出。氧气与 反应时,反应物
反应时,反应物 与O2的物质的量之比为
与O2的物质的量之比为___________ ,写出 与
与 作用生成N2的离子方程式
作用生成N2的离子方程式___________ 。
(1)在VL浓度为
 的氨水中滴加等体积
的氨水中滴加等体积 的盐酸,使pH=7,则产物中一水合氨浓度为
的盐酸,使pH=7,则产物中一水合氨浓度为 。
。(2)在自然界的氮循环过程中,硝化细菌将土壤中的
 转化为
转化为 后,土壤中的O2进一步将
后,土壤中的O2进一步将 氧化为
氧化为 ,在氧气较少的环境下,
,在氧气较少的环境下, 又可以在反硝化细菌的作用下与
又可以在反硝化细菌的作用下与 反应,使氮以N2形式放出。氧气与
反应,使氮以N2形式放出。氧气与 反应时,反应物
反应时,反应物 与O2的物质的量之比为
与O2的物质的量之比为 与
与 作用生成N2的离子方程式
作用生成N2的离子方程式
您最近半年使用:0次
9 . Ⅰ.硒( )在人体内可以起到提高免疫力、抗氧化等功效,含硒化合物在材料和药物领域具有重要作用。铬(
)在人体内可以起到提高免疫力、抗氧化等功效,含硒化合物在材料和药物领域具有重要作用。铬( )被广泛应用在冶金、化工、铸铁、耐火及高精端科技等领域。
)被广泛应用在冶金、化工、铸铁、耐火及高精端科技等领域。
(1)在元素周期表中,硒是第34号元素,与氧同主族,硒原子的电子式表示为___________ ,比较硫和硒的氢化物的热稳定性:
___________  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
Ⅱ.工业制备高纯硒的流程如下:
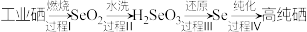
(2)下列说法正确的是___________。
(3)过程Ⅲ中还需要用的反应物为 ,对应产物为
,对应产物为 ,标况下,当有
,标况下,当有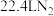 生成时,该反应中转移的电子数目为
生成时,该反应中转移的电子数目为___________ 。
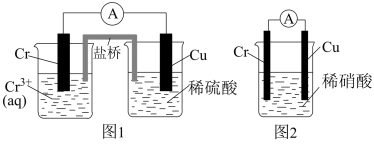
(4)工业上常将铬镀在其他金属表面,同铁、镍组成各种性质的不锈钢,在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电极上无气体产生,铬电极上产生大量有色气体,则下列叙述正确的是___________。
Ⅲ.+6价铬的化合物毒性较大,常用甲醇酸性燃料电池电解处理酸性含铬废水(主要含有 ),其原理示意图如下图所示:
),其原理示意图如下图所示:
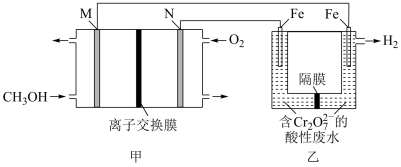
(5)M极为原电池的___________ 极(填“正”或“负”)。
(6)N极附近的
___________ (填“变大”或“变小”或“不变”)。
(7)写出电解池中阳极产物将 转化为
转化为 的离子方程式
的离子方程式___________ 。
 )在人体内可以起到提高免疫力、抗氧化等功效,含硒化合物在材料和药物领域具有重要作用。铬(
)在人体内可以起到提高免疫力、抗氧化等功效,含硒化合物在材料和药物领域具有重要作用。铬( )被广泛应用在冶金、化工、铸铁、耐火及高精端科技等领域。
)被广泛应用在冶金、化工、铸铁、耐火及高精端科技等领域。(1)在元素周期表中,硒是第34号元素,与氧同主族,硒原子的电子式表示为

 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。Ⅱ.工业制备高纯硒的流程如下:
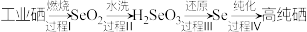
(2)下列说法正确的是___________。
| A.过程Ⅰ只发生氧化反应 |
| B.过程Ⅱ的水洗过程属于非氧化还原反应 |
C. 能与 能与 反应生成 反应生成 和 和 |
D. 在过程Ⅲ的反应中体现了还原性 在过程Ⅲ的反应中体现了还原性 |
(3)过程Ⅲ中还需要用的反应物为
 ,对应产物为
,对应产物为 ,标况下,当有
,标况下,当有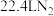 生成时,该反应中转移的电子数目为
生成时,该反应中转移的电子数目为(4)工业上常将铬镀在其他金属表面,同铁、镍组成各种性质的不锈钢,在下图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电极上无气体产生,铬电极上产生大量有色气体,则下列叙述正确的是___________。

A.由实验现象可知:金属活动性 |
B.图1为原电池装置, 电极上产生的是 电极上产生的是 |
C.两个装置中,电子均由 电极流向 电极流向 电极 电极 |
D.图2装置中 电极上发生的电极反应式为 电极上发生的电极反应式为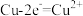 |
Ⅲ.+6价铬的化合物毒性较大,常用甲醇酸性燃料电池电解处理酸性含铬废水(主要含有
 ),其原理示意图如下图所示:
),其原理示意图如下图所示:
(5)M极为原电池的
(6)N极附近的

(7)写出电解池中阳极产物将
 转化为
转化为 的离子方程式
的离子方程式
您最近半年使用:0次
名校
解题方法
10 . 含氯物质在生产、生活中有重要作用。工业上常用次氯酸钠处理含有 NO 等氮氧化物的尾气,反应方程式如下:NaClO + NO + H2O — NaCl + HNO3 (未配平)。
(1)氯在元素周期表中的位置是_______ ,其所在主族的元素中,最高价氧化物对应的水化物酸性最强的是_______ (填化学式)。其所在周期的元素中,第一电离能最大的是______ (填化学式)。
(2)配平上述反应方程式_______ 。每有 0.3mol 电子发生转移,可消耗标准状况下 NO 气体的体积约为______ L。
(3)NaClO 溶液中存在如下关系:c(OH-)_____ c(HClO)(填“>”、“=”、或“<”)。
其他条件相同,随着 NaClO 溶液初始 pH(用稀硫酸调节)的不同,NO 转化率如图。
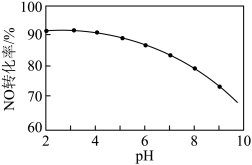
(4)NaClO 溶液的初始pH 越大,NO 的转化率越________ (填“高”或“低”),其原因是_________ 。
(5)取少量 NaClO 溶液和 KClO3 溶液,分别置于 A 试管和 B 试管,滴加试剂,观察现象,记录于下表。请将表格填写完整。
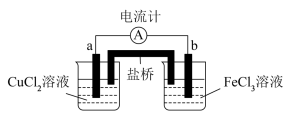
(6)某化学学习小组设计原电池装置如下图 (a 为铜电极 b 为石墨电极) :,请写出负极的电极反应式________ ;盐桥在原电池中所起的作用(任意写出一条)__________ 。
(1)氯在元素周期表中的位置是
(2)配平上述反应方程式
(3)NaClO 溶液中存在如下关系:c(OH-)
其他条件相同,随着 NaClO 溶液初始 pH(用稀硫酸调节)的不同,NO 转化率如图。

(4)NaClO 溶液的初始pH 越大,NO 的转化率越
(5)取少量 NaClO 溶液和 KClO3 溶液,分别置于 A 试管和 B 试管,滴加试剂,观察现象,记录于下表。请将表格填写完整。
| 滴加 KI 溶液 | 再滴加 CCl4,振荡、静置 | 结论 | |
| A 试管 | 溶液变为棕黄色 | 溶液分层,下层显 | 氧化性强弱:(填“>”或“<”) KClO3 |
| B 试管 | 无现象 | 溶液分层,均无色 |
(6)某化学学习小组设计原电池装置如下图 (a 为铜电极 b 为石墨电极) :,请写出负极的电极反应式

您最近半年使用:0次



