1 . 医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。回答下列问题:___ H++___ MnO +
+___ H2C2O4=___ CO2↑+___ Mn2++___
(1)配平上述离子方程式,在横线上填上正确的系数并在中填上所需的微粒。
(2)该反应中,若生成1molCO2,则转移电子的数目为___ 。
(3)测定血钙含量的方法为:取2mL血液,用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①溶解CaC2O4沉淀时不能用稀盐酸,原因是___ 。
②若消耗了5.0×10-5mol·L-1的KMnO4溶液20.00mL,则100mL该血液中含钙___ g。
 +
+(1)配平上述离子方程式,在横线上填上正确的系数并在中填上所需的微粒。
(2)该反应中,若生成1molCO2,则转移电子的数目为
(3)测定血钙含量的方法为:取2mL血液,用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①溶解CaC2O4沉淀时不能用稀盐酸,原因是
②若消耗了5.0×10-5mol·L-1的KMnO4溶液20.00mL,则100mL该血液中含钙
您最近一年使用:0次
名校
解题方法
2 . 已知还原性:SO >I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )
>I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )
 >I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )
>I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )A.当a=b时,发生的离子反应为SO +Cl2+H2O=SO +Cl2+H2O=SO +2H++2Cl- +2H++2Cl- |
B.当5a=4b时,发生的离子反应为4SO +2I-+5Cl2+4H2O=4SO +2I-+5Cl2+4H2O=4SO +I2+8H++10Cl- +I2+8H++10Cl- |
C.当a≤b≤ a时,反应中转移电子的物质的量n(e-)为a mol≤n(e-)≤3a mol a时,反应中转移电子的物质的量n(e-)为a mol≤n(e-)≤3a mol |
D.当a<b< a时,溶液中SO a时,溶液中SO 、I-与Cl-的物质的量之比为a∶(3a-2b)∶2b 、I-与Cl-的物质的量之比为a∶(3a-2b)∶2b |
您最近一年使用:0次
2020-08-18更新
|
3378次组卷
|
7卷引用:黑龙江省哈尔滨师范大学附属中学2020-2021学年高二下学期期末考试化学试题
黑龙江省哈尔滨师范大学附属中学2020-2021学年高二下学期期末考试化学试题浙江省瑞安市上海新纪元高级中学2019-2020学年高一下学期期末考试化学试题(2)(已下线)解密04 离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密04 离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)课时06 与量有关的离子方程式书写-2022年高考化学一轮复习小题多维练(全国通用)辽宁省实验中学2021-2022学年高一上学期11月期中阶段测试化学试题福建省泉州市永春第一中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
3 . 二氯化二硫 ( S2Cl2)是一种黄红色液体,常用作橡胶的低温硫化剂和粘结剂。S2Cl2分子中各原子最外层均有8个电子。S2Cl2遇水反应会产生淡黄色沉淀和刺激性气味气体。下列说法不正确 的是
| A.S2Cl2的结构式为 Cl—S —S—Cl |
| B.S2Cl2 可能使品红溶液褪色 |
| C.S2Cl2 与水反应时 ,氧化产物与还原产物的物质的量之比为 1 : 3 |
| D.将S2Cl2气体通入 AgNO3溶液中,若有白色沉淀产生,则 S2Cl2气体中有 HCl |
您最近一年使用:0次
2020-07-24更新
|
2104次组卷
|
13卷引用:黑龙江省齐齐哈尔市第八中学校2020-2021学年高二上学期开学考试化学试题
黑龙江省齐齐哈尔市第八中学校2020-2021学年高二上学期开学考试化学试题黑龙江齐齐哈尔第八中学校2021-2022学年高二上学期开学考试化学试题浙江省丽水市2019-2020学年高二下学期期末教学质量监控化学试题浙江省温州新力量联盟2020-2021学年高二上学期期末联考化学试题(已下线)【绍兴新东方】绍兴高中化学00012(已下线)高二上期末考化学194上海市建平中学2020-2021学年高三上学期期中考试化学试题湖北省天门中学、仙桃中学2021-2022学年高一下学期2月联考化学试题湖南省邵阳市隆回县第一中学2021-2022学年高三下学期第三次模拟考试化学试题(已下线)专题10 常见非金属元素的性质及应用-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)浙江省杭州第十四中学2022-2023学年高一上学期期末考试化学试题甘肃省定西市渭源县第一中学2022-2023学年高一下学期第一次阶段考试化学试题(已下线)【2023】【高一下】【其他】【余高1】【高中化学】【刘尼尼收集】
名校
4 . CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是
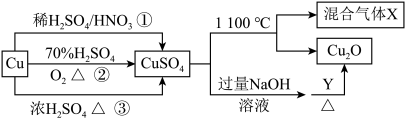
| A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为2:3 |
| B.相对于途径①、③,途径②更好地体现了绿色化学思想 |
| C.已知1molCuSO4在1100℃所得混合气体X为SO2和O2,则O2为0.75mol |
| D.Y可以是葡萄糖 |
您最近一年使用:0次
2020-07-17更新
|
815次组卷
|
8卷引用:黑龙江省大兴安岭实验中学2023-2024学年高二上学期开学考试化学试卷
5 . I已知:还原性HSO >I-,氧化性IO
>I-,氧化性IO > I2 。
> I2 。
(1)在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目_______ 。
囗NaIO3+囗NaHSO3→ 囗I2+囗Na2SO4+囗H2SO4+囗H2O
(2)在含5molNaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出I2单质的物质的量的关系曲线如图所示。写出反应过程中与AB段曲线对应的离子方程式_______ ;当溶液中I-与I2的物质的量之比为5:3时,加入的NaIO3为_______ mol。

II 已知:KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2、KHSO4等物质。写出该反应的化学方程式________________ 。
 >I-,氧化性IO
>I-,氧化性IO > I2 。
> I2 。(1)在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目
囗NaIO3+囗NaHSO3→ 囗I2+囗Na2SO4+囗H2SO4+囗H2O
(2)在含5molNaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出I2单质的物质的量的关系曲线如图所示。写出反应过程中与AB段曲线对应的离子方程式

II 已知:KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2、KHSO4等物质。写出该反应的化学方程式
您最近一年使用:0次
名校
解题方法
6 . 铝元素含量居金属首位,主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。铝的单质及其化合物在生产、生活、科研等领域应用广泛。
Ⅰ.工业上用铝土矿制备铝的某种化合物的工艺流程如图:
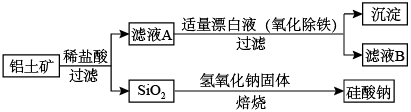
(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①该过程中涉及某氧化还原反应如下,请完成:___ Fe2++___ ClO-+___ =___ Fe(OH)3↓+___ C1-+___
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为___ (选填代号)
A.氢氧化钠溶液B.硫酸溶液C.氨水D.二氧化碳
③由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、___ (填操作名称)、过滤、洗涤。
Ⅱ.铵明矾(NH4Al(SO4)2•12H2O)是常见的食品添加剂,在日常生活、生产中也占有一席之地。
(1)铵明矾可用于净水,用离子方程式表示其净水原理___ ;向其溶液中逐滴加入NaOH溶液至过量,可观察到的现象是___ 。
(2)实验证明铵明矾高温分解后气体的组成成分是NH3、N2、SO3、SO2和H2O,且相同条件下测得生成N2和SO2的体积比是定值,V(N2):V(SO2)=___ 。
(3)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为___ (填代号)。

Ⅰ.工业上用铝土矿制备铝的某种化合物的工艺流程如图:

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①该过程中涉及某氧化还原反应如下,请完成:
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为
A.氢氧化钠溶液B.硫酸溶液C.氨水D.二氧化碳
③由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、
Ⅱ.铵明矾(NH4Al(SO4)2•12H2O)是常见的食品添加剂,在日常生活、生产中也占有一席之地。
(1)铵明矾可用于净水,用离子方程式表示其净水原理
(2)实验证明铵明矾高温分解后气体的组成成分是NH3、N2、SO3、SO2和H2O,且相同条件下测得生成N2和SO2的体积比是定值,V(N2):V(SO2)=
(3)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为

您最近一年使用:0次
名校
解题方法
7 . 海水中溴含量约为65mg·L-1,从海水中提取溴的工艺流程如图:
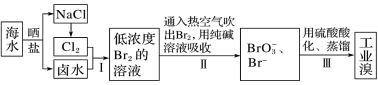
(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是_____ 。
(2)步骤Ⅱ通入热空气吹出Br2,利用了溴的______ (填字母)。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数:
________ Br2+________  =
=________  +
+_ Br-+_ CO2↑
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的化学方程式:______ 。
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是______ (填字母)。
A.稀硫酸 B.四氯化碳 C.烧碱溶液 D.水

(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是
(2)步骤Ⅱ通入热空气吹出Br2,利用了溴的
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数:
 =
= +
+(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的化学方程式:
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是
A.稀硫酸 B.四氯化碳 C.烧碱溶液 D.水
您最近一年使用:0次
2020-07-06更新
|
534次组卷
|
4卷引用:黑龙江省哈尔滨市第一中学2019-2020 学年高二下学期期末考试化学试题
名校
解题方法
8 . 方程式书写:
(1)S+Ca(OH)2—CaS5+CaS2O3+H2O___ 。
(2)H2O2+Cr2(SO4)3+ —K2SO4+K2CrO4+H2O___ 。
(3)氯酸镁加入含有KSCN的酸性硫酸亚铁溶液中立即出现红色,写出相关反应的离子方程式___ 。
(4)写出用氯化铁溶液浸取辉铜矿石(主要成分是Cu2S)发生反应的离子方程式___ 。
(1)S+Ca(OH)2—CaS5+CaS2O3+H2O
(2)H2O2+Cr2(SO4)3+ —K2SO4+K2CrO4+H2O
(3)氯酸镁加入含有KSCN的酸性硫酸亚铁溶液中立即出现红色,写出相关反应的离子方程式
(4)写出用氯化铁溶液浸取辉铜矿石(主要成分是Cu2S)发生反应的离子方程式
您最近一年使用:0次
9 . 钯的化合物PdCl2通过化学反应可用来检测有毒气体CO,该反应的反应物与生成物有CO、Pd、H2O、HCl、PdCl2和一种未知物质X。下列说法正确 的是( )
| A.未知物质X为CO2,属于还原产物 |
| B.每转移1mole-时,生成2molX |
| C.反应中PdCl2作还原剂,被氧化 |
| D.还原性:CO>Pd |
您最近一年使用:0次
名校
解题方法
10 . 某反应体系的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O.下列选项正确的是( )


| A.Na2S4O6、H2O、Na2S2O3、Au2O、NaOH |
| B.Na2S2O3、H2O、Na2S4O6、Au2O、NaOH |
| C.Na2S2O3、NaOH、Na2S4O6、Au2O、H2O |
| D.当1mol Au2O3完全反应时,转移电子的物质的量为8mol |
您最近一年使用:0次
2020-06-15更新
|
299次组卷
|
11卷引用:【全国百强校】黑龙江省哈尔滨市第六中学2017-2018学年高二下学期期末考试化学试题
【全国百强校】黑龙江省哈尔滨市第六中学2017-2018学年高二下学期期末考试化学试题2016届浙江省宁波市柴桥中学高三上学期10月月考化学试卷四川省攀枝花市第十二中学2019届高三上学期第一次月考化学试题(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第3讲 氧化还原反应【押题专练】甘肃省靖远县第一中学2019届高三上学期9月月考化学试题【全国百强校】贵州省铜仁市第一中学2019届高三上学期第二次月考化学试题(已下线)【南昌新东方】江西省九江市第一中学2015-2016学年高一上学期第二次(12月)月考化学试题(已下线)【南昌新东方】江西省九江一中2015-2016学年高一上学期第二次月考化学试卷(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点04 氧化还原反应-备战2022年高考化学学霸纠错(全国通用)



