名校
1 . 铁粉具有平肝镇心解毒之功效,主治惊痫、癫狂、脚气冲心、贫血等。某兴趣小组设计利用 制备还原铁粉的流程如下。
制备还原铁粉的流程如下。

实验室中可用 (用废铁屑和稀硫酸反应制得)和
(用废铁屑和稀硫酸反应制得)和 在如图装置模拟上述流程中的“转化”环节。
在如图装置模拟上述流程中的“转化”环节。

(1)植物油的作用是___________ 。
(2)实验过程中,欲将得到的 溶液和
溶液和 溶液混合,操作方法是
溶液混合,操作方法是___________ 。混合后反应生成 的离子方程式为
的离子方程式为___________ 。
(3) 溶液要现用现配的原因是
溶液要现用现配的原因是___________ 。
(4)“干燥”的主要目的是脱去游离水,该过程中会有少量 在空气中被氧化为
在空气中被氧化为 ,该反应的化学方程式为
,该反应的化学方程式为___________ ;取干燥后的 样品11.33g,与木炭混合后焙烧,所有铁都被还原为还原铁粉,最终得到还原铁粉5.6g,样品中杂质
样品11.33g,与木炭混合后焙烧,所有铁都被还原为还原铁粉,最终得到还原铁粉5.6g,样品中杂质 的质量为
的质量为___________ g。在高温条件下,过量的木炭与 反应,写出此反应的化学方程式:
反应,写出此反应的化学方程式:___________ 。
 制备还原铁粉的流程如下。
制备还原铁粉的流程如下。
实验室中可用
 (用废铁屑和稀硫酸反应制得)和
(用废铁屑和稀硫酸反应制得)和 在如图装置模拟上述流程中的“转化”环节。
在如图装置模拟上述流程中的“转化”环节。
(1)植物油的作用是
(2)实验过程中,欲将得到的
 溶液和
溶液和 溶液混合,操作方法是
溶液混合,操作方法是 的离子方程式为
的离子方程式为(3)
 溶液要现用现配的原因是
溶液要现用现配的原因是(4)“干燥”的主要目的是脱去游离水,该过程中会有少量
 在空气中被氧化为
在空气中被氧化为 ,该反应的化学方程式为
,该反应的化学方程式为 样品11.33g,与木炭混合后焙烧,所有铁都被还原为还原铁粉,最终得到还原铁粉5.6g,样品中杂质
样品11.33g,与木炭混合后焙烧,所有铁都被还原为还原铁粉,最终得到还原铁粉5.6g,样品中杂质 的质量为
的质量为 反应,写出此反应的化学方程式:
反应,写出此反应的化学方程式:
您最近一年使用:0次
2024-01-23更新
|
325次组卷
|
3卷引用:山东省肥城市第一高级中学等学校2023-2024学年高一上学期12月大联考化学试题
解题方法
2 . 生活污水中的氮和磷主要以铵盐和磷酸盐形式存在,可用电解法从溶液中去除,电解装置如图1,除氮的原理如图2,除磷的原理是利用 将
将 转化为
转化为 沉淀。图3为某含
沉淀。图3为某含 污水在氮磷联合脱除过程中溶液pH变化。
污水在氮磷联合脱除过程中溶液pH变化。

下列说法正确的是
 将
将 转化为
转化为 沉淀。图3为某含
沉淀。图3为某含 污水在氮磷联合脱除过程中溶液pH变化。
污水在氮磷联合脱除过程中溶液pH变化。
下列说法正确的是
| A.图2中0~20min 脱除的元素是氮元素,此时石墨作阴极 |
| B.溶液pH越小有效氯浓度越大,氮的去除率越高 |
C.电解法除氮中 氧化 氧化 的离子方程式为 的离子方程式为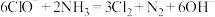 |
D.图2中20~40 min脱除的元素是磷元素,此时阳极的电极反应式为 |
您最近一年使用:0次
解题方法
3 . 由含硒废料(主要含SiO2、S、Se、Fe2O3、CuO、ZnO等)制取硒的流程如图:
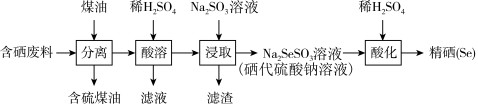
| A.加入煤油的目的是溶解S |
B.“酸溶”所得的滤液中存在 |
| C.“酸溶”时能除去废料中的全部氧化物杂质 |
D.“酸化”的离子反应为: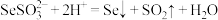 |
您最近一年使用:0次
2024-01-22更新
|
194次组卷
|
2卷引用:山东省淄博市张店区潘庄高级中学2023-2024学年高一下学期第一次月考化学试题
名校
4 . 氧化亚铜主要用于制造船底防污漆(用来杀死低级海生动物)、杀虫剂,以及各种铜盐、分析试剂、红色玻璃,还用于镀铜及镀铜合金溶液的配制。用某铜矿(主要含CuS、FeO)制备Cu2O的一种工艺流程如下图:
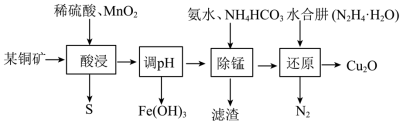
已知:常温下,相关金属离子生成氢氧化物沉淀的pH见表:
请回答下列问题:
(1)基态Cu原子价层电子的排布图为_______ 。
(2)滤渣的主要成分是_______ (填化学式)。
(3)“酸浸”中加入MnO2的作用是_______ ;写出其中生成单质S的化学方程式_______ 。
(4)“调pH”的范围是_______ 。
(5)“还原”前Cu元素以[Cu(NH3)4](OH)2的形式存在,水合肼被氧化的化学方程式为_______ ;一定体积下,保持其它条件不变,水合肼浓度对Cu2O的产率的影响如图所示。当水合肼浓度大于3.25mol·L-1时,[Cu(NH3)4]2+的转化率仍增大,但Cu2O的产率下降,其可能的原因是_______ 。
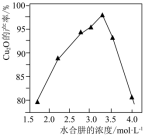

已知:常温下,相关金属离子生成氢氧化物沉淀的pH见表:
| 氢氧化物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 4.8 | 1.9 | 7.5 | 8.8 |
| 沉淀完全的pH | 6.4 | 3.2 | 9.7 | 10.4 |
(1)基态Cu原子价层电子的排布图为
(2)滤渣的主要成分是
(3)“酸浸”中加入MnO2的作用是
(4)“调pH”的范围是
(5)“还原”前Cu元素以[Cu(NH3)4](OH)2的形式存在,水合肼被氧化的化学方程式为

您最近一年使用:0次
5 .  为白色立方结晶或白色粉末,难溶于水,露置于空气中易被氧化为绿色的碱式氯化铜。以工业废铜泥为原料制备
为白色立方结晶或白色粉末,难溶于水,露置于空气中易被氧化为绿色的碱式氯化铜。以工业废铜泥为原料制备 的流程如下图(工业废铜泥的主要成分为
的流程如下图(工业废铜泥的主要成分为 、
、 、
、 还含有Fe等金属杂质)
还含有Fe等金属杂质)

下列说法错误的是
 为白色立方结晶或白色粉末,难溶于水,露置于空气中易被氧化为绿色的碱式氯化铜。以工业废铜泥为原料制备
为白色立方结晶或白色粉末,难溶于水,露置于空气中易被氧化为绿色的碱式氯化铜。以工业废铜泥为原料制备 的流程如下图(工业废铜泥的主要成分为
的流程如下图(工业废铜泥的主要成分为 、
、 、
、 还含有Fe等金属杂质)
还含有Fe等金属杂质)
下列说法错误的是
A.“灼烧”不充分会降低 的产率 的产率 |
| B.溶液1经处理后可循环使用 |
| C.“除杂”步骤中,应加过量的氢氧化钠溶液 |
| D.为了保证产品纯度,应采用减压过滤及真空干燥的方式 |
您最近一年使用:0次
名校
6 . 按要求完成下列填空:
(1)写出 在水中的电离方程式
在水中的电离方程式___________ 。
(2)向新制氯水中滴加石蕊试液,溶液变红,起作用的微粒是___________ ;然后又褪色,起作用的微粒是___________ 。
(3)实验证明铜、不能在低温下与 反应,也不能与稀
反应,也不能与稀 共热发生反应,但工业上却是将废铜屑倒入热的稀
共热发生反应,但工业上却是将废铜屑倒入热的稀 中并通入空气来制备
中并通入空气来制备 溶液的。铜屑在此状态下被溶解的化学方程式为
溶液的。铜屑在此状态下被溶解的化学方程式为___________ 。
(4)过量铁粉与稀硝酸反应方程式为: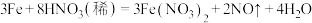 此反应中,被还原和未被还原的硝酸的物质的量之比为
此反应中,被还原和未被还原的硝酸的物质的量之比为___________ 。当产生 气体在标况下体积为
气体在标况下体积为 时,转移电子
时,转移电子___________  ,被还原的硝酸的物质的量为
,被还原的硝酸的物质的量为___________  。
。
(5)漂白粉是常用的消毒剂。漂白粉的有效成分是(填化学式)___________ 。
(1)写出
 在水中的电离方程式
在水中的电离方程式(2)向新制氯水中滴加石蕊试液,溶液变红,起作用的微粒是
(3)实验证明铜、不能在低温下与
 反应,也不能与稀
反应,也不能与稀 共热发生反应,但工业上却是将废铜屑倒入热的稀
共热发生反应,但工业上却是将废铜屑倒入热的稀 中并通入空气来制备
中并通入空气来制备 溶液的。铜屑在此状态下被溶解的化学方程式为
溶液的。铜屑在此状态下被溶解的化学方程式为(4)过量铁粉与稀硝酸反应方程式为:
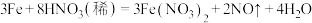 此反应中,被还原和未被还原的硝酸的物质的量之比为
此反应中,被还原和未被还原的硝酸的物质的量之比为 气体在标况下体积为
气体在标况下体积为 时,转移电子
时,转移电子 ,被还原的硝酸的物质的量为
,被还原的硝酸的物质的量为 。
。(5)漂白粉是常用的消毒剂。漂白粉的有效成分是(填化学式)
您最近一年使用:0次
名校
7 . 元素周期表与元素周期律在化学学习研究中有很重要的作用。如表是元素周期表的一部分,回答下列问题(用相关化学用语回答)。
(1)③、⑥、⑨的简单离子半径由小到大的顺序___________ (用离子符号表示)。
(2)写出元素⑪的单质与水反应的化学方程式___________ 。
(3)元素③、④、⑩的简单气态氢化物的稳定性最强的是___________ (用化学式表示)。
(4)配制0.1mol/L500mL元素⑤的氢氧化物溶液,需用托盘天平称取该氢氧化物的质量是___________ g。
(5)⑤2⑨③3在加热条件下发生分解反应生成两种盐,其中氧化产物与还原产物的物质的量之比为3:1,该反应的化学方程式:___________ 。
(6)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是___________(填字母)。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
| 四 | ⑪ |
(2)写出元素⑪的单质与水反应的化学方程式
(3)元素③、④、⑩的简单气态氢化物的稳定性最强的是
(4)配制0.1mol/L500mL元素⑤的氢氧化物溶液,需用托盘天平称取该氢氧化物的质量是
(5)⑤2⑨③3在加热条件下发生分解反应生成两种盐,其中氧化产物与还原产物的物质的量之比为3:1,该反应的化学方程式:
(6)欲比较④和⑨两种元素的非金属性强弱,可以作为验证的证据是___________(填字母)。
| A.比较这两种元素单质的沸点 |
| B.比较这两种元素单质与氢气化合的难易 |
| C.比较这两种元素的最高价氧化物对应水化物的酸性强弱 |
| D.比较这两种元素的单质与酸或碱反应的难易程度 |
您最近一年使用:0次
解题方法
8 . 实验室用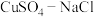 混合液与
混合液与 溶液反应制取
溶液反应制取 (装置如下图),已知溶液
(装置如下图),已知溶液 时产率最高,
时产率最高, 可发生反应:
可发生反应: ,
, 。
。

下列叙述正确的是
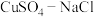 混合液与
混合液与 溶液反应制取
溶液反应制取 (装置如下图),已知溶液
(装置如下图),已知溶液 时产率最高,
时产率最高, 可发生反应:
可发生反应: ,
, 。
。
下列叙述正确的是
A.仪器2中所加试剂应为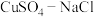 混合液或 混合液或 溶液 溶液 |
B. 与 与 溶液反应的离子方程式为 溶液反应的离子方程式为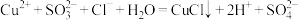 |
C.实验过程中用 混合溶液代替 混合溶液代替 溶液,可保证 溶液,可保证 产率较高 产率较高 |
| D.反应完成后需经稀释、过滤、洗涤、干燥后才可获得产品 |
您最近一年使用:0次
解题方法
9 . 三氯化铁浸出硫化锑(Sb2S3)精矿提取锑的工艺流程如下,电解液可回收循环利用,下列说法不正确的是


| A.“矿渣”中含有单质硫 | B.浸出过程中会产生H2S |
| C.电解过程中可采用阳离子隔膜 | D.氯化铁溶液可循环使用 |
您最近一年使用:0次
10 . 工业上常采用铬铁矿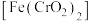 为主要原料制备红矾钠
为主要原料制备红矾钠 ,实验室模拟红矾钠的制备步骤如下,与相关步骤对应的叙述正确的是
,实验室模拟红矾钠的制备步骤如下,与相关步骤对应的叙述正确的是
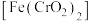 为主要原料制备红矾钠
为主要原料制备红矾钠 ,实验室模拟红矾钠的制备步骤如下,与相关步骤对应的叙述正确的是
,实验室模拟红矾钠的制备步骤如下,与相关步骤对应的叙述正确的是| 步骤 | 叙述 | |
| A | Ⅰ.煅烧:将难溶于水的铬铁矿在碱性介质中熔融煅烧,生成了可溶性的 | 熔融煅烧可在石英坩埚中进行,该反应中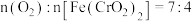 |
| B | Ⅱ.浸取:煅烧后的熟料成分比较复杂,含有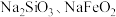 等,其中 等,其中 遇水强烈水解生成沉淀,浸取后可获得 遇水强烈水解生成沉淀,浸取后可获得 的浸取液 的浸取液 |  水解的化学方程式为: 水解的化学方程式为: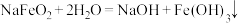 |
| C | Ⅲ.中和除杂、酸化:酸化可以使 转变为 转变为 | 酸化时可选用盐酸 |
| D | Ⅳ.结晶:结晶后得到橙红色晶体红矾钠 | 先蒸发浓缩、后降温结晶获得红矾钠 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



