名校
1 . 纯碱在生产、生活中有广泛应用。例如可用足量的纯碱溶液吸收含氯气的尾气,生成三种盐(反应1);工业上从海水中提取溴的流程中也用到了纯碱溶液,其主要原理如下:反应2: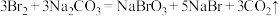 。下列说法正确的是
。下列说法正确的是
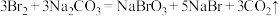 。下列说法正确的是
。下列说法正确的是| A.反应2中氧化产物与还原产物的质量之比为1∶5 |
| B.标准状况下,22.4L溴单质中含有2mol溴原子 |
| C.反应1中生成的三种盐是NaClO,NaClO3和NaHCO3 |
| D.反应2中的Br2与反应1中的Cl2表现出了相似的化学性质 |
您最近一年使用:0次
2 . 硫酸锌(ZnSO4)是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为ZnCO3,杂质为SiO2以及Ca、Mg、Fe、Cu等的化合物。其制备流程如下:

回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______ 。
(2)为了提高锌的浸取效果,可采取的措施有_______ 。
(3)加入物质X调节溶液pH=5,最适宜使用的X是_______ (填标号)。
A.NH3·H2O B.Ca(OH)2 C.NaOH
滤渣①的主要成分是Fe(OH)3、_______ 、_______ 。
(4)向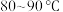 的滤液①中分批加入适量KMnO4溶液充分反应后过滤,滤渣②中有MnO2、Fe(OH)3 ,该步反应的离子方程式为
的滤液①中分批加入适量KMnO4溶液充分反应后过滤,滤渣②中有MnO2、Fe(OH)3 ,该步反应的离子方程式为_______ 。
(5)滤液②中加入锌粉的目的是_______ 。
(6)滤渣④与浓H2SO4反应可以释放HF并循环利用,同时得到的副产物是_______ 。

回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为
(2)为了提高锌的浸取效果,可采取的措施有
(3)加入物质X调节溶液pH=5,最适宜使用的X是
A.NH3·H2O B.Ca(OH)2 C.NaOH
滤渣①的主要成分是Fe(OH)3、
(4)向
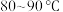 的滤液①中分批加入适量KMnO4溶液充分反应后过滤,滤渣②中有MnO2、Fe(OH)3 ,该步反应的离子方程式为
的滤液①中分批加入适量KMnO4溶液充分反应后过滤,滤渣②中有MnO2、Fe(OH)3 ,该步反应的离子方程式为(5)滤液②中加入锌粉的目的是
(6)滤渣④与浓H2SO4反应可以释放HF并循环利用,同时得到的副产物是
您最近一年使用:0次
名校
解题方法
3 . 物质集合M中含有常见物质Na2O2、NaHCO3、Al、SO2、Fe、NH3、Na、F2。这些物质按照以下方法进行分类后如图所示,请按照要求回答问题。
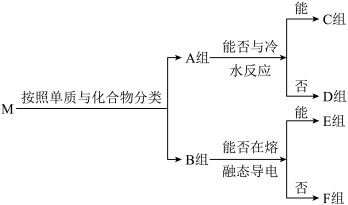
(1)B组物质中属于非电解质的物质为____ ,其中能作制冷剂的物质的电子式为____ 。
(2)C组物质中能与水反应生成还原性气体的化学方程式为____ 。
(3)D组物质中其中一种物质可以制备出另外一种物质,请写出一种该反应在工业上的应用:____ 。
(4)请写出F组中的酸性氧化物与酸性KMnO4溶液反应的离子方程式:____ 。
(5)在密闭容器中,将E组中的两种物质加热反应,若混合物中金属原子与氧原子的物质的量之比为1:2,混合加热充分反应后,排出气体,剩余固体的成分为____ ;反应中氧化剂与还原剂的物质的量之比为____ 。

(1)B组物质中属于非电解质的物质为
(2)C组物质中能与水反应生成还原性气体的化学方程式为
(3)D组物质中其中一种物质可以制备出另外一种物质,请写出一种该反应在工业上的应用:
(4)请写出F组中的酸性氧化物与酸性KMnO4溶液反应的离子方程式:
(5)在密闭容器中,将E组中的两种物质加热反应,若混合物中金属原子与氧原子的物质的量之比为1:2,混合加热充分反应后,排出气体,剩余固体的成分为
您最近一年使用:0次
2022-09-23更新
|
601次组卷
|
2卷引用:宁夏石嘴山市平罗中学2022-2023学年高三上学期期中考试(重点班)化学试题
名校
解题方法
4 . 物质之间的转化关系如图,部分生成物省略。A是由四种元素组成的化合物。C、D是由元素X、Y、Z中两种组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用。
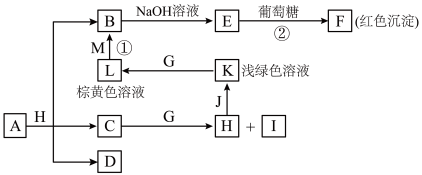
请回答下列问题:
(1)C的电子式____ 。
(2)写出反应①的离子反应方程式____ ,反应②中体现葡萄糖的____ 性。
(3)比较Y与Z的原子半径大小_____>_____(填写元素符号)。____
(4)写出A的化学式____ 。
(5)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体;请写出该反应的化学方程式____ 。
(6)研究表明:气体D在480℃、800大气压条件下可被活泼金属钠还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出该反应的化学方程式____ ,N的一种同素异形体的名称为____ 。

请回答下列问题:
(1)C的电子式
(2)写出反应①的离子反应方程式
(3)比较Y与Z的原子半径大小_____>_____(填写元素符号)。
(4)写出A的化学式
(5)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体;请写出该反应的化学方程式
(6)研究表明:气体D在480℃、800大气压条件下可被活泼金属钠还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出该反应的化学方程式
您最近一年使用:0次
2022-09-20更新
|
344次组卷
|
5卷引用:宁夏固原市第一中学2023届高三上学期第二次月考化学试题
名校
5 . 氧化还原反应在工业生产、环保及科研中有广泛的应用。氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50 ℃时反应可生成它。CuH具有的性质有:不稳定,易分解,在氯气中能燃烧;与稀盐酸反应能生成气体,Cu+在酸性条件下发生的反应是2Cu+=Cu2++Cu。
(1)写出CuH在氯气中燃烧的化学反应方程式:_______ 。
(2)CuH溶解在稀盐酸中反应的离子化学方程式是_______ 。
(3)如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:_______ 。
(1)写出CuH在氯气中燃烧的化学反应方程式:
(2)CuH溶解在稀盐酸中反应的离子化学方程式是
(3)如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:
您最近一年使用:0次
名校
6 . 由软锰矿(主要成分为MnO2)制备KMnO4的实验流程可表示如下:
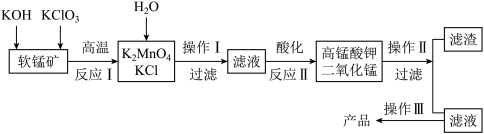
(1)实验时,首先将软锰矿研细,然后和KOH、 KClO3混合高温发生反应I,将软锰矿研细的目的是_______ 。
(2)反应I发生反应的化学方程式是_______ ,该反应中氧化剂是_______ ;反应II发生反应的离子方程式是_______ 。
(3)操作III的实验步骤为_______ 、_______ 、过滤;可循环利用的物质的化学式为_______ 。
(4)取制得的产品6.5g,配成250mL溶液;准确称取纯1.34gNa2C2O4配成适量溶液。用上述KMnO4溶液滴定Na2C2O4溶液,恰好反应(氧化产物为CO2,还原产物为Mn2+)时,消耗KMnO4溶液的体积为25.00mL。该KMnO4的纯度为_______ (保留小数点后一位)。

(1)实验时,首先将软锰矿研细,然后和KOH、 KClO3混合高温发生反应I,将软锰矿研细的目的是
(2)反应I发生反应的化学方程式是
(3)操作III的实验步骤为
(4)取制得的产品6.5g,配成250mL溶液;准确称取纯1.34gNa2C2O4配成适量溶液。用上述KMnO4溶液滴定Na2C2O4溶液,恰好反应(氧化产物为CO2,还原产物为Mn2+)时,消耗KMnO4溶液的体积为25.00mL。该KMnO4的纯度为
您最近一年使用:0次
名校
7 . 下列离子方程式中,不 正确的是
A.向NaHCO3溶液中加入过量的NaOH溶液: +OH-= +OH-= +H2O +H2O |
| B.稀硫酸中加入铁粉:2Fe+6H+=2Fe3++3H2↑ |
| C.FeBr2溶液中通入过量的Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
D.向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++ =3Fe3++NO↑+2H2O =3Fe3++NO↑+2H2O |
您最近一年使用:0次
2022-09-14更新
|
244次组卷
|
2卷引用:宁夏固原市第一中学2023届高三上学期第一次月考化学试题
名校
解题方法
8 . 某同学在实验室欲配制物质的量浓度均为1.0mol·L-1的NaOH溶液、稀硫酸各450mL。提供的试剂是:NaOH固体、18.4mol·L-1的浓硫酸(密度为1.84g·cm-3)和蒸馏水。
(1)请你观察图示判断其中不正确的操作有_______ 。(填序号)
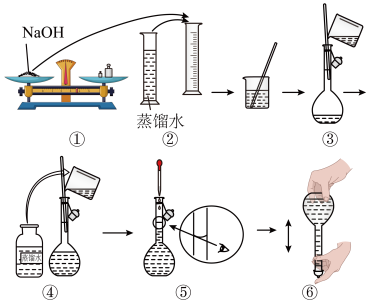
(2)应用托盘天平称量NaOH_______ g,应用量筒量取浓硫酸_______ mL。
(3)在配制上述溶液实验中,下列操作引起结果偏低的有_______ 。
A.该学生在量取浓硫酸时,仰视刻度线
B.溶解硫酸后没有冷却至室温就立即完成后面的配制操作
C.在烧杯中溶解搅拌时,溅出少量溶液
D.没有用蒸馏水洗涤烧杯2~3次,并将洗涤液移入容量瓶中
E.将量筒洗涤2~3次,并全部转移至容量瓶中
F.容量瓶中原来存有少量蒸馏水
G.胶头滴管加水定容时俯视刻度线
(4)若用0.01000mol·L-1K2Cr2O7(酸性)溶液滴定20.00mL未知浓度的含Fe2+的溶液,恰好完全反应时消10.00mLK2Cr2O7溶液,写出该反应的离子反应方程式_______ ,待测液中Fe2+的浓度是_______ g/L(保留4位有效数字)。
(1)请你观察图示判断其中不正确的操作有

(2)应用托盘天平称量NaOH
(3)在配制上述溶液实验中,下列操作引起结果偏低的有
A.该学生在量取浓硫酸时,仰视刻度线
B.溶解硫酸后没有冷却至室温就立即完成后面的配制操作
C.在烧杯中溶解搅拌时,溅出少量溶液
D.没有用蒸馏水洗涤烧杯2~3次,并将洗涤液移入容量瓶中
E.将量筒洗涤2~3次,并全部转移至容量瓶中
F.容量瓶中原来存有少量蒸馏水
G.胶头滴管加水定容时俯视刻度线
(4)若用0.01000mol·L-1K2Cr2O7(酸性)溶液滴定20.00mL未知浓度的含Fe2+的溶液,恰好完全反应时消10.00mLK2Cr2O7溶液,写出该反应的离子反应方程式
您最近一年使用:0次
2022-08-30更新
|
328次组卷
|
2卷引用:宁夏回族自治区银川一中2022-2023学年高三上学期第一次月考理科综合化学试题
名校
9 . 焦亚硫酸钠 在医药、橡胶、印染、食品等方面应用广泛,其制备流程如图所示。
在医药、橡胶、印染、食品等方面应用广泛,其制备流程如图所示。
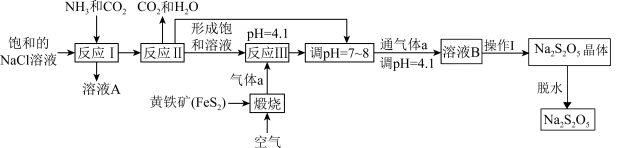
已知:① 过饱和溶液中更易形成
过饱和溶液中更易形成 ;
;
②焦亚硫酸钠 在空气中易氧化,受热易分解。
在空气中易氧化,受热易分解。
回答下列问题:
(1)反应I中先通入气体____ (填化学式),反应III中通入的气体a为_____ (填化学式)。
(2)溶液A中含有三种阳离子,分别为 、
、 和离子X。检验溶液A中离子X的方法是
和离子X。检验溶液A中离子X的方法是_______ 。
(3)反应III调节pH为4.1,发生反应的离子方程式为_______ 。
(4)再次通入气体a得到溶液B的目的是_______ 。
(5)操作I为:在氮气氛围中,_______ ,_______ ,过滤,洗涤。其中洗涤 晶体时依次用饱和
晶体时依次用饱和 水溶液、无水乙醇。用饱和
水溶液、无水乙醇。用饱和 水溶液洗涤的目的是
水溶液洗涤的目的是_______ 。
(6)久置的 固体中若含有
固体中若含有 杂质,其可能的原因是
杂质,其可能的原因是_______ 。(用化学反应方程式表示)
 在医药、橡胶、印染、食品等方面应用广泛,其制备流程如图所示。
在医药、橡胶、印染、食品等方面应用广泛,其制备流程如图所示。
已知:①
 过饱和溶液中更易形成
过饱和溶液中更易形成 ;
;②焦亚硫酸钠
 在空气中易氧化,受热易分解。
在空气中易氧化,受热易分解。回答下列问题:
(1)反应I中先通入气体
(2)溶液A中含有三种阳离子,分别为
 、
、 和离子X。检验溶液A中离子X的方法是
和离子X。检验溶液A中离子X的方法是(3)反应III调节pH为4.1,发生反应的离子方程式为
(4)再次通入气体a得到溶液B的目的是
(5)操作I为:在氮气氛围中,
 晶体时依次用饱和
晶体时依次用饱和 水溶液、无水乙醇。用饱和
水溶液、无水乙醇。用饱和 水溶液洗涤的目的是
水溶液洗涤的目的是(6)久置的
 固体中若含有
固体中若含有 杂质,其可能的原因是
杂质,其可能的原因是
您最近一年使用:0次
2022-08-26更新
|
304次组卷
|
2卷引用:宁夏石嘴山市平罗中学2022-2023学年高三上学期11月期中考试化学试题
名校
解题方法
10 . 碱式硫酸铁[Fe(OH)SO4]是一种絮疑剂,常用于污水处理。工业上利用废铁屑(含少量Al2O3、Fe2O3等)生产碱式硫酸铁的工艺流程如图所示。
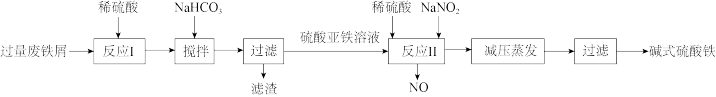
下列说法错误的是

下列说法错误的是
| A.“反应I”后的溶液中主要存在的阳离子有H+、Fe2+、Al3+ |
| B.“反应II”中加入稀硫酸可抑制Fe3+的水解 |
C.“反应II”对应的离子方程式为Fe2++NO +2H+=Fe3++NO↑+H2O +2H+=Fe3++NO↑+H2O |
| D.若用O2代替NaNO2,则每消耗112mL(标准状况)O2相当于节约了2.76gNaNO2 |
您最近一年使用:0次
2022-08-23更新
|
831次组卷
|
3卷引用:宁夏回族自治区石嘴山市第三中学2022-2023学年高三上学期第一次月考化学试题



