1 . 请回答:
(1)Na2O2的电子式___________ 。
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由___________ 。
(3)KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为
_______KClO3+_______HCl(浓)=_______KCl+_______ClO2↑+_______Cl2↑+_______
① 请配平上述化学方程式。___________
② 浓盐酸在反应中显示出来的性质是___________
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③若反应中生成标准状况下13.44L气体,则消耗还原剂的物质的量为___________ 。
④ClO2具有很强的氧化性,常用作消毒剂,其消毒的效率(以单位物质的量得到的电子数表示)是H2O2的___________ 倍。
(4)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为___________ 。
(1)Na2O2的电子式
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由
(3)KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为
_______KClO3+_______HCl(浓)=_______KCl+_______ClO2↑+_______Cl2↑+_______

① 请配平上述化学方程式。
② 浓盐酸在反应中显示出来的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③若反应中生成标准状况下13.44L气体,则消耗还原剂的物质的量为
④ClO2具有很强的氧化性,常用作消毒剂,其消毒的效率(以单位物质的量得到的电子数表示)是H2O2的
(4)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 物质之间的转化关系如图,部分生成物省略。A是由四种元素组成的化合物。C、D是由元素X、Y、Z中两种组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用。
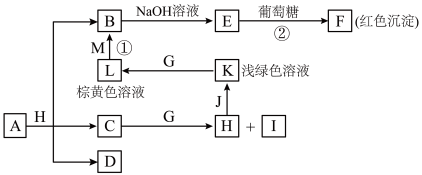
请回答下列问题:
(1)C的电子式____ 。
(2)写出反应①的离子反应方程式____ ,反应②中体现葡萄糖的____ 性。
(3)比较Y与Z的原子半径大小_____>_____(填写元素符号)。____
(4)写出A的化学式____ 。
(5)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体;请写出该反应的化学方程式____ 。
(6)研究表明:气体D在480℃、800大气压条件下可被活泼金属钠还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出该反应的化学方程式____ ,N的一种同素异形体的名称为____ 。

请回答下列问题:
(1)C的电子式
(2)写出反应①的离子反应方程式
(3)比较Y与Z的原子半径大小_____>_____(填写元素符号)。
(4)写出A的化学式
(5)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体;请写出该反应的化学方程式
(6)研究表明:气体D在480℃、800大气压条件下可被活泼金属钠还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出该反应的化学方程式
您最近一年使用:0次
2022-09-20更新
|
343次组卷
|
5卷引用:宁夏固原市第一中学2023届高三上学期第二次月考化学试题
名校
3 . 氧化还原反应在工业生产、环保及科研中有广泛的应用。氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50 ℃时反应可生成它。CuH具有的性质有:不稳定,易分解,在氯气中能燃烧;与稀盐酸反应能生成气体,Cu+在酸性条件下发生的反应是2Cu+=Cu2++Cu。
(1)写出CuH在氯气中燃烧的化学反应方程式:_______ 。
(2)CuH溶解在稀盐酸中反应的离子化学方程式是_______ 。
(3)如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:_______ 。
(1)写出CuH在氯气中燃烧的化学反应方程式:
(2)CuH溶解在稀盐酸中反应的离子化学方程式是
(3)如果把CuH溶解在足量的稀硝酸中生成的气体只有NO,请写出CuH溶解在足量稀硝酸中反应的离子方程式:
您最近一年使用:0次
名校
4 . 由软锰矿(主要成分为MnO2)制备KMnO4的实验流程可表示如下:
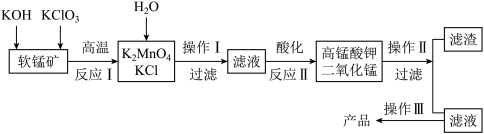
(1)实验时,首先将软锰矿研细,然后和KOH、 KClO3混合高温发生反应I,将软锰矿研细的目的是_______ 。
(2)反应I发生反应的化学方程式是_______ ,该反应中氧化剂是_______ ;反应II发生反应的离子方程式是_______ 。
(3)操作III的实验步骤为_______ 、_______ 、过滤;可循环利用的物质的化学式为_______ 。
(4)取制得的产品6.5g,配成250mL溶液;准确称取纯1.34gNa2C2O4配成适量溶液。用上述KMnO4溶液滴定Na2C2O4溶液,恰好反应(氧化产物为CO2,还原产物为Mn2+)时,消耗KMnO4溶液的体积为25.00mL。该KMnO4的纯度为_______ (保留小数点后一位)。

(1)实验时,首先将软锰矿研细,然后和KOH、 KClO3混合高温发生反应I,将软锰矿研细的目的是
(2)反应I发生反应的化学方程式是
(3)操作III的实验步骤为
(4)取制得的产品6.5g,配成250mL溶液;准确称取纯1.34gNa2C2O4配成适量溶液。用上述KMnO4溶液滴定Na2C2O4溶液,恰好反应(氧化产物为CO2,还原产物为Mn2+)时,消耗KMnO4溶液的体积为25.00mL。该KMnO4的纯度为
您最近一年使用:0次
名校
5 . 下列离子方程式中,不 正确的是
A.向NaHCO3溶液中加入过量的NaOH溶液: +OH-= +OH-= +H2O +H2O |
| B.稀硫酸中加入铁粉:2Fe+6H+=2Fe3++3H2↑ |
| C.FeBr2溶液中通入过量的Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
D.向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++ =3Fe3++NO↑+2H2O =3Fe3++NO↑+2H2O |
您最近一年使用:0次
2022-09-14更新
|
244次组卷
|
2卷引用:宁夏固原市第一中学2023届高三上学期第一次月考化学试题
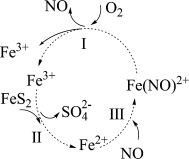
6 . 黄铁矿(主要成分为 )因其呈浅黄铜色,且具有明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。在酸性条件和催化剂的作用下
)因其呈浅黄铜色,且具有明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。在酸性条件和催化剂的作用下 可发生如图所示的转化。下列分析错误的是
可发生如图所示的转化。下列分析错误的是
 )因其呈浅黄铜色,且具有明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。在酸性条件和催化剂的作用下
)因其呈浅黄铜色,且具有明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。在酸性条件和催化剂的作用下 可发生如图所示的转化。下列分析错误的是
可发生如图所示的转化。下列分析错误的是 
| A.反应Ⅰ、Ⅱ为氧化还原反应 |
B.反应Ⅰ的离子方程式: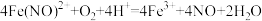 |
C.反应Ⅱ中,每消耗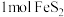 ,转移电子的物质的量为 ,转移电子的物质的量为 |
D.在酸性条件下,黄铁矿催化氧化中 和 和 均作催化剂 均作催化剂 |
您最近一年使用:0次
2022-04-20更新
|
368次组卷
|
5卷引用:宁夏固原市第一中学2023届高三上学期第二次月考化学试题
宁夏固原市第一中学2023届高三上学期第二次月考化学试题辽宁省沈阳市同泽高级中学2020--2021 学年高一下学期4月月考化学试卷(已下线)第03练 氧化还原反应-2023年高考化学一轮复习小题多维练(全国通用)宁夏青铜峡市宁朔中学2022-2023学年高三上学期期中考试化学试题江西省宜春市丰城市东煌学校2022-2023学年高三上学期期中考试化学试卷
名校
解题方法
7 . 下列解释有关实验现象的离子方程式错误的是
| 选项 | 实验操作 | 实验现象 | 离子方程式 |
| A | 大理石中加入足量醋酸溶液 | 大理石逐渐溶解 | CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
| B | 新制氯水中加过量氢氧化钠溶液 | 溶液由黄绿色变无色 | Cl2+2OH-=Cl-+ClO-+H2O |
| C | 酸性KMnO4溶液中加H2O2溶液 | 溶液紫色褪去,有气泡产生 | 2MnO +3H2O2+10H+=2Mn2++3O2↑+8H2O +3H2O2+10H+=2Mn2++3O2↑+8H2O |
| D | 将稀硫酸滴入淀粉-KI溶液中 | 在空气中放置一段时间后,溶液呈蓝色 | 4H++4I-+O2=2I2+2H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-10-10更新
|
537次组卷
|
8卷引用:宁夏回族自治区固原市第一中学2021届高三上学期第四次月考理综化学试题
名校
解题方法
8 . 羟胺( )是一种还原剂,能将某些氧化剂还原。现用25.00mL
)是一种还原剂,能将某些氧化剂还原。现用25.00mL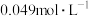 羟胺溶液与足量的硫酸铁溶液在煮沸条件下反应,生成的
羟胺溶液与足量的硫酸铁溶液在煮沸条件下反应,生成的 恰好与24.50mL
恰好与24.50mL '酸性
'酸性 溶液完全反应。已知:
溶液完全反应。已知: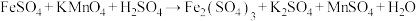 (未配平),则羟胺的氧化产物是
(未配平),则羟胺的氧化产物是
 )是一种还原剂,能将某些氧化剂还原。现用25.00mL
)是一种还原剂,能将某些氧化剂还原。现用25.00mL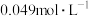 羟胺溶液与足量的硫酸铁溶液在煮沸条件下反应,生成的
羟胺溶液与足量的硫酸铁溶液在煮沸条件下反应,生成的 恰好与24.50mL
恰好与24.50mL '酸性
'酸性 溶液完全反应。已知:
溶液完全反应。已知: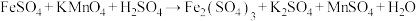 (未配平),则羟胺的氧化产物是
(未配平),则羟胺的氧化产物是A. | B. | C.NO | D. |
您最近一年使用:0次
2020-09-23更新
|
386次组卷
|
15卷引用:宁夏固原市第一中学2023届高三上学期第一次月考化学试题
宁夏固原市第一中学2023届高三上学期第一次月考化学试题(已下线)2014-2015浙江省宁波市效实中学高一上学期期中化学试卷2014-2015浙江省杭州市西湖中学高一12月月考化学试卷2018-2019学年人教版高中化学必修一模块综合测评题(A)2018-2019学年苏教版高中化学必修一 模块综合测评(A)【全国百强校】吉林省实验中学2019届高三上学期期中考试化学试题江西省上饶中学2019届高三上学期期中考试化学试题2020届高三化学二轮复习 氧化还原反应过关检测(强化训练)(已下线)【南昌新东方】莲塘一中化学高一10月份高一必修第一册(鲁科2019)考试帮 模块综合测评B卷福建师范大学第二附属中学2020届高三上学期期中考试化学试题(已下线)【苏州新东方】 江苏省吴江中学2021-2022学年高二上学期开学检测化学试卷辽宁省沈阳市第一二〇中学2021-2022学年高一上学期期中考试化学试题(已下线)第一章 化学物质及其变化 第5练 氧化还原反应的计算与方程式的配平(已下线)第5讲 氧化还原反应方程式的配平与计算
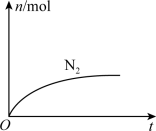
9 . 某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒。其中N2的物质的量随时间变化的曲线如图所示。下列判断正确的是

| A.该反应的还原剂是Cl- |
| B.消耗1 mol还原剂,转移6 mol电子 |
| C.氧化剂与还原剂的物质的量之比为2:3 |
| D.反应后溶液的酸性明显增强 |
您最近一年使用:0次
2020-06-16更新
|
651次组卷
|
36卷引用:宁夏固原市第一中学2023届高三上学期第一次月考化学试题
宁夏固原市第一中学2023届高三上学期第一次月考化学试题(已下线)2014届北京市朝阳区高三上学期期末考试化学试卷(已下线)2015届黑龙江省双鸭山市第一中学高三9月月考化学试卷(已下线)2015届黑龙江省双鸭山一中高三9月月考化学试卷2016届湖北省天门中学高三普通班8月月考化学试卷2016届陕西西安第一中学高三上学期期中考试化学试卷2016届浙江省嘉兴、杭州、宁波五校高三上第一次联考化学试卷2016届河南省三门峡市灵宝三中高三上第四次质检化学试卷2017届河北武邑中学高三上学期周考(8.14)化学试题2017届河北省石家庄市辛集中学高三上第一次阶段考试化学卷2017届甘肃省兰州一中高三上12月月考化学试卷福建省永安一中、德化一中、漳平一中2017-2018学年高一上学期第二次联考化学试题湖北省来风县实验中学2018届高三上学期11月月考试化学试题(已下线)二轮复习 专题3 氧化还原反应 押题专练【全国百强校】甘肃省会宁县第一中学2019届高三上学期第一次月考理科综合化学试题甘肃省武威市第十八中学2019届高三第一次月考化学试题四川省德阳市第五中学2018-2019学年高二上学期10月月考化学试题陕西省西安市长安区第五中学2019届高三上学期期中考试化学试题河北省衡水市衡水中学2019届高三上学期期中考试化学试题(已下线)2019高考备考二轮复习精品资料-专题3 氧化还原反应(押题专练)【市级联考】陕西省咸阳市2019届高三下学期第一次模拟考试化学试题福建省三明第一中学2020届高三上学期第二次月考化学试题2020届高三化学大二轮增分强化练——氧化还原反应夯基提能2020届高三化学选择题对题专练——氧化还原反应(强化练习)2020届高三化学总复习考点强化练习:物质及其变化(已下线)考点03 氧化还原反应-2020年高考化学命题预测与模拟试题分类精编陕西省榆林市绥德县绥德中学2019-2020学年高二下学期第二次阶段性测试化学试题高一必修第一册(鲁科2019)第2章第3节 氧化还原反应(已下线)湖南省湘潭县一中、双峰一中、邵东一中、永州四中2018-2019学年高一下学期优生联考化学试题江苏省宜兴第一中学2020-2021学年高一上学期期中考化学试题黑龙江省七台河市勃利县高级中学2021届高三上学期期中考试化学试题黑龙江省佳木斯市第一中学2021-2022学年高一上学期期中考试化学试题陕西省榆林市绥德中学2022-2023学年高二上学期第二次阶段性考试化学试题新疆实验中学2023-2024学年高一上学期10月月考化学试题浙江省瑞安中学2023-2024学年高一上学期12月月考化学试卷浙江省杭州学军中学2023-2024学年高一上学期期末模拟考试化学试卷
名校
10 . 在上海召开的第七届全球人类基因大会上,我国科学家第一次提出可以用砒霜(As2O3)来治疗早期幼粒白血病。
(1)完成并配平下列化学方程式:_____________
As2O3+ Zn+ H2SO4 → AsH3+ ZnSO4+ ______
(2)As2O3在上述反应中显示出来的性质是_____________ 。
A.氧化性 B.还原性 C.酸性 D.碱性
(3)若生成0.1 mol AsH3,则转移电子的物质的量为___________ mol。
(1)完成并配平下列化学方程式:
As2O3+ Zn+ H2SO4 → AsH3+ ZnSO4+ ______
(2)As2O3在上述反应中显示出来的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(3)若生成0.1 mol AsH3,则转移电子的物质的量为
您最近一年使用:0次
2018-12-11更新
|
125次组卷
|
4卷引用:宁夏固原市隆德县2020-2021学年高一上学期期末考试化学试题
宁夏固原市隆德县2020-2021学年高一上学期期末考试化学试题(已下线)2010年福建省厦门市杏南中学高三上学期10月月考化学卷福建省惠安惠南中学2019届高三上学期期中考试化学试题【全国百强校】山东省泰安市第一中学2019届高三上学期12月学情诊断化学试题



