13-14高一下·全国·课时练习
解题方法
1 . 铝热反应不仅用于焊接钢轨,而且还常用于冶炼熔点较高的金属如钒、铬、锰等。
请配平下列用铝热反应冶炼金属钒和钴的化学方程式,指出哪些物质是还原剂、哪些物质是氧化剂,并计算生成1 mol各种金属分别需要纯铝的质量。
V2O5+Al——Al2O3+V Co3O4+Al——Al2O3+Co
请配平下列用铝热反应冶炼金属钒和钴的化学方程式,指出哪些物质是还原剂、哪些物质是氧化剂,并计算生成1 mol各种金属分别需要纯铝的质量。
V2O5+Al——Al2O3+V Co3O4+Al——Al2O3+Co
您最近半年使用:0次
2016-12-09更新
|
1817次组卷
|
10卷引用:2014年高一下学期化学必修2 4-1-1 开发金属和海水资源练习卷
(已下线)2014年高一下学期化学必修2 4-1-1 开发金属和海水资源练习卷人教版高中化学必修2第四章《化学与自然资源的开发利用》测试卷1人教版高中化学必修二第四单元《化学与自然资源的开发利用》测试卷人教版高中化学必修二第四章《化学与自然资源的开发利用》测试卷2020年春季高中化学人教版必修2第四章《化学与自然资源的开发利用》测试卷2019-2020人教版高中化学必修2第四章《化学与自然资源开发利用》测试卷人教版高中化学必修2第四章《化学与自然资源的开发利用》测试卷22020年人教版高中化学必修2第四章《化学与自然资源开发利用》测试卷2020年人教版高中化学必修2第四章《化学与自然资源的开发利用》测试卷2020年春季人教版高中化学必修2第四章《化学与自然资源的开发利用》测试卷
10-11高一下·安徽宿州·阶段练习
名校
2 . 氮化硅(Si3N4)是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定,工业上普遍采用高纯硅与纯氮在1300℃反应获得。
(1)根据性质,推测氮化硅陶瓷的用途是______ 。
A.制汽轮机叶片 B.制有色玻璃 C.制永久性模具 D.制造柴油机
(2)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,它不与其他无机酸反应。试推测该陶瓷被氢氟酸腐蚀的化学方程式为______ 。
(3)现用四氯化硅和氮气在氢气中加强热发生反应,可制得高纯度氮化硅,反应的化学方程式为______ 。
(1)根据性质,推测氮化硅陶瓷的用途是
A.制汽轮机叶片 B.制有色玻璃 C.制永久性模具 D.制造柴油机
(2)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,它不与其他无机酸反应。试推测该陶瓷被氢氟酸腐蚀的化学方程式为
(3)现用四氯化硅和氮气在氢气中加强热发生反应,可制得高纯度氮化硅,反应的化学方程式为
您最近半年使用:0次
9-10高一下·浙江金华·期末
名校
解题方法
3 . 化学反应SO2 + H2O + HNO3 — H2SO4 + NO经配平后,还原剂的化学计量数为
| A.1 | B.2 | C.3 | D.4 |
您最近半年使用:0次
2016-12-09更新
|
524次组卷
|
5卷引用:09-10年金华市普通高中高一下学期期末考试化学卷
(已下线)09-10年金华市普通高中高一下学期期末考试化学卷(已下线)2011-2012学年浙江省宁波市高一下学期期末考试化学试卷(已下线)2014-2015河北保定某重点中学同步作业(必修1苏教版)4.2.3硝酸的性质四川省广安市武胜烈面中学校2021-2022学年高一下学期入学考试化学试题 新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高一上学期10月第一次月考化学试卷
12-13高一上·重庆·期末
4 . 某一反应体系中,有反应物和生成物共六种物质,这六种物质是:Cl2、KMnO4、MnCl2、H2O、HCl(浓)、KCl,其中KMnO4→ MnCl2。
(1)该反应中的化学方程式为_____________________________________________ 。
(2)该反应中,氧化产物与还原产物的物质的量之比为_____________________________ 。
(3)若产生的气体在标准状况下体积为2.24 L,则反应过程中被氧化的物质为________ NA(NA表示阿伏加德罗常数的值)。
(4)市售的浓盐酸(密度为1.19g/cm3)在工业上是用500 L HCl气体(标准状况)与1 L H2O的比例配制成的,则该盐酸的物质的量浓度是___________ mol/L(结果保留一位小数)。
(5)现需用1.20 mol/L的稀盐酸480 mL, 应量取市售浓盐酸________ mL进行配制。
(6)取6.00 g硬铝合金(假设只含铝铜硅),与 (5) 中所配稀盐酸进行充分反应,收集到气体5.60 L(标准状况),则硬铝合金中铝的质量分数为____________ 。
(1)该反应中的化学方程式为
(2)该反应中,氧化产物与还原产物的物质的量之比为
(3)若产生的气体在标准状况下体积为2.24 L,则反应过程中被氧化的物质为
(4)市售的浓盐酸(密度为1.19g/cm3)在工业上是用500 L HCl气体(标准状况)与1 L H2O的比例配制成的,则该盐酸的物质的量浓度是
(5)现需用1.20 mol/L的稀盐酸480 mL, 应量取市售浓盐酸
(6)取6.00 g硬铝合金(假设只含铝铜硅),与 (5) 中所配稀盐酸进行充分反应,收集到气体5.60 L(标准状况),则硬铝合金中铝的质量分数为
您最近半年使用:0次
11-12高三上·河北唐山·期中
名校
解题方法
5 . 前一时期“非典型肺炎”在我国部分地区流行,严重危害广大人民的身体健康,做好环境消毒是预防“非典型肺炎”的重要措施,常用的消毒剂是ClO2或Cl2等的稀溶液,其中ClO2溶液的消毒效果较好。已知ClO2常温下呈气态,其分子构型与水分子的分子构型相似,在自然环境中ClO2最终变为Cl-。下列有关说法中正确的是
| A.ClO2的分子结构呈V形,属非极性分子 |
| B.ClO2中氯元素显+4价,具有很强的氧化性,其消毒效率(以单位体积得电子的数目表示)是Cl2的5倍 |
| C.ClO2、Cl2的稀溶液用于环境消毒,具有广谱高效的特点,对人畜无任何危害 |
| D.常用Na2SO3在H2SO4的酸性条件下,还原NaClO3来制ClO2,这一反应的化学方程式可表示为Na2SO3+2NaClO3+H2SO4=2Na2SO4+2ClO2↑+H2O |
您最近半年使用:0次
2016-12-09更新
|
1110次组卷
|
4卷引用:2012届河北省唐山一中高三上学期期中考试化学试卷
(已下线)2012届河北省唐山一中高三上学期期中考试化学试卷宁夏吴忠市高二人教版选修3第2章 分子结构与性质综合练习2云南省西双版纳州民族中学2017-2018学年高二6月份考试化学试题贵州省普定县一中2018-2019学年高二上学期期中考试化学试题
6 . J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。

(1)M的离子结构示意图为_____ ;元素T在周期表中位于第_____ 族。
(2)J和氢组成的化合物分子有6个原子,其结构简式为______ 。
(3)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为_____ 。
(4)L的最简单气态氢化物甲的水溶液显碱性。
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为______ 。
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是_______ (选填序号)。
(5)由J、R形成的液态化合物JR2 0.2mol在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ。 该反应的热化学方程式为________ 。

(1)M的离子结构示意图为
(2)J和氢组成的化合物分子有6个原子,其结构简式为
(3)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为
(4)L的最简单气态氢化物甲的水溶液显碱性。
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是
| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入H2的物质的量 | 加入甲的物质的量 |
| y | 甲的物质的量 | 平衡常数K | 甲的转化率 | 生成物物质的量总和 |
您最近半年使用:0次
2016-12-09更新
|
143次组卷
|
4卷引用:2010年高考化学试题分项专题六 物质结构和元素周期律
9-10高一·全国·单元测试
7 . 在空气中加热S粉和Fe粉的混合物,可观察到下列现象:
(1)有淡蓝色火焰,且生成刺激性气味的气体。
(2)混合粉末变红,放出热量,最后变成黑色固体。
(3)不时有火星从混合物中射出。
请分别写出以上三种情况发生反应的化学方程式:__________ 、__________ 、__________ 。
(1)有淡蓝色火焰,且生成刺激性气味的气体。
(2)混合粉末变红,放出热量,最后变成黑色固体。
(3)不时有火星从混合物中射出。
请分别写出以上三种情况发生反应的化学方程式:
您最近半年使用:0次
2016-12-09更新
|
1435次组卷
|
4卷引用:鲁版必修1第03章第3节 硫的转化
13-14高一·全国·课时练习
8 . 钛(Ti)因为具有神奇的性能越来越引起人们的关注。常温下,钛不和非金属、强酸反应;红热时,却可与常见的非金属单质反应。钛是航空、军工、电力等方面的必需原料。地壳中含钛矿石之一称金红石(TiO2)目前大规模生产钛的方法是:
第一步:金红石、碳粉混合,在高温条件下通入氯气制得TiCl4和一种可燃性气体。该反应的化学方程式是______ ,该反应的还原剂是______ 。
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)此反应的化学方程式是______ 。
(2)简述由上述所得产物中获取金属钛的步骤______ 。
第一步:金红石、碳粉混合,在高温条件下通入氯气制得TiCl4和一种可燃性气体。该反应的化学方程式是
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)此反应的化学方程式是
(2)简述由上述所得产物中获取金属钛的步骤
您最近半年使用:0次
10-11高一下·福建福州·阶段练习
解题方法
9 . 利用氧化还原反应原理配平
(1)__ NH3+___ O2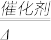
____ NO +____ H2O
(2)____ FeSO4+____ KNO3+____ H2SO4=____ K2SO4+____ Fe2(SO4)3+____ NO↑+____ H2O
(1)
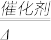
(2)
您最近半年使用:0次
9-10高一·全国·单元测试
10 . 古代的药金外观与金相似,常被误认为是金子,冶炼的方法如下:将碳酸锌、赤铜(Cu2O)、木炭混合加热到800℃,得到金光闪闪的“药金”.
(1)药金的主要成分是______________________________________________________ .
(2)冶炼时发生反应的化学方程式为___________________________________________ .
(1)药金的主要成分是
(2)冶炼时发生反应的化学方程式为
您最近半年使用:0次
2010-03-23更新
|
1158次组卷
|
6卷引用:新课标高一化学第三节 用途广泛的金属材料练习
(已下线)新课标高一化学第三节 用途广泛的金属材料练习(已下线)2010~2011学年辽宁省瓦房店市高级中学高一下学期期末考试人教版2017-2018学年高一化学必修1:3.3 用途广泛的金属材料 同步测试2(已下线)【走进新高考】(人教版必修一)3.3用途广泛的金属材料 同步练习01(已下线)5.1.2 金属的性质(第二课时)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)课时2 氧化剂和还原剂



