名校
1 . SO2、NOx为常见的空气污染物,会引起酸雨、光化学烟雾等污染问题。为消除燃煤烟气中含有的SO2、NO,研究者以NaClO溶液作为吸收剂进行一体化“脱硫”“脱硝”。控制溶液的pH=5.5,一定时间内,温度对SO2、NO脱除率的影响如图所示:

已知烟气中SO2与NO的体积比为4:1,且吸收后转化为: 、
、 。下列说法正确的是
。下列说法正确的是

已知烟气中SO2与NO的体积比为4:1,且吸收后转化为:
 、
、 。下列说法正确的是
。下列说法正确的是| A.SO2和NO均为酸性氧化物 |
| B.温度越高,“脱硫”“脱硝”效率越高 |
C.SO2在吸收过程中,反应的离子方程式是: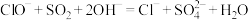 |
D.50℃时,吸收液中烟气转化生成的Cl-和 的物质的量之比13:2 的物质的量之比13:2 |
您最近一年使用:0次
名校
解题方法
2 . 利用硫铁矿烧渣(主要成分为 和
和 等)制备
等)制备 的工艺流程如图所示:
的工艺流程如图所示:
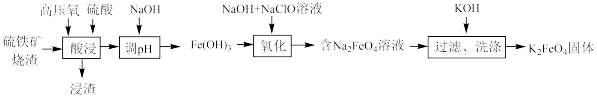
下列说法错误的是
A.“酸浸”时,充入高压氧的目的是增大溶解氧的量,使 充分被氧化 充分被氧化 |
B.浸渣的主要成分为硅酸,若酸浸时不进行过滤,其将会导致 产品纯度降低 产品纯度降低 |
C.“氧化”时,发生反应的离子方程式为 |
D.根据流程可知 的溶解度小于 的溶解度小于 ,洗涤 ,洗涤 固体时可选择 固体时可选择 溶液 溶液 |
您最近一年使用:0次
2024-02-26更新
|
357次组卷
|
3卷引用:湖南省岳阳市岳阳县第一中学2023-2024学年高一下学期3月月考化学试题
名校
3 . 将 和空气的混合气体通入
和空气的混合气体通入 、
、 和
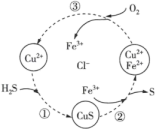
和 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法错误的是
的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法错误的是
 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法错误的是
的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法错误的是
A.回收S的总反应为 |
B.过程②中,发生的反应为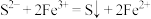 |
C.过程③中,标准状况下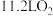 参加反应转移2mol电子 参加反应转移2mol电子 |
D.整个转化过程中 可以循环使用 可以循环使用 |
您最近一年使用:0次
2023-12-23更新
|
96次组卷
|
2卷引用:湖南省岳阳市湘阴县知源高级中学等多校2023-2024学年高一上学期12月月考化学试题
名校
4 . 含氯物质在日常生活中具有许多重要用途,回答下列问题:
(1)亚氯酸钠( )较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的两种产物可能为___________。
)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的两种产物可能为___________。
(2)我国用 替代氯气进行消毒,工业上常利用反应
替代氯气进行消毒,工业上常利用反应 制备
制备 ,用单线桥法表示反应中电子得失的方向和数目:
,用单线桥法表示反应中电子得失的方向和数目:___________ 。将该反应化学方程式改写为离子方程式:___________ 。
(3)工业上可利用 制备亚氯酸钠(
制备亚氯酸钠( ),反应体系中涉及下列6种物质:
),反应体系中涉及下列6种物质: 、
、 、
、 、NaOH、
、NaOH、 、
、 ,写出反应的化学方程式:
,写出反应的化学方程式:___________ 。
(4)某温度下降 通入KOH溶液里,反应后得到KCl、KClO、
通入KOH溶液里,反应后得到KCl、KClO、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为11:1,则
的个数之比为11:1,则 与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为___________ 。
(5)实验室用下列方法均可制取氯气
① ③
③
② ②
②
③ ④
④
若各反应转移的电子数相同,①②③生成的氯气质量比为___________ 。
(1)亚氯酸钠(
 )较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的两种产物可能为___________。
)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的两种产物可能为___________。A.NaCl、 | B.NaCl、NaClO |
C. 、 、 | D.NaCl、 |
 替代氯气进行消毒,工业上常利用反应
替代氯气进行消毒,工业上常利用反应 制备
制备 ,用单线桥法表示反应中电子得失的方向和数目:
,用单线桥法表示反应中电子得失的方向和数目:(3)工业上可利用
 制备亚氯酸钠(
制备亚氯酸钠( ),反应体系中涉及下列6种物质:
),反应体系中涉及下列6种物质: 、
、 、
、 、NaOH、
、NaOH、 、
、 ,写出反应的化学方程式:
,写出反应的化学方程式:(4)某温度下降
 通入KOH溶液里,反应后得到KCl、KClO、
通入KOH溶液里,反应后得到KCl、KClO、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为11:1,则
的个数之比为11:1,则 与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为(5)实验室用下列方法均可制取氯气
①
 ③
③②
 ②
②③
 ④
④若各反应转移的电子数相同,①②③生成的氯气质量比为
您最近一年使用:0次
名校
解题方法
5 . 重铬酸钾( )在实验室和工业中都有很广泛的应用,用于制铬矾、火柴、铬颜料、鞣革、电镀、有机合成等。以铬铁矿(主要成分可表示为
)在实验室和工业中都有很广泛的应用,用于制铬矾、火柴、铬颜料、鞣革、电镀、有机合成等。以铬铁矿(主要成分可表示为 ,还含杂质
,还含杂质 )为原料制备重铬酸钾晶体(不含结晶水)的工艺流程如图所示:
)为原料制备重铬酸钾晶体(不含结晶水)的工艺流程如图所示:
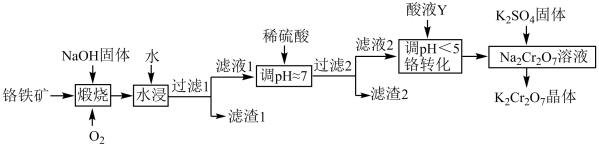
回答下列问题:
(1)基态Cr原子的未成对电子数为_______ 。二氧化硅比二氧化碳熔点高得多的最主要原因是_______ 。
(2)煅烧铬铁矿后生成 和
和 等,已知
等,已知 遇水强烈水解,生成红褐色沉淀,
遇水强烈水解,生成红褐色沉淀, 水解的离子方程式为
水解的离子方程式为_______ ;滤液1中的阴离子主要有 、
、_______ 。
(3)流程中若省去 这一操作,产品中可能含有的杂质是
这一操作,产品中可能含有的杂质是_______ 。
(4)结合离子方程式,从化学平衡移动的角度分析加入酸液Y的作用:_______ 。
(5)由于 是一种有毒且有致癌性的强氧化剂,它被国际癌症研究机构划归为第一类致癌物质。排出的含
是一种有毒且有致癌性的强氧化剂,它被国际癌症研究机构划归为第一类致癌物质。排出的含 酸性废水需要进行处理,可用焦亚硫酸钠(
酸性废水需要进行处理,可用焦亚硫酸钠( )将
)将 转化为毒性较低的
转化为毒性较低的 ,室温下再调节溶液的pH,生成
,室温下再调节溶液的pH,生成 沉淀,分离出污泥,保证废水中
沉淀,分离出污泥,保证废水中 的质量浓度小于
的质量浓度小于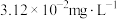 。已知室温下,
。已知室温下,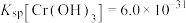 。
。
① 参加反应的离子方程式为
参加反应的离子方程式为_______ 。
②溶液的pH至少要大于_______ 。
 )在实验室和工业中都有很广泛的应用,用于制铬矾、火柴、铬颜料、鞣革、电镀、有机合成等。以铬铁矿(主要成分可表示为
)在实验室和工业中都有很广泛的应用,用于制铬矾、火柴、铬颜料、鞣革、电镀、有机合成等。以铬铁矿(主要成分可表示为 ,还含杂质
,还含杂质 )为原料制备重铬酸钾晶体(不含结晶水)的工艺流程如图所示:
)为原料制备重铬酸钾晶体(不含结晶水)的工艺流程如图所示:
回答下列问题:
(1)基态Cr原子的未成对电子数为
(2)煅烧铬铁矿后生成
 和
和 等,已知
等,已知 遇水强烈水解,生成红褐色沉淀,
遇水强烈水解,生成红褐色沉淀, 水解的离子方程式为
水解的离子方程式为 、
、(3)流程中若省去
 这一操作,产品中可能含有的杂质是
这一操作,产品中可能含有的杂质是(4)结合离子方程式,从化学平衡移动的角度分析加入酸液Y的作用:
(5)由于
 是一种有毒且有致癌性的强氧化剂,它被国际癌症研究机构划归为第一类致癌物质。排出的含
是一种有毒且有致癌性的强氧化剂,它被国际癌症研究机构划归为第一类致癌物质。排出的含 酸性废水需要进行处理,可用焦亚硫酸钠(
酸性废水需要进行处理,可用焦亚硫酸钠( )将
)将 转化为毒性较低的
转化为毒性较低的 ,室温下再调节溶液的pH,生成
,室温下再调节溶液的pH,生成 沉淀,分离出污泥,保证废水中
沉淀,分离出污泥,保证废水中 的质量浓度小于
的质量浓度小于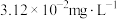 。已知室温下,
。已知室温下,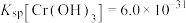 。
。①
 参加反应的离子方程式为
参加反应的离子方程式为②溶液的pH至少要大于
您最近一年使用:0次
2023-02-17更新
|
354次组卷
|
4卷引用:湖南省岳阳市第一中学2023届高三下学期第七次月考化学试题
湖南省岳阳市第一中学2023届高三下学期第七次月考化学试题湖南省名校联盟2022-2023学年高三下学期2月联考化学试题(已下线)云南师范大学附属中学2023-2024学年高三上学期开学考试化学试题云南师范大学附属中学2023-2024学年高三上学期开学考试化学试题
名校
解题方法
6 . 下列化学反应的离子方程式书写正确的是
A.海水提溴中用 的水溶液富集溴: 的水溶液富集溴: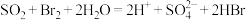 |
B. 溶液和 溶液和 溶液等体积、等浓度混合: 溶液等体积、等浓度混合: |
C.向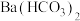 溶液中滴加 溶液中滴加 溶液至恰好沉淀完全: 溶液至恰好沉淀完全: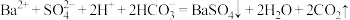 |
D.少量 与 与 溶液反应: 溶液反应: |
您最近一年使用:0次
2023-02-14更新
|
411次组卷
|
4卷引用:湖南省岳阳市第一中学2023届高三下学期第七次月考化学试题
湖南省岳阳市第一中学2023届高三下学期第七次月考化学试题湖南省湘潭市第一中学2023届高三下学期入学考试化学试题(已下线)安徽省、云南省、吉林省、黑龙江省2023届高三2月适应性测试变式题(选择题7-10)(已下线)河北省石家庄市2023届高中毕业年级教学质量检测(一模)变式题(选择题1-5)
名校
7 . 硫酸镍一般用于电镀印染媒染剂、金属着色剂等。电镀污泥中主要含有 、
、 、
、 、
、 、
、 和
和 等化合物。一种从电镀污泥中回收金属铜和制备硫酸镍的工艺流程如图1,回答下列问题:
等化合物。一种从电镀污泥中回收金属铜和制备硫酸镍的工艺流程如图1,回答下列问题:

已知:①焙烧时 和
和 ,分别转化为
,分别转化为 、
、 。
。
②几种金属离子开始沉淀和沉淀完全的 如表:
如表:
(1)镍具有优良的物理和化学特性。羰基法提纯粗镍涉及反应:
 。已知
。已知 (忽略
(忽略 、
、 随温度的变化),当
随温度的变化),当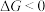 时,反应可以自发进行。若要提高反应中
时,反应可以自发进行。若要提高反应中 的产率且使反应自发进行,采取的反应条件为_______。
的产率且使反应自发进行,采取的反应条件为_______。
(2)“焙烧”时, 参与反应的化学方程式为
参与反应的化学方程式为_______ 。
(3)“滤液”的主要成分是含有少量重金属阳离子的 溶液,除杂装置如图2所示,
溶液,除杂装置如图2所示,
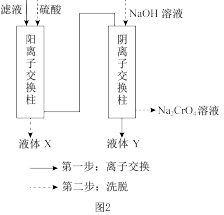
离子交换柱原理为: ;
;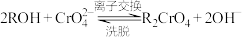
液体X的溶质主要是_______ (填化学式),液体Y是_______ (填名称)。
(4)“沉铁”时_______ (填“能”或“不能”)一并除去含铝杂质,理由是_______ 。
(5)下列金属的冶炼原理与本工艺流程中制Cu的方法相似的是_______(填标号)。
 、
、 、
、 、
、 、
、 和
和 等化合物。一种从电镀污泥中回收金属铜和制备硫酸镍的工艺流程如图1,回答下列问题:
等化合物。一种从电镀污泥中回收金属铜和制备硫酸镍的工艺流程如图1,回答下列问题:
已知:①焙烧时
 和
和 ,分别转化为
,分别转化为 、
、 。
。②几种金属离子开始沉淀和沉淀完全的
 如表:
如表:| 金属离子 |  |  |  |  |
开始沉淀的 | 1.1 | 4.1 | 6.7 | 4.2 |
完全沉淀的 | 3.2 | 5.4 | 9.5 | 6.7 |

 。已知
。已知 (忽略
(忽略 、
、 随温度的变化),当
随温度的变化),当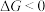 时,反应可以自发进行。若要提高反应中
时,反应可以自发进行。若要提高反应中 的产率且使反应自发进行,采取的反应条件为_______。
的产率且使反应自发进行,采取的反应条件为_______。| A.高温高压 | B.低温高压 | C.低温低压 | D.高温低压 |
 参与反应的化学方程式为
参与反应的化学方程式为(3)“滤液”的主要成分是含有少量重金属阳离子的
 溶液,除杂装置如图2所示,
溶液,除杂装置如图2所示,
离子交换柱原理为:
 ;
;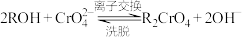
液体X的溶质主要是
(4)“沉铁”时
(5)下列金属的冶炼原理与本工艺流程中制Cu的方法相似的是_______(填标号)。
| A.加热氧化银制银 | B.四氯化钛中加镁冶炼钛 |
| C.焙烧辰砂(HgS)制汞 | D.电解硫酸锰制锰 |
您最近一年使用:0次
2022-12-12更新
|
122次组卷
|
2卷引用:湖南省岳阳市第一中学等3校2022-2023学年高二上学期12月月考化学试题
名校
8 . 我国科研人员通过控制光沉积的方法构建 型复合材料光催化剂,其中
型复合材料光催化剂,其中 和
和 离子渗透Nafion膜可协同
离子渗透Nafion膜可协同 、
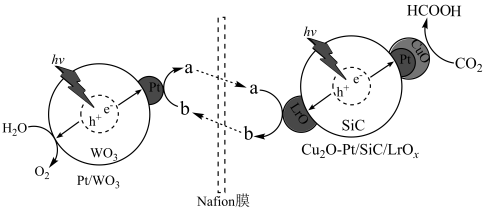
、 分别反应,构建了一个人工光合作用体系,其反应机理如图,下列说法
分别反应,构建了一个人工光合作用体系,其反应机理如图,下列说法错误 的是
 型复合材料光催化剂,其中
型复合材料光催化剂,其中 和
和 离子渗透Nafion膜可协同
离子渗透Nafion膜可协同 、
、 分别反应,构建了一个人工光合作用体系,其反应机理如图,下列说法
分别反应,构建了一个人工光合作用体系,其反应机理如图,下列说法
A.图中a、b分别代表 、 、 |
| B.该反应能量转化形式为光能→化学能 |
C.该反应为 |
D.转化 的路径中, 的路径中, 被氧化为 被氧化为 |
您最近一年使用:0次
2022-12-12更新
|
79次组卷
|
2卷引用:湖南省岳阳市第一中学等3校2022-2023学年高二上学期12月月考化学试题
解题方法
9 .  是重要的化工原料,易溶于水,难溶于乙醇,在中性或碱性溶液中稳定存在,在酸性溶液中易生成S和
是重要的化工原料,易溶于水,难溶于乙醇,在中性或碱性溶液中稳定存在,在酸性溶液中易生成S和 。工业上用硫化碱法制备
。工业上用硫化碱法制备 的反应方程式为:
的反应方程式为: ,实验室用此法制备
,实验室用此法制备 的装置如图所示:
的装置如图所示:

请回答下列问题:
(1)仪器a的名称为_______ 。
(2) 的制备:①先组装好仪器,然后检验装置的气密性,将所需药品加入各仪器装置;打开
的制备:①先组装好仪器,然后检验装置的气密性,将所需药品加入各仪器装置;打开  ,关闭
,关闭 ,调节
,调节 使硫酸缓缓滴下,导管口有气泡冒出,pH计读数逐渐减小,当pH计读数接近7时,必须立即打开
使硫酸缓缓滴下,导管口有气泡冒出,pH计读数逐渐减小,当pH计读数接近7时,必须立即打开  ,关闭
,关闭 、
、 ,原因是
,原因是 _______ ;②将装置C中所得溶液经一系列操作,最后洗涤、干燥,得到 样品。洗涤时为尽可能避免产品损失应选用的试剂是
样品。洗涤时为尽可能避免产品损失应选用的试剂是 _______ 。
a.水 b.乙醇 c.氢氧化钠溶液 d.稀盐酸
制备 的上述装置的明显不足是
的上述装置的明显不足是 _______ 。
(3) 样品纯度的测定:称取
样品纯度的测定:称取 样品,配制成200mL溶液;在锥形瓶中加入
样品,配制成200mL溶液;在锥形瓶中加入

 溶液和过量的酸性KI溶液,再滴入几滴淀粉溶液,立即用所配
溶液和过量的酸性KI溶液,再滴入几滴淀粉溶液,立即用所配  溶液滴定,当
溶液滴定,当 _______ 时达到滴定终点,测得消耗 溶液的体积为
溶液的体积为  ,则样品中硫代硫酸钠的质量分数为
,则样品中硫代硫酸钠的质量分数为 _______  。
。 已知:
已知: 的相对分子质量为158 , 相关反应:
的相对分子质量为158 , 相关反应: ;
; 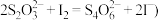
(4) 的应用:其溶液可除去漂白的织物及纸浆中残留的氯气,硫代硫酸钠被氧化成
的应用:其溶液可除去漂白的织物及纸浆中残留的氯气,硫代硫酸钠被氧化成 ,反应的离子方程式为
,反应的离子方程式为_______ 。
 是重要的化工原料,易溶于水,难溶于乙醇,在中性或碱性溶液中稳定存在,在酸性溶液中易生成S和
是重要的化工原料,易溶于水,难溶于乙醇,在中性或碱性溶液中稳定存在,在酸性溶液中易生成S和 。工业上用硫化碱法制备
。工业上用硫化碱法制备 的反应方程式为:
的反应方程式为: ,实验室用此法制备
,实验室用此法制备 的装置如图所示:
的装置如图所示:
请回答下列问题:
(1)仪器a的名称为
(2)
 的制备:①先组装好仪器,然后检验装置的气密性,将所需药品加入各仪器装置;打开
的制备:①先组装好仪器,然后检验装置的气密性,将所需药品加入各仪器装置;打开  ,关闭
,关闭 ,调节
,调节 使硫酸缓缓滴下,导管口有气泡冒出,pH计读数逐渐减小,当pH计读数接近7时,必须立即打开
使硫酸缓缓滴下,导管口有气泡冒出,pH计读数逐渐减小,当pH计读数接近7时,必须立即打开  ,关闭
,关闭 、
、 ,原因是
,原因是  样品。洗涤时为尽可能避免产品损失应选用的试剂是
样品。洗涤时为尽可能避免产品损失应选用的试剂是 a.水 b.乙醇 c.氢氧化钠溶液 d.稀盐酸
制备
 的上述装置的明显不足是
的上述装置的明显不足是 (3)
 样品纯度的测定:称取
样品纯度的测定:称取 样品,配制成200mL溶液;在锥形瓶中加入
样品,配制成200mL溶液;在锥形瓶中加入

 溶液和过量的酸性KI溶液,再滴入几滴淀粉溶液,立即用所配
溶液和过量的酸性KI溶液,再滴入几滴淀粉溶液,立即用所配  溶液滴定,当
溶液滴定,当  溶液的体积为
溶液的体积为  ,则样品中硫代硫酸钠的质量分数为
,则样品中硫代硫酸钠的质量分数为  。
。 已知:
已知: 的相对分子质量为158 , 相关反应:
的相对分子质量为158 , 相关反应: ;
; 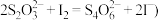
(4)
 的应用:其溶液可除去漂白的织物及纸浆中残留的氯气,硫代硫酸钠被氧化成
的应用:其溶液可除去漂白的织物及纸浆中残留的氯气,硫代硫酸钠被氧化成 ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次
解题方法
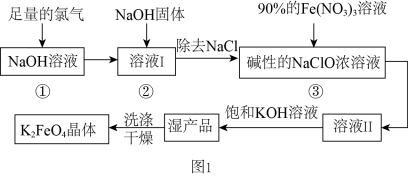
10 . 高铁酸钾( )为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定,是一种新型多功能水处理剂。其生产工艺如图1所示,下列说法正确的是
)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定,是一种新型多功能水处理剂。其生产工艺如图1所示,下列说法正确的是
 )为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定,是一种新型多功能水处理剂。其生产工艺如图1所示,下列说法正确的是
)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定,是一种新型多功能水处理剂。其生产工艺如图1所示,下列说法正确的是
| A.反应①应在较高温度下进行,升高温度加快反应速率 |
B.在溶液Ⅰ中加入NaOH固体可与过量的 继续反应,生成更多的NaClO 继续反应,生成更多的NaClO |
C.反应③的离子方程式为: |
| D.该工艺流程中可循环使用的物质是NaOH |
您最近一年使用:0次



