1 . “细菌冶金”是利用某些细菌的特殊代谢功能开采金属矿石,例如溶液中氧化亚铁硫杆菌能利用空气中的氧气将黄铁矿(主要成分FeS2,其中硫元素化合价为-1价)氧化为Fe2(SO4)3,并使溶液酸性增强(生成硫酸)。
①该过程反应的化学方程式为________________________ 。
②人们可利用Fe2(SO4)3作强氧化剂溶解铜矿石(Cu2S),然后加入铁屑进一步得到铜,该过程中发生的离子反应方程式如下,请补充完整并配平:
_____ Cu2S+___ Fe3++____ H2O
___ Cu2++____ Fe2++____ ( ) +____ SO42-
①该过程反应的化学方程式为
②人们可利用Fe2(SO4)3作强氧化剂溶解铜矿石(Cu2S),然后加入铁屑进一步得到铜,该过程中发生的离子反应方程式如下,请补充完整并配平:

您最近一年使用:0次
11-12高二上·广东·阶段练习
2 . 铁单质及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为:3FeS2+8O2 6SO2+Fe3O4,3 mol FeS2参加反应转移
6SO2+Fe3O4,3 mol FeS2参加反应转移___________ mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式______________ 。
从腐蚀废液回收得到金属铜还需要的试剂为_______________________________ 。
(3)与明矾相似,硫酸铁也可用作絮凝剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是_________________________________ 。
(4)下表中,对陈述I、II的正确性及其有无因果关系的判断都正确的是________ 。(填字母)
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为:3FeS2+8O2
 6SO2+Fe3O4,3 mol FeS2参加反应转移
6SO2+Fe3O4,3 mol FeS2参加反应转移(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式
从腐蚀废液回收得到金属铜还需要的试剂为
(3)与明矾相似,硫酸铁也可用作絮凝剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是
(4)下表中,对陈述I、II的正确性及其有无因果关系的判断都正确的是
| 选项 | 陈述I | 陈述II | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | I对;II对;有 |
| B | 常温下铁与稀硫酸反应生成氢气 | 高温下氢气能还原氧化铁生成铁 | I对;II对;无 |
| C | 铁属于过渡金属元素 | 铁和铁的某些化合物可以用作催化剂 | I错;II对;无 |
| D | 铁在空气中表面生成致密氧化膜 | 可用铁罐储存运输浓硫酸、浓硝酸 | I对;II对;有 |
您最近一年使用:0次
11-12高三上·广东中山·阶段练习
解题方法
3 . (1)胃舒平主要成分是氢氧化铝,同时含有三硅酸镁(Mg2Si3O8.nH2O)等化合物。三硅酸镁的氧化物形式为_______ ,某元素与铝元素同周期且原子半径比镁原子半径大,该元素离子半径比铝离子半径_______ (填“大”或“小”),该元素与铝元素的最高价氧化物的水化物之间发生反应的离子方程式为:_______
(2) Al2O3、MgO和SiO2都可以制耐火材料,其原因是_______ 。
a.Al2O3、MgO和SiO2都不溶于水 b.Al2O3、MgO和SiO2都是白色固体
c.Al2O3、MgO和SiO2都是氧化物 d.Al2O3、MgO和SiO2都有很高的熔点
(3)向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。
完成下列填空:
①写出并配平CCl4层由紫色变成无色的化学反应方程式(如果系数是1,要填写):_______

②)向盛有KI溶液滴加氯水的整个过程中的还原剂是_______ 。
③把KI换成KBr,则CCl4层变为红棕色,继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是_______ 。
④加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)1000kg,若将KI与Cl2反应制KIO3,至少需要消耗Cl2_______ L(标准状况,保留2位小数)。
(2) Al2O3、MgO和SiO2都可以制耐火材料,其原因是
a.Al2O3、MgO和SiO2都不溶于水 b.Al2O3、MgO和SiO2都是白色固体
c.Al2O3、MgO和SiO2都是氧化物 d.Al2O3、MgO和SiO2都有很高的熔点
(3)向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。
完成下列填空:
①写出并配平CCl4层由紫色变成无色的化学反应方程式(如果系数是1,要填写):

②)向盛有KI溶液滴加氯水的整个过程中的还原剂是
③把KI换成KBr,则CCl4层变为红棕色,继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是
④加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)1000kg,若将KI与Cl2反应制KIO3,至少需要消耗Cl2
您最近一年使用:0次
10-11高三上·广东深圳·阶段练习
4 . 硫铁矿烧渣(主要成分为 Fe2O3、Fe3O4、FeO、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用硫铁矿烧渣制备铁红等产品的实验流程如下:
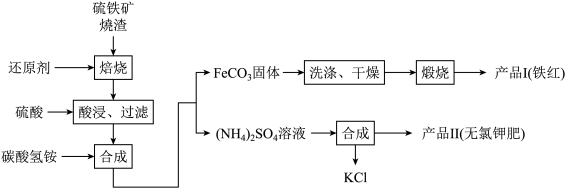
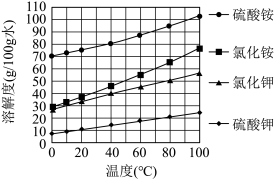
已知几种盐的溶解度随温度变化的曲线如右图所示:
回答下列问题:
(1)酸浸、过滤后滤液中的金属阳离子是________________ 。
(2)煅烧FeCO3生成产品 I的化学反应方程式为_______ 。
实验室进行煅烧操作所需仪器除了酒精喷灯、泥三角、三脚架、玻璃棒外,还有__________ 。
(3)产品Ⅱ的化学式为_______________ ,为了获得产品Ⅱ,向(NH4)2SO4溶液中加入KCl溶液后,还需要进行的操作是:________ 。
(4)检验产品Ⅱ中是否含有氯化物杂质的实验操作是:取少量产品Ⅱ于试管中配成溶液,________________________________ 。

已知几种盐的溶解度随温度变化的曲线如右图所示:

回答下列问题:
(1)酸浸、过滤后滤液中的金属阳离子是
(2)煅烧FeCO3生成产品 I的化学反应方程式为
实验室进行煅烧操作所需仪器除了酒精喷灯、泥三角、三脚架、玻璃棒外,还有
(3)产品Ⅱ的化学式为
(4)检验产品Ⅱ中是否含有氯化物杂质的实验操作是:取少量产品Ⅱ于试管中配成溶液,
您最近一年使用:0次
10-11高三上·广东深圳·阶段练习
5 . xR2++yH++O2 mR3++nH2O中,对m和R2+、R3+判断正确的是
| A.m = 4,R2+是氧化剂 | B.2m = y,R3+是氧化产物 |
| C.m = 4,R2+是还原剂 | D.m = y/2,R3+是还原产物 |
您最近一年使用:0次
10-11高三上·广东广州·阶段练习
6 . 氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
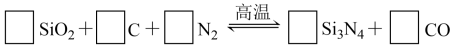
(1)配平上述反应的化学方程式(将化学计量数填在方框内);_____ SiO2+_____ C+_____ N2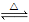
_____ Si3O4+_____ CO
(2)该反应的氧化剂是_________ ,其还原产物是_________ ;
(3)该反应产生标准状况下11.2升CO气体,则电子转移________ 摩尔。
(4)若有1摩尔焦炭与足量的SiO2、氮气反应,电子转移______ (填大于、等于或小于)2摩尔,理由是__________________________ 。
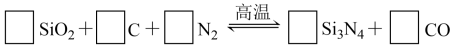
(1)配平上述反应的化学方程式(将化学计量数填在方框内);

(2)该反应的氧化剂是
(3)该反应产生标准状况下11.2升CO气体,则电子转移
(4)若有1摩尔焦炭与足量的SiO2、氮气反应,电子转移
您最近一年使用:0次
解题方法
7 . 某工业废玻璃粉末含SiO2、Fe2O3、CeO2、FeO等。某课题小组设计如下工艺流程对资源进行回收,得到Ce(OH)4和硫酸铁铵矾。
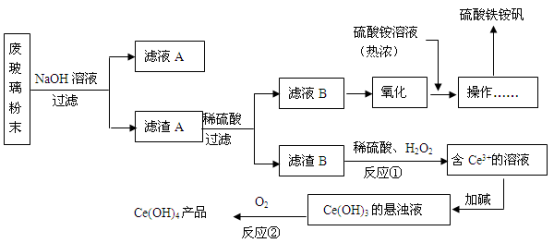
已知:CeO2不溶于稀硫酸;酸性条件下,Ce3+易水解,Ce4+有较强氧化性。
(1)硫酸铁铵矾可净水,其原理是(写离子方程式)________________________________ 。
(2)滤液A的主要成分_______________ (填写化学式)。
(3)反应①的离子方程式是_____________________________ 。
(4)反应②的化学反应方程式是__________________________ 。
(5)已知制硫酸铁铵矾晶体[Fe2(SO4) 3·(NH4) 2SO4·24H2O,式量964]的产率为80%,若加入13.2g (NH4) 2SO4(式量132),可制得晶体的质量是_________ 。
(6)化合物HT可作为萃取剂能将铈离子从水溶液中萃取出来,过程表示为:
Ce2(SO4)3(水层)+ 6HT(有机层) 2CeT3 (有机层)+3H2SO4(水层)
2CeT3 (有机层)+3H2SO4(水层)
分液得到CeT3(有机层),再加入H2SO4 获得较纯的含Ce3+的水溶液。可选择硫酸作反萃取剂的原因是___ (从平衡移动角度回答)。

已知:CeO2不溶于稀硫酸;酸性条件下,Ce3+易水解,Ce4+有较强氧化性。
(1)硫酸铁铵矾可净水,其原理是(写离子方程式)
(2)滤液A的主要成分
(3)反应①的离子方程式是
(4)反应②的化学反应方程式是
(5)已知制硫酸铁铵矾晶体[Fe2(SO4) 3·(NH4) 2SO4·24H2O,式量964]的产率为80%,若加入13.2g (NH4) 2SO4(式量132),可制得晶体的质量是
(6)化合物HT可作为萃取剂能将铈离子从水溶液中萃取出来,过程表示为:
Ce2(SO4)3(水层)+ 6HT(有机层)
 2CeT3 (有机层)+3H2SO4(水层)
2CeT3 (有机层)+3H2SO4(水层)分液得到CeT3(有机层),再加入H2SO4 获得较纯的含Ce3+的水溶液。可选择硫酸作反萃取剂的原因是
您最近一年使用:0次
2016-12-08更新
|
583次组卷
|
4卷引用:2015届广东省湛江市高三普通高考测试(二)理综化学试卷
2015届广东省湛江市高三普通高考测试(二)理综化学试卷2015届广东湛江高三第二次模拟考试理综化学试卷2020届高三化学大二轮增分强化练—— 化学工艺流程题(已下线)专题七 工艺流程题(提分特训)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训
2013·安徽马鞍山·一模
名校
8 . 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂;其分子结构中如右图所示:.常温下,S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体,化学方程式为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl.下列说法中错误的是
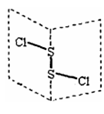

| A.S2Cl2的结构式为Cl-S-S-Cl |
| B.S2Cl2分子中既有有极性键又有非极性键 |
| C.反应中SO2是还原产物,S是氧化产物 |
| D.反应中,生成 1molSO2,转移电子为3mol |
您最近一年使用:0次
2016-04-20更新
|
918次组卷
|
11卷引用:广东省梅州市虎山中学、蕉岭中学、平远中学、宪梓中学四校2021-2022学年高二下学期5月联考化学试题
广东省梅州市虎山中学、蕉岭中学、平远中学、宪梓中学四校2021-2022学年高二下学期5月联考化学试题2016届湖南省衡阳市第八中学高三上学期第一次月考化学试卷2016届广东省潮州市朝安区凤凰中学高三上学期期中化学试卷2015-2016学年湖北省宜昌一中高二下3月月考化学试卷2015-2016学年甘肃天水一中高一下第一次月考化学试卷2017届湖南省衡阳八中高三上学期9月月考化学试卷湖南省邵东县第一中学2017届高三上学期第三次月考化学试题福建省龙岩市武平县第一中学2021届高三上学期10月月考化学试题(已下线)2013届安徽省马鞍山市高中毕业班第一次教学质量检测理综化学试卷2016届江西省吉安一中高三上学期期中测试化学试卷(已下线)练习15分子的结构与物质的性质-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)
10-11高三上·江西九江·阶段练习
名校
9 . 储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应中的反应物和生成物有C、CO2、H2SO4、K2Cr2O7、K2SO4、Cr2(SO4)3和H2O七种。
(1)请用上述物质填空(不用配平):C+________ +H2SO4——________ +______ +Cr2(SO4)3+H2O。
(2)上述反应中氧化剂是(填化学式)________ ,被氧化的元素是(填元素符号)________ 。
(3)H2SO4在上述反应中表现出来的性质是(填选项序号)________ 。
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(4)若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为________ 。
(1)请用上述物质填空(不用配平):C+
(2)上述反应中氧化剂是(填化学式)
(3)H2SO4在上述反应中表现出来的性质是(填选项序号)
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(4)若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为
您最近一年使用:0次
10-11高三上·江苏无锡·期中
10 . 高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程。
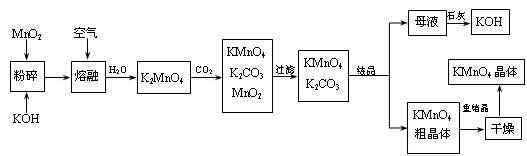
(1)KMnO4稀溶液是一种常用的消毒剂。其消毒机理与下列___ (填序号)物质相似。
A.75%酒精 B.双氧水 C.苯酚 D.84消毒液(NaClO溶液)
(2)写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
___________________________________________________________________ 。
(3)向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是:_______ 。
(4)上述流程中可以循环使用的物质有石灰、二氧化碳、___ 和___ (写化学式)。
(5)若不考虑物质循环与制备过程中的损失,则1 mol MnO2可制得_____ mol KMnO4。

(1)KMnO4稀溶液是一种常用的消毒剂。其消毒机理与下列
A.75%酒精 B.双氧水 C.苯酚 D.84消毒液(NaClO溶液)
(2)写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
(3)向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是:
(4)上述流程中可以循环使用的物质有石灰、二氧化碳、
(5)若不考虑物质循环与制备过程中的损失,则1 mol MnO2可制得
您最近一年使用:0次
2011-03-11更新
|
1160次组卷
|
7卷引用:2011届广东省电白一中高三下学期二轮复习综合测试(4)理综化学部分
(已下线)2011届广东省电白一中高三下学期二轮复习综合测试(4)理综化学部分安徽省庐巢七校联盟2020届高三第五次联考化学试题(已下线)2011届江苏省无锡一中高三上学期期中考试化学卷云南省大理州漾濞一中2020届高三上学期开学考试化学试题云南省大理白族自治州宾川县第三完全中学2019-2020学年高二上学期开学考试化学试题云南省绿春县二中2019-2020学年高一上学期期中考试化学试题贵州省黔南布依族苗族自治州瓮安第二中学2019-2020学年高三上学期期末考试化学试题



