1 . 铁是人类较早使用的金属之一,铁及其化合物在生产、生活中有重要的用途。运用所学知识回答下列问题。
(1) 的价层电子排布式为
的价层电子排布式为___________ 。
(2)实验室鉴别 胶体与饱和
胶体与饱和 溶液的方法是
溶液的方法是___________ 。
(3)工业上用黄铁矿制硫酸的第一步反应化学反应方程式为___________ 。
(4)电子工业用 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
①为检验 腐蚀铜后所得溶液中含有
腐蚀铜后所得溶液中含有 ,应使用的试剂为
,应使用的试剂为___________ 。
②欲从腐蚀后的废液中回收铜并重新获得 溶液循环利用,现有下列试剂:
溶液循环利用,现有下列试剂:
A.浓硝酸 B.铁粉 C.氯气 D.烧碱 E.浓氨水
需要用到的试剂除盐酸外还需要___________ (填字母)。
(5)高铁酸钠( )是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,
)是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么, 、
、 、
、 三种消毒杀菌剂的消毒效率最高的是
三种消毒杀菌剂的消毒效率最高的是___________ 。
(6)近年来, 作为制备锂离子电池正极材料
作为制备锂离子电池正极材料 的重要原料而成为研究热点。一种以
的重要原料而成为研究热点。一种以 、
、 、氨水为主要原料制备
、氨水为主要原料制备 ,并测定产物样品中铁元素的质量分数,主要步骤如下:
,并测定产物样品中铁元素的质量分数,主要步骤如下:
i.取 样品,加入过量盐酸充分溶解,再滴加
样品,加入过量盐酸充分溶解,再滴加 (还原剂)至溶液呈浅黄色;
(还原剂)至溶液呈浅黄色;
ii.加入 ,恰好将i中残余的少量
,恰好将i中残余的少量 还原为
还原为 ;
;
iii.用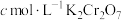 标准溶液滴定
标准溶液滴定 ,消耗
,消耗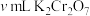 标准溶液。
标准溶液。
①步骤iii的离子方程式是:___________ 。
②产物中铁元素的质量分数为___________ 。
(1)
 的价层电子排布式为
的价层电子排布式为(2)实验室鉴别
 胶体与饱和
胶体与饱和 溶液的方法是
溶液的方法是(3)工业上用黄铁矿制硫酸的第一步反应化学反应方程式为
(4)电子工业用
 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。①为检验
 腐蚀铜后所得溶液中含有
腐蚀铜后所得溶液中含有 ,应使用的试剂为
,应使用的试剂为②欲从腐蚀后的废液中回收铜并重新获得
 溶液循环利用,现有下列试剂:
溶液循环利用,现有下列试剂:A.浓硝酸 B.铁粉 C.氯气 D.烧碱 E.浓氨水
需要用到的试剂除盐酸外还需要
(5)高铁酸钠(
 )是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么,
)是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么, 、
、 、
、 三种消毒杀菌剂的消毒效率最高的是
三种消毒杀菌剂的消毒效率最高的是(6)近年来,
 作为制备锂离子电池正极材料
作为制备锂离子电池正极材料 的重要原料而成为研究热点。一种以
的重要原料而成为研究热点。一种以 、
、 、氨水为主要原料制备
、氨水为主要原料制备 ,并测定产物样品中铁元素的质量分数,主要步骤如下:
,并测定产物样品中铁元素的质量分数,主要步骤如下:i.取
 样品,加入过量盐酸充分溶解,再滴加
样品,加入过量盐酸充分溶解,再滴加 (还原剂)至溶液呈浅黄色;
(还原剂)至溶液呈浅黄色;ii.加入
 ,恰好将i中残余的少量
,恰好将i中残余的少量 还原为
还原为 ;
;iii.用
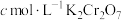 标准溶液滴定
标准溶液滴定 ,消耗
,消耗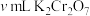 标准溶液。
标准溶液。①步骤iii的离子方程式是:
②产物中铁元素的质量分数为
您最近一年使用:0次
名校
解题方法
2 . 氧化还原反应在日常生活和工业生产中有重要应用。
I.K2Cr2O7是火柴工业用作制造火柴头的原料之一
已知反应:
(1)用“双线桥”标明该反应中电子转移的方向和数目。__________

(2)该反应中被氧化的元素是___________ ,还原产物是___________ 。
(3)该反应中氧化剂与还原剂的微粒个数比为___________ 。
Ⅱ.阅读下面一段材料并回答问题。
【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化1L水投放5mgK2FeO4即可达到卫生标准
……
(4) K2FeO4中铁元素的化合价为___________ 。
(5)下列关于K2FeO4的说法中,不正确的是___________ 。
a.是强氧化性的盐 b.固体保存需要防潮
b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(6)工业制备K2FeO4需要在碱性环境下进行,现提供反应体系中7种物质,Fe(NO3)3、Cl2、H2O、KOH、K2FeO4、KCl、KNO3请写出制备K2FeO4的化学反应方程式___________ 。
(7)将K2FeO4与水反应的化学方程式补充完整并配平:____________
___________ +___________
+___________ =___________
=___________ (胶体)+___________+___________
(胶体)+___________+___________
该反应消耗1个K2FeO4时,转移的电子数为___________ 个
(8)消毒净化198L水,按照卫生标准投入K2FeO4,则K2FeO4与水充分反应后产生的KOH质量为___________ g。
I.K2Cr2O7是火柴工业用作制造火柴头的原料之一
已知反应:

(1)用“双线桥”标明该反应中电子转移的方向和数目。

(2)该反应中被氧化的元素是
(3)该反应中氧化剂与还原剂的微粒个数比为
Ⅱ.阅读下面一段材料并回答问题。
高铁酸钾使用说明书
【化学式】K2FeO4【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化1L水投放5mgK2FeO4即可达到卫生标准
……
(4) K2FeO4中铁元素的化合价为
(5)下列关于K2FeO4的说法中,不正确的是
a.是强氧化性的盐
 b.固体保存需要防潮
b.固体保存需要防潮c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(6)工业制备K2FeO4需要在碱性环境下进行,现提供反应体系中7种物质,Fe(NO3)3、Cl2、H2O、KOH、K2FeO4、KCl、KNO3请写出制备K2FeO4的化学反应方程式
(7)将K2FeO4与水反应的化学方程式补充完整并配平:
___________
 +___________
+___________ =___________
=___________ (胶体)+___________+___________
(胶体)+___________+___________
该反应消耗1个K2FeO4时,转移的电子数为
(8)消毒净化198L水,按照卫生标准投入K2FeO4,则K2FeO4与水充分反应后产生的KOH质量为
您最近一年使用:0次
名校
解题方法
3 . 软锰矿的主要成分是 ,还含有少量重金属化合物等杂质。黄铁矿的主要成分是
,还含有少量重金属化合物等杂质。黄铁矿的主要成分是 ,还含有Si、Al的氧化物等杂质。工业上采用同槽酸浸工艺制备
,还含有Si、Al的氧化物等杂质。工业上采用同槽酸浸工艺制备 并回收
并回收 ,其主要流程如下:
,其主要流程如下:
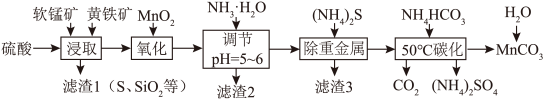
(1)为了提高锰元素的浸出率,在“浸取”时可以采取的措施有___________ (写两条)。
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,浸取时发生反应的离子方程式为___________ 。
(3)“氧化”过程中,反应消耗的氧化剂与还原剂的比为___________ ,还可使用___________ 代替 。
。
(4)滤渣2主要成分的化学式是___________ 。
(5)“50℃”碳化得到碳酸锰发生的化学反应方程式是___________ 。
(6)生成的碳酸锰产品需要充分洗涤,检验碳酸锰产品已完全洗净的方法是___________ 。
 ,还含有少量重金属化合物等杂质。黄铁矿的主要成分是
,还含有少量重金属化合物等杂质。黄铁矿的主要成分是 ,还含有Si、Al的氧化物等杂质。工业上采用同槽酸浸工艺制备
,还含有Si、Al的氧化物等杂质。工业上采用同槽酸浸工艺制备 并回收
并回收 ,其主要流程如下:
,其主要流程如下:
(1)为了提高锰元素的浸出率,在“浸取”时可以采取的措施有
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,浸取时发生反应的离子方程式为
(3)“氧化”过程中,反应消耗的氧化剂与还原剂的比为
 。
。(4)滤渣2主要成分的化学式是
(5)“50℃”碳化得到碳酸锰发生的化学反应方程式是
(6)生成的碳酸锰产品需要充分洗涤,检验碳酸锰产品已完全洗净的方法是
您最近一年使用:0次
2023-10-13更新
|
391次组卷
|
3卷引用:重庆市西南大学附属中学校高2023-2024学年高二上学期10月阶段性检测化学试题
名校
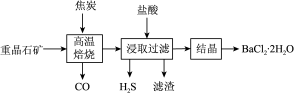
4 . 由重晶石矿(主要成分是 ,还含有
,还含有 等杂质)可制得氯化钡晶体,某兴趣小组设计实验流程如图。下列说法正确的是
等杂质)可制得氯化钡晶体,某兴趣小组设计实验流程如图。下列说法正确的是
 ,还含有
,还含有 等杂质)可制得氯化钡晶体,某兴趣小组设计实验流程如图。下列说法正确的是
等杂质)可制得氯化钡晶体,某兴趣小组设计实验流程如图。下列说法正确的是
A.浸取过滤操作中得到的滤渣主要成分为 |
B.“高温焙烧”时焦炭和 反应的化学方程式为: 反应的化学方程式为: |
| C.“高温焙烧”和“结晶”两处操作均需用到蒸发皿 |
| D.上述过程中可以用稀硫酸代替盐酸进行浸取 |
您最近一年使用:0次
名校
解题方法
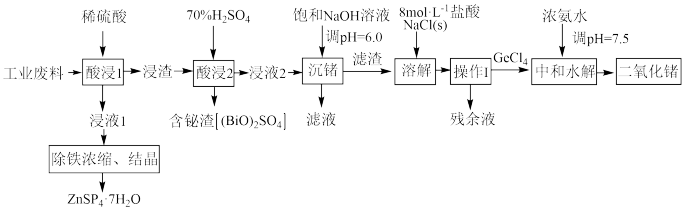
5 . 利用某冶锌工厂的工业废料[除ZnO和少量Fe2O3外,还含有铋(Bi)、锗(Ge)的氧化物]制取几种金属化合物的工业流程如图:
已知:①该工艺条件下,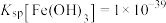 ,
, 。
。
② 的熔点为-49.5℃,沸点为84℃,其在水中或酸的稀溶液中易水解。
的熔点为-49.5℃,沸点为84℃,其在水中或酸的稀溶液中易水解。
请回答下列问题:
(1)基态锗原子的价层电子排布式为___________ 。
(2)“酸浸1”步骤中有利于提高浸取率的措施有___________ (答两点)。
(3)“浸液1”中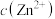 约为
约为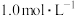 ,则除
,则除 时应控制pH的范围为
时应控制pH的范围为___________ (已知:当溶液中某离子浓度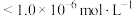 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。
(4)“酸浸2”时铋的氧化物( )发生反应的化学方程式为
)发生反应的化学方程式为___________ 。
(5)固态 为
为___________ 晶体,“操作Ⅰ”分离获得液态 所使用的装置为
所使用的装置为___________ (填标号)。
A. B.
B.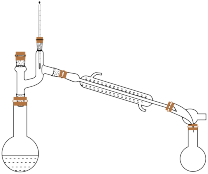 C.
C.
为了提高 的纯度,在所选装置的基础上进行改进,方法是
的纯度,在所选装置的基础上进行改进,方法是___________ 。
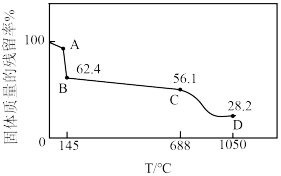
(6)隔绝空气加热 固体,固体质量的残留率与温度的关系如图所示。已知C→D的过程中产生两种气体,写出该过程的化学方程式
固体,固体质量的残留率与温度的关系如图所示。已知C→D的过程中产生两种气体,写出该过程的化学方程式___________ 。

已知:①该工艺条件下,
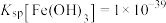 ,
, 。
。②
 的熔点为-49.5℃,沸点为84℃,其在水中或酸的稀溶液中易水解。
的熔点为-49.5℃,沸点为84℃,其在水中或酸的稀溶液中易水解。请回答下列问题:
(1)基态锗原子的价层电子排布式为
(2)“酸浸1”步骤中有利于提高浸取率的措施有
(3)“浸液1”中
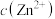 约为
约为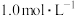 ,则除
,则除 时应控制pH的范围为
时应控制pH的范围为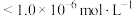 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。(4)“酸浸2”时铋的氧化物(
 )发生反应的化学方程式为
)发生反应的化学方程式为(5)固态
 为
为 所使用的装置为
所使用的装置为A.
 B.
B. C.
C.
为了提高
 的纯度,在所选装置的基础上进行改进,方法是
的纯度,在所选装置的基础上进行改进,方法是(6)隔绝空气加热
 固体,固体质量的残留率与温度的关系如图所示。已知C→D的过程中产生两种气体,写出该过程的化学方程式
固体,固体质量的残留率与温度的关系如图所示。已知C→D的过程中产生两种气体,写出该过程的化学方程式
您最近一年使用:0次
2023-10-13更新
|
283次组卷
|
2卷引用:重庆市2024届高三上学期第二次质量检测化学试题
名校
6 . DCCNa(二氯异氰尿酸钠)固体是一种高效、安全的消毒剂,20℃以上易溶于水。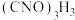 (异氰尿酸)为三元弱酸。
(异氰尿酸)为三元弱酸。
I.制备DCCA(二氯异氰尿酸)的装置如下图。其中发生的反应为:
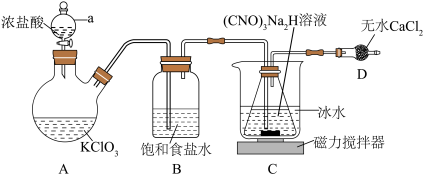
回答下列问题:
(1)仪器a的名称是___________ 。
(2)装置A中反应的离子方程式为___________ 。
(3)上面装置中存在一个明显的错误是___________ 。
II.制备DCCNa
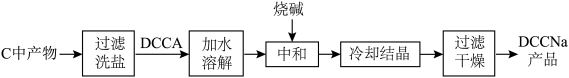
(4)步骤Ⅱ中“洗盐”操作中证明盐已经洗净的实验方案是___________ 。
(5)氯含量的测定:称取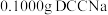 样品,加入一定量醋酸溶液溶解,样品中的氯元素全部转化成HClO,再加入足量的KI溶液,用淀粉作指示剂,用
样品,加入一定量醋酸溶液溶解,样品中的氯元素全部转化成HClO,再加入足量的KI溶液,用淀粉作指示剂,用 的
的 标准溶液进行滴定,消耗标准液
标准溶液进行滴定,消耗标准液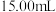 。已知:
。已知:
①滴定过程中,判断滴定终点的依据是___________ ;
②样品中氯元素的质量分数为___________ (精确到0.1%)。
(6)下列操作可能使氯元素的质量分数测定结果偏高的是___________ (填标号)。
A.滴定前滴定管未用标准液润洗
B.滴定前滴定管尖嘴无气泡,滴定后尖嘴有气泡
C.滴定后,滴定管尖嘴外还悬着一滴液体
D.锥形瓶盛放待测液前未干燥
E.读数时,滴定前仰视,滴定后俯视
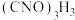 (异氰尿酸)为三元弱酸。
(异氰尿酸)为三元弱酸。I.制备DCCA(二氯异氰尿酸)的装置如下图。其中发生的反应为:


回答下列问题:
(1)仪器a的名称是
(2)装置A中反应的离子方程式为
(3)上面装置中存在一个明显的错误是
II.制备DCCNa
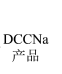

(4)步骤Ⅱ中“洗盐”操作中证明盐已经洗净的实验方案是
(5)氯含量的测定:称取
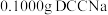 样品,加入一定量醋酸溶液溶解,样品中的氯元素全部转化成HClO,再加入足量的KI溶液,用淀粉作指示剂,用
样品,加入一定量醋酸溶液溶解,样品中的氯元素全部转化成HClO,再加入足量的KI溶液,用淀粉作指示剂,用 的
的 标准溶液进行滴定,消耗标准液
标准溶液进行滴定,消耗标准液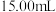 。已知:
。已知:
①滴定过程中,判断滴定终点的依据是
②样品中氯元素的质量分数为
(6)下列操作可能使氯元素的质量分数测定结果偏高的是
A.滴定前滴定管未用标准液润洗
B.滴定前滴定管尖嘴无气泡,滴定后尖嘴有气泡
C.滴定后,滴定管尖嘴外还悬着一滴液体
D.锥形瓶盛放待测液前未干燥
E.读数时,滴定前仰视,滴定后俯视
您最近一年使用:0次
解题方法
7 . I.某研究性学习小组进行SO2的制备及性质探究实验,装置如图(a为活塞,加热及固定装置已略去)。
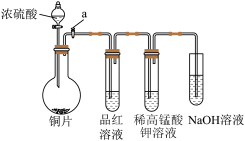
(1)连接仪器、___________ 、加药品后,打开a,然后滴入浓硫酸,加热。
(2)铜与浓硫酸反应制备SO2的化学方程式为___________ 。
(3)实验过程中依次体现SO2的性质为___________ ,若反应的 为20mL,0.6mol/L,则至少反应中消耗铜
为20mL,0.6mol/L,则至少反应中消耗铜___________ g。
Ⅱ.上述实验中NaOH溶液用于吸收剩余的SO2生成,是抗氧剂。向烧碱和的混合溶液中加入少许溴水,振荡后溶液变为无色。
(4)写出在碱性溶液中 氧化
氧化 的离子方程式:
的离子方程式:___________ 。
(5)反应后的溶液中含有 、
、 、
、 、
、 等阴离子,
等阴离子,请选择最佳试剂 ,填写鉴定其中 和
和 的实验报告。
的实验报告。
限选试剂: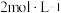 盐酸;
盐酸;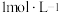
 溶液;
溶液;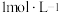
 溶液;
溶液;
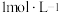
 溶液;
溶液;
 溶液;
溶液; ;新制氯水。
;新制氯水。

(1)连接仪器、
(2)铜与浓硫酸反应制备SO2的化学方程式为
(3)实验过程中依次体现SO2的性质为
 为20mL,0.6mol/L,则至少反应中消耗铜
为20mL,0.6mol/L,则至少反应中消耗铜Ⅱ.上述实验中NaOH溶液用于吸收剩余的SO2生成,是抗氧剂。向烧碱和的混合溶液中加入少许溴水,振荡后溶液变为无色。
(4)写出在碱性溶液中
 氧化
氧化 的离子方程式:
的离子方程式:(5)反应后的溶液中含有
 、
、 、
、 、
、 等阴离子,
等阴离子, 和
和 的实验报告。
的实验报告。限选试剂:
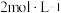 盐酸;
盐酸;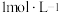
 溶液;
溶液;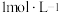
 溶液;
溶液;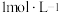
 溶液;
溶液;
 溶液;
溶液; ;新制氯水。
;新制氯水。| 编号 | 实验操作 | 预期现象和结论 |
| 步骤i | 取少量待测液加入试管中,加入过量的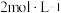 盐酸,再滴加① 盐酸,再滴加① | 有② |
| 步骤ii | 取出步骤i中适量上层清液于试管中,加入适量氯水,再加入③ | 下层液体呈④ |
您最近一年使用:0次
解题方法
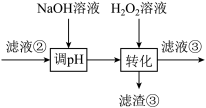
8 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(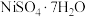 ):
):
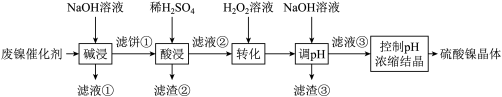
常温溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是___________ 。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式___________ 。
(2)“滤液②”中含有的金属离子可能是___________ 。
(3)“转化”中可替代 的物质是
的物质是___________ 。若工艺流程改为先“调pH”后“转化”,即“滤液③”中可能含有的杂质离子为___________ 。
(4)将废镍催化剂a克按流程制成硫酸镍晶体,(镍元素损失10%)并溶于水中配成250ml溶液,取其中25ml于锥形瓶,加入足量的氯化钡溶液充分反应,产生b克沉淀,则废镍催化剂中镍元素的质量分数为___________ (用a、b列式表示)。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍锅电池正极材料的NiOOH。写出该反应的离子方程式___________ 。
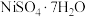 ):
):
常温溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离 |  |  |  |  |
开始沉淀时( )的pH )的pH | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时(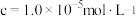 )的pH )的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”中NaOH的两个作用分别是
(2)“滤液②”中含有的金属离子可能是
(3)“转化”中可替代
 的物质是
的物质是
(4)将废镍催化剂a克按流程制成硫酸镍晶体,(镍元素损失10%)并溶于水中配成250ml溶液,取其中25ml于锥形瓶,加入足量的氯化钡溶液充分反应,产生b克沉淀,则废镍催化剂中镍元素的质量分数为
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍锅电池正极材料的NiOOH。写出该反应的离子方程式
您最近一年使用:0次
名校
9 . 下列方程式正确的是
A. 和稀 和稀 反应: 反应: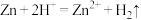 |
B. 与 与 反应: 反应: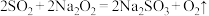 |
C.使用 作电极电解 作电极电解 溶液: 溶液: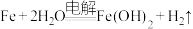 |
D.向 溶液中滴加少量 溶液中滴加少量 溶液: 溶液: |
您最近一年使用:0次
名校
解题方法
10 . 三氯化铬(CrCl3) 是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。某化学小组用 Cr2O3和 CCl4(沸点76.8℃) 在高温下制备无水 CrCl3,实验装置如图所示:

回答下列问题:
(1)装置E中仪器甲的名称是___________ ,实验装置合理的连接顺序为 A→___________ (填装置字母标号,可重复使用)。
(2)装置A中发生反应的离子方程式为___________ ,实验开始后,应先加热装置___________ (填“A” 或“B” )。
(3)装置B中生成由三种元素组成的平面三角形分子,有毒且易水解,写出装置D 中发生反应的化学方程式:___________ 。
(4)从安全的角度考虑,该实验装置的不足之处是___________ 。
(5)由CrCl3溶液制备纯净的 Cr(OH)3的实验方案:取适量 CrCl3溶液,加入 NaOH 溶液调节pH 充分反应后过滤,用蒸馏水洗涤沉淀,___________ ,则证明沉淀已洗涤干净;低温烘干沉淀,得到 Cr(OH)3晶体。
(6)取三氯化铬样品9.00g,配制成250mL 溶液,移取 25.00mL 加热至沸腾后,加适量NaOH溶液,生成沉淀0.515g,则样品中无水三氯化铬的质量分数为___________ (结果保留三位有效数字)。
(7)铬、钙、氧可形成一种具有特殊导电性的复合氧化物,其晶胞结构如图 甲所示。

①请在图乙中画出该晶胞沿z轴方向的投影图___________ [已知: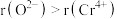 ]。
]。
②氧离子与钙离子的最近距离为 a pm,阿伏加德罗常数为NA,则该复合氧化物晶体的密度为___________ 


回答下列问题:
(1)装置E中仪器甲的名称是
(2)装置A中发生反应的离子方程式为
(3)装置B中生成由三种元素组成的平面三角形分子,有毒且易水解,写出装置D 中发生反应的化学方程式:
(4)从安全的角度考虑,该实验装置的不足之处是
(5)由CrCl3溶液制备纯净的 Cr(OH)3的实验方案:取适量 CrCl3溶液,加入 NaOH 溶液调节pH 充分反应后过滤,用蒸馏水洗涤沉淀,
(6)取三氯化铬样品9.00g,配制成250mL 溶液,移取 25.00mL 加热至沸腾后,加适量NaOH溶液,生成沉淀0.515g,则样品中无水三氯化铬的质量分数为
(7)铬、钙、氧可形成一种具有特殊导电性的复合氧化物,其晶胞结构如图 甲所示。

①请在图乙中画出该晶胞沿z轴方向的投影图
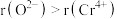 ]。
]。②氧离子与钙离子的最近距离为 a pm,阿伏加德罗常数为NA,则该复合氧化物晶体的密度为


您最近一年使用:0次



