名校
解题方法
1 . 铬是人体必需的微量元素,对维持人体正常的生理功能有着重要的作用。铬是胰岛素不可缺少的辅助成分,它参与糖代谢过程,能够促进脂肪和蛋白质的合成,对于人体的生长发育起着积极的促进作用。虽然铬对维护人体健康有着十分重要的作用,但食用不当也会带来很大的危害。由于无机铬很不容易被人体所吸收,铬只有以有机化合物的形式进入人体内才能被吸收。而在铬的化合物中,六价铬具有很强的毒性,尤以铬酸盐和重铬酸盐的毒性最为突出。
(1)铬原子的基态电子排布式为_______ 。
(2)氯化铬酰(CrO2Cl2)常温下为暗红色液体,熔点-96.5℃、沸点117℃,能与丙酮(CH3COCH3)、CCl4、CS2等互溶。
①丙酮中碳原子采取的杂化方式为_______ ;
②CS2属于_______ (填极性”或“非极性”)分子,其电子式为_______ ;
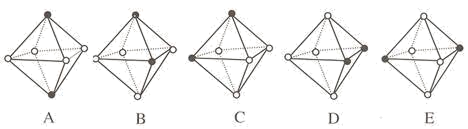
(3)CrCl3·6H2O(相对分子质量为266.5)有多种不同颜色的异构体(均是配合物,配位数为6)。为测定蒸发CrCl3溶液析出的暗绿色晶体是哪种异构体,取2.665gCrCl3·6H2O配成溶液,滴加足量AgNO3溶液,得到沉淀1.435g。该异构体为_______ (填化学式)。下列是暗绿色晶体配离子的空间结构(中心原子位于正八面体的中心,已省去),其中B与_______ 具有完全相同的结构。(填字母)
(4)六价铬的化合物有剧毒,所以要对Cr(VI)(罗马数字表示元素的化合价,下同)废水进行化学处理,使其转化为毒性较低的Cr(III)。最常见的是铁氧磁体法,即把FeSO4·7H2O加入含Cr(VI)的废水中,在pH<4时,Fe2+将Cr(VI)还原为Cr(III),调节溶液pH达8~10,使溶液中的Fe(II)、Fe(III)、Cr(III)析出组成相当于Fe(II)[Fex(III)·Cr2-x(III)]O4(磁性材料铁氧体的组成)沉淀。试回答:
①若废水中六价铬以Cr2O 存在。试写出在酸性条件下硫酸亚铁还原Cr2O
存在。试写出在酸性条件下硫酸亚铁还原Cr2O 的离子方程式并配平
的离子方程式并配平_______ 。
②根据上述结果可确定铁氧磁体中x=_______ 。
(1)铬原子的基态电子排布式为
(2)氯化铬酰(CrO2Cl2)常温下为暗红色液体,熔点-96.5℃、沸点117℃,能与丙酮(CH3COCH3)、CCl4、CS2等互溶。
①丙酮中碳原子采取的杂化方式为
②CS2属于
(3)CrCl3·6H2O(相对分子质量为266.5)有多种不同颜色的异构体(均是配合物,配位数为6)。为测定蒸发CrCl3溶液析出的暗绿色晶体是哪种异构体,取2.665gCrCl3·6H2O配成溶液,滴加足量AgNO3溶液,得到沉淀1.435g。该异构体为

(4)六价铬的化合物有剧毒,所以要对Cr(VI)(罗马数字表示元素的化合价,下同)废水进行化学处理,使其转化为毒性较低的Cr(III)。最常见的是铁氧磁体法,即把FeSO4·7H2O加入含Cr(VI)的废水中,在pH<4时,Fe2+将Cr(VI)还原为Cr(III),调节溶液pH达8~10,使溶液中的Fe(II)、Fe(III)、Cr(III)析出组成相当于Fe(II)[Fex(III)·Cr2-x(III)]O4(磁性材料铁氧体的组成)沉淀。试回答:
①若废水中六价铬以Cr2O
 存在。试写出在酸性条件下硫酸亚铁还原Cr2O
存在。试写出在酸性条件下硫酸亚铁还原Cr2O 的离子方程式并配平
的离子方程式并配平②根据上述结果可确定铁氧磁体中x=
您最近一年使用:0次
2021-01-09更新
|
381次组卷
|
2卷引用:辽宁省五校2021届高三上学期期末联考化学试题
2 . 磷酸亚铁锂是锂离子电池中常用的正极材料, (磷酸铁)是制备磷酸亚铁锂的前驱体。用磷铁渣(含Fe、FeP、
(磷酸铁)是制备磷酸亚铁锂的前驱体。用磷铁渣(含Fe、FeP、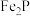 及
及 )制备
)制备 的工艺流程如下:
的工艺流程如下:
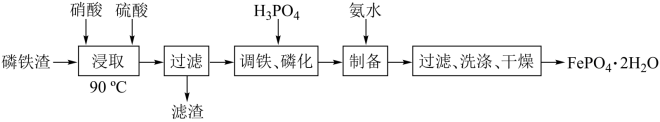
已知 溶于强酸。
溶于强酸。
(1)锂在元素周期表中的位置为___________ 。 的电离方程式为
的电离方程式为___________ 。
(2)“浸取”时,在密闭反应器中依次加入硝酸、硫酸,硝酸首先分解生成 和
和 ,
, 将铁和磷分别氧化为
将铁和磷分别氧化为 、
、 。
。
①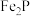 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
②加入硫酸的目的是___________ 。
(3)“制备”时发生反应的离子方程式为___________ ;上述流程制得的 中含有的杂质是
中含有的杂质是___________ 。
(4) 与
与 及C在高温条件下生成
及C在高温条件下生成 和等物质的量的
和等物质的量的 、CO,该反应中还原剂与氧化剂的物质的量之比为
、CO,该反应中还原剂与氧化剂的物质的量之比为___________ 。
 (磷酸铁)是制备磷酸亚铁锂的前驱体。用磷铁渣(含Fe、FeP、
(磷酸铁)是制备磷酸亚铁锂的前驱体。用磷铁渣(含Fe、FeP、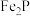 及
及 )制备
)制备 的工艺流程如下:
的工艺流程如下:
已知
 溶于强酸。
溶于强酸。(1)锂在元素周期表中的位置为
 的电离方程式为
的电离方程式为(2)“浸取”时,在密闭反应器中依次加入硝酸、硫酸,硝酸首先分解生成
 和
和 ,
, 将铁和磷分别氧化为
将铁和磷分别氧化为 、
、 。
。①
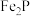 与
与 反应的化学方程式为
反应的化学方程式为②加入硫酸的目的是
(3)“制备”时发生反应的离子方程式为
 中含有的杂质是
中含有的杂质是(4)
 与
与 及C在高温条件下生成
及C在高温条件下生成 和等物质的量的
和等物质的量的 、CO,该反应中还原剂与氧化剂的物质的量之比为
、CO,该反应中还原剂与氧化剂的物质的量之比为
您最近一年使用:0次
解题方法
3 . 中国传统绘画颜料迄今已有七千多年的历史,如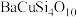 (中国蓝)、
(中国蓝)、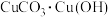 2(石绿),
2(石绿), (绛矾)、
(绛矾)、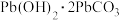 (铅白)等。下列说法错误的是
(铅白)等。下列说法错误的是
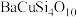 (中国蓝)、
(中国蓝)、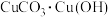 2(石绿),
2(石绿), (绛矾)、
(绛矾)、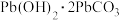 (铅白)等。下列说法错误的是
(铅白)等。下列说法错误的是A.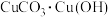 2难溶于水和强酸 2难溶于水和强酸 |
B.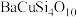 属于硅酸盐 属于硅酸盐 |
C.青矾 有“烧之赤色,故名绛矾矣”,该过程中发生了氧化还原反应 有“烧之赤色,故名绛矾矣”,该过程中发生了氧化还原反应 |
D. 修复发黑(PbS)的铅白绘画的原理为 修复发黑(PbS)的铅白绘画的原理为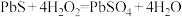 |
您最近一年使用:0次
2021-01-08更新
|
340次组卷
|
3卷引用:辽宁省辽阳市2021届高三上学期期末考试化学试题
名校
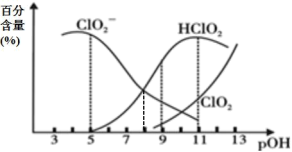
4 . 亚氯酸钠(NaClO2)在溶液中会生成ClO2、HClO2、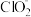 、Cl-等,其中HClO2和ClO2都具有漂白性。已知pOH=-lgc(OH-),经测定25℃时各组分百分含量随pOH变化情况如图所示(Cl-没有画出),则下列分析正确的是
、Cl-等,其中HClO2和ClO2都具有漂白性。已知pOH=-lgc(OH-),经测定25℃时各组分百分含量随pOH变化情况如图所示(Cl-没有画出),则下列分析正确的是
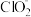 、Cl-等,其中HClO2和ClO2都具有漂白性。已知pOH=-lgc(OH-),经测定25℃时各组分百分含量随pOH变化情况如图所示(Cl-没有画出),则下列分析正确的是
、Cl-等,其中HClO2和ClO2都具有漂白性。已知pOH=-lgc(OH-),经测定25℃时各组分百分含量随pOH变化情况如图所示(Cl-没有画出),则下列分析正确的是
A.HClO2的电离平衡常数的数值Ka=1 10-8 10-8 |
B.pOH=11时,ClO 部分转化成ClO2和Cl-离子的方程式为:5ClO 部分转化成ClO2和Cl-离子的方程式为:5ClO +2H2O=4ClO2+Cl-+4OH- +2H2O=4ClO2+Cl-+4OH- |
| C.ClO2与SO2混合后,气体漂白纸浆效果更好 |
| D.同浓度HClO2溶液和NaClO2溶液等体积混合(不考虑ClO2和Cl-),则混合溶液中有:c(Na+)+c(OH-)=c(H+)+c(HClO2) |
您最近一年使用:0次
2021-01-05更新
|
832次组卷
|
4卷引用:辽宁省沈阳市第二中学2021-2022学年高二上学期期末考试化学试题
名校
解题方法
5 . 镍是一种常用的有机催化剂,且在电磁领域应用广泛。某工厂以含镍废料(主要含NiO、Fe2O3、FeO、Al2O3、SiO2、CaO)为原料制备镍单质的流程如图:
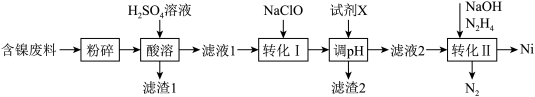
已知:ⅰ.Ni2+在弱酸性环境中易水解,氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度);
ⅱ.常温下,Ksp[Fe(OH)3]=4×10-38,Ksp[Fe(OH)2]=8×10-16,Ksp[Al(OH)3]=1×10-33,Ksp[Ni(OH)2]=2×10-15,离子浓度低于1×10-5 mol·L-1时,认为沉淀完全。
回答下列问题:
(1)“粉碎”的目的是___________ ;“滤渣1”的主要成分为___________ 、___________ 。
(2)“转化Ⅰ”的目的为___________ (用离子方程式表示)。
(3)为了更加环保,有人用H2O2代替NaClO进行“转化Ⅰ”,发现所用H2O2远远高于理论用量,分析造成这一结果的原因为___________ 。
(4)调pH的目的是沉淀溶液中的铁和铝,调节pH=5时,___________ (选填“能”或“不能”)达到目的,“试剂X”可以是___________ (填选项字母)。
A.FeO B.Fe2O3 C.NiO D.Al2O3
(5)N2H4的电子式为___________ ;“转化Ⅱ”中发生反应的离子方程式为___________ 。

已知:ⅰ.Ni2+在弱酸性环境中易水解,氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度);
ⅱ.常温下,Ksp[Fe(OH)3]=4×10-38,Ksp[Fe(OH)2]=8×10-16,Ksp[Al(OH)3]=1×10-33,Ksp[Ni(OH)2]=2×10-15,离子浓度低于1×10-5 mol·L-1时,认为沉淀完全。
回答下列问题:
(1)“粉碎”的目的是
(2)“转化Ⅰ”的目的为
(3)为了更加环保,有人用H2O2代替NaClO进行“转化Ⅰ”,发现所用H2O2远远高于理论用量,分析造成这一结果的原因为
(4)调pH的目的是沉淀溶液中的铁和铝,调节pH=5时,
A.FeO B.Fe2O3 C.NiO D.Al2O3
(5)N2H4的电子式为
您最近一年使用:0次
2020-12-24更新
|
284次组卷
|
2卷引用:辽宁省兴城市高级中学2022-2023学年高二上学期期末线上质量检测化学试题
6 . 二氧化氯(ClO2)是一种优良的消毒剂,可用氯酸钠和双氧水在酸性条件下制备,反应方程式为NaClO3H2O2H2SO4ClO2Na2SO4H2OO2(未配平)。下列说法不正确的是
| A.NaClO3做氧化剂,发生还原反应 |
| B.将该方程式配平后H2O的化学计量数应为2 |
| C.NaClO3与H2O2的化学计量系数之比为2:1 |
| D.反应过程中每生成2.24LO2转移0.2mol电子 |
您最近一年使用:0次
2020-11-10更新
|
857次组卷
|
7卷引用:辽宁省东北师范大学连山实验高中2022-2023学年高一上学期1月期末化学试题
辽宁省东北师范大学连山实验高中2022-2023学年高一上学期1月期末化学试题黑龙江省富锦市第一中学2022-2023学年高一上学期期末考试化学试题黑龙江省鹤岗市第一中学2022-2023学年高一上学期期末考试化学试题 湖南省长沙市长郡教育集团2020-2021学年高一上学期期中考试化学试题湖南省长沙市长郡中学2020-2021学年高一上学期期中考试化学试题(已下线)第二章 海水中的重要元素——钠和氯(A卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)黑龙江省鹤岗市第一中学2022-2023学年高一下学期开学考试化学试题
名校
7 . 铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)向沸水中逐滴滴加1mol·L-1FeCl3溶液至液体呈透明的红褐色,所得分散系中微粒直径的范围是______________ ,区别该液体和FeCl3溶液的方法是______________ 。
(2)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2 Fe3O4+6SO2,氧化产物为
Fe3O4+6SO2,氧化产物为________ ,若有3mol FeS2参加反应,转移________ mol电子。
(3)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有气体逸出,请配平该化学方程式:
___ FeSO4+____ KNO3+___ H2SO4═____ K2SO4+_____ Fe2(SO4)3+__ NO↑+_____ H2O。
(4)铁红是一种红色颜料,其成分是Fe2O3,将一定量的铁红溶于160mL 5mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L(标准状况)H2,经检测,溶液中无Fe3+,则参加反应的铁粉的质量为________ g。
(1)向沸水中逐滴滴加1mol·L-1FeCl3溶液至液体呈透明的红褐色,所得分散系中微粒直径的范围是
(2)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2
 Fe3O4+6SO2,氧化产物为
Fe3O4+6SO2,氧化产物为(3)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有气体逸出,请配平该化学方程式:
(4)铁红是一种红色颜料,其成分是Fe2O3,将一定量的铁红溶于160mL 5mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L(标准状况)H2,经检测,溶液中无Fe3+,则参加反应的铁粉的质量为
您最近一年使用:0次
2020-04-27更新
|
282次组卷
|
2卷引用:辽宁省丹东市2017-2018学年高一上学期期末质量监测化学试题
8 . 黄铁矿(FeS2)中-1价硫元素在酸性条件下可以与ClO3-发生反应,其离子方程式如下
_____ ClO3-+_____ FeS2+_____H+=_____ClO2↑+_____Fe3++_____ SO42-+_____H2O(未配平):下列说法正确的是
_____ ClO3-+_____ FeS2+_____H+=_____ClO2↑+_____Fe3++_____ SO42-+_____H2O(未配平):下列说法正确的是
| A. ClO3-是氧化剂,Fe3+是还原产物 |
| B. ClO3-的氧化性强于Fe3+ |
| C.生成l mol SO42-时,转移7mol 电子 |
| D.取反应后的溶液加KSCN溶液,可观察到有红色沉淀产生 |
您最近一年使用:0次
2020-02-20更新
|
569次组卷
|
3卷引用:辽宁师范大学附属中学2017-2018学年高一上学期期末考试化学试题
辽宁师范大学附属中学2017-2018学年高一上学期期末考试化学试题2020届高三化学化学二轮复习——高考常考题:氧化还原反应的规律:先后律、强弱律【精编选择25题】(已下线)考点05 氧化还原反应方程式的配平与计算(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
9 . 铁是应用最广泛的金属,铁的卤化物,氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)铁元素在周期表中的位置为_______ 。
(2)要确定铁的某氯化物FeClx的化学式,可利用离子交换和滴定的方法。实验中称取0.54 g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40 mol·L-1的盐酸滴定,滴至终点时消耗盐酸25.0 mL。则x=_____ 。
(3)实验室用铁氰化钾确定某铁的氯化物中是否含有FeCl2,该反应的离子方程式为_____ 。
(4)Fe(OH)3固体与氢碘酸反应时可生成棕色物质的离子方程式为________ 。
(5)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为_______ 。
(6)实验室准确称取1.44g草酸亚铁固体,在空气中灼烧,得到0.773g铁的氧化物,写出该铁的氧化物的化学式__________ 。
(1)铁元素在周期表中的位置为
(2)要确定铁的某氯化物FeClx的化学式,可利用离子交换和滴定的方法。实验中称取0.54 g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40 mol·L-1的盐酸滴定,滴至终点时消耗盐酸25.0 mL。则x=
(3)实验室用铁氰化钾确定某铁的氯化物中是否含有FeCl2,该反应的离子方程式为
(4)Fe(OH)3固体与氢碘酸反应时可生成棕色物质的离子方程式为
(5)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为
(6)实验室准确称取1.44g草酸亚铁固体,在空气中灼烧,得到0.773g铁的氧化物,写出该铁的氧化物的化学式
您最近一年使用:0次
名校
解题方法
10 . 硫元素的几种化合物存在下列转化关系:
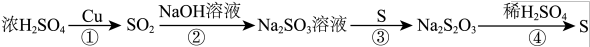
下列判断正确的是
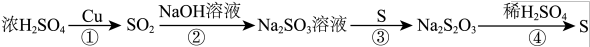
下列判断正确的是
| A.反应①中生成的SO2具有还原性,故可作漂白剂 |
| B.反应④中当消耗1mol稀硫酸时,电子转移为6mol |
| C.可以用CS2清洗做过实验③后附着在试管壁上的硫 |
| D.反应④生成S的原子利用率是100% |
您最近一年使用:0次
2020-02-05更新
|
170次组卷
|
2卷引用:辽宁省丹东市2019—2020学年高三上学期期末考试理综化学试题



