名校
解题方法
1 . 我国稀土产业发达,利用稀土元素制备新型电池材料是一个潜在的研究热点。铈(元素符号为Ce)是最重要的稀土元素之一,以氟碳铈矿(假设只含 、BaO、
、BaO、 )为原料制备氧化铈,其工艺流程如图所示:
)为原料制备氧化铈,其工艺流程如图所示:

提示:稀土元素离子易与 形成复盐沉淀。
形成复盐沉淀。 在空气中易被氧化为
在空气中易被氧化为 。
。
请回答下列问题:
(1)为提高焙烧效率,在焙烧前会将矿石粉碎,简要解释原因__________________ 。
(2)滤渣A的主要成分是 和
和______ (填化学式)。
(3)焙烧后加入稀硫酸浸出,Ce的浸出率和稀硫酸浓度、温度有关,其关系如图所示:
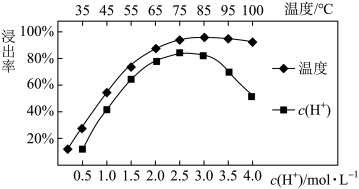
应选择的适宜条件为______ 。硫酸浓度过大时,浸出率降低的原因是______ 。
(4)在进行步骤③时,应该特别注意的问题是_____________________ 。
(5)写出步骤⑤中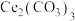 在空气中灼烧的化学反应方程式
在空气中灼烧的化学反应方程式__________________ 。
 、BaO、
、BaO、 )为原料制备氧化铈,其工艺流程如图所示:
)为原料制备氧化铈,其工艺流程如图所示:
提示:稀土元素离子易与
 形成复盐沉淀。
形成复盐沉淀。 在空气中易被氧化为
在空气中易被氧化为 。
。请回答下列问题:
(1)为提高焙烧效率,在焙烧前会将矿石粉碎,简要解释原因
(2)滤渣A的主要成分是
 和
和(3)焙烧后加入稀硫酸浸出,Ce的浸出率和稀硫酸浓度、温度有关,其关系如图所示:

应选择的适宜条件为
(4)在进行步骤③时,应该特别注意的问题是
(5)写出步骤⑤中
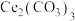 在空气中灼烧的化学反应方程式
在空气中灼烧的化学反应方程式
您最近一年使用:0次
名校
解题方法
2 . 大力发展新能源汽车产业是我国兑现碳中和承诺的重要战略之一。随着这一产业的发展,如何处理废旧锂电池成为一个亟需解决的问题。某废弃的钴酸锂( )电池中含有少量氧化铝、氧化铁和碳单质,为回收利用有关元素,某小组设计如下实验流程:
)电池中含有少量氧化铝、氧化铁和碳单质,为回收利用有关元素,某小组设计如下实验流程:

已知: 与草酸根离子(
与草酸根离子( )结合生成较稳定的
)结合生成较稳定的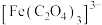 ,
,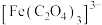 在强酸性条件下分解重新生成
在强酸性条件下分解重新生成 。
。
(1)操作①的名称为______ ;由此可推测,氧化铝______ (填“能”或“不能”)溶于氢氧化钠溶液。
(2)溶液②中所含主要溶质为LiCl、 ,请写出
,请写出 和盐酸反应的化学方程式中LiCoO2和HCl的最简系数比(提示:产物有氯气)
和盐酸反应的化学方程式中LiCoO2和HCl的最简系数比(提示:产物有氯气)______ 。
(3)将溶液中的 转化为
转化为 沉淀也是常用的沉钴方案。在此流程中选用草酸铵而不用碳酸盐的原因是
沉淀也是常用的沉钴方案。在此流程中选用草酸铵而不用碳酸盐的原因是__________________ 。
(4)为证明操作④获得的 沉淀表面的杂质已被洗涤干净,所需进行的实验操作为:取少量的最后一次洗涤液于试管中,加入
沉淀表面的杂质已被洗涤干净,所需进行的实验操作为:取少量的最后一次洗涤液于试管中,加入______ ,若无白色沉淀生成,则证明沉淀洗涤干净。
(5)取3.66 g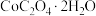 (相对分子质量183)隔绝空气加热,在205℃条件下反应完全后,剩余固体质量为2.94 g,此时分解产生的气体为
(相对分子质量183)隔绝空气加热,在205℃条件下反应完全后,剩余固体质量为2.94 g,此时分解产生的气体为______ (填化学式);在956℃条件下反应完全后,剩余固体相对最开始反应前失重59%,此时固体成分的化学式为 ,
,
______ 。
(6)某同学设计如图装置测定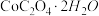 晶体中结晶水的含量以检验样品的纯度。下列有关说法不正确的是
晶体中结晶水的含量以检验样品的纯度。下列有关说法不正确的是______ (填选项)。

A. B中应装入浓硫酸,目的是除去水蒸气
B. 利用干燥管前后质量差可计算出结晶水的含量
C. 图中半透膜可让气体通过又可防止固体粉末进入导管
D. 反应结束后,应先停止加热,一段时间后再停止通空气
(7)溶液④中,铁元素主要以______ 离子形态存在,应加入______ 后再进行后续操作。
(8) 溶液在工业上常用于电路板的蚀刻,发生的反应为
溶液在工业上常用于电路板的蚀刻,发生的反应为 。某同学向含有
。某同学向含有 、
、 和
和 三种溶质的溶液中加入一定量的铁粉,若反应完成后有固体剩余,则固体的成分可能为
三种溶质的溶液中加入一定量的铁粉,若反应完成后有固体剩余,则固体的成分可能为______ (填选项)。
A. Fe B. Fe和Zn C. Fe和Cu D. Cu和Zn
(9)某a g混合粉末中含有铁、石墨、硫和碳酸氢铵,在空气中充分加热至完全反应后,重新称量剩余固体质量,仍为a g,则混合物中铁的质量分数为______ 。
 )电池中含有少量氧化铝、氧化铁和碳单质,为回收利用有关元素,某小组设计如下实验流程:
)电池中含有少量氧化铝、氧化铁和碳单质,为回收利用有关元素,某小组设计如下实验流程:
已知:
 与草酸根离子(
与草酸根离子( )结合生成较稳定的
)结合生成较稳定的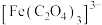 ,
,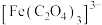 在强酸性条件下分解重新生成
在强酸性条件下分解重新生成 。
。(1)操作①的名称为
(2)溶液②中所含主要溶质为LiCl、
 ,请写出
,请写出 和盐酸反应的化学方程式中LiCoO2和HCl的最简系数比(提示:产物有氯气)
和盐酸反应的化学方程式中LiCoO2和HCl的最简系数比(提示:产物有氯气)(3)将溶液中的
 转化为
转化为 沉淀也是常用的沉钴方案。在此流程中选用草酸铵而不用碳酸盐的原因是
沉淀也是常用的沉钴方案。在此流程中选用草酸铵而不用碳酸盐的原因是(4)为证明操作④获得的
 沉淀表面的杂质已被洗涤干净,所需进行的实验操作为:取少量的最后一次洗涤液于试管中,加入
沉淀表面的杂质已被洗涤干净,所需进行的实验操作为:取少量的最后一次洗涤液于试管中,加入(5)取3.66 g
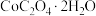 (相对分子质量183)隔绝空气加热,在205℃条件下反应完全后,剩余固体质量为2.94 g,此时分解产生的气体为
(相对分子质量183)隔绝空气加热,在205℃条件下反应完全后,剩余固体质量为2.94 g,此时分解产生的气体为 ,
,
(6)某同学设计如图装置测定
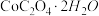 晶体中结晶水的含量以检验样品的纯度。下列有关说法不正确的是
晶体中结晶水的含量以检验样品的纯度。下列有关说法不正确的是
A. B中应装入浓硫酸,目的是除去水蒸气
B. 利用干燥管前后质量差可计算出结晶水的含量
C. 图中半透膜可让气体通过又可防止固体粉末进入导管
D. 反应结束后,应先停止加热,一段时间后再停止通空气
(7)溶液④中,铁元素主要以
(8)
 溶液在工业上常用于电路板的蚀刻,发生的反应为
溶液在工业上常用于电路板的蚀刻,发生的反应为 。某同学向含有
。某同学向含有 、
、 和
和 三种溶质的溶液中加入一定量的铁粉,若反应完成后有固体剩余,则固体的成分可能为
三种溶质的溶液中加入一定量的铁粉,若反应完成后有固体剩余,则固体的成分可能为A. Fe B. Fe和Zn C. Fe和Cu D. Cu和Zn
(9)某a g混合粉末中含有铁、石墨、硫和碳酸氢铵,在空气中充分加热至完全反应后,重新称量剩余固体质量,仍为a g,则混合物中铁的质量分数为
您最近一年使用:0次
3 . 在“价-类”二维图中融入“杠杆模型”,可直观辨析部分物质间的转化及其定量关系。图中字母代表常见的含氯元素的物质,b、e均为钠盐。下列说法正确的是


| A.a、d、f都属于一元强酸 |
| B.c、d均具有强氧化性和漂白性 |
C.的转化中,每消耗1mol c转移 个电子 个电子 |
D.b、e在一定条件下反应生成c时,物质的量之比 |
您最近一年使用:0次
4 . 向酸性 溶液中滴加KI溶液,发生的离子反应为:□
溶液中滴加KI溶液,发生的离子反应为:□ □
□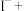 □
□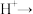 □
□ □
□ □
□ (未配平)。下列说法正确的是
(未配平)。下列说法正确的是
 溶液中滴加KI溶液,发生的离子反应为:□
溶液中滴加KI溶液,发生的离子反应为:□ □
□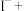 □
□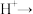 □
□ □
□ □
□ (未配平)。下列说法正确的是
(未配平)。下列说法正确的是| A.溶液由紫红色变成无色 | B. 是氧化产物 是氧化产物 |
C. 的系数为8 的系数为8 | D.生成1mol  时转移5mol电子 时转移5mol电子 |
您最近一年使用:0次
名校
解题方法
5 . 钨是熔点最高的金属,是重要的战略物资,广泛用于钢铁工业、电真空照明材料等方面。钨在自然界主要以钨(+6价)酸盐的形式存在。有开采价值的钨矿石是白钨矿和黑钨矿。黑钨矿的主要成分是铁和锰的钨酸盐,化学式常写成FeWO4、MnWO4.黑钨矿传统冶炼工艺的第一阶段是碱熔法(如下图,已知钨酸是一种难溶性强酸、对热不稳定)。
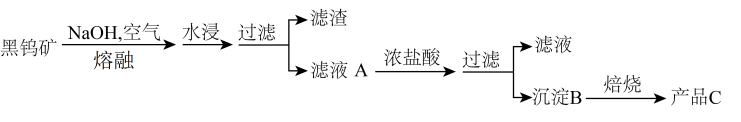
(1)第一次过滤除掉铁、锰元素,滤液A的成分(写化学式):_________ 。
(2)生成沉淀B的化学方程式:_________ ;沉淀B焙烧可得到同价态的氧化物产品C,用H2作还原剂,得到高纯度的钨。写出H2与产品C反应的化学方程式:_________ 。
(3)目前,冶炼拉制钨丝的金属钨,都用组成为非整比的钨氧化物为原料,这种氧化钨中存在五价和六价两种价态的钨。试确定组成为WO2.9的氧化钨中五价和六价的钨原子数之比等于_________ 。

(1)第一次过滤除掉铁、锰元素,滤液A的成分(写化学式):
(2)生成沉淀B的化学方程式:
(3)目前,冶炼拉制钨丝的金属钨,都用组成为非整比的钨氧化物为原料,这种氧化钨中存在五价和六价两种价态的钨。试确定组成为WO2.9的氧化钨中五价和六价的钨原子数之比等于
您最近一年使用:0次
6 . 钴 使某析氧反应催化剂中流失
使某析氧反应催化剂中流失 的原位自修复机理如图。下列说法错误的是
的原位自修复机理如图。下列说法错误的是

 使某析氧反应催化剂中流失
使某析氧反应催化剂中流失 的原位自修复机理如图。下列说法错误的是
的原位自修复机理如图。下列说法错误的是
A.催化析氧反应和自修复反应中的催化剂分别为 和 和 |
B.维持相对稳定的 有助于催化析氧和自修复的进行 有助于催化析氧和自修复的进行 |
C.自修复反应的方程式为: |
D.图中所示物质之间的转化只有 和 和 的化合价发生了变化 的化合价发生了变化 |
您最近一年使用:0次
名校
解题方法
7 . 2020年11月24日,搭载“嫦娥五号”探测器的“长征五号”大型运载火箭成功发射升空,12月17日“嫦娥五号”返回器顺利返回。
(1)“长征五号”的第一、二子级火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4) 做推进剂,该反应的能量转化形式是___________ ,化学方程式为C2H8N2+2N2O4=3N2+4H2O+2X, 则X的化学式是___________ 。
(2)“长征五号”的第三子级火箭采用液氢、液氧做推进剂。制取与储存氢气是氢能源利用领域的研究热点。
I.制氢:铁酸锌(ZnFe2O4)可用于循环分解水制氢气。如图所示,制氢过程中,ZnFe2O4的作用是____________ , 该循环制氢中不断消耗的物质是___________ (填化学式)。
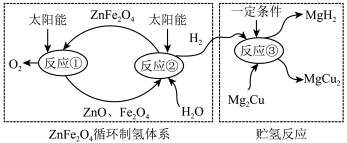
II.贮氢:请写出反应③的化学方程式___________ 。氢化物MgH2与水反应生成一种碱,并释放出H2,其化学方程式为___________ 。
III.如图是氢气和氧气在密闭容器中燃烧的微观示意图,请回答:
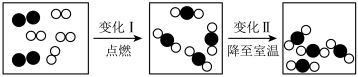
变化I和变化II的本质区别是___________ 。
(3)本次探月的重要任务是寻找月球矿物成分,以探索未来新能源。月壤中含有丰富的氦-3,氦-3是世界公认的高效、清洁、安全的核聚变发电燃料。下列关于氦- 3的叙述正确的是___________(填字母序号)。
(1)“长征五号”的第一、二子级火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4) 做推进剂,该反应的能量转化形式是
(2)“长征五号”的第三子级火箭采用液氢、液氧做推进剂。制取与储存氢气是氢能源利用领域的研究热点。
I.制氢:铁酸锌(ZnFe2O4)可用于循环分解水制氢气。如图所示,制氢过程中,ZnFe2O4的作用是

II.贮氢:请写出反应③的化学方程式
III.如图是氢气和氧气在密闭容器中燃烧的微观示意图,请回答:

变化I和变化II的本质区别是
(3)本次探月的重要任务是寻找月球矿物成分,以探索未来新能源。月壤中含有丰富的氦-3,氦-3是世界公认的高效、清洁、安全的核聚变发电燃料。下列关于氦- 3的叙述正确的是___________(填字母序号)。
| A.其原子核内质子数为3 | B.其原子核外电子数为2 |
| C.其相对原子质量约为2 | D.其化学性质肯定比较活泼 |
您最近一年使用:0次
名校
8 . 稀土元素铈的化合物具有良好的光学、电学性质,广泛应用于阴极射线管( )玻壳、各种平板显示、光学玻璃镜头和计算机芯片等领域。以氟碳铈矿(主要成分为
)玻壳、各种平板显示、光学玻璃镜头和计算机芯片等领域。以氟碳铈矿(主要成分为 ,还有少量其它稀土元素)为原料提取铈元素的一种工艺流程如图所示。
,还有少量其它稀土元素)为原料提取铈元素的一种工艺流程如图所示。

已知:①铈常见化合价为+3、+4,四价铈有强氧化性;
② 既不溶于水,也不溶于稀硫酸。
既不溶于水,也不溶于稀硫酸。
回答下列问题:
(1)已知“氧化焙烧”中铈元素转化为 ,写出该步反应的化学方程式
,写出该步反应的化学方程式___________ 。
(2)“酸浸Ⅱ”中发生反应的离子方程式为___________ ;该步骤通常控制温度为 之间的原因是
之间的原因是___________ 。
(3)“萃取”原理为 ,“反萃取”得到硫酸铈溶液的原理为
,“反萃取”得到硫酸铈溶液的原理为___________ 。
(4)实验室中进行操作1所用到的玻璃仪器有___________ 。
(5) 是汽车尾气净化器中的关键催化剂,能在还原性气氛中供氧,在氧化性气氛中耗氧,在尾气净化过程中发生着
是汽车尾气净化器中的关键催化剂,能在还原性气氛中供氧,在氧化性气氛中耗氧,在尾气净化过程中发生着 的循环。则
的循环。则 在消除
在消除 的反应中,物质的量比
的反应中,物质的量比 为
为___________ 。
 )玻壳、各种平板显示、光学玻璃镜头和计算机芯片等领域。以氟碳铈矿(主要成分为
)玻壳、各种平板显示、光学玻璃镜头和计算机芯片等领域。以氟碳铈矿(主要成分为 ,还有少量其它稀土元素)为原料提取铈元素的一种工艺流程如图所示。
,还有少量其它稀土元素)为原料提取铈元素的一种工艺流程如图所示。
已知:①铈常见化合价为+3、+4,四价铈有强氧化性;
②
 既不溶于水,也不溶于稀硫酸。
既不溶于水,也不溶于稀硫酸。回答下列问题:
(1)已知“氧化焙烧”中铈元素转化为
 ,写出该步反应的化学方程式
,写出该步反应的化学方程式(2)“酸浸Ⅱ”中发生反应的离子方程式为
 之间的原因是
之间的原因是(3)“萃取”原理为
 ,“反萃取”得到硫酸铈溶液的原理为
,“反萃取”得到硫酸铈溶液的原理为(4)实验室中进行操作1所用到的玻璃仪器有
(5)
 是汽车尾气净化器中的关键催化剂,能在还原性气氛中供氧,在氧化性气氛中耗氧,在尾气净化过程中发生着
是汽车尾气净化器中的关键催化剂,能在还原性气氛中供氧,在氧化性气氛中耗氧,在尾气净化过程中发生着 的循环。则
的循环。则 在消除
在消除 的反应中,物质的量比
的反应中,物质的量比 为
为
您最近一年使用:0次
2021-10-13更新
|
431次组卷
|
2卷引用:山东省青岛市2022届高三期初学习质量调研检测化学试卷
名校
解题方法
9 . W、X、Y、Z 是原子序数依次增大的同一短周期主族元素,W、X是金属元素,它们的最高价氧化物对应的水化物可以反应生成盐和水,Y、Z 是非金属元素。
(1)W 与 Y 可形成化合物 W2Y,该化合物在溶液中与氯气发生反应的离子方程式为_______ 。
(2)Y 的低价氧化物通入 Z 单质的水溶液中,发生反应的化学方程式为_______ 。
(3)比较 Y、Z 气态氢化物的稳定性:_______ >_______ (用化学式表示)。
(4)W、X、Y、Z 四种元素简单离子的离子半径由大到小的顺序是_______ >_______ >_______ >_______ 。
(5)Z 的最高价氧化物为无色液体,该物质与一定量水混合得到一种稀溶液,写出该反应的化学方程式:_______ 。
(1)W 与 Y 可形成化合物 W2Y,该化合物在溶液中与氯气发生反应的离子方程式为
(2)Y 的低价氧化物通入 Z 单质的水溶液中,发生反应的化学方程式为
(3)比较 Y、Z 气态氢化物的稳定性:
(4)W、X、Y、Z 四种元素简单离子的离子半径由大到小的顺序是
(5)Z 的最高价氧化物为无色液体,该物质与一定量水混合得到一种稀溶液,写出该反应的化学方程式:
您最近一年使用:0次
2021-03-09更新
|
183次组卷
|
2卷引用:山东省青岛市莱西市第一中学2023-2024学年高一下学期开学化学试题



