21-22高一上·江西宜春·期末
名校
1 . I.元素的价—类二维图是我们学习元素及其化合物相关知识的重要模型工具,也是发展证据推理与模型认知这一科学核心素养的重要途径.如图为氯元素的价一类二维图,回答下列问题:

(1)实验室常用的制取 的离子方程式为
的离子方程式为_______ .
(2)物质的量均为1mol的 和Fe充分反应,转移电子的物质的量为
和Fe充分反应,转移电子的物质的量为_______ .
(3)写出 与NaOH反应生成等物质的量的氧化产物与还原产物的离子方程式
与NaOH反应生成等物质的量的氧化产物与还原产物的离子方程式_______
II.ClO2又称百毒净,可用于水的净化和纸张、纺织品的漂白.用如图所示装置(夹持装置和加热装置省略)制备ClO2并探究ClO2的某些性质

回答下列问题:
(4)装置A用于制备 且生成的
且生成的 中混有
中混有 ,该反应的化学方程式为
,该反应的化学方程式为_______
(5)关闭止水夹②,打开止水夹①③,通空气一段时间后,装置C中生成了 和气体,该反应体现了
和气体,该反应体现了 的
的_______ 性.若关闭止水夹③,打开止水夹②,B中可观察到的现象为_______
(6)城市饮用水处理,新技术用 替代
替代 ,如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么消毒杀菌剂
,如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么消毒杀菌剂 的消毒效率是
的消毒效率是 的
的_______ 倍(结果保留两位小数)

(1)实验室常用的制取
 的离子方程式为
的离子方程式为(2)物质的量均为1mol的
 和Fe充分反应,转移电子的物质的量为
和Fe充分反应,转移电子的物质的量为(3)写出
 与NaOH反应生成等物质的量的氧化产物与还原产物的离子方程式
与NaOH反应生成等物质的量的氧化产物与还原产物的离子方程式II.ClO2又称百毒净,可用于水的净化和纸张、纺织品的漂白.用如图所示装置(夹持装置和加热装置省略)制备ClO2并探究ClO2的某些性质

回答下列问题:
(4)装置A用于制备
 且生成的
且生成的 中混有
中混有 ,该反应的化学方程式为
,该反应的化学方程式为(5)关闭止水夹②,打开止水夹①③,通空气一段时间后,装置C中生成了
 和气体,该反应体现了
和气体,该反应体现了 的
的(6)城市饮用水处理,新技术用
 替代
替代 ,如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么消毒杀菌剂
,如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么消毒杀菌剂 的消毒效率是
的消毒效率是 的
的
您最近一年使用:0次
名校
2 . 现取一定量的硫酸酸化的硫酸锰( )溶液,向其中依次加入下列试剂,对应的现象如下表所示:
)溶液,向其中依次加入下列试剂,对应的现象如下表所示:
已知:①金属铋(Bi)价态为+3价时较稳定, 无色;
无色;
②铋酸钠( )无色,难溶于水;
)无色,难溶于水;
③淀粉溶液遇到 变成蓝色。
变成蓝色。
(1)由上述现象可得 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为___________ ;
(2)根据上述结论,请写出 与硫酸锰溶液在酸性条件下反应的离子方程式
与硫酸锰溶液在酸性条件下反应的离子方程式___________ ;
(3)硫酸酸化的 溶液和双氧水反应产生氧气,请将反应的化学方程式补充完整:
溶液和双氧水反应产生氧气,请将反应的化学方程式补充完整:_________

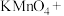



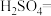



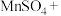

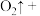

___________
(4)软锰矿的主要成分为 ,现以软锰矿和闪锌矿为原料制备单质Zn,在工艺流程中
,现以软锰矿和闪锌矿为原料制备单质Zn,在工艺流程中 和FeS发生反应,化学方程式为
和FeS发生反应,化学方程式为 。
。
①该反应中,氧化剂是___________ ,氧化产物是___________ 。
②用双线桥法标出该反应的电子转移情况:___________ 。
③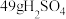 参加反应时转移电子的个数为
参加反应时转移电子的个数为___________ 。
 )溶液,向其中依次加入下列试剂,对应的现象如下表所示:
)溶液,向其中依次加入下列试剂,对应的现象如下表所示:| 试剂 | 少量铋酸钠 | 过量的双氧水 | 适量KI—淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 溶液变成蓝色 |
 无色;
无色;②铋酸钠(
 )无色,难溶于水;
)无色,难溶于水;③淀粉溶液遇到
 变成蓝色。
变成蓝色。(1)由上述现象可得
 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(2)根据上述结论,请写出
 与硫酸锰溶液在酸性条件下反应的离子方程式
与硫酸锰溶液在酸性条件下反应的离子方程式(3)硫酸酸化的
 溶液和双氧水反应产生氧气,请将反应的化学方程式补充完整:
溶液和双氧水反应产生氧气,请将反应的化学方程式补充完整:
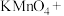



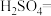



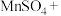

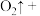

(4)软锰矿的主要成分为
 ,现以软锰矿和闪锌矿为原料制备单质Zn,在工艺流程中
,现以软锰矿和闪锌矿为原料制备单质Zn,在工艺流程中 和FeS发生反应,化学方程式为
和FeS发生反应,化学方程式为 。
。①该反应中,氧化剂是
②用双线桥法标出该反应的电子转移情况:
③
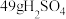 参加反应时转移电子的个数为
参加反应时转移电子的个数为
您最近一年使用:0次
2023-11-16更新
|
349次组卷
|
2卷引用:河北省石家庄市高中五校(一中,正中等)2023-2024学年高一上学期期中联考化学试题
21-22高一上·福建三明·期末
3 . 化学对生产、生活有重要的价值。
(1)工业上利用氨制备硝酸,写出氨被催化氧化生成NO的化学方程式:___ 。
(2)汽车尾气是城市空气的污染源之一。
①汽车的“催化转换器”能使尾气中的NO与CO发生反应,生成可参与大气循环的物质,写出该反应的化学方程式:___ 。
②用甲醇(CH3OH)作汽车燃料,可以降低汽车尾气对大气的污染。若80g甲醇完全燃烧转化为CO2,转移的电子数为____ 。
(3)水污染是常见的环境问题。某工业废水中可能含有大量Na+、Cl-、Cu2+和SO ,需净化后排放。
,需净化后排放。
①写出检验废水中含有SO 的实验操作、现象及结论。
的实验操作、现象及结论。___ 。
②现需将废水中Cu2+除去,且回收金属Cu。请设计处理方案并用流程图表示____ 。
(流程图示例: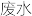
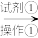
 ……)
……)
(1)工业上利用氨制备硝酸,写出氨被催化氧化生成NO的化学方程式:
(2)汽车尾气是城市空气的污染源之一。
①汽车的“催化转换器”能使尾气中的NO与CO发生反应,生成可参与大气循环的物质,写出该反应的化学方程式:
②用甲醇(CH3OH)作汽车燃料,可以降低汽车尾气对大气的污染。若80g甲醇完全燃烧转化为CO2,转移的电子数为
(3)水污染是常见的环境问题。某工业废水中可能含有大量Na+、Cl-、Cu2+和SO
 ,需净化后排放。
,需净化后排放。①写出检验废水中含有SO
 的实验操作、现象及结论。
的实验操作、现象及结论。②现需将废水中Cu2+除去,且回收金属Cu。请设计处理方案并用流程图表示
(流程图示例:
 ……)
……)
您最近一年使用:0次
19-20高三上·宁夏石嘴山·阶段练习
名校
4 . 根据下列实验现象或要求写离子方程式(描述现象的,需要写出所有涉及的离子方程式。非特殊说明,书写离子方程式)
| 实验现象 | 离子方程式 |
| 1.向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解 | |
| 2.制备氢氧化铁胶体的化学方程式 | |
| 3.二氧化硫使酸性高锰酸钾溶液褪色 | |
| 4.Fe3O4溶于稀硝酸 | |
| 5.氯化亚铁溶液通入少量氯气,变为黄色溶液,加入过量碘化钾溶液,溶液颜色加深,继续加入NaOH溶液,出现白色沉淀,且颜色不断加深至红褐色。 | |
| 6.澄清石灰水中通入CO2出现白色沉淀,继续通入二氧化碳,沉淀溶解,加热后又出现白色沉淀。 | |
| 7.三氯化铝溶液中加逐滴加入NaOH溶液,先出现白色沉淀,然后溶解,再通入CO2至刚开始出现沉淀。 | |
| 8.NH4Al(SO4)2溶液与Ba(OH)2溶液物质的量1∶2混合 | |
| 9.FeI2与Cl2物质的量1∶2反应 | |
| 10.Ba(OH)2中加入硫酸铝溶液,至沉淀质量不再改变。再加入过量NaHCO3溶液,又出白色沉淀。 | |
| 11.生产硫化钠大多采用无水芒硝(Na2SO4)—碳粉还原法,若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生反应的化学方程式 | |
| 12.温度高于200 ℃时,硝酸铝完全分解成氧化铝和两种气体(其体积比为4∶1),写出该反应的化学方程式 | |
| 13.湿法制备高铁酸钾(K2FeO4)的过程为,在氢氧化铁固体中加入KClO和KOH的混合液。写出该过程的离子方程式并配平。 |
您最近一年使用:0次
2019-09-07更新
|
249次组卷
|
3卷引用:第二节 离子反应(二)-2020-2021学年高一化学必修第一册课时同步练(新人教)
(已下线)第二节 离子反应(二)-2020-2021学年高一化学必修第一册课时同步练(新人教)9.2.1反应的合理选择(课后)-2019苏教版必修2课前课中课后宁夏石嘴山市第三中学2020届高三上学期第一次适应性(开学)考试化学试题
5 . 水合肼 常用于生产火箭燃料,其沸点是
常用于生产火箭燃料,其沸点是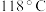 ,受热易分解。尿素法合成水合肼的基本流程如图所示。
,受热易分解。尿素法合成水合肼的基本流程如图所示。

回答下列问题:
(1) 是二元弱碱,在水中的电离方式与氨相似,写出
是二元弱碱,在水中的电离方式与氨相似,写出 第二步电离的方程式:
第二步电离的方程式:___________ 。
(2)已知次氯酸钠与盐酸混合能够生成 ,说明氧化性
,说明氧化性
___________  (填“>”或“<”)。实验发现,
(填“>”或“<”)。实验发现, 与烧碱溶液反应可以生成
与烧碱溶液反应可以生成 ,说明
,说明 与
与 的氧化性强弱关系与
的氧化性强弱关系与___________ 有关。
(3) 强碱性溶液与尿素
强碱性溶液与尿素 水溶液加热制备水合肼的离子方程式为
水溶液加热制备水合肼的离子方程式为___________ 。
(4)常通过减压蒸馏从反应后的混合溶液中获得水合肼,采用该操作的原因是___________ 。
(5)水合肼与硫酸反应生成的盐是农业上重要的杀虫剂、灭菌剂,写出水合肼与硫酸反应生成的碱式盐的化学式:___________ 。
(6)电化学方法制备 的装置如图所示。其中双极膜是阴、阳复合膜,层间的
的装置如图所示。其中双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。

①双极膜中产生的___________ (填“ ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。
②若电路中转移2mol电子,理论上负极区溶液增重___________ g。
 常用于生产火箭燃料,其沸点是
常用于生产火箭燃料,其沸点是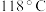 ,受热易分解。尿素法合成水合肼的基本流程如图所示。
,受热易分解。尿素法合成水合肼的基本流程如图所示。
回答下列问题:
(1)
 是二元弱碱,在水中的电离方式与氨相似,写出
是二元弱碱,在水中的电离方式与氨相似,写出 第二步电离的方程式:
第二步电离的方程式:(2)已知次氯酸钠与盐酸混合能够生成
 ,说明氧化性
,说明氧化性
 (填“>”或“<”)。实验发现,
(填“>”或“<”)。实验发现, 与烧碱溶液反应可以生成
与烧碱溶液反应可以生成 ,说明
,说明 与
与 的氧化性强弱关系与
的氧化性强弱关系与(3)
 强碱性溶液与尿素
强碱性溶液与尿素 水溶液加热制备水合肼的离子方程式为
水溶液加热制备水合肼的离子方程式为(4)常通过减压蒸馏从反应后的混合溶液中获得水合肼,采用该操作的原因是
(5)水合肼与硫酸反应生成的盐是农业上重要的杀虫剂、灭菌剂,写出水合肼与硫酸反应生成的碱式盐的化学式:
(6)电化学方法制备
 的装置如图所示。其中双极膜是阴、阳复合膜,层间的
的装置如图所示。其中双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。
①双极膜中产生的
 ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。②若电路中转移2mol电子,理论上负极区溶液增重
您最近一年使用:0次
2023高二·全国·专题练习
解题方法
6 . 用二氧化氯(ClO2)可制备用途广泛的亚氯酸钠(NaClO2),实验室可用下列装置(略去部分夹持仪器)制备少量的亚氯酸钠
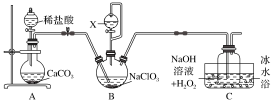
已知:①ClO2沸点为9.9 ℃,可溶于水,有毒,浓度较高时易发生爆炸
②NaClO2饱和溶液低于38 ℃时析出NaClO2·3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解为NaClO3和NaCl
③B装置为ClO2发生装置,所用试剂NaClO3、H2SO4(浓)、CH3OH
请回答下列问题:
实验过程中需持续通入一定量的CO2,其目的是_______ ;反应结束后需再通入一定量的CO2,其目的是_______

已知:①ClO2沸点为9.9 ℃,可溶于水,有毒,浓度较高时易发生爆炸
②NaClO2饱和溶液低于38 ℃时析出NaClO2·3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解为NaClO3和NaCl
③B装置为ClO2发生装置,所用试剂NaClO3、H2SO4(浓)、CH3OH
请回答下列问题:
实验过程中需持续通入一定量的CO2,其目的是
您最近一年使用:0次
名校
解题方法
7 . 物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据下图,回答下列问题:

(1)检验Y所用的试剂是_________ 。
(2)W的稀溶液与铁反应的离子方程式为_________ 。
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是_________ (填标号)。
a.Na2S+S b.Na2SO3+S c.Na2SO3 +Na2SO4 d.SO2+Na2SO4
(4)将X与Y 的溶液混合,现象为_________ ,该反应的氧化剂与还原剂的物质的量之比为_________ 。

(1)检验Y所用的试剂是
(2)W的稀溶液与铁反应的离子方程式为
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是
a.Na2S+S b.Na2SO3+S c.Na2SO3 +Na2SO4 d.SO2+Na2SO4
(4)将X与Y 的溶液混合,现象为
您最近一年使用:0次
2018-01-09更新
|
290次组卷
|
2卷引用:专题4 专题强化练4硫及其化合物-高中化学苏教2019版必修第一册
解题方法
8 . 铁是目前人类使用量最大的金属,它能形成多种化合物。
(1)取5.6 g的生铁与足量的稀硫酸混合反应,无论怎样进行实验,最终收集的气体体积均小于2.24 L(标准状况),最主要的原因是_____________________ ;所得溶液在长时间放置过程中会慢慢出现浅黄色,试用离子方程式解释这一变化的原因:___________ 。
(2)ZnFe2Ox是一种新型纳米材料,可将工业废气中的某些元素转化为游离态,制取纳米ZnFe2Ox和用于除去废气的转化关系为ZnFe2O4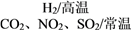 ZnFe2Ox。若上述转化反应中消耗的n(ZnFe2O4)∶n(H2)=2∶1,x的值为
ZnFe2Ox。若上述转化反应中消耗的n(ZnFe2O4)∶n(H2)=2∶1,x的值为________ 。请写出 ZnFe2Ox与NO2反应的化学方程式:_________________________ (x用前一问求出的具体值)。
(3)LiFePO4(难溶于水)材料被视为最有前途的锂离子电池材料之一。
①以 FePO4(难溶于水)、Li2CO3、单质碳为原料在高温下制备LiFePO4,该反应还生成一种可燃性气体,则反应的化学方程式为___________________________ 。
②磷酸铁锂动力电池有几种类型,其中一种(中间是锂离子聚合物的隔膜,它把正极与负极隔开)工作原理为FePO4+Li LiFePO4。则放电时正极上的电极反应式为
LiFePO4。则放电时正极上的电极反应式为___________________________________ 。
(4)已知25 ℃时Ksp[Fe(OH3)]=4.0×10-38,此温度下若在实验室中配制5 mol·L-1 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入______ mL 2 mol·L-1的盐酸(忽略加入盐酸时溶液体积的变化)。
(1)取5.6 g的生铁与足量的稀硫酸混合反应,无论怎样进行实验,最终收集的气体体积均小于2.24 L(标准状况),最主要的原因是
(2)ZnFe2Ox是一种新型纳米材料,可将工业废气中的某些元素转化为游离态,制取纳米ZnFe2Ox和用于除去废气的转化关系为ZnFe2O4
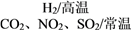 ZnFe2Ox。若上述转化反应中消耗的n(ZnFe2O4)∶n(H2)=2∶1,x的值为
ZnFe2Ox。若上述转化反应中消耗的n(ZnFe2O4)∶n(H2)=2∶1,x的值为(3)LiFePO4(难溶于水)材料被视为最有前途的锂离子电池材料之一。
①以 FePO4(难溶于水)、Li2CO3、单质碳为原料在高温下制备LiFePO4,该反应还生成一种可燃性气体,则反应的化学方程式为
②磷酸铁锂动力电池有几种类型,其中一种(中间是锂离子聚合物的隔膜,它把正极与负极隔开)工作原理为FePO4+Li
 LiFePO4。则放电时正极上的电极反应式为
LiFePO4。则放电时正极上的电极反应式为(4)已知25 ℃时Ksp[Fe(OH3)]=4.0×10-38,此温度下若在实验室中配制5 mol·L-1 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入
您最近一年使用:0次
2023·江苏南通·模拟预测
名校
9 . 电催化还原 是当今资源化利用二氧化碳的重点课题,常用的阴极材料有有机多孔电极材料、铜基复合电极材料等。
是当今资源化利用二氧化碳的重点课题,常用的阴极材料有有机多孔电极材料、铜基复合电极材料等。
(1)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原 的装置示意图如图-1所示。控制其他条件相同,将一定量的
的装置示意图如图-1所示。控制其他条件相同,将一定量的 通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图-2所示。
通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图-2所示。
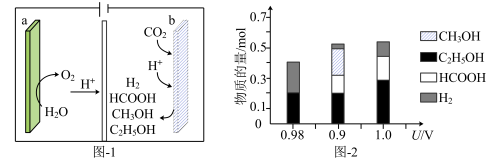
①电解前需向电解质溶液中持续通入过量 的原因是
的原因是___________ 。
②控制电压为0.8V,电解时转移电子的物质的量为___________ mol。
③科研小组利用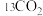 代替原有的
代替原有的 进行研究,其目的是
进行研究,其目的是___________ 。
(2)一种铜基复合电极材料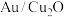 的制备方法:将一定量
的制备方法:将一定量 分散至水与乙醇的混合溶液中,向溶液中逐滴滴加
分散至水与乙醇的混合溶液中,向溶液中逐滴滴加 (一种强酸)溶液,搅拌一段时间后离心分离,得
(一种强酸)溶液,搅拌一段时间后离心分离,得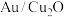 ,溶液呈蓝色。写出
,溶液呈蓝色。写出 还原
还原 的离子方程式:
的离子方程式:___________ 。
(3)金属Cu/La复合电极材料电催化还原CO₂制备甲醛和乙醇的可能机理如图-3所示。研究表明,在不同电极材料上形成中间体的部分反应活化能如图-4所示。
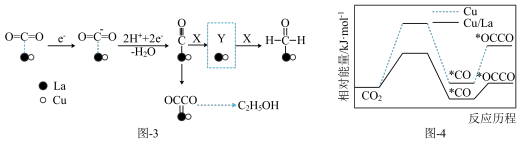
①X为___________ 。在答题卡上相应位置补充完整虚线框内Y的结构。_________
②与单纯的Cu电极相比,利用Cu/La复合电极材料电催化还原 的优点是
的优点是___________ 。
 是当今资源化利用二氧化碳的重点课题,常用的阴极材料有有机多孔电极材料、铜基复合电极材料等。
是当今资源化利用二氧化碳的重点课题,常用的阴极材料有有机多孔电极材料、铜基复合电极材料等。(1)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原
 的装置示意图如图-1所示。控制其他条件相同,将一定量的
的装置示意图如图-1所示。控制其他条件相同,将一定量的 通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图-2所示。
通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图-2所示。
①电解前需向电解质溶液中持续通入过量
 的原因是
的原因是②控制电压为0.8V,电解时转移电子的物质的量为
③科研小组利用
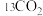 代替原有的
代替原有的 进行研究,其目的是
进行研究,其目的是(2)一种铜基复合电极材料
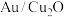 的制备方法:将一定量
的制备方法:将一定量 分散至水与乙醇的混合溶液中,向溶液中逐滴滴加
分散至水与乙醇的混合溶液中,向溶液中逐滴滴加 (一种强酸)溶液,搅拌一段时间后离心分离,得
(一种强酸)溶液,搅拌一段时间后离心分离,得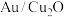 ,溶液呈蓝色。写出
,溶液呈蓝色。写出 还原
还原 的离子方程式:
的离子方程式:(3)金属Cu/La复合电极材料电催化还原CO₂制备甲醛和乙醇的可能机理如图-3所示。研究表明,在不同电极材料上形成中间体的部分反应活化能如图-4所示。

①X为
②与单纯的Cu电极相比,利用Cu/La复合电极材料电催化还原
 的优点是
的优点是
您最近一年使用:0次
2023-05-27更新
|
741次组卷
|
6卷引用:考点19 电解池(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
(已下线)考点19 电解池(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第25讲电解池与金属的电化学腐蚀四川省宜宾市叙州区第一中学校2023-2024学年高二上学期1月期末化学试题江苏省南通市2023届高三下学期第四次模拟考试化学试题江苏省盐城市伍佑中学2023届高三下学期模拟预测化学试题江苏省南京师范大学苏州实验学校2023-2024学年高三上学期零模考试热身练化学试题
22-23高一上·广东佛山·期中
名校
解题方法
10 . 分类是认识和研究物质及其变化的一种常用的科学方法。依据物质类别和元素价态可以对物质的性质进行解释和预测。以下为含氯物质的价类二维图,请回答下列问题:
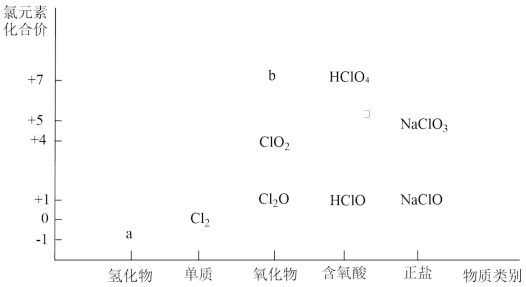
(1)a物质的化学式为_______ ,b属于_______ (填“酸性”或“碱性”)氧化物。
(2)用 消毒水时,
消毒水时, 还可将水中的
还可将水中的 转化为
转化为 ,
, 再水解生成
再水解生成 胶体,说明
胶体,说明 具有
具有_______ 性,在此水处理过程中生成的 胶体有
胶体有_______ 作用。
(3)工业上可以用反应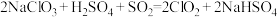 制备
制备 ,用单线桥法标出电子转移的数目和方向。
,用单线桥法标出电子转移的数目和方向。_______
(4)实验室制取氯气时,下列装置能达到相应实验目的是_______ 。
写出实验室用二氧化锰与浓盐酸反应制取氯气的离子方程式:_______ 。
(5)阅读资料,回答相关问题。
① 与
与 溶液反应的化学方程式是
溶液反应的化学方程式是_______ 。
②“84”消毒液不能与洁厕灵(含盐酸)混用,混用会产生氯气,写出反应的离子方程式:_______ 。

(1)a物质的化学式为
(2)用
 消毒水时,
消毒水时, 还可将水中的
还可将水中的 转化为
转化为 ,
, 再水解生成
再水解生成 胶体,说明
胶体,说明 具有
具有 胶体有
胶体有(3)工业上可以用反应
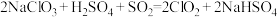 制备
制备 ,用单线桥法标出电子转移的数目和方向。
,用单线桥法标出电子转移的数目和方向。(4)实验室制取氯气时,下列装置能达到相应实验目的是
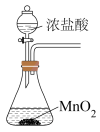 |  | 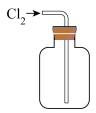 |  |
A.制备 | B.除去 中的 中的 | C.收集 | D.尾气处理 |
(5)阅读资料,回答相关问题。
资料:人们常用“84”消毒液进行消毒。“84”消毒液的名称源于北京某医院在1984年研制成功的一种高效含氯消毒液。“84”消毒液呈无色或淡黄色,可由 与 与 溶液反应制得,其主要成分为 溶液反应制得,其主要成分为 、 、 。 。 |
 与
与 溶液反应的化学方程式是
溶液反应的化学方程式是②“84”消毒液不能与洁厕灵(含盐酸)混用,混用会产生氯气,写出反应的离子方程式:
您最近一年使用:0次



