名校
解题方法
1 . 二氧化氯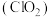 是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
(1)在处理废水时, 可将废水中的
可将废水中的 氧化成
氧化成 和
和 ,该反应的离子方程式是
,该反应的离子方程式是_______ 。
(2)某小组按照文献中制备 的方法设计了如图所示的实验装置用于制备
的方法设计了如图所示的实验装置用于制备 。
。

①装置A用于生成 气体,该反应的化学方程式是
气体,该反应的化学方程式是_______ 。
②通入氮气的作用有两个,一个是起到搅拌作用,二是_______ 装置B的作用是_______ 。
(3)测定装置C中 溶液的浓度:取
溶液的浓度:取 中溶液于锥形瓶中,加入足量的
中溶液于锥形瓶中,加入足量的 溶液和
溶液和 酸化,然后加入
酸化,然后加入_______ 作指示剂,用 的
的 标准液滴定锥形瓶中的溶液(
标准液滴定锥形瓶中的溶液( ),消耗标准溶液的体积为
),消耗标准溶液的体积为 ,滴定终点的现象是
,滴定终点的现象是_______ 。
(4)计算C中 溶液的物质的量浓度,写出计算过程
溶液的物质的量浓度,写出计算过程_______ 。
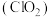 是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:
是一种黄绿色气体,易溶于水,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。回答下列问题:(1)在处理废水时,
 可将废水中的
可将废水中的 氧化成
氧化成 和
和 ,该反应的离子方程式是
,该反应的离子方程式是(2)某小组按照文献中制备
 的方法设计了如图所示的实验装置用于制备
的方法设计了如图所示的实验装置用于制备 。
。
①装置A用于生成
 气体,该反应的化学方程式是
气体,该反应的化学方程式是②通入氮气的作用有两个,一个是起到搅拌作用,二是
(3)测定装置C中
 溶液的浓度:取
溶液的浓度:取 中溶液于锥形瓶中,加入足量的
中溶液于锥形瓶中,加入足量的 溶液和
溶液和 酸化,然后加入
酸化,然后加入 的
的 标准液滴定锥形瓶中的溶液(
标准液滴定锥形瓶中的溶液( ),消耗标准溶液的体积为
),消耗标准溶液的体积为 ,滴定终点的现象是
,滴定终点的现象是(4)计算C中
 溶液的物质的量浓度,写出计算过程
溶液的物质的量浓度,写出计算过程
您最近一年使用:0次
2021-09-19更新
|
286次组卷
|
5卷引用:【全国百强校】重庆市西南大学附属中学校2019届高三第十次月考理科综合化学试题
名校
解题方法
2 . 硝酸铁是一种工业和医药行业常用的原料,用作媒染剂、铜着色剂等。Fe(NO3)3∙9H2O是浅紫色晶体,易溶于水、乙醇和丙酮。
Ⅰ. 利用稀硝酸和铁屑制备硝酸铁。目前常见的生产流程如图所示。
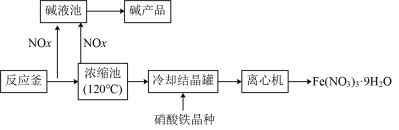
(1)反应釜中原料是稀硝酸和细铁屑,反应的离子方程式是_______ 。硝酸需要过量,原因是_______ 。
(2) 会污染空气,不能随意排放,浓缩池中也会产生
会污染空气,不能随意排放,浓缩池中也会产生 ,请用化学用语解释产生
,请用化学用语解释产生 的原因
的原因_______ 。
(3)冷却结晶后的硝酸铁晶体,最适宜用下列哪种试剂进行洗涤_______。
Ⅱ. 利用工业废水制备硝酸铁。不锈钢酸洗废液中含有大量 、
、 、
、 等金属离子,可对不锈钢酸洗废液中的各金属元素进行分离,并利用分离的含铁物质制备硝酸铁,同时回收其他金属。
等金属离子,可对不锈钢酸洗废液中的各金属元素进行分离,并利用分离的含铁物质制备硝酸铁,同时回收其他金属。
已知:①Cr(OH)3是两性氢氧化物。
②各金属离子沉淀的范围如下表所示:
(4)分离出 适宜的
适宜的 范围是
范围是_______ 。
(5)请设计实验,继续从废液中分别分离出Cr元素和Ni元素_______ 。
Ⅰ. 利用稀硝酸和铁屑制备硝酸铁。目前常见的生产流程如图所示。

(1)反应釜中原料是稀硝酸和细铁屑,反应的离子方程式是
(2)
 会污染空气,不能随意排放,浓缩池中也会产生
会污染空气,不能随意排放,浓缩池中也会产生 ,请用化学用语解释产生
,请用化学用语解释产生 的原因
的原因(3)冷却结晶后的硝酸铁晶体,最适宜用下列哪种试剂进行洗涤_______。
| A.水 | B.四氯化碳 | C.20%稀硝酸 | D.乙醇 |
Ⅱ. 利用工业废水制备硝酸铁。不锈钢酸洗废液中含有大量
 、
、 、
、 等金属离子,可对不锈钢酸洗废液中的各金属元素进行分离,并利用分离的含铁物质制备硝酸铁,同时回收其他金属。
等金属离子,可对不锈钢酸洗废液中的各金属元素进行分离,并利用分离的含铁物质制备硝酸铁,同时回收其他金属。已知:①Cr(OH)3是两性氢氧化物。
②各金属离子沉淀的范围如下表所示:
 |  |  | |
开始沉淀 | 1.5 | 4.6 | 6.7 |
完全沉淀 | 3.2 | 6.9 | 9.5 |
 适宜的
适宜的 范围是
范围是(5)请设计实验,继续从废液中分别分离出Cr元素和Ni元素
您最近一年使用:0次
2021-08-23更新
|
543次组卷
|
4卷引用:2020年北京高考化学真题变式题11-19
3 . 五氧化二氮(N2O5)是有机合成中常用的绿色硝化剂。N2O5常温下为白色固体,可溶于CH2Cl2等氯代烃溶剂,微溶于水且与水反应生成强酸,高于室温时对热不稳定。
(1)1840年,Devill首次将干燥的氯气通入硝酸银,在试管壁上得到了N2O5。已知反应的氧化产物为空气中的成分之一,写出反应的化学方程式:________________________ 。
(2)某化学兴趣小组设计臭氧(O3)氧化法制备N2O5,反应原理为N2O4+O3=N2O5+O2。实验装置如图:
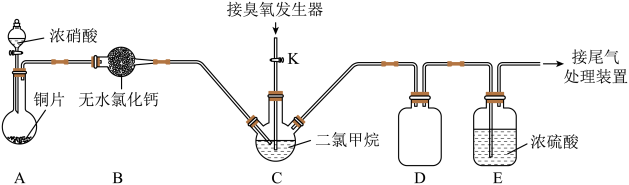
回答下列问题:
①写出装置A中发生反应的离子方程式:________________________ 。
②装置B的作用是________ ;装置E的作用是________________________ 。
③实验时,将三口烧瓶C浸入冰水中,打开装置A中分液漏斗的活塞,一段时间后C中液体变为红棕色。然后打开活塞K,通过臭氧发生器向三口烧瓶中通入含有臭氧的氧气。C中二氯甲烷(CH2Cl2)的作用是________ (填序号)。
A.溶解反应物NO2 B.充分混合反应物使其反应更加充分
C.控制O3的通入速度 D.溶解生成物N2O5
(3)判断C中反应已结束的简单方法是________________________ 。
(4)该兴趣小组用滴定法测定N2O5粗产品中N2O4的含量。取2.0 g粗产品,加入25.00 mL 0.1000 mol/L酸性高锰酸钾溶液。充分反应后,用0.1000 mol/L H2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液20.00 mL。(已知:H2O2与HNO3不反应且不考虑其分解)
①产品中N2O4与KMnO4发生反应的离子方程式为________________ 。
②产品中N2O4的含量为________ (质量分数,结果保留三位有效数字)。
(1)1840年,Devill首次将干燥的氯气通入硝酸银,在试管壁上得到了N2O5。已知反应的氧化产物为空气中的成分之一,写出反应的化学方程式:
(2)某化学兴趣小组设计臭氧(O3)氧化法制备N2O5,反应原理为N2O4+O3=N2O5+O2。实验装置如图:

回答下列问题:
①写出装置A中发生反应的离子方程式:
②装置B的作用是
③实验时,将三口烧瓶C浸入冰水中,打开装置A中分液漏斗的活塞,一段时间后C中液体变为红棕色。然后打开活塞K,通过臭氧发生器向三口烧瓶中通入含有臭氧的氧气。C中二氯甲烷(CH2Cl2)的作用是
A.溶解反应物NO2 B.充分混合反应物使其反应更加充分
C.控制O3的通入速度 D.溶解生成物N2O5
(3)判断C中反应已结束的简单方法是
(4)该兴趣小组用滴定法测定N2O5粗产品中N2O4的含量。取2.0 g粗产品,加入25.00 mL 0.1000 mol/L酸性高锰酸钾溶液。充分反应后,用0.1000 mol/L H2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液20.00 mL。(已知:H2O2与HNO3不反应且不考虑其分解)
①产品中N2O4与KMnO4发生反应的离子方程式为
②产品中N2O4的含量为
您最近一年使用:0次
2021-07-20更新
|
477次组卷
|
2卷引用:重庆市西南大学附属中学2020-2021学年高三下学期第六次月考化学试题
名校
解题方法
4 . I.NaClO2是重要的含氯化工产品,工业上生产NaClO2有多种方法,某工业生产的流程图如下:

(1)NaClO2氯元素的化合价为_______ 。
(2)电解槽中阳极上的电极反应式为_______ 。
(3)反应器Ⅱ中发生的反应中氧化剂与还原剂物质的量之比为_______ 。
II、有关数据如下表所示:
用废电池的锌皮制作ZnSO4•7H2O的过程中,需除去锌皮中的少量杂质铁,其方法是:加入稀H2SO4和H2O2溶解,铁变为_______ ,加碱调节 pH为_______ 时,铁刚好沉淀完全(离子浓度小于1×10-5mol•L-1时,即可认为该离子沉淀完全),继续加碱调节pH为_______ 时,锌开始沉淀(假定Zn2+浓度为0.1mol•L-1),若上述过程不加H2O2的后果是_______ 。

(1)NaClO2氯元素的化合价为
(2)电解槽中阳极上的电极反应式为
(3)反应器Ⅱ中发生的反应中氧化剂与还原剂物质的量之比为
II、有关数据如下表所示:
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-38 |
用废电池的锌皮制作ZnSO4•7H2O的过程中,需除去锌皮中的少量杂质铁,其方法是:加入稀H2SO4和H2O2溶解,铁变为
您最近一年使用:0次
5 . 镍行业发展蕴藏着巨大的潜力。某小组用废镍催化剂(成分为Al2O3、Ni、Fe、SiO2、CaO等)制备草酸镍晶体(NiC2O4·2H2O)的部分实验流程如下:

已知:①Ksp(CaF2)=1.6×10-10、Ksp[Fe(OH)2]=8.0×10-16、Ksp[Fe(OH)3]=4.0×10-38、Ksp[Al(OH)3]=2.7×10-34;
②认为残留在溶液中的离子浓度小于1×10-5mol/L即沉淀完全。
(1)“粉碎”的目的是___________ 。滤渣Ⅰ的成分有___________ (化学式)。
(2)在“调pH”过程中,应先加入H2O2,发生反应的离子方程式为___________ ,沉淀剂可选择___________ 。(填序号)
a.NiOb.NaOHc.Ni(OH)2d.NiCO3
为将Al3+、Fe3+沉淀完全,至少应调节pH到___________ (已知lg3≈0.5)。
(3)在“沉淀”过程中,Ca2+刚好沉淀完全时,溶液中c(F-)=___________ mol/L。
(4)将得到的草酸镍晶体在真空中加热至320℃分解,可重新制得单质镍,且还生成一种气体,请写出该制备过程的化学方程式:___________ 。

已知:①Ksp(CaF2)=1.6×10-10、Ksp[Fe(OH)2]=8.0×10-16、Ksp[Fe(OH)3]=4.0×10-38、Ksp[Al(OH)3]=2.7×10-34;
②认为残留在溶液中的离子浓度小于1×10-5mol/L即沉淀完全。
(1)“粉碎”的目的是
(2)在“调pH”过程中,应先加入H2O2,发生反应的离子方程式为
a.NiOb.NaOHc.Ni(OH)2d.NiCO3
为将Al3+、Fe3+沉淀完全,至少应调节pH到
(3)在“沉淀”过程中,Ca2+刚好沉淀完全时,溶液中c(F-)=
(4)将得到的草酸镍晶体在真空中加热至320℃分解,可重新制得单质镍,且还生成一种气体,请写出该制备过程的化学方程式:
您最近一年使用:0次
2021-02-08更新
|
346次组卷
|
3卷引用:四川省成都市第七中学2020-2021学年高二上学期12月阶段性测试化学试题
名校
解题方法
6 . 三氧化二钴(Co2O3)主要用作颜料、釉料、磁性材料、催化剂和氧化剂等。以含钴废料(主要成分为Co2O3,含有少量MnO2、NiO、Fe3O4)为原料制备Co2O3的流程如下图所示:

已知:
Ⅰ.“酸浸”后的浸出液中含的阳离子有H+、Co2+、Fe3+、Ni2+等。
Ⅱ.部分阳离子以氢氧化物形式完全沉淀时溶液的pH如下表:
回答下列问题:
(1)“酸浸”含钴废料的温度不宜过高,原因是___________ 。
(2)“酸浸”时发生的主要反应是___________ (离子方程式)。
(3)某萃取剂对金属离子的萃取率与溶液pH的关系如图所示:

使用该萃取剂时应控制的pH约为___________ ,理由是___________ 。
(4)写出高温煅烧时发生的化学反应方程式___________ 。
(5)操作1得到的主要副产品是___________ (填名称);
已知该物质的溶液加热到100℃时会变质,该物质的溶解度见下表:
操作1是___________ (填字母)。
a.蒸发结晶 b.降温结晶 c.减压蒸发结晶

已知:
Ⅰ.“酸浸”后的浸出液中含的阳离子有H+、Co2+、Fe3+、Ni2+等。
Ⅱ.部分阳离子以氢氧化物形式完全沉淀时溶液的pH如下表:
| 沉淀物 | Fe(OH)3 | Co(OH)2 | Ni(OH)2 |
| 完全沉淀时的pH | 3.7 | 9.0 | 9.2 |
(1)“酸浸”含钴废料的温度不宜过高,原因是
(2)“酸浸”时发生的主要反应是
(3)某萃取剂对金属离子的萃取率与溶液pH的关系如图所示:

使用该萃取剂时应控制的pH约为
(4)写出高温煅烧时发生的化学反应方程式
(5)操作1得到的主要副产品是
已知该物质的溶液加热到100℃时会变质,该物质的溶解度见下表:
| 湿度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ |
| 溶解度 | 70.6 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 88.0 |
a.蒸发结晶 b.降温结晶 c.减压蒸发结晶
您最近一年使用:0次
名校
解题方法
7 . 为探究Na2SO3溶液和铬(VI)盐溶液的反应规律,某同学进行实验如下:
已知: (橙色) +H2O
(橙色) +H2O
 (黄色) + 2H+
(黄色) + 2H+
(1)进行实验ⅰ和ⅱ:
①用离子方程式表示饱和Na2SO3溶液pH约为9的原因:______________________ 。
②用离子方程式解释i中现象:______________________ 。
(2)继续进行实验ⅲ:
为了说明产生上述现象的原因,补充实验ⅳ:
向2 mL蒸馏水中滴加pH=2的0.05 mol/L K2Cr2O7橙色溶液3滴,溶液变成浅橙色。
①补充实验ⅳ的目的是______________________ 。
②用化学平衡移动原理解释iii中现象:______________________ 。
③根据实验ⅰ~ⅲ,可推测:Na2SO3溶液和铬( VI)盐溶液的反应与溶液酸碱性有关。
a.碱性条件下,Na2SO3溶液和铬( VI)盐溶液不发生氧化还原反应;
b.______________________ 。
④向实验ⅲ所得黄色溶液中继续滴加硫酸,产生的现象证实了上述推测。该现象是______________ 。
已知:
 (橙色) +H2O
(橙色) +H2O
 (黄色) + 2H+
(黄色) + 2H+(1)进行实验ⅰ和ⅱ:
| 序号 | 操作 | 现象 |
| ⅰ | 向2 mLpH=2的0.05 mol/LK2Cr2O7的橙色溶液中滴加饱和Na2SO3溶液(pH约为9)3滴 | 溶液变绿色(含Cr3+) |
| ⅱ | 向2 mLpH=8的0.1 mol/L的K2CrO4黄色溶液中滴加饱和Na2SO3溶液3滴 | 溶液没有明显变化 |
②用离子方程式解释i中现象:
(2)继续进行实验ⅲ:
| 序号 | 操作 | 现象 |
| ⅲ | 向2 mL饱和Na2SO3溶液中滴加pH=2的0.05 mol/LK2Cr2O7的橙色溶液3滴 | 溶液变黄色 |
向2 mL蒸馏水中滴加pH=2的0.05 mol/L K2Cr2O7橙色溶液3滴,溶液变成浅橙色。
①补充实验ⅳ的目的是
②用化学平衡移动原理解释iii中现象:
③根据实验ⅰ~ⅲ,可推测:Na2SO3溶液和铬( VI)盐溶液的反应与溶液酸碱性有关。
a.碱性条件下,Na2SO3溶液和铬( VI)盐溶液不发生氧化还原反应;
b.
④向实验ⅲ所得黄色溶液中继续滴加硫酸,产生的现象证实了上述推测。该现象是
您最近一年使用:0次
2020-12-29更新
|
469次组卷
|
5卷引用:广东省广州市执信中学(广雅,执信,二中联考)2019-2020学年高二上学期期末考试化学试题
名校
8 . Ⅰ.某厂废水中含KCN,其浓度为0.01 mol·L-1,现用氯氧化法处理,发生如下反应(化合物中N化合价均为-3价):KCN+2KOH+Cl2=KOCN+2KCl+H2O
(1)被氧化的元素是_______ 。(用元素符号表示)
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:_______
____KOCN+_______Cl2 +_____KOH→_______K2CO3+_____N2+_____KCl+_____H2O
(3)若将10 L含KCN的浓度为0.01 mol·L-1的废水中KCN氧化除去,最少需要氯气_______ mol。
Ⅱ.某实验小组为了测定(3)中溶液多余Cl2的含量,常用Na2S2O3标准溶液进行定量测定。
(4)现实验室需用480 mL一定浓度的Na2S2O3溶液,配制该溶液所需玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要_______ 。
(5)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO ,因此Na2S2O3常用作脱氯剂,该反应的离子方程式为
,因此Na2S2O3常用作脱氯剂,该反应的离子方程式为_______ (碱性环境)。
(6)现取(3)中溶液20.00 mL,用a mol·L-1Na2S2O3溶液进行滴定,经过平行实验测得消耗Na2S2O3标准溶液b mL,计算废液中Cl2的浓度为_______ mol·L-1(用含a、b的表达式表示)。
(1)被氧化的元素是
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:
____KOCN+_______Cl2 +_____KOH→_______K2CO3+_____N2+_____KCl+_____H2O
(3)若将10 L含KCN的浓度为0.01 mol·L-1的废水中KCN氧化除去,最少需要氯气
Ⅱ.某实验小组为了测定(3)中溶液多余Cl2的含量,常用Na2S2O3标准溶液进行定量测定。
(4)现实验室需用480 mL一定浓度的Na2S2O3溶液,配制该溶液所需玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要
(5)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO
 ,因此Na2S2O3常用作脱氯剂,该反应的离子方程式为
,因此Na2S2O3常用作脱氯剂,该反应的离子方程式为(6)现取(3)中溶液20.00 mL,用a mol·L-1Na2S2O3溶液进行滴定,经过平行实验测得消耗Na2S2O3标准溶液b mL,计算废液中Cl2的浓度为
您最近一年使用:0次
名校
9 . 海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:

(1)请列举海水淡化的两种方法:___________ 、___________ 。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是___________ 。
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为___________ 。
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为59℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:

请你参与分析讨论:
①图中仪器B的名称是___________ ;
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是___________ ;
③实验装置气密性良好,要达到提纯溴的目的,操作中控制温度计b为___________ ℃
④C中溶液颜色为___________ ,为除去该产物中残留的Cl2可向其中加入NaBr溶液,反应离子方程式为___________ 。

(1)请列举海水淡化的两种方法:
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为59℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:

请你参与分析讨论:
①图中仪器B的名称是
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是
③实验装置气密性良好,要达到提纯溴的目的,操作中控制温度计b为
④C中溶液颜色为
您最近一年使用:0次
2020-12-24更新
|
285次组卷
|
3卷引用:重庆市复旦中学2020-2021学度高二上学期第一次段考化学试题
重庆市复旦中学2020-2021学度高二上学期第一次段考化学试题(已下线)微专题20 海水资源的综合利用(提取溴和碘)-备战2022年高考化学考点微专题河南省濮阳市元龙高级中学2021-2022学年高一下学期第二次质量检测化学试题
名校
解题方法
10 . 锰元素在溶液中主要以Mn2+(很浅的肉色,近乎无色)、MnO (绿色)、MnO
(绿色)、MnO (紫色)形式存在,MnO2不溶于稀硫酸。
(紫色)形式存在,MnO2不溶于稀硫酸。
(1)草酸与高锰酸钾在酸性条件下可以发生化学反应。请写出离子方程式:_______ 。
(2)现有0.00lmol/L的酸性KMnO4溶液和0.0lmol/L的草酸溶液,为探讨外界条件对化学反应速率的影响,设计的实验方案如下表:
①通过实验①、②可探究_______ 对反应速率的影响,支持该结论的实验现象是_______ 。
②通过实验①、③可探究草酸的浓度对反应速率的影响,表中Vx=_______ mL,理由是_______ 。
③若实验①5s后,颜色不再变化,用草酸的浓度变化来表示反应速率为_______ 。
(3)电解法制备单质锰的实验装置如图,阳极以稀硫酸为电解液,阴极以硫酸锰和硫酸混合液为电解液,中间用阴离子交换膜将两室隔开,电解过程中阴离子向右移动,一段时间后两极均有气体生成。
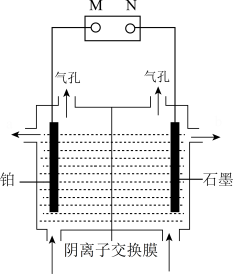
①单质锰将会在_______ 电极上析出(填"铂"或"石墨")。
②写出发生在阴极上的所有电极反应方程式_______ 。
 (绿色)、MnO
(绿色)、MnO (紫色)形式存在,MnO2不溶于稀硫酸。
(紫色)形式存在,MnO2不溶于稀硫酸。(1)草酸与高锰酸钾在酸性条件下可以发生化学反应。请写出离子方程式:
(2)现有0.00lmol/L的酸性KMnO4溶液和0.0lmol/L的草酸溶液,为探讨外界条件对化学反应速率的影响,设计的实验方案如下表:
实验序号 | 体积V/mL | 温度/℃ | ||
KMnO4溶液 | 水 | H2C2O4溶液 | ||
① | 40.0 | 0.0 | 20.0 | 25 |
② | 40.0 | 0.0 | 20.0 | 60 |
③ | 40.0 | Vx | 10.0 | 25 |
②通过实验①、③可探究草酸的浓度对反应速率的影响,表中Vx=
③若实验①5s后,颜色不再变化,用草酸的浓度变化来表示反应速率为
(3)电解法制备单质锰的实验装置如图,阳极以稀硫酸为电解液,阴极以硫酸锰和硫酸混合液为电解液,中间用阴离子交换膜将两室隔开,电解过程中阴离子向右移动,一段时间后两极均有气体生成。

①单质锰将会在
②写出发生在阴极上的所有电极反应方程式
您最近一年使用:0次



