1 . “宏观辨识与微观探析”是化学学科核心素养之一。下列过程的微观解释正确的是
A.醋酸除去茶壶中的水垢: |
B. 使酸性 使酸性 溶液褪色: 溶液褪色: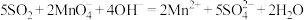 |
C. 溶液中通入少量 溶液中通入少量 |
D. 溶液中通入少量 溶液中通入少量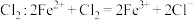 |
您最近一年使用:0次
2024-03-26更新
|
465次组卷
|
3卷引用:压轴题01?离子方程式与离子共存的判断(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
(已下线)压轴题01?离子方程式与离子共存的判断(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)2024届陕西省榆林市高三上学期第一次模拟检测理综试题-高中化学2024届陕西省商洛市高三上学期第二次模拟考试理综试题-高中化学
名校
解题方法
2 . 从废弃的声光器件( ,含
,含 、
、 、
、 杂质)中提取粗碲的工艺流程如图,已知
杂质)中提取粗碲的工艺流程如图,已知 性质与
性质与 相似,氧化沉碲得
相似,氧化沉碲得 ,下列说法错误的是
,下列说法错误的是
 ,含
,含 、
、 、
、 杂质)中提取粗碲的工艺流程如图,已知
杂质)中提取粗碲的工艺流程如图,已知 性质与
性质与 相似,氧化沉碲得
相似,氧化沉碲得 ,下列说法错误的是
,下列说法错误的是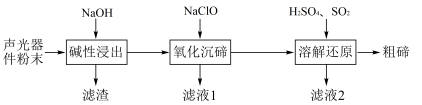
A.滤渣的主要成分为 |
| B.滤液1和滤液2混合可能产生白色沉淀 |
C.“氧化沉碲”中离子方程式为 |
| D.“溶解还原”中氧化剂和还原剂的物质的量之比为1:3 |
您最近一年使用:0次
2024-03-21更新
|
672次组卷
|
3卷引用:压轴题02 氧化还原反应的概念及规律(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
(已下线)压轴题02 氧化还原反应的概念及规律(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)山东省淄博市2024届高三一模化学试题四川省成都市盐道街中学2023-2024学年高一下学期3月月考化学试卷
名校
解题方法
3 . 1,2-丙二醇可用作制备不饱和聚酯树脂的原料,在化妆品、牙膏和香皂中可与甘油配合用作润湿剂。已知1,2-丙二醇脱氧脱水反应的催化循环机理如图所示。下列说法不正确的是

A. 的化学式为 的化学式为 |
B.催化过程中金属元素 成键数发生改变 成键数发生改变 |
C. 是该反应的催化剂,可通过降低反应的活化能来提高化学反应速率 是该反应的催化剂,可通过降低反应的活化能来提高化学反应速率 |
D.整个反应的化学方程式为 |
您最近一年使用:0次
2024-03-21更新
|
496次组卷
|
5卷引用:压轴题04?化学反应机理、历程、能垒图分析(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
(已下线)压轴题04?化学反应机理、历程、能垒图分析(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)(已下线)选择题11-15黑龙江省部分学校2024届高三第二次模拟考试化学试题2024届云南省楚雄彝族自治州高三下学期二模理综试题-高中化学黑龙江省牡丹江市第二高级中学2023-2024学年高三下学期考前热身卷化学(一)
名校
解题方法
4 . 金属镓在工业和医学中有广泛应用。一种利用锌粉置换渣(主要成分为 、
、 、
、 、
、 、
、 、
、 )制备粗镓的工艺流程如图所示:
)制备粗镓的工艺流程如图所示:
回答下列问题。
(1)浸渣的主要成分是___________ ,“富氧浸出”中高压 的作用是
的作用是___________ 。
(2)用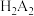 代表P204,RH代表YW100,“协同萃取”过程中发生反应:
代表P204,RH代表YW100,“协同萃取”过程中发生反应: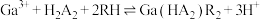 ,“协同萃取”后无机相含有的主要金属离子为
,“协同萃取”后无机相含有的主要金属离子为___________ , 随
随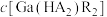 变化关系如图所示,“反萃取”加入稀硫酸的目的是
变化关系如图所示,“反萃取”加入稀硫酸的目的是___________ (用化学方程式表示)。 系中电势随pH变化的图像。“中和沉镓”时所调pH合理范围为4~
系中电势随pH变化的图像。“中和沉镓”时所调pH合理范围为4~___________ (填正整数),“碱溶造液”过程中发生反应的离子方程式为___________ 。___________ 。
(5)填隙方钴矿锑化物是一类新型热电材料,钴形成的六面体空隙中分别填充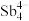 和As,该化合物的化学式为
和As,该化合物的化学式为___________ ;设阿伏加德罗常数的值为 ,已知该晶胞参数为a nm,则该晶体的密度是
,已知该晶胞参数为a nm,则该晶体的密度是___________  。
。
 、
、 、
、 、
、 、
、 、
、 )制备粗镓的工艺流程如图所示:
)制备粗镓的工艺流程如图所示:
回答下列问题。
(1)浸渣的主要成分是
 的作用是
的作用是(2)用
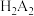 代表P204,RH代表YW100,“协同萃取”过程中发生反应:
代表P204,RH代表YW100,“协同萃取”过程中发生反应: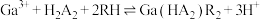 ,“协同萃取”后无机相含有的主要金属离子为
,“协同萃取”后无机相含有的主要金属离子为 随
随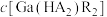 变化关系如图所示,“反萃取”加入稀硫酸的目的是
变化关系如图所示,“反萃取”加入稀硫酸的目的是
 系中电势随pH变化的图像。“中和沉镓”时所调pH合理范围为4~
系中电势随pH变化的图像。“中和沉镓”时所调pH合理范围为4~
(5)填隙方钴矿锑化物是一类新型热电材料,钴形成的六面体空隙中分别填充
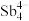 和As,该化合物的化学式为
和As,该化合物的化学式为 ,已知该晶胞参数为a nm,则该晶体的密度是
,已知该晶胞参数为a nm,则该晶体的密度是 。
。
您最近一年使用:0次
2024-03-01更新
|
477次组卷
|
4卷引用:大题01 化工流程综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
(已下线)大题01 化工流程综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)甘肃省平凉市静宁县第一中学2023-2024学年高三下学期开学化学试题甘肃省张掖市某重点校2023-2024学年高三下学期开年摸底联考化学试题2024届河北省百师联盟高三下学期开学摸底联考化学试题
2024高三下·全国·专题练习
5 . 8月1日起,为了国家信息安全,我国禁止镓和锗的出口,锗是一种重要的半导体材料,工业上用精硫锗矿(主要成分为GeS2)制取高纯度锗的工艺流程如图所示:

(1)COCl2分子中各原子均达到8电子稳定结构,其结构式为___________ 。
(2)800℃升华时通入N2的目的是:___________ 、___________ 。
(3)酸浸时Ge、S元素均被氧化到最高价态,写出该反应的离子方程式:___________ ,酸浸时温度不能过高的原因是___________ 。
(4)GeCl4易水解生成GeCl4·n H2O,证明GeCl4·n H2O沉淀洗涤干净的方法是___________ 。

(1)COCl2分子中各原子均达到8电子稳定结构,其结构式为
(2)800℃升华时通入N2的目的是:
(3)酸浸时Ge、S元素均被氧化到最高价态,写出该反应的离子方程式:
(4)GeCl4易水解生成GeCl4·n H2O,证明GeCl4·n H2O沉淀洗涤干净的方法是
您最近一年使用:0次
名校
解题方法
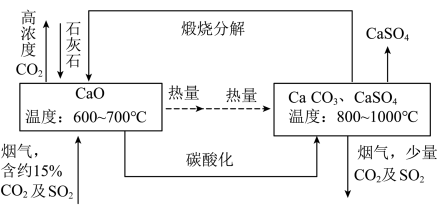
6 . 烟气中的 易造成酸雨,一种烟气脱硫技术如图所示.下列说法
易造成酸雨,一种烟气脱硫技术如图所示.下列说法错误 的是
 易造成酸雨,一种烟气脱硫技术如图所示.下列说法
易造成酸雨,一种烟气脱硫技术如图所示.下列说法
| A.煅烧分解产物CaO可以循环利用 | B.烟气脱硫过程中,氧元素发生了氧化反应 |
| C.图中涉及了分解反应、化合反应和氧化还原反应 | D.高浓度 收集后可用作灭火器的原料 收集后可用作灭火器的原料 |
您最近一年使用:0次
7 . 联氨(N2H4)又称“肼”,具高吸湿性、沸点386.5K、毒性强、还原性强等特性,燃烧释放出大量的热,常用于做火箭的燃料以及分析试剂中的还原剂。
I.联氨的制备
(1)联氨可用次氯酸钠溶液氧化过量的氨气制得,写出此反应得离子方程式___________ ;此反应中,被氧化的元素是_____ 。每生成1mol肼,转移的电子数为________ 。
Ⅱ .联氨的结构
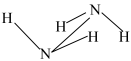
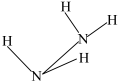
(2)联氨具强极性,推测下列结构最接近联氨分子真实结构的是________ 。
Ⅲ .联氨的性质
(3)①一定条件下, 联氨与二氯化钴(CoCl2)溶液能形成配位化合物Co(N2H4)6Cl2,关于此配位化合物的下列说法中不正确的是_____ 。
A.中心离子是Co2+ B.配位数是8
C.配位原子是N原子 D.向此配合物的溶液中滴入硝酸银,会产生白色沉淀
②联氨具高吸湿性,原因是_____ 。
③联氨水溶液与氨水类性质相似,将联氨溶于一定浓度的稀硫酸中,除形成N2H6SO4外,还可以生成的盐是_____ (填写化学式)。实验发现0.1mol·L-1N2H6SO4溶液显酸性,原因是_____ (用离子方程式表示),溶液中各种含氮微粒存在关系c(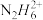 )+c(N2H6OH+)
)+c(N2H6OH+)____ 0.1-c(N2H4·2H2O)(选填“>”,“<”或“=”)。
(4)1mol液态联氨在空气中完全燃烧生成氮气和水蒸气放出621.74KJ的热量,此反应的热化学方程式是_______ 。肼有剧毒,但目前仍被普遍用作火箭的燃料,原因是________ 。
(5)联氨在一定条件下被亚硝酸氧化为叠氮酸(HN3),室温下亚硝酸、叠氮酸的电离平衡常数如表所示:
室温下,则同浓度的HNO2和HN3,其pH值:HNO2____ HN3(选填“>”、“<”或“=”),  反应性能类似卤素离子,则难溶物AgN3的Ksp表达式为
反应性能类似卤素离子,则难溶物AgN3的Ksp表达式为_________ 。
(6)某研究小组研究联氨和双氧水反应,查阅相关键能数据
并已知1molN2H4(l)→N2H4(g)与2molH2O2(l)→H2O2(g)共吸热23.76kJ,据此估算化学反应N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)的焓变ΔH=_______ kJ·mol-1,反应的熵变ΔS _____ 0(选填“>”、“<”)。研究小组利用此反应设计出如下电池,负极电极反应式:N2H4+4OH-−4e-=N2+4H2O。则正极电极反应式:________ 。
I.联氨的制备
(1)联氨可用次氯酸钠溶液氧化过量的氨气制得,写出此反应得离子方程式
Ⅱ .联氨的结构
(2)联氨具强极性,推测下列结构最接近联氨分子真实结构的是
|
|
| A. 反式结构 | B. 顺式结构 |
Ⅲ .联氨的性质
(3)①一定条件下, 联氨与二氯化钴(CoCl2)溶液能形成配位化合物Co(N2H4)6Cl2,关于此配位化合物的下列说法中不正确的是
A.中心离子是Co2+ B.配位数是8
C.配位原子是N原子 D.向此配合物的溶液中滴入硝酸银,会产生白色沉淀
②联氨具高吸湿性,原因是
③联氨水溶液与氨水类性质相似,将联氨溶于一定浓度的稀硫酸中,除形成N2H6SO4外,还可以生成的盐是
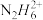 )+c(N2H6OH+)
)+c(N2H6OH+)(4)1mol液态联氨在空气中完全燃烧生成氮气和水蒸气放出621.74KJ的热量,此反应的热化学方程式是
(5)联氨在一定条件下被亚硝酸氧化为叠氮酸(HN3),室温下亚硝酸、叠氮酸的电离平衡常数如表所示:
| 酸名 | 亚硝酸(HNO2) | 叠氮酸(HN3) |
| 电离平衡常数 | 5.1 x 10-4 | 1.8 x 10-5 |
 反应性能类似卤素离子,则难溶物AgN3的Ksp表达式为
反应性能类似卤素离子,则难溶物AgN3的Ksp表达式为(6)某研究小组研究联氨和双氧水反应,查阅相关键能数据
| 化学键 | N-H | O-H | O-O | N-N | N≡N |
| 键能(kJ·mol-1) | 391 | 467 | 138 | 159 | 945 |
您最近一年使用:0次
解题方法
8 . 下列化学反应与方程式不相符 的是
A.黑火药爆炸:S+2KNO3+3C K2S+N2↑+3CO2↑ K2S+N2↑+3CO2↑ |
| B.加热氯化铜溶液:[Cu(H2O)4]2++4Cl-=[CuCl4]2-+4H2O |
C.向1mol FeBr2溶液中通入一定量氯气发生反应,当转移电子数1NA为时: |
D.以水杨酸为原料生产阿司匹林(乙酰水杨酸): |
您最近一年使用:0次
9 . 反应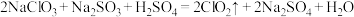 可制备高效消毒剂
可制备高效消毒剂 。对于该反应,下列说法正确的是
。对于该反应,下列说法正确的是
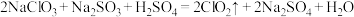 可制备高效消毒剂
可制备高效消毒剂 。对于该反应,下列说法正确的是
。对于该反应,下列说法正确的是A. 是氧化剂 是氧化剂 | B. 被氧化 被氧化 |
C. 是还原产物 是还原产物 | D.当转移1mol电子时,该反应生成1mol  |
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
10 . 下列离子方程式正确的是_______ 。
A.(2023·浙江卷)碘化亚铁溶液与等物质的量的氯气:
B.(2023·浙江卷)向次氯酸钙溶液通入足量二氧化碳: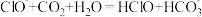
C.(2022·全国卷)将等物质的量浓度的Ba(OH)2和NH4HSO4溶液以体积比1∶2混合:Ba2++2OH-+2H++SO =BaSO4↓+2H2O
=BaSO4↓+2H2O
D.(2021·全国卷)硫酸铝溶液中滴加少量氢氧化钾溶液: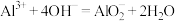
E.(2021·湖北卷)向次氯酸钙溶液中通入少量二氧化碳气体:ClO-+CO2+H2O=HClO+HCO
A.(2023·浙江卷)碘化亚铁溶液与等物质的量的氯气:

B.(2023·浙江卷)向次氯酸钙溶液通入足量二氧化碳:
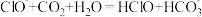
C.(2022·全国卷)将等物质的量浓度的Ba(OH)2和NH4HSO4溶液以体积比1∶2混合:Ba2++2OH-+2H++SO
 =BaSO4↓+2H2O
=BaSO4↓+2H2OD.(2021·全国卷)硫酸铝溶液中滴加少量氢氧化钾溶液:
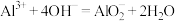
E.(2021·湖北卷)向次氯酸钙溶液中通入少量二氧化碳气体:ClO-+CO2+H2O=HClO+HCO

您最近一年使用:0次