1 . 我国的冶金工业十分发达,钢铁年产量已达到十亿吨,占世界产量的一半以上,同时有色金属产量也超过了七千万吨。
(1)铜是人类最早使用的金属,其电阻率小、延展性好,常用于制作电路板,在使用氯化铁溶液蚀刻铜制电路板时,发生反应的化学方程式为___________ 。
(2)铝与 溶液反应的化学方程式为
溶液反应的化学方程式为___________ ;铝的化学性质较活泼,但在空气中不会完全锈蚀,其原因是___________ 。
(3)电镀是一种常见的金属处理工艺,然而在生产过程中,电镀厂会产生大量的高毒性废水,将其直接排放会造成严重的污染。因此,废水的处理是电镀行业面临的主要问题之一。
①在电镀之前,镀件需要用酸性 溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的
溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的 固体,将
固体,将 还原为
还原为 ,则还原过程中发生反应的离子方程式为
,则还原过程中发生反应的离子方程式为___________ ,当有 被完全处理时,理论上需要加入
被完全处理时,理论上需要加入 的质量为
的质量为___________ 。
②为了减缓镀件表面的金属沉积速率,得到均匀、光滑的镀层,电解液中除重金属盐外,还需要加入剧毒的 。已知
。已知 中各原子均满足8电子稳定结构,则
中各原子均满足8电子稳定结构,则 的电子式为
的电子式为___________ 。在碱性的废电解液中通入氯气可以将 氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为___________ 。
(1)铜是人类最早使用的金属,其电阻率小、延展性好,常用于制作电路板,在使用氯化铁溶液蚀刻铜制电路板时,发生反应的化学方程式为
(2)铝与
 溶液反应的化学方程式为
溶液反应的化学方程式为(3)电镀是一种常见的金属处理工艺,然而在生产过程中,电镀厂会产生大量的高毒性废水,将其直接排放会造成严重的污染。因此,废水的处理是电镀行业面临的主要问题之一。
①在电镀之前,镀件需要用酸性
 溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的
溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的 固体,将
固体,将 还原为
还原为 ,则还原过程中发生反应的离子方程式为
,则还原过程中发生反应的离子方程式为 被完全处理时,理论上需要加入
被完全处理时,理论上需要加入 的质量为
的质量为②为了减缓镀件表面的金属沉积速率,得到均匀、光滑的镀层,电解液中除重金属盐外,还需要加入剧毒的
 。已知
。已知 中各原子均满足8电子稳定结构,则
中各原子均满足8电子稳定结构,则 的电子式为
的电子式为 氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
您最近一年使用:0次
2 . 下列类比或推理结果正确的是
A.已知 和浓硫酸可发生归中反应,则 和浓硫酸可发生归中反应,则 和硝酸也可发生归中反应 和硝酸也可发生归中反应 |
B.已知加热时Cu与 反应生成 反应生成 ,则加热时Cu与S反应生成 ,则加热时Cu与S反应生成 |
C.已知C、Si形成的氧化物晶体类型不同,可推知等物质的量的 和 和 中σ键数目不相同 中σ键数目不相同 |
D.已知氧化性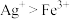 ,根据溶液中 ,根据溶液中 和 和 易发生氧化还原反应,推断溶液中 易发生氧化还原反应,推断溶液中 和 和 也易发生氧化还原反应 也易发生氧化还原反应 |
您最近一年使用:0次
3 . 已知离子反应: (已配平),下列说法错误的是
(已配平),下列说法错误的是
A. 是 是 | B. 是还原产物 是还原产物 |
C.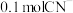 反应,转移的电子数目为 反应,转移的电子数目为 | D.该反应中 体现氧化性 体现氧化性 |
您最近一年使用:0次
名校
解题方法
4 . 含氯消毒剂在生产生活中被广泛用于杀菌、消毒和漂白。
(1)氯水具有漂白性,其中起漂白作用的物质是
(2)氯水需要避光保存,原因是
(3)通常将Cl2与NaOH或
 反应制成便于保存的消毒液或漂白粉。Cl2与NaOH溶液反应的离子方程式为
反应制成便于保存的消毒液或漂白粉。Cl2与NaOH溶液反应的离子方程式为(4)漂白粉[成分为
 、
、 和CaCl2]可用于鱼塘的消毒,防治水生生物细菌性疾病。使用注意事项如下:
和CaCl2]可用于鱼塘的消毒,防治水生生物细菌性疾病。使用注意事项如下:a.不宜用金属容器盛装
b.勿与酸性物质混用
c.水体中铵盐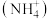 含量高,使用时产生NH3
含量高,使用时产生NH3
d.水体中亚硝酸盐(NO2)含量高,会降低其消毒效果
①注意事项a说明漂白粉具有
②为了验证注意事项b,向漂白粉中滴加稀硫酸,产生黄绿色气体,被还原的微粒是
③注意事项c中NH3产生的原因是
④从物质性质的角度解释注意事项d中漂白粉消毒效果降低的原因 浓度较高的鱼塘使用漂白粉,会使水中
浓度较高的鱼塘使用漂白粉,会使水中 含量升高,池水富营养化。)
含量升高,池水富营养化。)
您最近一年使用:0次
名校
解题方法
5 . 从宏观现象探究微观本质是重要的化学学科素养。为研究FeCl3溶液的性质,某小组同学进行了如下探究实验。
Ⅰ.配制FeCl3溶液
(1)先将FeCl3固体溶于浓盐酸,再稀释至指定浓度。浓盐酸的作用是______ 。
Ⅱ.FeCl3溶液与Na2CO3溶液反应
(2)向2mL1mol/L的Na2CO3溶液中加入2mL1mol/LFeCl3溶液,产生了红褐色沉淀和无色气体。反应的离子方程式为______ 。
Ⅲ.FeCl3溶液与Na2S溶液反应
(3)甲同学认为Fe3+和S2-的水解平衡相互促进并完全水解,实验中会观察到红褐色沉淀并闻到臭鸡蛋气味;乙同学认为会发生氧化还原反应,并预测还原产物为______ (填化学式)。两位同学实验如下:
(4)两位同学猜测实验a中的黑色沉淀可能是Fe2S3。继续实验:
根据实验b说明黑色沉淀是Fe2S3,写出实验b中Fe2S3与盐酸反应的化学方程式:______ 。
(5)①实验a中生成黑色沉淀Fe2S3的离子方程式为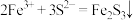 。该反应类型从四种基本反应类型看属于
。该反应类型从四种基本反应类型看属于______ 。
②实验a中Fe2S3溶解时生成的黄色固体为______ ,乙同学推测是因为随着FeCl3溶液滴加至一定量, 浓度增大,其氧化性增强,将Fe2S3氧化所致。
浓度增大,其氧化性增强,将Fe2S3氧化所致。
(6)已知: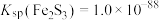 ,
,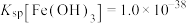 。针对实验a过程中未观察到红褐色沉淀,甲同学认为可能是产生的量比较少,被黑色所遮盖。乙同学根据
。针对实验a过程中未观察到红褐色沉淀,甲同学认为可能是产生的量比较少,被黑色所遮盖。乙同学根据 数据计算认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出该转化过程的离子方程式:
数据计算认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出该转化过程的离子方程式:______ 。
Ⅰ.配制FeCl3溶液
(1)先将FeCl3固体溶于浓盐酸,再稀释至指定浓度。浓盐酸的作用是
Ⅱ.FeCl3溶液与Na2CO3溶液反应
(2)向2mL1mol/L的Na2CO3溶液中加入2mL1mol/LFeCl3溶液,产生了红褐色沉淀和无色气体。反应的离子方程式为
Ⅲ.FeCl3溶液与Na2S溶液反应
(3)甲同学认为Fe3+和S2-的水解平衡相互促进并完全水解,实验中会观察到红褐色沉淀并闻到臭鸡蛋气味;乙同学认为会发生氧化还原反应,并预测还原产物为
| 实验a | 向稀Na2S溶液中逐滴加入FeCl3稀溶液,直至过量 |
| 实验现象 | 立即产生黑色沉淀并逐渐增加,无臭鸡蛋气味;FeCl3溶液过量后,黑色沉淀部分溶解,出现黄色沉淀 |
| 实验b | 将实验a中黑色沉淀过滤,并用CS2处理后洗净。向沉淀中加入6mol/L的盐酸,振荡试管 |
| 实验现象 | 加入盐酸后黑色沉淀溶解,转为乳黄色沉淀,并伴有臭鸡蛋气味 |
(5)①实验a中生成黑色沉淀Fe2S3的离子方程式为
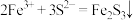 。该反应类型从四种基本反应类型看属于
。该反应类型从四种基本反应类型看属于②实验a中Fe2S3溶解时生成的黄色固体为
 浓度增大,其氧化性增强,将Fe2S3氧化所致。
浓度增大,其氧化性增强,将Fe2S3氧化所致。(6)已知:
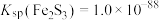 ,
,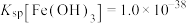 。针对实验a过程中未观察到红褐色沉淀,甲同学认为可能是产生的量比较少,被黑色所遮盖。乙同学根据
。针对实验a过程中未观察到红褐色沉淀,甲同学认为可能是产生的量比较少,被黑色所遮盖。乙同学根据 数据计算认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出该转化过程的离子方程式:
数据计算认为就算产生红褐色沉淀,也会转化为黑色沉淀,写出该转化过程的离子方程式:
您最近一年使用:0次
6 . 下图为氯元素的“价-类”二维图,下列说法错误的是
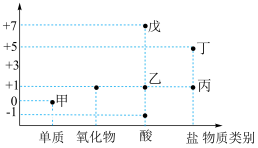

| A.甲可以通过一步反应生成乙 | B.丙的焰色为紫色,则丙为 |
| C.丁可用于实验室制取氧气 | D.戊中氯元素只具有氧化性 |
您最近一年使用:0次
名校
解题方法
7 . 资料显示, 能还原
能还原 、
、 ,某小组对此进行探究。
,某小组对此进行探究。
实验:将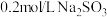 溶液滴入到物质a中,记录如下:
溶液滴入到物质a中,记录如下:
(1)用化学用语解释 溶液呈碱性的原因
溶液呈碱性的原因___________ 。
(2)经检验,I中白色沉淀是 。用酸性
。用酸性 溶液证实白色沉淀中含有
溶液证实白色沉淀中含有 ,现象是
,现象是___________ 。
(3)重新设计实验(III),证实了: 能还原
能还原 ,装置如下图所示。
,装置如下图所示。
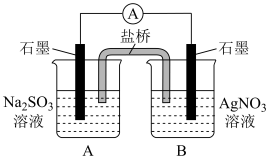
现象:i.电流表指针偏转。
ii.B中石墨电极上析出白色固体。
取出少量白色固体,洗涤后,___________ (填操作和现象),证明白色固体中含有Ag。
(4)经检验,II中的棕黄色沉淀不含 ,含有
,含有 、
、 和
和 。
。
资料: ,
, 。
。
①用稀 溶解沉淀,析出红色固体,说明棕黄色沉淀中含有
溶解沉淀,析出红色固体,说明棕黄色沉淀中含有___________ 。
②通过下列实验证实,沉淀中含有 和上层清液中仍检出了
和上层清液中仍检出了 (忽略空气的影响)。
(忽略空气的影响)。
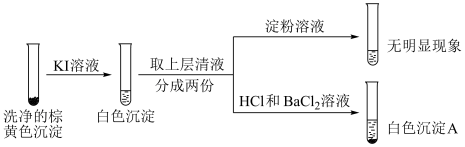
i.白色沉淀A是 。
。
ii.根据资料,上层清液加入淀粉后应该变蓝。分析现象与资料不符的原因:
原因一:KI未被氧化。则将 氧化的微粒是
氧化的微粒是___________ 。
原因二:KI被氧化,由于___________ (用离子方程式表示),所以无明显现象。
③当加入的KI过量且反应充分时,白色沉淀中不含Cu单质,上层清液中仍检出了 。结合物质组成、化学反应等解释上层清液中检出
。结合物质组成、化学反应等解释上层清液中检出 的原因
的原因___________ 。
小结:I中: 未能还原
未能还原 的原因与反应速率、离子浓度变化等因素有关。
的原因与反应速率、离子浓度变化等因素有关。
 能还原
能还原 、
、 ,某小组对此进行探究。
,某小组对此进行探究。实验:将
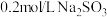 溶液滴入到物质a中,记录如下:
溶液滴入到物质a中,记录如下:| 序号 | 装置 | 物质a | 现象 |
| I |  2 mL 物质a | 饱和 溶液 溶液 | 产生白色沉淀 |
| II | 0.2 mol/L  溶液 溶液 | 溶液变绿,继续滴加产生棕黄色沉淀 |
(1)用化学用语解释
 溶液呈碱性的原因
溶液呈碱性的原因(2)经检验,I中白色沉淀是
 。用酸性
。用酸性 溶液证实白色沉淀中含有
溶液证实白色沉淀中含有 ,现象是
,现象是(3)重新设计实验(III),证实了:
 能还原
能还原 ,装置如下图所示。
,装置如下图所示。
现象:i.电流表指针偏转。
ii.B中石墨电极上析出白色固体。
取出少量白色固体,洗涤后,
(4)经检验,II中的棕黄色沉淀不含
 ,含有
,含有 、
、 和
和 。
。资料:
 ,
, 。
。①用稀
 溶解沉淀,析出红色固体,说明棕黄色沉淀中含有
溶解沉淀,析出红色固体,说明棕黄色沉淀中含有②通过下列实验证实,沉淀中含有
 和上层清液中仍检出了
和上层清液中仍检出了 (忽略空气的影响)。
(忽略空气的影响)。
i.白色沉淀A是
 。
。ii.根据资料,上层清液加入淀粉后应该变蓝。分析现象与资料不符的原因:
原因一:KI未被氧化。则将
 氧化的微粒是
氧化的微粒是原因二:KI被氧化,由于
③当加入的KI过量且反应充分时,白色沉淀中不含Cu单质,上层清液中仍检出了
 。结合物质组成、化学反应等解释上层清液中检出
。结合物质组成、化学反应等解释上层清液中检出 的原因
的原因小结:I中:
 未能还原
未能还原 的原因与反应速率、离子浓度变化等因素有关。
的原因与反应速率、离子浓度变化等因素有关。
您最近一年使用:0次
名校
解题方法
8 . 金属镓在工业和医学中有广泛应用。一种利用锌粉置换渣(主要成分为 、
、 、
、 、
、 、
、 、
、 )制备粗镓的工艺流程如图所示:
)制备粗镓的工艺流程如图所示:
回答下列问题。
(1)浸渣的主要成分是___________ ,“富氧浸出”中高压 的作用是
的作用是___________ 。
(2)用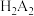 代表P204,RH代表YW100,“协同萃取”过程中发生反应:
代表P204,RH代表YW100,“协同萃取”过程中发生反应: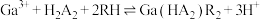 ,“协同萃取”后无机相含有的主要金属离子为
,“协同萃取”后无机相含有的主要金属离子为___________ , 随
随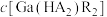 变化关系如图所示,“反萃取”加入稀硫酸的目的是
变化关系如图所示,“反萃取”加入稀硫酸的目的是___________ (用化学方程式表示)。 系中电势随pH变化的图像。“中和沉镓”时所调pH合理范围为4~
系中电势随pH变化的图像。“中和沉镓”时所调pH合理范围为4~___________ (填正整数),“碱溶造液”过程中发生反应的离子方程式为___________ 。___________ 。
(5)填隙方钴矿锑化物是一类新型热电材料,钴形成的六面体空隙中分别填充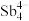 和As,该化合物的化学式为
和As,该化合物的化学式为___________ ;设阿伏加德罗常数的值为 ,已知该晶胞参数为a nm,则该晶体的密度是
,已知该晶胞参数为a nm,则该晶体的密度是___________  。
。
 、
、 、
、 、
、 、
、 、
、 )制备粗镓的工艺流程如图所示:
)制备粗镓的工艺流程如图所示:
回答下列问题。
(1)浸渣的主要成分是
 的作用是
的作用是(2)用
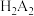 代表P204,RH代表YW100,“协同萃取”过程中发生反应:
代表P204,RH代表YW100,“协同萃取”过程中发生反应: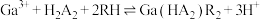 ,“协同萃取”后无机相含有的主要金属离子为
,“协同萃取”后无机相含有的主要金属离子为 随
随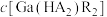 变化关系如图所示,“反萃取”加入稀硫酸的目的是
变化关系如图所示,“反萃取”加入稀硫酸的目的是
 系中电势随pH变化的图像。“中和沉镓”时所调pH合理范围为4~
系中电势随pH变化的图像。“中和沉镓”时所调pH合理范围为4~
(5)填隙方钴矿锑化物是一类新型热电材料,钴形成的六面体空隙中分别填充
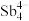 和As,该化合物的化学式为
和As,该化合物的化学式为 ,已知该晶胞参数为a nm,则该晶体的密度是
,已知该晶胞参数为a nm,则该晶体的密度是 。
。
您最近一年使用:0次
2024-03-01更新
|
469次组卷
|
4卷引用:甘肃省平凉市静宁县第一中学2023-2024学年高三下学期开学化学试题
甘肃省平凉市静宁县第一中学2023-2024学年高三下学期开学化学试题甘肃省张掖市某重点校2023-2024学年高三下学期开年摸底联考化学试题2024届河北省百师联盟高三下学期开学摸底联考化学试题(已下线)大题01 化工流程综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
9 . 小组同学探究金属钠与KMnO4溶液的反应。
①向KMnO4溶液中投入一小块金属钠,溶液颜色略有变浅;继续依次投入五小块金属钠,溶液变为绿色,产生气体
②向KMnO4溶液中加入少量NaOH固体,溶液颜色无明显变化;继续加入NaOH固体,溶液变为绿色,产生气体
已知:Mn2+无色,MnO 绿色。
绿色。
对比①②,下列有关说法不正确的是
①向KMnO4溶液中投入一小块金属钠,溶液颜色略有变浅;继续依次投入五小块金属钠,溶液变为绿色,产生气体
②向KMnO4溶液中加入少量NaOH固体,溶液颜色无明显变化;继续加入NaOH固体,溶液变为绿色,产生气体
已知:Mn2+无色,MnO
 绿色。
绿色。对比①②,下列有关说法不正确的是
| A.①中溶液颜色变浅,说明KMnO4发生还原反应 |
B.①中溶液变为绿色,说明MnO 被钠还原为MnO 被钠还原为MnO |
C.②中溶液变为绿色,可能发生4MnO +4OH-=4MnO +4OH-=4MnO +O2↑+2H2O +O2↑+2H2O |
| D.②中溶液颜色变化表明,溶液pH会影响物质氧化性或还原性的强弱 |
您最近一年使用:0次
2024-03-01更新
|
104次组卷
|
3卷引用:北京九中2023-2024学年高一下学期开学测试化学试题
名校
10 . 二氧化铅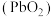 是一种强氧化剂,可以用作铅蓄电池的正极材料。
是一种强氧化剂,可以用作铅蓄电池的正极材料。 在酸性条件氧化
在酸性条件氧化 为
为 的方程式为
的方程式为 (方程式未配平)。已知:双氧水可以使酸性高锰酸钾溶液褪色。下列说法正确的是
(方程式未配平)。已知:双氧水可以使酸性高锰酸钾溶液褪色。下列说法正确的是
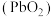 是一种强氧化剂,可以用作铅蓄电池的正极材料。
是一种强氧化剂,可以用作铅蓄电池的正极材料。 在酸性条件氧化
在酸性条件氧化 为
为 的方程式为
的方程式为 (方程式未配平)。已知:双氧水可以使酸性高锰酸钾溶液褪色。下列说法正确的是
(方程式未配平)。已知:双氧水可以使酸性高锰酸钾溶液褪色。下列说法正确的是A.X是 ,Y是 ,Y是 |
B.还原产物与氧化产物的物质的量之比为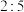 |
C.当生成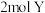 时,转移 时,转移 电子 电子 |
D.根据上述反应推测 不能氧化 不能氧化 |
您最近一年使用:0次
2024-02-27更新
|
215次组卷
|
3卷引用:山东省济宁市育才中学2023-2024学年高一下学期开学化学试题



