名校
解题方法
1 . 铁、铝是两种常见的金属,其合金在生产、生活中扮演着重要的角色,对混合物进行如下实验:

(1)操作X是___________ ;
(2)A与Cl2混合光照可能发生爆炸,A在该反应中作___________ (填“氧化剂”或“还原剂”);
(3)合金中加入足量NaOH溶液发生反应的离子方程式___________ ;
(4)加入稀盐酸发生反应的离子方程式为___________ ;
(5)向溶液D中加入NaOH溶液,观察到产生的现象是___________ ,写出相应的化学方程式:___________ ,___________ 。

(1)操作X是
(2)A与Cl2混合光照可能发生爆炸,A在该反应中作
(3)合金中加入足量NaOH溶液发生反应的离子方程式
(4)加入稀盐酸发生反应的离子方程式为
(5)向溶液D中加入NaOH溶液,观察到产生的现象是
您最近一年使用:0次
2024-03-12更新
|
53次组卷
|
2卷引用:青海省西宁市海湖中学2023-2024学年高一下学期开学考试化学试卷
解题方法
2 . 氯是重要的非金属元素,某校化学兴趣小组进行了下列实验。回答下列问题:
实验Ⅰ:利用如图所示装置制取并收集干燥的氯气。
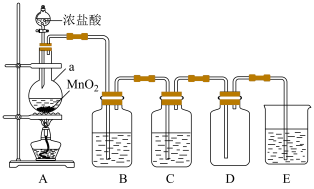
(1)仪器a的名称是___________ 。装置B、C中的试剂依次是___________ 、___________ 。
(2)装置E的作用为___________ ;写出该反应的化学方程式:___________ 。
实验Ⅱ:利用实验Ⅰ制得的氯气按下图所示装置进行氯气的性质探究。

已知:G中为干燥的有色布条、H中为紫色石蕊试液、I中为淀粉碘化钾溶液(淀粉遇碘单质变蓝)。
(3)G中干燥的有色布条不褪色,说明___________ 。
(4)H中的现象为___________ 。
(5)I中反应的离子方程式为___________ 。
实验Ⅰ:利用如图所示装置制取并收集干燥的氯气。

(1)仪器a的名称是
(2)装置E的作用为
实验Ⅱ:利用实验Ⅰ制得的氯气按下图所示装置进行氯气的性质探究。

已知:G中为干燥的有色布条、H中为紫色石蕊试液、I中为淀粉碘化钾溶液(淀粉遇碘单质变蓝)。
(3)G中干燥的有色布条不褪色,说明
(4)H中的现象为
(5)I中反应的离子方程式为
您最近一年使用:0次
2023-11-28更新
|
100次组卷
|
2卷引用:青海省西宁市大通县2023-2024学年高一上学期期末考试化学试题
名校
3 . 高铁酸钾( ,极易溶于水,溶液呈紫红色)是一种绿色净水剂,易溶于水。某小组在实验室条件下制备
,极易溶于水,溶液呈紫红色)是一种绿色净水剂,易溶于水。某小组在实验室条件下制备 并探究其性质。回答下列问题:
并探究其性质。回答下列问题:
实验(一)制备
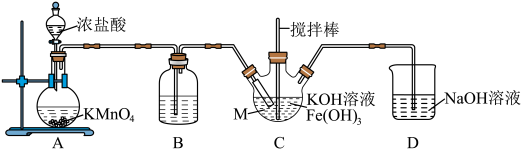
(1)仪器M的名称是_______ ,装置B的作用是_______ 。
(2)装置C中生成 的化学方程式为
的化学方程式为______ 。
(3)实验得知装置C中吸收 的量为装置A中生成
的量为装置A中生成 总量的75%,若装置D中的氧化产物只有0.02mol NaClO,且不考虑其他消耗,则理论上生成
总量的75%,若装置D中的氧化产物只有0.02mol NaClO,且不考虑其他消耗,则理论上生成 的质量为
的质量为_______ g。
实验(二)探究 的性质。
的性质。
Ⅰ.探究 在酸性条件下的稳定性。
在酸性条件下的稳定性。
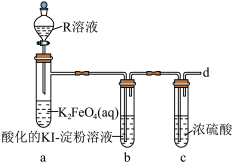
已知:实验中观察到试管b中溶液变为蓝色,试管a中溶液由紫红色变黄色并产生气泡。
(4)R溶液为_______ (填“稀硫酸”或“盐酸”),写出装置a中的离子方程式:______ ,不选择另一种酸的主要原因是_______ 。
(5)设计一种方案检验从d中逸出的气体:_______
Ⅱ.探究在酸性条件下的氧化性。
(6)向 溶液中滴加少量用稀硫酸酸化后的
溶液中滴加少量用稀硫酸酸化后的 溶液,溶液呈紫红色。
溶液,溶液呈紫红色。_______ (填“能”或“不能”)证明氧化性: ,原因是
,原因是_______ (用文字说明)。
 ,极易溶于水,溶液呈紫红色)是一种绿色净水剂,易溶于水。某小组在实验室条件下制备
,极易溶于水,溶液呈紫红色)是一种绿色净水剂,易溶于水。某小组在实验室条件下制备 并探究其性质。回答下列问题:
并探究其性质。回答下列问题:实验(一)制备


(1)仪器M的名称是
(2)装置C中生成
 的化学方程式为
的化学方程式为(3)实验得知装置C中吸收
 的量为装置A中生成
的量为装置A中生成 总量的75%,若装置D中的氧化产物只有0.02mol NaClO,且不考虑其他消耗,则理论上生成
总量的75%,若装置D中的氧化产物只有0.02mol NaClO,且不考虑其他消耗,则理论上生成 的质量为
的质量为实验(二)探究
 的性质。
的性质。Ⅰ.探究
 在酸性条件下的稳定性。
在酸性条件下的稳定性。
已知:实验中观察到试管b中溶液变为蓝色,试管a中溶液由紫红色变黄色并产生气泡。
(4)R溶液为
(5)设计一种方案检验从d中逸出的气体:
Ⅱ.探究在酸性条件下的氧化性。
(6)向
 溶液中滴加少量用稀硫酸酸化后的
溶液中滴加少量用稀硫酸酸化后的 溶液,溶液呈紫红色。
溶液,溶液呈紫红色。 ,原因是
,原因是
您最近一年使用:0次
2023-09-27更新
|
354次组卷
|
11卷引用:青海省海南州贵德高级中学2023-2024学年高三上学期10月月考化学试卷
青海省海南州贵德高级中学2023-2024学年高三上学期10月月考化学试卷河北省邢台市五岳联盟2023-2024学年高三上学期9月月考化学试题河北省部分学校2023-2024学年高三上学期9月月考化学试题河南省2023-2024学年高三上学期一轮复习阶段性检测(三)化学试题河南省驻马店市第一次联考2023-2024学年高三上学期9月月考化学试题江西省部分高中学校2024届高三上学期9月大联考化学试题福建省2023-2024学年高三上学期10月百万大联考化学试题 河南省洛阳市洛宁县第一高级中学2023-2024学年高三上学期阶段性考试(三)化学试题河北省保定部分高中2023-2024学年高三上学期9月月考化学试题福建省福州高新区第一中学(闽侯县第三中学)2023-20024学年高三上学期第一次月考化学试题河南省濮阳市油田第一中学2024届高三上学期第一次考试理科综合化学试题
名校
解题方法
4 . 在光照条件下,甲烷和氯气可以发生一系列反应。某课外活动小组利用如图所示装置探究甲烷和氯气的反应:
(2)用饱和食盐水而不用水的原因是_____ 。
(3)请写出生成一氯甲烷的化学反应方程式:_____ 。

| A.试管内液面上升,最终充满试管 | B.试管内气体颜色逐渐变深 |
| C.试管内壁出现油状液滴 | D.试管内有少量白雾生成 |
(3)请写出生成一氯甲烷的化学反应方程式:
您最近一年使用:0次
2023-06-21更新
|
157次组卷
|
3卷引用: 青海省西宁市2022-2023学年高一下学期期末考试化学试题
青海省西宁市2022-2023学年高一下学期期末考试化学试题上海市金山中学2022-2023学年高二下学期期末考试(合格)化学试题(已下线)综合02 期末压轴80题之非选择题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)
5 . 某同学设计如图装置(省略夹持装置)制备氯气并探究其性质,请回答下列问题。

(1)盛装浓盐酸的仪器名称为___________ ,试管内发生反应的化学方程式为___________ 。
(2)湿润的蓝色石蕊试纸先变红后褪色,请结合化学方程式和文字解释该现象产生的原因:___________ 。
(3)浸有溴化钠溶液的试纸变橙黄色,反应的离子方程式为___________ 。
(4)一段时间之后,湿润的淀粉碘化钾试纸会变蓝(I2遇淀粉会变蓝),___________ (填“能”或“不能”)说明Br2的氧化性比I2强;烧杯中的溶液可以为___________ (填标号),倒置漏斗的作用是___________ 。
A.饱和食盐水 B.饱和NaOH溶液
C.澄清石灰水 D.浓盐酸

(1)盛装浓盐酸的仪器名称为
(2)湿润的蓝色石蕊试纸先变红后褪色,请结合化学方程式和文字解释该现象产生的原因:
(3)浸有溴化钠溶液的试纸变橙黄色,反应的离子方程式为
(4)一段时间之后,湿润的淀粉碘化钾试纸会变蓝(I2遇淀粉会变蓝),
A.饱和食盐水 B.饱和NaOH溶液
C.澄清石灰水 D.浓盐酸
您最近一年使用:0次
2023-04-25更新
|
151次组卷
|
3卷引用:青海省海东市2022-2023学年高一下学期联考化学试题
青海省海东市2022-2023学年高一下学期联考化学试题 福建省龙岩市连城二中等校2022-2023学年高一下学期期中联考化学试题(已下线)第07讲 氯气的性质和次氯酸-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)
6 . 某实验小组在实验室制备干燥纯净的氯气,并探究其性质。所用仪器及药品如下图,回答问题。
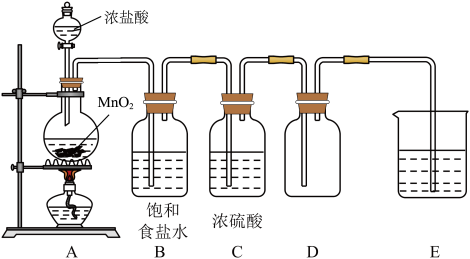
(1)根据实验设计上述制取氯气装置时,按照各装置的功能,连接顺序为:气体发生装置→___________ →收集装置→___________ 。
(2)A中盛放浓盐酸的仪器名称为___________ ,反应的化学方程式为___________ 。
(3)E中反应的离子方程式为___________ 。
(4)若要验证干燥的氯气不具有漂白性,可将下图所示装置连接到原实验装置中,连接的最佳位置是___________ (填选项序号)。
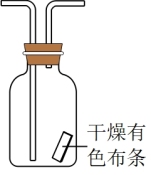
①A、B间 ②B、C间 ③C、D间
(5)该小组同学将制得的氯气配制成氯水,以探究FeI2的还原性。进行了如下实验:取一定量的FeI2溶液,向其中滴加少量新制氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:I-被Cl2氧化
假设2:Fe2+被Cl2氧化
完成下表,设计实验验证假设。
(6)若用MnO2与浓盐酸反应制取常温常压下1LCl2,计算:理论上需要MnO2的质量是___________ 克?(已知常温常压下气体的摩尔体积Vm≈24.5L/mol;写出计算过程,结果保留两位小数。)

(1)根据实验设计上述制取氯气装置时,按照各装置的功能,连接顺序为:气体发生装置→
(2)A中盛放浓盐酸的仪器名称为
(3)E中反应的离子方程式为
(4)若要验证干燥的氯气不具有漂白性,可将下图所示装置连接到原实验装置中,连接的最佳位置是

①A、B间 ②B、C间 ③C、D间
(5)该小组同学将制得的氯气配制成氯水,以探究FeI2的还原性。进行了如下实验:取一定量的FeI2溶液,向其中滴加少量新制氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:I-被Cl2氧化
假设2:Fe2+被Cl2氧化
完成下表,设计实验验证假设。
| 实验步骤 | 预期现象 | 结论 |
| ①取少量黄色溶液于试管中,滴加几滴淀粉溶液 | 假设1正确 | |
| ②取少量黄色溶液于试管中,滴加几滴 | 溶液变成血红色 | 假设2正确 |
您最近一年使用:0次
2023-04-05更新
|
154次组卷
|
2卷引用:青海省西宁市2022-2023学年高一上学期期末考试化学试题
7 . 化学小组同学设计如下实验验证氯气的部分性质,并探究氯水的成分和性质。
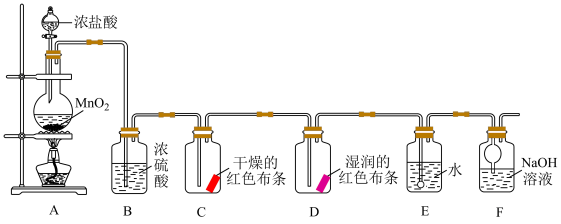
回答下列问题:
(1)装置A中发生反应的化学方程式为___________ 。
(2)验证干燥的氯气没有漂白性的现象为___________ 。
(3)装置F的作用是___________ 。
(4)研究新制氯水成分和性质。
以装置E的溶液进行下列实验
资料:淀粉的特征反应一一遇 变蓝色;
变蓝色; 。
。
①根据实验1可知,氧化性:
___________ (填“>”或“<”) 。
。
②实验2中证明溶液中含有___________ (填微粒的化学式)。
③若用实验3证明氯水中含有氯离子,则实验操作为___________ 。

回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)验证干燥的氯气没有漂白性的现象为
(3)装置F的作用是
(4)研究新制氯水成分和性质。
以装置E的溶液进行下列实验
| 实验序号 | 实验1 | 实验2 | 实验3 |
| 实验现象 |  | 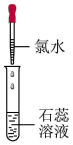 | |
| 实验现象 | 溶液变蓝 | 石蕊溶液先变红,后褪色 | 有白色沉淀生成 |
 变蓝色;
变蓝色; 。
。①根据实验1可知,氧化性:

 。
。②实验2中证明溶液中含有
③若用实验3证明氯水中含有氯离子,则实验操作为
您最近一年使用:0次
名校
解题方法
8 . 钌(Ru)是一种极其昂贵的稀有贵金属,广泛应用于电子、航空航天、石油化工、有机合成等领域。钌的矿产资源很少,因此从含钌废液中回收钌尤为重要。某含钌的废渣主要成分为Ru、 、
、 、
、 ,回收钌的工艺流程如下:
,回收钌的工艺流程如下:
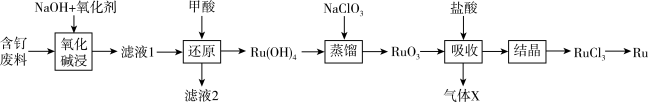
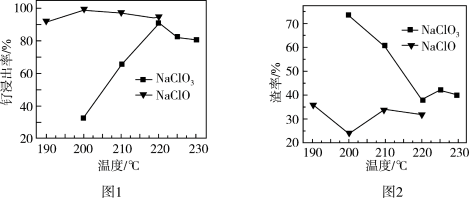
(1)“氧化碱浸”时,两种氧化剂在不同温度下对钌浸出率和渣率的影响分别如图1、图2所示,则适宜选择的氧化剂为_______ ;最佳反应温度为_______ 。
(2)滤液1中溶质的主要成分包括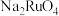 、
、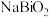 、
、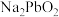 等,其中Si的存在形式为
等,其中Si的存在形式为_______ (填化学式); 转化为
转化为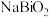 的化学方程式为
的化学方程式为_______ 。
(3)滤液1先用盐酸调节滤液pH,后用甲酸“还原”提取钌并同时生成 ,则该过程的离子方程式为
,则该过程的离子方程式为_______ ;“蒸馏”过程中氧化剂与还原剂的物质的量之比为_______ 。
(4)“吸收”过程产生的气体X经Y溶液吸收后,经进一步处理可以循环利用,则X和Y的化学式分别为_______ 、_______ 。
(5)可用氢气还原重量法测定产品中 的纯度,所得实验数据记录如下:
的纯度,所得实验数据记录如下:
则产品的纯度为_______ (保留小数点后一位)。
 、
、 、
、 ,回收钌的工艺流程如下:
,回收钌的工艺流程如下:
(1)“氧化碱浸”时,两种氧化剂在不同温度下对钌浸出率和渣率的影响分别如图1、图2所示,则适宜选择的氧化剂为

(2)滤液1中溶质的主要成分包括
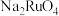 、
、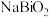 、
、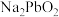 等,其中Si的存在形式为
等,其中Si的存在形式为 转化为
转化为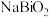 的化学方程式为
的化学方程式为(3)滤液1先用盐酸调节滤液pH,后用甲酸“还原”提取钌并同时生成
 ,则该过程的离子方程式为
,则该过程的离子方程式为(4)“吸收”过程产生的气体X经Y溶液吸收后,经进一步处理可以循环利用,则X和Y的化学式分别为
(5)可用氢气还原重量法测定产品中
 的纯度,所得实验数据记录如下:
的纯度,所得实验数据记录如下:| 实验序号 | 产品的质量/g | 固体Ru的质量/g |
| ① | 2.4225 | 1.0110 |
| ② | 2.4225 | 1.0090 |
| ③ | 2.4225 | 1.0100 |
您最近一年使用:0次
2022-08-03更新
|
922次组卷
|
4卷引用:青海省海东市第一中学2022届高三第二次模拟考试理科综合化学试题
青海省海东市第一中学2022届高三第二次模拟考试理科综合化学试题(已下线)专题讲座(八) 无机化工流程题的解题策略(练)-2023年高考化学一轮复习讲练测(全国通用)山东省历城第二中学等学校2023届高三上学期10月月考联合考试化学试题 山东省泰安新泰市第一中学(实验部)2023-2024学年高三上学期第一次质量检测化学试题
解题方法
9 . 某学生利用以下装置探究氯气与氨气之间的反应,A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
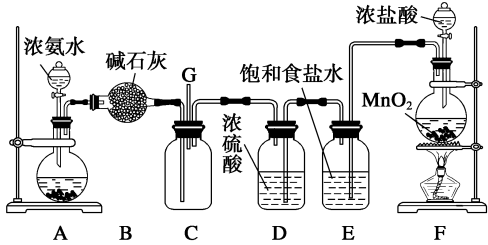
(1)装置A中的烧瓶内固体可选用___________(填字母)。
(2)装置B的作用为___________ ;装置E的作用为___________ 。
(3)通入装置C的两导管要左边长、右边短,原因是___________ 。
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一、请写出该反应的化学方程式:___________ 。
(5)从装置C的G处逸出的尾气中可能含有有毒的黄绿色气体,为避免空气污染可将尾气通入___________ 溶液。

(1)装置A中的烧瓶内固体可选用___________(填字母)。
| A.生石灰 | B.二氧化硅 | C.五氧化二磷 | D.烧碱 |
(3)通入装置C的两导管要左边长、右边短,原因是
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一、请写出该反应的化学方程式:
(5)从装置C的G处逸出的尾气中可能含有有毒的黄绿色气体,为避免空气污染可将尾气通入
您最近一年使用:0次
2022-06-22更新
|
208次组卷
|
2卷引用:青海玉树州三校2021-2022学年高一上学期期末考试化学试题
名校
解题方法
10 . 天然脑砂含少量 ,《唐本草》记载脑砂入药可以散瘀消肿。某学习小组设计下列步骤制取
,《唐本草》记载脑砂入药可以散瘀消肿。某学习小组设计下列步骤制取 ,并进行天然脑砂含量的测定。请回答相关问题:
,并进行天然脑砂含量的测定。请回答相关问题:
步骤Ⅰ:用氨气与适量氯气反应制取 。
。_______ ;若用浓盐酸与 反应制取氯气,则该反应的离子方程式为
反应制取氯气,则该反应的离子方程式为_______ 。
(2)要得到干燥纯净的氯气,C的作用是_______ 。
(3)氨气与适量氯气混合反应可生成 和一种无污染的气体,利用E装置模拟该反应,氨气应从
和一种无污染的气体,利用E装置模拟该反应,氨气应从_______ (填“f”或“g”)通入,反应的化学方程式为_______ 。
步骤Ⅱ:天然脑砂中 含量的测定。
含量的测定。
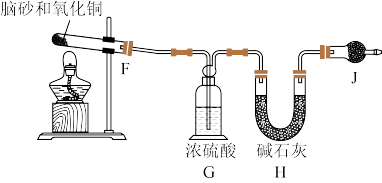
准确称取一定质量脑砂,与足量的氧化铜混合,如图所示进行实验。
已知: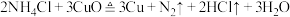 。
。 含量的测定,请完成下列实验步骤:加热前,称量H装置的总质量;当观察到G中不再有气泡冒出时,停止加热,冷却,
含量的测定,请完成下列实验步骤:加热前,称量H装置的总质量;当观察到G中不再有气泡冒出时,停止加热,冷却,_______ 。
(5)如果不用J装置,测出 的含量将
的含量将_______ (填“偏高”“偏低”或“无影响”)。
 ,《唐本草》记载脑砂入药可以散瘀消肿。某学习小组设计下列步骤制取
,《唐本草》记载脑砂入药可以散瘀消肿。某学习小组设计下列步骤制取 ,并进行天然脑砂含量的测定。请回答相关问题:
,并进行天然脑砂含量的测定。请回答相关问题:步骤Ⅰ:用氨气与适量氯气反应制取
 。
。
 反应制取氯气,则该反应的离子方程式为
反应制取氯气,则该反应的离子方程式为(2)要得到干燥纯净的氯气,C的作用是
(3)氨气与适量氯气混合反应可生成
 和一种无污染的气体,利用E装置模拟该反应,氨气应从
和一种无污染的气体,利用E装置模拟该反应,氨气应从步骤Ⅱ:天然脑砂中
 含量的测定。
含量的测定。准确称取一定质量脑砂,与足量的氧化铜混合,如图所示进行实验。
已知:
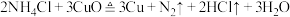 。
。
 含量的测定,请完成下列实验步骤:加热前,称量H装置的总质量;当观察到G中不再有气泡冒出时,停止加热,冷却,
含量的测定,请完成下列实验步骤:加热前,称量H装置的总质量;当观察到G中不再有气泡冒出时,停止加热,冷却,(5)如果不用J装置,测出
 的含量将
的含量将
您最近一年使用:0次
2022-06-19更新
|
371次组卷
|
3卷引用:青海省西宁市第五中学2023-2024学年高一下学期4月月考化学试题



