1 . 含氯化合物在日常生活中有多种用途,根据要求完成下列问题:
(1)漂白粉的有效成分是___________ ,家庭中使用漂白粉加水配置消毒液,与空气发生反应的化学方程式为___________ 。
(2)84消毒液的有效成分中NaClO中Cl的化合价为___________ ,请写出氯气与NaOH反应的化学方程式:___________ 。向NaOH溶液中通入11.2L(标准状况)氯气恰好完全反应生成三种含氯盐:0.7molNaCl、0.2molNaClO和X。则X是___________ 。
a.0.1molNaClO4 b.0.1molNaClO3 c.0.2molNaClO2 d.0.1molNaClO2
(3)日常生活中84消毒液若与洁厕灵(较浓的盐酸)混用,发生反应:NaClO+2HCl=NaCl+Cl2+H2O,该反应的氧化剂为___________ ,被氧化的物质为___________ 。若反应中电子转移为2mol,生成的氯气为___________ mol。
(1)漂白粉的有效成分是
(2)84消毒液的有效成分中NaClO中Cl的化合价为
a.0.1molNaClO4 b.0.1molNaClO3 c.0.2molNaClO2 d.0.1molNaClO2
(3)日常生活中84消毒液若与洁厕灵(较浓的盐酸)混用,发生反应:NaClO+2HCl=NaCl+Cl2+H2O,该反应的氧化剂为
您最近一年使用:0次
2022高一·全国·专题练习
解题方法
2 . 实验结束,这些消毒液可以用于室内消毒,但是水蒸发干后,物品表面会留有白色污渍,这个白色污渍是什么________ ?
您最近一年使用:0次
3 . 碱式次氯酸镁[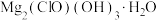 ]微溶于水,是一种有开发价值的无机抗菌剂。请回答:
]微溶于水,是一种有开发价值的无机抗菌剂。请回答:
(1)工业上利用 、NaOH、
、NaOH、 为原料合成碱式次氯酸镁,写出发生反应的化学方程式
为原料合成碱式次氯酸镁,写出发生反应的化学方程式_______ 。
(2)碱式次氯酸镁也可通过电解法制备,在无隔膜状况下以铁为阴极、 为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是
为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是_______ ,阴极电极反应方程式为_______ 。
(3)碱式次氯酸镁经醋酸酸化后杀菌功能增强,原因是_______ (用离子方程式表示)。
(4)碱式次氯酸镁( )的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用
)的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用 标准溶液测定生成的
标准溶液测定生成的 ,将碘单质折算为
,将碘单质折算为 ,有效氯含量
,有效氯含量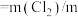 (样品)。则产品的理论有效氯含量为
(样品)。则产品的理论有效氯含量为_______ 。
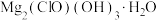 ]微溶于水,是一种有开发价值的无机抗菌剂。请回答:
]微溶于水,是一种有开发价值的无机抗菌剂。请回答:(1)工业上利用
 、NaOH、
、NaOH、 为原料合成碱式次氯酸镁,写出发生反应的化学方程式
为原料合成碱式次氯酸镁,写出发生反应的化学方程式(2)碱式次氯酸镁也可通过电解法制备,在无隔膜状况下以铁为阴极、
 为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是
为阳极电解氯化镁溶液制得。采取无隔膜工艺的目的是(3)碱式次氯酸镁经醋酸酸化后杀菌功能增强,原因是
(4)碱式次氯酸镁(
 )的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用
)的品质可通过其中的有效氯含量来衡量,测定有效氯的方法是:称取一定质量的样品,加入适量乙酸和KI溶液溶解,再用 标准溶液测定生成的
标准溶液测定生成的 ,将碘单质折算为
,将碘单质折算为 ,有效氯含量
,有效氯含量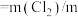 (样品)。则产品的理论有效氯含量为
(样品)。则产品的理论有效氯含量为
您最近一年使用:0次
名校
4 . 请按要求回答下列问题:
(1)Al2O3能溶于强酸或强碱溶液生成盐和水,则Al2O3是一种_______ (填“酸性”、“碱性”或“两性”) 氧化物。
(2)氨气极易溶于水,其水溶液显_______ (填“酸”、“碱”或“中”)性。
(3)在常温下,将Cl2通入NaOH溶液中,可以得到漂白液。请写出该反应的离子方程式_______ 。
(4)高锰酸钾与浓盐酸在常温下能反应生成氯气,请写出反应的化学方程式_______ 。
(5)等质量的下列气体HCl、NH3、CO2、O2四种气体中,在相同温度和相同压强条件下,体积最大的是_______ 。
(6)设NA为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则cg该气体在标准状况下的体积约是_______ L (用NA的式子表示)。
(1)Al2O3能溶于强酸或强碱溶液生成盐和水,则Al2O3是一种
(2)氨气极易溶于水,其水溶液显
(3)在常温下,将Cl2通入NaOH溶液中,可以得到漂白液。请写出该反应的离子方程式
(4)高锰酸钾与浓盐酸在常温下能反应生成氯气,请写出反应的化学方程式
(5)等质量的下列气体HCl、NH3、CO2、O2四种气体中,在相同温度和相同压强条件下,体积最大的是
(6)设NA为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则cg该气体在标准状况下的体积约是
您最近一年使用:0次
名校
5 . 完成下列问题
(1)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用某溶液吸收多余的氯气,原理是(用化学方程式表示)___________ ;
(2)长期露置于空气中的漂白粉,加稀盐酸后产生的气体是___________(用字母代号填)
(3)石英砂不能与碱性物质共同存放,以NaOH为例,用化学方程式表示其原因:___________ 。
(1)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用某溶液吸收多余的氯气,原理是(用化学方程式表示)
(2)长期露置于空气中的漂白粉,加稀盐酸后产生的气体是___________(用字母代号填)
| A.O2 | B.Cl2 | C.CO2 | D.HClO |
您最近一年使用:0次
2022-04-05更新
|
46次组卷
|
2卷引用:安徽工业大学附属中学2020-2021学年高二上学期文理分科考试化学试题
解题方法
6 . “84”消毒液是一种常见的含氯消毒剂。
(1)“84”消毒液的有效成分为_______ (用化学式表示)。
(2)常温下,将氯气通入NaOH溶液中可制得“84”消毒液。写出反应的离子方程式:_______ 。
(3)针对不同物品消毒,“84”消毒液需要稀释到不同浓度使用。取含次氯酸钠0.2mol·L-1的“84”消毒液1mL,加水稀释至100mL,稀释后的溶液中次氯酸钠的物质的量浓度为_______  。
。
(1)“84”消毒液的有效成分为
(2)常温下,将氯气通入NaOH溶液中可制得“84”消毒液。写出反应的离子方程式:
(3)针对不同物品消毒,“84”消毒液需要稀释到不同浓度使用。取含次氯酸钠0.2mol·L-1的“84”消毒液1mL,加水稀释至100mL,稀释后的溶液中次氯酸钠的物质的量浓度为
 。
。
您最近一年使用:0次
名校
解题方法
7 . 按要求书写化学方程式或离子方程式。
(1)工业上用将氯气通入石灰乳中制漂白粉,相应的化学方程式为___________ 。
(2)硫酸厂附近的新收集雨水pH不断降低,相应的化学方程式为___________ 。
(3)木炭和浓硫酸混合加热产生大量的CO2和SO2,相应的化学方程式为___________ 。
(4)工业上用FeCl3溶液腐蚀铜线路板,相应的离子 方程式为___________ 。
(5)SO2能使氯水褪色,相应的离子 方程式为___________ 。
(1)工业上用将氯气通入石灰乳中制漂白粉,相应的化学方程式为
(2)硫酸厂附近的新收集雨水pH不断降低,相应的化学方程式为
(3)木炭和浓硫酸混合加热产生大量的CO2和SO2,相应的化学方程式为
(4)工业上用FeCl3溶液腐蚀铜线路板,相应的
(5)SO2能使氯水褪色,相应的
您最近一年使用:0次
名校
解题方法
8 . 利用如图所示的“价-类”二维图,可以从物质类别、化合价角度认识含氯元素的物质的性质及其转化关系,图中甲~辛均为含氯元素的物质。回答下列问题:
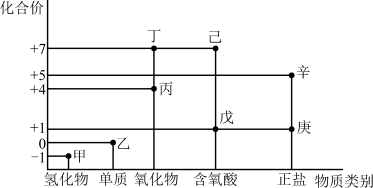
(1)戊的化学式为_______ 。
(2)甲、乙、丙中,属于非电解质的是_______ (填化学式)。根据氯元素的化合价判断乙_______ (填序号)。
a.只有氧化性 b.只有还原性 c.既有氧化性又有还原性
(3)庚是“84”消毒液的有效成分,能有效灭菌,某化学社团模拟生产厂家配制了 “84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:
“84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:
①写出氯气和 溶液生产此消毒液的离子方程式
溶液生产此消毒液的离子方程式_______ 。该“84消毒液”有效成分的物质的量浓度为_______ 。
②“84消毒液”与稀硫酸混合使用可增强消毒能力,该社团成员用 的浓硫酸配制
的浓硫酸配制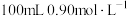 的稀硫酸用于增强“84消毒液”的消毒能力。若所配制的稀硫酸浓度偏高,则可能的原因是
的稀硫酸用于增强“84消毒液”的消毒能力。若所配制的稀硫酸浓度偏高,则可能的原因是_______ 。
A.配制前,容量瓶中有少量蒸馏水
B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容
D.未洗涤烧杯和玻璃棒

(1)戊的化学式为
(2)甲、乙、丙中,属于非电解质的是
a.只有氧化性 b.只有还原性 c.既有氧化性又有还原性
(3)庚是“84”消毒液的有效成分,能有效灭菌,某化学社团模拟生产厂家配制了
 “84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:
“84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:| 84消毒液 |
(有效成分) (规格)  (质量分数) 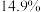 (密度)  |
 溶液生产此消毒液的离子方程式
溶液生产此消毒液的离子方程式②“84消毒液”与稀硫酸混合使用可增强消毒能力,该社团成员用
 的浓硫酸配制
的浓硫酸配制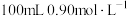 的稀硫酸用于增强“84消毒液”的消毒能力。若所配制的稀硫酸浓度偏高,则可能的原因是
的稀硫酸用于增强“84消毒液”的消毒能力。若所配制的稀硫酸浓度偏高,则可能的原因是A.配制前,容量瓶中有少量蒸馏水
B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容
D.未洗涤烧杯和玻璃棒
您最近一年使用:0次
2022-02-28更新
|
361次组卷
|
2卷引用:重庆第二外国语学校2021-2022学年高一上学期期末考试化学试题
解题方法
9 . 物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。下图为氯元素的单质及其化合物的“价~类”二维图。请回答下列问题:

(1)二维图中X的化学式(分子式)为_______ 。
(2)“84”消毒液(有效成分为NaClO)进行环境消毒时,会与空气中的CO2发生反应生成NaHCO3与次氯酸。写出该反应的离子方程式_______ 。
(3)舍勒是最早制取Cl2的化学家,请你写出舍勒制取Cl2的离子方程式_______ ,实验室对Cl2进行尾气处理的离子方程式为_______ 。
(4)二氧化氯(ClO2)是一种新型自来水消毒剂。工业上一种制备ClO2的反应原理为2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O,该反应中H2O2作_______ (填“氧化剂”或“还原剂”)。

(1)二维图中X的化学式(分子式)为
(2)“84”消毒液(有效成分为NaClO)进行环境消毒时,会与空气中的CO2发生反应生成NaHCO3与次氯酸。写出该反应的离子方程式
(3)舍勒是最早制取Cl2的化学家,请你写出舍勒制取Cl2的离子方程式
(4)二氧化氯(ClO2)是一种新型自来水消毒剂。工业上一种制备ClO2的反应原理为2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O,该反应中H2O2作
您最近一年使用:0次
10 . 按要求回答下列问题:
(1) 个
个 分子的质量为
分子的质量为_______ g。
(2)常温下可用铁槽车运输浓硫酸,原因是_______ 。
(3)氯气可用于制备“战略金属”钛,有关反应为: ,请用双线桥标出该反应中电子转移的方向和数目
,请用双线桥标出该反应中电子转移的方向和数目_______ 。
(4)氯气发生泄漏时,人员应_______ (填字母);同时喷 溶液进行吸收,发生反应的化学方程式为
溶液进行吸收,发生反应的化学方程式为_______ 。
a.顺风向高处转移 b.顺风向低处转移 c.逆风向高处转移 d.逆风向低处转移
(5)盛放 溶液的玻璃试剂瓶应选用
溶液的玻璃试剂瓶应选用_______ (填“玻璃”或“橡胶”)塞。
(1)
 个
个 分子的质量为
分子的质量为(2)常温下可用铁槽车运输浓硫酸,原因是
(3)氯气可用于制备“战略金属”钛,有关反应为:
 ,请用双线桥标出该反应中电子转移的方向和数目
,请用双线桥标出该反应中电子转移的方向和数目(4)氯气发生泄漏时,人员应
 溶液进行吸收,发生反应的化学方程式为
溶液进行吸收,发生反应的化学方程式为a.顺风向高处转移 b.顺风向低处转移 c.逆风向高处转移 d.逆风向低处转移
(5)盛放
 溶液的玻璃试剂瓶应选用
溶液的玻璃试剂瓶应选用
您最近一年使用:0次



