名校
1 . 氨在能源、化肥生产等领域有着非常重要的用途。
(1)氨气是重要的化工原料,回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:_______ ;
②下列试剂不能用于干燥NH3的是_______ (填字母)。
A.浓硫酸 B.碱石灰 C.NaOH固体
③氨气可以合成多种物质,写出氨催化氧化的化学方程式:_______ ;
(2)氨可用于燃料电池,氨易液化,运输和储存方便,安全性能更高。新型NH3-O2燃料电池原理如下图所示:

电极1为_______ (填“正极”或“负极”),电极2的反应式为_______ 。
(3) 工业生产中利用氨水吸收SO2和NO2,原理如下图所示:

NO2被吸收过程的离子方程式是_______ 。
(1)氨气是重要的化工原料,回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:
②下列试剂不能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.NaOH固体
③氨气可以合成多种物质,写出氨催化氧化的化学方程式:
(2)氨可用于燃料电池,氨易液化,运输和储存方便,安全性能更高。新型NH3-O2燃料电池原理如下图所示:

电极1为
(3) 工业生产中利用氨水吸收SO2和NO2,原理如下图所示:

NO2被吸收过程的离子方程式是
您最近一年使用:0次
2 . 已知氨可以与灼热的氧化铜反应生成氮气和金属铜,用下图中的装置可以实现该反应(部分夹持仪器已略去)。回答下列问题:

(1)组装好仪器后,应先检查整套装置的气密性,具体操作为___________ 。
(2)实验室用装置A制取氨气,反应的化学方程式为___________ 。
(3)B的仪器名称为___________ 。
(4)实验开始一段时间后装置C中观察到的现象是___________ ,反应的化学方程式为___________ ,该反应体现氨气的___________ (填“还原性”或“氧化性”)。
(5)实验后往D中收集到的液体滴加酚酞试液,溶液变成红色,原因是___________ (用电离方程式表示)。

(1)组装好仪器后,应先检查整套装置的气密性,具体操作为
(2)实验室用装置A制取氨气,反应的化学方程式为
(3)B的仪器名称为
(4)实验开始一段时间后装置C中观察到的现象是
(5)实验后往D中收集到的液体滴加酚酞试液,溶液变成红色,原因是
您最近一年使用:0次
3 . 下列颜色变化过程,气体被还原的是
A. 2使无色 2使无色 溶液变黄 溶液变黄 |
B. 使紫色酸性高锰酸钾溶液褪色 使紫色酸性高锰酸钾溶液褪色 |
C. 使黑色的 使黑色的 固体变红 固体变红 |
D. 使淡黄色过氧化钠固体变为白色 使淡黄色过氧化钠固体变为白色 |
您最近一年使用:0次
解题方法
4 . Ⅰ.硫元素是动植物生长不可缺少的元素,下图是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。
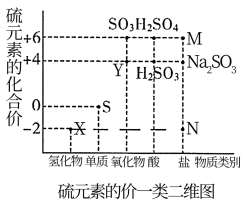
(1)图中X对应的物质是___________ ,将X气体通入 溶液中会出现淡黄色沉淀,反应物
溶液中会出现淡黄色沉淀,反应物 作
作___________ 剂(填“氧化”或“还原”)。
(2)空气中易造成硫酸酸雨的主要气体是___________ (填化学式);
(3)请写出铜和浓硫酸反应的化学方程式___________ 。
Ⅱ.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:
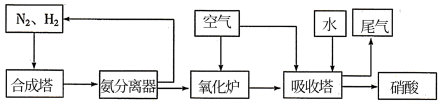
(1)氧化炉中, 转化为NO的化学方程式为
转化为NO的化学方程式为___________ 。
(2)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的___________ 性质。
(3)写出硝酸的电离方程式___________ 。
(4)吸收塔中出来的尾气可用 溶液吸收,主要反应为:
溶液吸收,主要反应为:
a.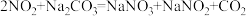
b.
根据反应b,每产生11.2L(标准状况下) ,吸收液质量将增加
,吸收液质量将增加___________ g。

(1)图中X对应的物质是
 溶液中会出现淡黄色沉淀,反应物
溶液中会出现淡黄色沉淀,反应物 作
作(2)空气中易造成硫酸酸雨的主要气体是
(3)请写出铜和浓硫酸反应的化学方程式
Ⅱ.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:

(1)氧化炉中,
 转化为NO的化学方程式为
转化为NO的化学方程式为(2)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的
(3)写出硝酸的电离方程式
(4)吸收塔中出来的尾气可用
 溶液吸收,主要反应为:
溶液吸收,主要反应为:a.
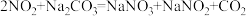
b.

根据反应b,每产生11.2L(标准状况下)
 ,吸收液质量将增加
,吸收液质量将增加
您最近一年使用:0次
解题方法
5 . 工业上制取硝酸铵的流程图如图,请回答下列问题:
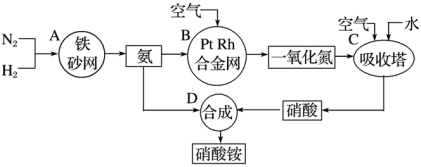
(1)在工业制硝酸的生产中,B中发生反应的化学方程式为:_______ 。
(2)在合成硝酸的吸收塔中通入空气的目的是:_______ 。
(3)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
碱液吸收法:NO+NO2+2NaOH2NaNO2+H2O
NH3还原法: NH3+ NO2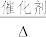 N2+ H2O
N2+ H2O
①配平NH3还原法的化学方程式_______ 。
②以上两种方法中,符合绿色化学的是_______ 。
③某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是96%、NO制HNO3的产率是92%,则制HNO3所用去的NH3的质量占总耗NH3质量(不考虑其它损耗)的百分比含量为_______ (计算结果精确到0.1)。

(1)在工业制硝酸的生产中,B中发生反应的化学方程式为:
(2)在合成硝酸的吸收塔中通入空气的目的是:
(3)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
碱液吸收法:NO+NO2+2NaOH2NaNO2+H2O
NH3还原法: NH3+ NO2
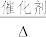 N2+ H2O
N2+ H2O①配平NH3还原法的化学方程式
②以上两种方法中,符合绿色化学的是
③某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是96%、NO制HNO3的产率是92%,则制HNO3所用去的NH3的质量占总耗NH3质量(不考虑其它损耗)的百分比含量为
您最近一年使用:0次
名校
解题方法
6 . 氨对人类生产、生活有重要影响。回答下列问题:
(1)合成氨是工业上人工固氮的重要方法,写出该反应的化学方程式:_______ 。
(2)氨气的制备

①氨气的发生装置可以选择图中的_______ (填字母),反应的化学方程式为_______ 。
②欲收集一瓶干燥的氨气,选择图中的装置,其连接顺序为:发生装置→_______ (按气流方向,用小写字母表示)。
③装置 中漏斗的作用是
中漏斗的作用是_______ 。
(3)氨的催化氧化:如图是探究氨的催化氧化简易装置,实验时观察到锥形瓶中铂丝保持红热,有红棕色气体或白烟产生。红棕色气体成分是_______ (填化学式,下同),白烟的成分是_______ 。

(1)合成氨是工业上人工固氮的重要方法,写出该反应的化学方程式:
(2)氨气的制备

①氨气的发生装置可以选择图中的
②欲收集一瓶干燥的氨气,选择图中的装置,其连接顺序为:发生装置→
③装置
 中漏斗的作用是
中漏斗的作用是(3)氨的催化氧化:如图是探究氨的催化氧化简易装置,实验时观察到锥形瓶中铂丝保持红热,有红棕色气体或白烟产生。红棕色气体成分是

您最近一年使用:0次
2021-07-12更新
|
234次组卷
|
2卷引用:安徽省合肥市六校2020-2021学年高一下学期期末联考化学试题
解题方法
7 . 部分含氮物质的类别与相应氮元素的化合价关系如图所示。下列说法正确的是
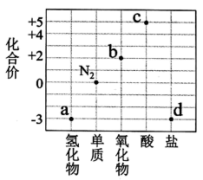

A.a与b在一定条件下可发生反应生成 |
| B.汽车尾气中的b物质是汽油不完全燃烧导致的 |
C.常温下,金属 在c的浓溶液中会钝化 在c的浓溶液中会钝化 |
| D.室温时,d的水溶液一定呈酸性 |
您最近一年使用:0次
8 . 氮的循环涉及多种化学物质(下图中的W、M、X、Y、Z均是化学物质)
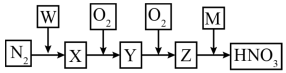
(1)由N2→X是工业合成氨的反应,每消耗7gN2放出23.4kJ的能量,写出该反应的热化学方程式_______ 。
(2)实验室中有一种物质常用作氧化剂,可以使Y直接转化为硝酸且绿色环保,写出该物质与Y反应的化学方程式:_______ 。
(3)某化学兴趣小组设计了如图所示的浓 与
与 反应的微型实验,下列说法中错误的是
反应的微型实验,下列说法中错误的是_______ (填标号)。

A.挤压塑料瓶使浓 进入干燥管就可引发反应
进入干燥管就可引发反应
B.将装置口向上提起就可停止反应
C.蘸碱液的棉花可用蘸水的棉花替代
D.该装置适用于木炭与浓硝酸或浓硫酸的反应实验
(4)某同学利用如图装置让氨气与氧化铜反应,验证氨气的性质并验证部分产物(部分装置未画出)。发现反应确实能发生,且反应后得到三种物质,其中有两种单质。

请回答下列问题:
①实验室制取氨气的化学方程式是_______ 。
②从氨中N元素的化合价角度看,该同学想证明的是氨的_______ ,实验中观察到_______ ,则能够证明氨具有这个性质。
③B装置的作用是_______ 。
④A中反应的化学方程式是_______ 。

(1)由N2→X是工业合成氨的反应,每消耗7gN2放出23.4kJ的能量,写出该反应的热化学方程式
(2)实验室中有一种物质常用作氧化剂,可以使Y直接转化为硝酸且绿色环保,写出该物质与Y反应的化学方程式:
(3)某化学兴趣小组设计了如图所示的浓
 与
与 反应的微型实验,下列说法中错误的是
反应的微型实验,下列说法中错误的是
A.挤压塑料瓶使浓
 进入干燥管就可引发反应
进入干燥管就可引发反应B.将装置口向上提起就可停止反应
C.蘸碱液的棉花可用蘸水的棉花替代
D.该装置适用于木炭与浓硝酸或浓硫酸的反应实验
(4)某同学利用如图装置让氨气与氧化铜反应,验证氨气的性质并验证部分产物(部分装置未画出)。发现反应确实能发生,且反应后得到三种物质,其中有两种单质。

请回答下列问题:
①实验室制取氨气的化学方程式是
②从氨中N元素的化合价角度看,该同学想证明的是氨的
③B装置的作用是
④A中反应的化学方程式是
您最近一年使用:0次
2021-07-10更新
|
241次组卷
|
2卷引用:河北省邯郸市2020-2021学年高一下学期期末考试化学试题
9 . 下列物质间的转化能一步实现的是
| A.Al→Al(OH)3 | B.Na2CO3→NaOH |
| C.NH3→HNO3 | D.Fe2(SO4)3→CuSO4 |
您最近一年使用:0次
名校
10 . 硅、硫、氮等非金属元素在化工生产中扮演着重要角色。
I.下列物品或设施:
①陶瓷餐具 ②门窗玻璃 ③水晶镜片 ④硅太阳能电池 ⑤光导纤维 ⑥手机芯片。
(1) 直接使用了硅单质的是(用序号填空)________________ ,
(2) 直接使用了二氧化硅的是(用序号填空)______________ ,
II.在学习了硫的转化后,某学生绘制了如图转化关系。
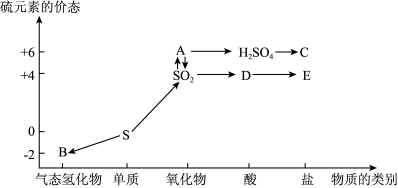
(1)写出简单气态氢化物B的结构式:______________ 。
(2)写出SO2转化为A的化学方程式:____________________________________ 。
(3)下列五种有色溶液与SO2作用均能褪色
①品红溶液 ②酸性KMnO4溶液 ③溴水 ④滴有酚酞的NaOH溶液 ⑤淀粉碘溶液
体现了SO2漂白性的是(用序号填空)____________________ 。
体现了SO2还原性的是(用序号填空)____________________ 。
写出SO2通入酸性KMnO4溶液反应的离子方程式:______________________ 。
(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:

NO2被吸收过程的离子方程式是__________________________________________
(5)若32.0 gCu与一定量的HNO3溶液反应,当Cu反应完时,共产生标准状况下的13.44 L气体(NO和NO2),则消耗的HNO3溶液中溶质的物质的量为________ 。
I.下列物品或设施:
①陶瓷餐具 ②门窗玻璃 ③水晶镜片 ④硅太阳能电池 ⑤光导纤维 ⑥手机芯片。
(1) 直接使用了硅单质的是(用序号填空)
(2) 直接使用了二氧化硅的是(用序号填空)
II.在学习了硫的转化后,某学生绘制了如图转化关系。

(1)写出简单气态氢化物B的结构式:
(2)写出SO2转化为A的化学方程式:
(3)下列五种有色溶液与SO2作用均能褪色
①品红溶液 ②酸性KMnO4溶液 ③溴水 ④滴有酚酞的NaOH溶液 ⑤淀粉碘溶液
体现了SO2漂白性的是(用序号填空)
体现了SO2还原性的是(用序号填空)
写出SO2通入酸性KMnO4溶液反应的离子方程式:
(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:

NO2被吸收过程的离子方程式是
(5)若32.0 gCu与一定量的HNO3溶液反应,当Cu反应完时,共产生标准状况下的13.44 L气体(NO和NO2),则消耗的HNO3溶液中溶质的物质的量为
您最近一年使用:0次
2021-07-09更新
|
1054次组卷
|
4卷引用:重庆市七校2020—2021学年高一下学期期末联考化学试题
重庆市七校2020—2021学年高一下学期期末联考化学试题2020年全国卷Ⅱ化学真题变式题(已下线)第四章 非金属及其化合物(测)-2023年高考化学一轮复习讲练测(全国通用)吉林省长春市第二实验中学2022-2023学年高一下学期4月月考化学试题



