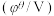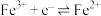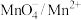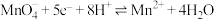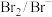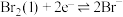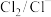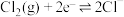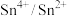解题方法
1 . 某校化学兴趣小组探究 与
与 溶液的反应,所用装置(部分夹持装置略去)如图所示。
溶液的反应,所用装置(部分夹持装置略去)如图所示。
(1)仪器a的名称为______ 。
(2)甲装置用于制 ,试管中盛放的试剂是
,试管中盛放的试剂是______ (填“浓硫酸”或“稀硫酸”)。
(3)实验室配制80mL1.5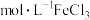 溶液,定容快接近刻度线时,应改用
溶液,定容快接近刻度线时,应改用______ (填仪器名称)。
(4)该小组同学向乙中的 溶液中通入足量的
溶液中通入足量的 ,发生反应的离子方程式为
,发生反应的离子方程式为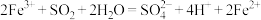 ,乙中试管最终呈
,乙中试管最终呈______ (填“浅绿色”或“浅黄色”)。
(5)反应后打开乙装置中仪器a的活塞,逐滴加入经煮沸后冷却的NaOH溶液,观察到有______ (填“灰绿色”或“白色”)沉淀生成。
 与
与 溶液的反应,所用装置(部分夹持装置略去)如图所示。
溶液的反应,所用装置(部分夹持装置略去)如图所示。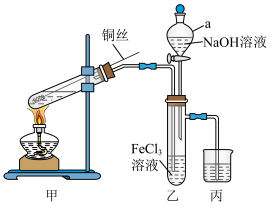
(1)仪器a的名称为
(2)甲装置用于制
 ,试管中盛放的试剂是
,试管中盛放的试剂是(3)实验室配制80mL1.5
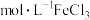 溶液,定容快接近刻度线时,应改用
溶液,定容快接近刻度线时,应改用(4)该小组同学向乙中的
 溶液中通入足量的
溶液中通入足量的 ,发生反应的离子方程式为
,发生反应的离子方程式为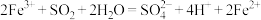 ,乙中试管最终呈
,乙中试管最终呈(5)反应后打开乙装置中仪器a的活塞,逐滴加入经煮沸后冷却的NaOH溶液,观察到有
您最近一年使用:0次
2 . 纯净物状态下的标准电极电势可用来比较对应氧化剂的氧化性强弱。现有六组标准电极电势数据如表所示:
下列分析正确的是
氧化还原电对(氧化型/还原型) | 电极反应式 | 标准电极电势 |
|
| 0.77 |
|
| 0.54 |
|
| 1.50 |
|
| 1.07 |
|
| 1.36 |
|
| 0.15 |
A.氧化性: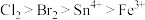 |
B.往含有 的 的 溶液中滴加少量氯水,溶液变红 溶液中滴加少量氯水,溶液变红 |
C.往淀粉- 溶液中加入过量 溶液中加入过量 溶液,溶液变蓝 溶液,溶液变蓝 |
D. 溶液与足量酸性 溶液与足量酸性 溶液反应的离子方程式: 溶液反应的离子方程式: |
您最近一年使用:0次
解题方法
3 . 高铁酸钠( )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为 。下列说法错误的是
。下列说法错误的是
 )是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为
)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为 。下列说法错误的是
。下列说法错误的是A. 中 中 原子的杂化轨道类型为 原子的杂化轨道类型为 |
B.该反应中氧化产物与还原产物的物质的量之比为 |
| C.依据该反应原理,可设计原电池 |
D.完全反应后,可用 溶液检验反应后的溶液中是否存在 溶液检验反应后的溶液中是否存在 |
您最近一年使用:0次
4 . 高铁酸钾( 极易溶于水)是常见的水处理剂,其原理如图所示。
极易溶于水)是常见的水处理剂,其原理如图所示。
(1) 中铁元素的化合价为
中铁元素的化合价为___________ 价。
(2)过程①中活细菌表现了___________ (填“氧化”或“还原”)性。
(3)净水利用了 胶体聚沉作用,请写出
胶体聚沉作用,请写出 胶体制备化学方程式
胶体制备化学方程式___________ 。
(4)根据上述原理分析,作水处理剂时, 的作用有
的作用有___________ 和净水剂。
(5)还可用干法制备高铁酸钠,主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,(Na2O2中氧元素为-1价)该反应中还原剂是___________ 。(填化学式)
(6)已知铁与水蒸气发生如下反应: ,请用单线桥法表示电子转移的方向和数目:
,请用单线桥法表示电子转移的方向和数目:___________ ;该反应的还原产物是___________ 。
 极易溶于水)是常见的水处理剂,其原理如图所示。
极易溶于水)是常见的水处理剂,其原理如图所示。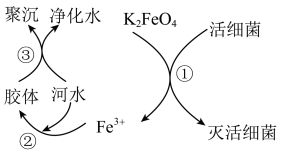
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)过程①中活细菌表现了
(3)净水利用了
 胶体聚沉作用,请写出
胶体聚沉作用,请写出 胶体制备化学方程式
胶体制备化学方程式(4)根据上述原理分析,作水处理剂时,
 的作用有
的作用有(5)还可用干法制备高铁酸钠,主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,(Na2O2中氧元素为-1价)该反应中还原剂是
(6)已知铁与水蒸气发生如下反应:
 ,请用单线桥法表示电子转移的方向和数目:
,请用单线桥法表示电子转移的方向和数目:
您最近一年使用:0次
5 . 铁与空气接触时会形成氧化物,如一块低碳钢可以被三种氧化物膜所覆盖与金属接触的一侧是FeO,与空气接触的一侧是 ,而中间则是
,而中间则是 。
。
(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的___________ (填化学式)。
(2) 的一种用途是
的一种用途是___________ 。(填“用作油漆、涂料 ”或“磁电机”);
(3)FeO可作化妆品中的色素,它还能进行一系列转化: 。
。
① 时应加入的试剂是
时应加入的试剂是___________ (填“H2SO4”或“Na2SO4”)。
②“速力菲”(主要有效成分是 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入___________ (填“KSCN”或“K2SO4”),若出现___________ (填“红色”或“浅绿色”)现象,则证明该药物已变质。
③在 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成___________ (填“红褐色”或“黄色”),其中沉淀颜色发生变化的化学方程式为___________ 。
 ,而中间则是
,而中间则是 。
。(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的
(2)
 的一种用途是
的一种用途是(3)FeO可作化妆品中的色素,它还能进行一系列转化:
 。
。①
 时应加入的试剂是
时应加入的试剂是②“速力菲”(主要有效成分是
 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入③在
 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
您最近一年使用:0次
名校
6 . 电子工业上常用氯化铁溶液作印刷电路板的腐蚀液,使用过的腐蚀废液中的金属阳离子主要有Fe3+、Fe2+和Cu2+。化学兴趣小组设计如下流程对废液进行处理并回收氯化铁溶液。___________ (填“氧化”或“还原”)成Fe3+;取少量溶液A于试管中,滴入1~2滴KSCN溶液,溶液显___________ (填“红色”或“蓝色”)。
(2)实验室常用H2O2溶液制取氧气。在一定温度下,10 mL 0.40 mol·L-1的H2O2溶液发生催化分解,5 min时测得生成O2的体积为22.4 mL(已折算为标准状况)。
①用H2O2表示该反应的速率为___________ mol·(L·min)-1;
②其他条件不变时,升高反应的温度,该反应的速率将___________ (填“加快”或“减慢”)。

(2)实验室常用H2O2溶液制取氧气。在一定温度下,10 mL 0.40 mol·L-1的H2O2溶液发生催化分解,5 min时测得生成O2的体积为22.4 mL(已折算为标准状况)。
①用H2O2表示该反应的速率为
②其他条件不变时,升高反应的温度,该反应的速率将
您最近一年使用:0次
7 . 黑木耳富含蛋白质、铁、具有还原性的维生素C等,每100 g黑木耳含铁量高达185 mg。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。____________ 。
(2)步骤④检验Fe3+所用试剂是_____________ (填化学式)溶液。
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的阳离子 的离子符号为____________ 。
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。_______ (填序号)。
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为_______________ 。
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是_______________ 。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。
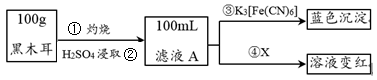
(2)步骤④检验Fe3+所用试剂是
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。
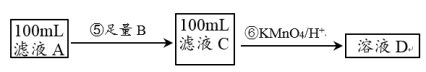
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是
您最近一年使用:0次
解题方法
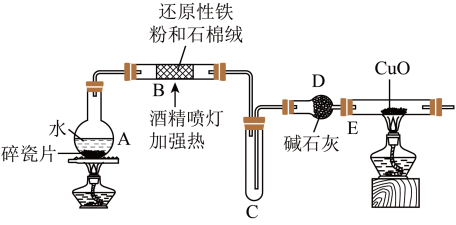
8 .  是常用的磁性材料,可用于录音磁带等的制作。某小组同学采用下列实验装置(夹持仪器略)制备
是常用的磁性材料,可用于录音磁带等的制作。某小组同学采用下列实验装置(夹持仪器略)制备 。回答下列问题:
。回答下列问题:
Ⅰ.制备
 的名称是
的名称是___________ ;装置 作用是
作用是___________ 。
(2)装置 中反应的化学方程式为
中反应的化学方程式为___________ 。
(3)实验过程中可观察到 中的现象是黑色固体变红,说明产生的气体是
中的现象是黑色固体变红,说明产生的气体是___________ 。
Ⅱ.探究 中铁粉是否完全反应
中铁粉是否完全反应
待硬质玻璃管 冷却后,取少许其中的固体物质进行如下实验(已知酸性
冷却后,取少许其中的固体物质进行如下实验(已知酸性 溶液能与盐酸发生反应):
溶液能与盐酸发生反应): 可以是
可以是___________ (填标号)。
A.盐酸 B.硫酸 C.次氯酸
(5)①现象1为___________ 。
②有同学认为现象2中溶液未变红色,说明 固体有铁粉剩余,写出在溶液中铁粉与铁离子发生反应的离子方程式:
固体有铁粉剩余,写出在溶液中铁粉与铁离子发生反应的离子方程式:___________ 。
(6)已知温度高于 时,铁与水蒸气反应的氧化产物只有
时,铁与水蒸气反应的氧化产物只有 ,甲同学称取
,甲同学称取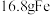 粉于装置
粉于装置 中,在
中,在 反应一段时间后停止加热,冷却后称得固体质量为
反应一段时间后停止加热,冷却后称得固体质量为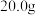 ,则未反应的
,则未反应的 粉的物质的量为
粉的物质的量为___________  。
。
 是常用的磁性材料,可用于录音磁带等的制作。某小组同学采用下列实验装置(夹持仪器略)制备
是常用的磁性材料,可用于录音磁带等的制作。某小组同学采用下列实验装置(夹持仪器略)制备 。回答下列问题:
。回答下列问题:Ⅰ.制备

 的名称是
的名称是 作用是
作用是(2)装置
 中反应的化学方程式为
中反应的化学方程式为(3)实验过程中可观察到
 中的现象是黑色固体变红,说明产生的气体是
中的现象是黑色固体变红,说明产生的气体是Ⅱ.探究
 中铁粉是否完全反应
中铁粉是否完全反应待硬质玻璃管
 冷却后,取少许其中的固体物质进行如下实验(已知酸性
冷却后,取少许其中的固体物质进行如下实验(已知酸性 溶液能与盐酸发生反应):
溶液能与盐酸发生反应):
 可以是
可以是A.盐酸 B.硫酸 C.次氯酸
(5)①现象1为
②有同学认为现象2中溶液未变红色,说明
 固体有铁粉剩余,写出在溶液中铁粉与铁离子发生反应的离子方程式:
固体有铁粉剩余,写出在溶液中铁粉与铁离子发生反应的离子方程式:(6)已知温度高于
 时,铁与水蒸气反应的氧化产物只有
时,铁与水蒸气反应的氧化产物只有 ,甲同学称取
,甲同学称取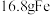 粉于装置
粉于装置 中,在
中,在 反应一段时间后停止加热,冷却后称得固体质量为
反应一段时间后停止加热,冷却后称得固体质量为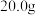 ,则未反应的
,则未反应的 粉的物质的量为
粉的物质的量为 。
。
您最近一年使用:0次
解题方法
9 . 下列实验操作与结论正确的是
| 实验操作 | 结论 | |
| A | 用玻璃棒蘸取待测液在酒精灯火焰上灼烧,火焰呈黄色 | 待测液中含有 |
| B | 用带火星的小木条检验过氧化钠与水反应生成的气体,小木条复燃 | 产生的气体是 |
| C | 将某气体通入石蕊试液后,溶液变红 | 该气体一定是 |
| D | 向某溶液中先加入氯水再加 溶液,溶液呈红色 溶液,溶液呈红色 | 原溶液中一定含 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 下列离子在指定溶液中一定能大量共存的是
A.无色透明的溶液中: 、 、 、 、 、 、 |
B.pH=3的溶液中: 、 、 、 、 、 、 |
C.使酚酞变红的溶液中: 、 、 、 、 、 、 |
D.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2024-04-25更新
|
504次组卷
|
5卷引用:湖南省娄底市涟源市2023-2024学年高一下学期3月月考化学试题