名校
解题方法
1 . 以废铁屑(含少量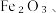 FeS等杂质)为原料,制备硫酸亚铁晶体
FeS等杂质)为原料,制备硫酸亚铁晶体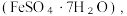 流程示意图如下:
流程示意图如下: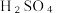 的作用是
的作用是
_________ (用离子方程式表示)。过程中产生的有毒气体,可用___________ 溶液吸收。
(2)酸浸时间对所得溶液的成分影响如下表所示。
用文字说明导致上述颜色变化的可能原因。___________
(3)已知: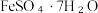 受热易失水,则操作X为:蒸发浓缩、
受热易失水,则操作X为:蒸发浓缩、________ 、过滤、洗涤。FeSO4强热后继续分解,推测产物为___________ 、Fe2O3和SO3。
测定所得硫酸亚铁晶体中的含量,步骤如下:
Ⅰ.称取ag硫酸亚铁晶体样品,配制成100mL溶液。
Ⅱ.取出10mL溶液,加入适量稀硫酸,滴入 的
的 溶液,至反应完全,共消耗
溶液,至反应完全,共消耗 溶液cmL。(反应原理:
溶液cmL。(反应原理:
(4)计算硫酸亚铁晶体样品中 质量分数
质量分数___________ 。
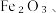 FeS等杂质)为原料,制备硫酸亚铁晶体
FeS等杂质)为原料,制备硫酸亚铁晶体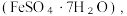 流程示意图如下:
流程示意图如下:
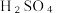 的作用是
的作用是
(2)酸浸时间对所得溶液的成分影响如下表所示。
| 酸浸时间 | 1min | 30min | 120min |
| 用KSCN溶液检验 | 变红 | 未变红 | 变红 |
(3)已知:
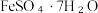 受热易失水,则操作X为:蒸发浓缩、
受热易失水,则操作X为:蒸发浓缩、测定所得硫酸亚铁晶体中的含量,步骤如下:
Ⅰ.称取ag硫酸亚铁晶体样品,配制成100mL溶液。
Ⅱ.取出10mL溶液,加入适量稀硫酸,滴入
 的
的 溶液,至反应完全,共消耗
溶液,至反应完全,共消耗 溶液cmL。(反应原理:
溶液cmL。(反应原理:
(4)计算硫酸亚铁晶体样品中
 质量分数
质量分数
您最近一年使用:0次
名校
解题方法
2 . 向含有Fe3+、Fe2+、Cu2+的蚀刻铜箔回收液中,加入一定量铁粉,反应一段时间后,对反应后的混合物进行分析,下列说法错误的是
| A.若有固体剩余,则该固体一定含有Cu |
| B.若有固体剩余,则该溶液可能含有Cu2+ |
| C.若无固体剩余,则该溶液不可能含有Fe3+ |
| D.无论固体是否剩余,该溶液中一定含有Fe2+ |
您最近一年使用:0次
名校
解题方法
3 . 聚合硫酸铝铁(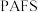 )是一种高效净水剂,广泛应用于饮用水处理、工业废水处理和污水处理。它能有效去除悬浊物、胶体颗粒、重金属、氨氨、有机物和色度等污染物,提高水质,保护环境。它的生产可以利用硫铁矿烧渣(主要成分为
)是一种高效净水剂,广泛应用于饮用水处理、工业废水处理和污水处理。它能有效去除悬浊物、胶体颗粒、重金属、氨氨、有机物和色度等污染物,提高水质,保护环境。它的生产可以利用硫铁矿烧渣(主要成分为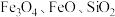 等)和粉煤灰(主要成分为
等)和粉煤灰(主要成分为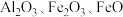 等),经过一系列的反应制得,具体流程如下:
等),经过一系列的反应制得,具体流程如下:___________ (填序号)。
A.降低温度 B.烧渣粉碎 C.适当提高硫酸浓度 D.加水稀释
“酸溶”后得到的溶液中,主要存在的金属阳离子有___________ (填化学符号)。
(2)检验“氧化”后溶液中金属阳离子的方法是___________ 。
(3)实验测得“氧化”过程中温度过高氧化效率会下降,原因可能是___________ 。
(4)“酸溶”过程中发生反应的离子方程式为___________ 。
(5)滤渣Ⅱ中可以循环利用的物质是___________ (填化学式)。
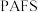 )是一种高效净水剂,广泛应用于饮用水处理、工业废水处理和污水处理。它能有效去除悬浊物、胶体颗粒、重金属、氨氨、有机物和色度等污染物,提高水质,保护环境。它的生产可以利用硫铁矿烧渣(主要成分为
)是一种高效净水剂,广泛应用于饮用水处理、工业废水处理和污水处理。它能有效去除悬浊物、胶体颗粒、重金属、氨氨、有机物和色度等污染物,提高水质,保护环境。它的生产可以利用硫铁矿烧渣(主要成分为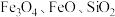 等)和粉煤灰(主要成分为
等)和粉煤灰(主要成分为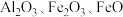 等),经过一系列的反应制得,具体流程如下:
等),经过一系列的反应制得,具体流程如下: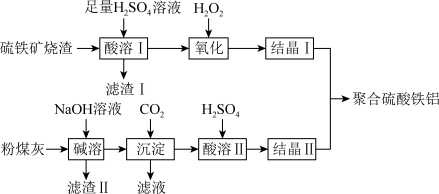
A.降低温度 B.烧渣粉碎 C.适当提高硫酸浓度 D.加水稀释
“酸溶”后得到的溶液中,主要存在的金属阳离子有
(2)检验“氧化”后溶液中金属阳离子的方法是
(3)实验测得“氧化”过程中温度过高氧化效率会下降,原因可能是
(4)“酸溶”过程中发生反应的离子方程式为
(5)滤渣Ⅱ中可以循环利用的物质是
您最近一年使用:0次
名校
4 . 下列离子在指定溶液中一定能大量共存的是
A.无色透明的溶液中: 、 、 、 、 、 、 |
B.pH=3的溶液中: 、 、 、 、 、 、 |
C.使酚酞变红的溶液中: 、 、 、 、 、 、 |
D.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2024-04-25更新
|
504次组卷
|
5卷引用:四川省内江市威远中学校2023-2024学年高一下学期期中考试化学试题
名校
5 . 利用金属矿渣(含有FeS2、SiO2及Cu2O)制备FeCO3的实验流程如下。已知煅烧过程中FeS2和Cu2O转化为Fe2O3和CuO。___________ (写化学式),该物质是工业制备硅的原料,写出该物质与焦炭反应制备硅的化学方程式:___________ 。
(2)FeS2在空气中煅烧的化学方程式为___________ 。
(3)在“还原”步骤,在向酸浸后溶液加入过量铁屑,除了能将 转化为
转化为 外,还能
外,还能___________ 。若将6g铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中,充分反应得到200mL FeSO4溶液和5.2g固体沉淀物。
FeSO4溶液和5.2g固体沉淀物。
①5.2g固体沉淀物的成份为___________ (写化学式)。
②原Fe2(SO4)3溶液的物质的量浓度是___________ 。(写出计算过程)
(4)检验 是否完全被还原的实验操作是
是否完全被还原的实验操作是___________ 。
(5)制备FeCO3,写出“沉铁”步骤发生反应的离子方程式:___________ 。
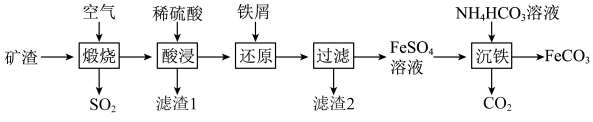
(2)FeS2在空气中煅烧的化学方程式为
(3)在“还原”步骤,在向酸浸后溶液加入过量铁屑,除了能将
 转化为
转化为 外,还能
外,还能 FeSO4溶液和5.2g固体沉淀物。
FeSO4溶液和5.2g固体沉淀物。①5.2g固体沉淀物的成份为
②原Fe2(SO4)3溶液的物质的量浓度是
(4)检验
 是否完全被还原的实验操作是
是否完全被还原的实验操作是(5)制备FeCO3,写出“沉铁”步骤发生反应的离子方程式:
您最近一年使用:0次
名校
6 .  的配位化合物较稳定且用运广泛。
的配位化合物较稳定且用运广泛。 可与
可与 、
、 、
、 等配体形成溶液呈浅紫色的
等配体形成溶液呈浅紫色的 、红色的
、红色的 、无色的
、无色的 配离子。某同学按如下步骤完成实验:
配离子。某同学按如下步骤完成实验: 的溶液中加入KSCN溶液生成蓝色的
的溶液中加入KSCN溶液生成蓝色的 的配离子,
的配离子, 不能与
不能与 形成配位离子。下列说法错误的是
形成配位离子。下列说法错误的是
 的配位化合物较稳定且用运广泛。
的配位化合物较稳定且用运广泛。 可与
可与 、
、 、
、 等配体形成溶液呈浅紫色的
等配体形成溶液呈浅紫色的 、红色的
、红色的 、无色的
、无色的 配离子。某同学按如下步骤完成实验:
配离子。某同学按如下步骤完成实验: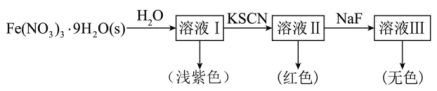
 的溶液中加入KSCN溶液生成蓝色的
的溶液中加入KSCN溶液生成蓝色的 的配离子,
的配离子, 不能与
不能与 形成配位离子。下列说法错误的是
形成配位离子。下列说法错误的是| A.Fe晶体中原子通过金属阳离子和自由电子间的静电作用相结合 |
B.可用NaF和KSCN溶液检验 溶液中是否含有 溶液中是否含有 |
C.溶液Ⅰ中 仅参与形成范德华力和氢键 仅参与形成范德华力和氢键 |
D.上述实验可得出,与 形成配合物的能力: 形成配合物的能力: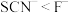 |
您最近一年使用:0次
2024-04-22更新
|
216次组卷
|
3卷引用:安徽省淮南第二中学2023-2024学年高二下学期期中测试化学试题
7 . 由下列实验方案、现象得出的结论不正确的是
实验方案 | 现象 | 结论 | |
| A | 向FeCl3溶液中加入几滴KSCN溶液 | 溶液立即变红 | KSCN溶液可用来检验Fe3+ |
| B | 用毛皮摩擦过的带电橡胶靠近CF2Cl2液流 | 液流方向改变 | CF2Cl2是正四面体结构,为非极性分子 |
| C | 在碘水中加入CCl4,振荡 | 分层,下层紫红色 | I2在水中的溶解度小于在CCl4中的溶解度 |
| D | [Cu(NH3)4]SO4溶液中加入乙醇 | 析出深蓝色固体 | [Cu(NH3)4]SO4在乙醇中溶解度小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-22更新
|
148次组卷
|
2卷引用:安徽省淮南第二中学2023-2024学年高二下学期期中测试化学试题
8 . 根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向 溶液中滴入硫酸酸化的 溶液中滴入硫酸酸化的 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 |  具有氧化性 具有氧化性 |
| B | 将 缓慢通入酸性 缓慢通入酸性 溶液中,溶液紫红色褪去 溶液中,溶液紫红色褪去 |  具有漂白性 具有漂白性 |
| C | 向盛有 溶液的试管中滴加几滴 溶液的试管中滴加几滴 溶液,振荡,再滴加几滴新制的氯水,观察溶液颜色变化 溶液,振荡,再滴加几滴新制的氯水,观察溶液颜色变化 |  具有还原性 具有还原性 |
| D | 向溶液X中加入 稀溶液,将湿润的红色石蕊试纸置于试管口,试纸未变蓝 稀溶液,将湿润的红色石蕊试纸置于试管口,试纸未变蓝 | 原溶液中不存在 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-22更新
|
231次组卷
|
2卷引用:四川省内江市威远中学校2023-2024学年高一下学期期中考试化学试题
名校
9 . 下列实验操作、现象和所得出的结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将溶液X与盐酸反应产生的气体通入品红溶液中 | 品红溶液褪色 | 溶液X中一定含有SO |
| B | 将少量碳酸钠溶液滴入足量稀盐酸中 | 有气泡产生 | 非金属性:Cl>C |
| C | 向3 mL KI溶液中滴加几滴溴水,振荡,再滴加 1 mL淀粉溶液 | 溶液显蓝色 | Br2的氧化性比I2强 |
| D | 将Fe(NO3)2样品溶于稀硫酸后,滴加KSCN溶液 | 溶液变红 | Fe(NO3)2样品已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-22更新
|
172次组卷
|
2卷引用:四川省内江市威远中学校2023-2024学年高一下学期期中考试化学试题
名校
10 . 根据信息书写指定反应的方程式。
(1)请从下列试剂中选择合适的完成指定转化(试剂可以重复选择)。
试剂:稀硫酸、氨水、HI(强酸)溶液、 溶液、NaCl溶液、NaOH溶液
溶液、NaCl溶液、NaOH溶液
①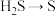 的离子方程式:
的离子方程式:____________ 。
② 的离子方程式:
的离子方程式:____________ 。
③ (两性氧化物)
(两性氧化物) 的
的化学方程式 :____________ 。
(2)CuCl常用作杀菌剂、催化剂等。一种利用废弃铜锌合金制取CuCl的流程如下图所示:化学方程式 :____________ 。
②写出氧化步骤时发生的主要反应的离子方程式:____________ 。
③写出沉铜步骤时发生的主要反应的离子方程式:____________ 。
(1)请从下列试剂中选择合适的完成指定转化(试剂可以重复选择)。
试剂:稀硫酸、氨水、HI(强酸)溶液、
 溶液、NaCl溶液、NaOH溶液
溶液、NaCl溶液、NaOH溶液①
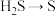 的离子方程式:
的离子方程式:②
 的离子方程式:
的离子方程式:③
 (两性氧化物)
(两性氧化物) 的
的(2)CuCl常用作杀菌剂、催化剂等。一种利用废弃铜锌合金制取CuCl的流程如下图所示:
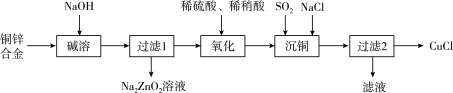
②写出氧化步骤时发生的主要反应的离子方程式:
③写出沉铜步骤时发生的主要反应的离子方程式:
您最近一年使用:0次



