名校
1 . 从含砷氧化锌废渣(还含有Cu、Ni、Ag的氧化物等)制取活性氧化锌的工艺流程如下:

回答下列问题:
(1)写出“氨浸”时, 生成
生成 的离子方程式:
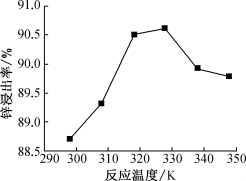
的离子方程式:_______ ;该工序锌的浸出率与温度关系如图,当温度高于328K时,锌的浸出率反而下降的原因是_______ 。
(2)“除砷”时, 需过量,一是生成
需过量,一是生成 [或
[或 ]胶体吸附含砷微粒,二是
]胶体吸附含砷微粒,二是_______ ;写出砷酸铁的化学式:_______ 。
(3)“除铁”时, 被
被 全部氧化为
全部氧化为 ,再调pH将
,再调pH将 、
、 转化为沉淀而除去。检验铁元素是否被完全除去的试剂是
转化为沉淀而除去。检验铁元素是否被完全除去的试剂是_______ 。
(4)写出“蒸氨”时, 生成
生成 的化学方程式:
的化学方程式:_______ 。
(5)以1 t含锌元素10%的含砷氧化锌制得活性氧化锌113.4 kg,依据以上数据能否计算出锌元素的回收率。若能,写出计算结果,若不能,请说明理由:_______ 。

回答下列问题:
(1)写出“氨浸”时,
 生成
生成 的离子方程式:
的离子方程式:
(2)“除砷”时,
 需过量,一是生成
需过量,一是生成 [或
[或 ]胶体吸附含砷微粒,二是
]胶体吸附含砷微粒,二是(3)“除铁”时,
 被
被 全部氧化为
全部氧化为 ,再调pH将
,再调pH将 、
、 转化为沉淀而除去。检验铁元素是否被完全除去的试剂是
转化为沉淀而除去。检验铁元素是否被完全除去的试剂是(4)写出“蒸氨”时,
 生成
生成 的化学方程式:
的化学方程式:(5)以1 t含锌元素10%的含砷氧化锌制得活性氧化锌113.4 kg,依据以上数据能否计算出锌元素的回收率。若能,写出计算结果,若不能,请说明理由:
您最近一年使用:0次
2022-12-31更新
|
164次组卷
|
2卷引用:江苏省苏州市梁丰高级中学2023-2024学年高二上学期期末化学模拟试卷
名校
解题方法
2 . 化学小组探究 与
与 溶液的反应,实验如下:
溶液的反应,实验如下:
已知:经检验白色沉淀为
(1)实验ⅰ中发生的离子方程式为_______ 。
(2)实验ⅱ中检测到 ,依据的实验现象是
,依据的实验现象是_______ 。
(3)从平衡移动的原理解释实验ⅱ红色消失的原因_______ 。
(4)对实验ⅱ中 产生的原因作如下假设:
产生的原因作如下假设:
假设1:溶液中的 被_______氧化
被_______氧化
假设2: 与
与 的反应是一个可逆反应
的反应是一个可逆反应
假设3:在实验ⅱ的条件下, 被
被 氧化
氧化
请将假设1补充完整_______ 。
(5)设计实验验证假设。
实验ⅲ 取2mL溶液a,向其中滴加5滴0.1mol/L 溶液,放置较长时间,溶液颜色不变红,证明假设1不成立。
溶液,放置较长时间,溶液颜色不变红,证明假设1不成立。
实验ⅳ 实验装置如下图所示,闭合开关K,电流计指针不动。向右侧 溶液中滴加0.1mol/L
溶液中滴加0.1mol/L ,指针向右大幅度偏转,溶液中有白色浑浊物产生。取出左侧溶液,滴加0.1mol/L
,指针向右大幅度偏转,溶液中有白色浑浊物产生。取出左侧溶液,滴加0.1mol/L ,溶液变红。
,溶液变红。_______ 。
②假设2不成立的实验证据是_______ 。
③实验证明假设3成立。
请结合电极反应式解释实验ⅱ中 产生的原因
产生的原因_______ 。
 与
与 溶液的反应,实验如下:
溶液的反应,实验如下:| 序号 | 实验方案 | 实验现象 |
| 实验ⅰ |
| 振荡试管,观察到溶液变为蓝色,待反应充分后,试管底部有 粉剩余。 粉剩余。 |
| 实验ⅱ | 取实验ⅰ中的上层清液,向其中滴加0.1mol/L 溶液 溶液 | 溶液局部变红,同时产生白色沉淀,振荡试管,红色消失。 |

(1)实验ⅰ中发生的离子方程式为
(2)实验ⅱ中检测到
 ,依据的实验现象是
,依据的实验现象是(3)从平衡移动的原理解释实验ⅱ红色消失的原因
(4)对实验ⅱ中
 产生的原因作如下假设:
产生的原因作如下假设:假设1:溶液中的
 被_______氧化
被_______氧化假设2:
 与
与 的反应是一个可逆反应
的反应是一个可逆反应假设3:在实验ⅱ的条件下,
 被
被 氧化
氧化请将假设1补充完整
(5)设计实验验证假设。
实验ⅲ 取2mL溶液a,向其中滴加5滴0.1mol/L
 溶液,放置较长时间,溶液颜色不变红,证明假设1不成立。
溶液,放置较长时间,溶液颜色不变红,证明假设1不成立。实验ⅳ 实验装置如下图所示,闭合开关K,电流计指针不动。向右侧
 溶液中滴加0.1mol/L
溶液中滴加0.1mol/L ,指针向右大幅度偏转,溶液中有白色浑浊物产生。取出左侧溶液,滴加0.1mol/L
,指针向右大幅度偏转,溶液中有白色浑浊物产生。取出左侧溶液,滴加0.1mol/L ,溶液变红。
,溶液变红。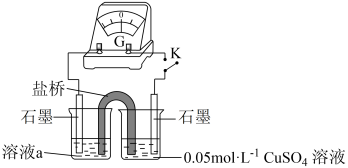
②假设2不成立的实验证据是
③实验证明假设3成立。
请结合电极反应式解释实验ⅱ中
 产生的原因
产生的原因
您最近一年使用:0次
2022-12-30更新
|
232次组卷
|
3卷引用:北京市延庆区2022-2023学年高二上学期期末考试化学试题
3 . 根据下图的化学反应框图回答下列问题。已知:粉状化合物A是红棕色,粉状单质B是金属单质。
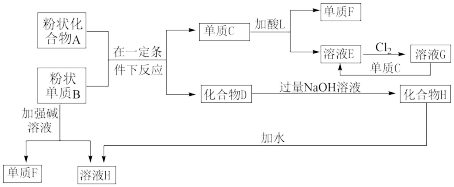
(1)溶液E加入氢氧化钠溶液的现象是_______ 。
(2)写出下列反应的化学方程式:
 →
→ :
:_______ ;
D→H:_______ 。
(3)写出下列反应的离子方程式:
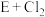 →G:
→G:_______ ;
 →E:
→E:_______ ;
B→ :
:_______ 。

(1)溶液E加入氢氧化钠溶液的现象是
(2)写出下列反应的化学方程式:
 →
→ :
:D→H:
(3)写出下列反应的离子方程式:
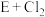 →G:
→G: →E:
→E:B→
 :
:
您最近一年使用:0次
解题方法
4 . 某校化学兴趣小组探究SO2与FeCl3溶液的反应。
资料:铁氰化钾 可以与Fe2+形成蓝色沉淀,常用于Fe2+检验。
可以与Fe2+形成蓝色沉淀,常用于Fe2+检验。

(1)实验室常用70%硫酸与亚硫酸钠固体制备SO2,写出反应的化学方程式_______ 。
(2)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由黄色变成浅绿色,写出相关反应的离子方程式_______ 。
(3)向试管B中溶液通入SO2至饱和,溶液变成红色,静置5min后,溶液的颜色从红色慢慢变回黄色。静置9h后,溶液慢慢由黄色变为浅绿色。
①甲同学认为溶液变红的原因是通入SO2后,Fe3+水解程度增大,形成Fe(OH)3胶体。乙同学根据SO2的性质否定了这一推论,原因是_______ 。
②丙同学取上述5min后的黄色溶液,滴加盐酸酸化的BaCl2溶液,产生白色沉淀。该同学认为SO2与Fe3+发生氧化还原反应。丁同学认为该结论不严谨,重新设计并进行实验,证明两者发生了氧化还原反应,写出实验方案及现象_______ 。
(4)查阅资料:Fe3+能与S(IV)微粒形成红色配合物。
该小组同学分析SO2水溶液成分,猜想可能是其中含S(IV)微粒SO2、H2SO3、_______ 与Fe3+形成配合物而使溶液呈现红色。进行如下实验:
①a=_______ 。
②根据实验I现象,溶液中SO2、H2SO3浓度增大,红色消失,说明红色物质可能与SO2、H2SO3无关;_______ ,红色物质可能与 有关。
有关。
(5)通过上述实验可得结论:
①SO2与FeCl3溶液的反应,可以发生配位反应、氧化还原反应。
②_______ 。
资料:铁氰化钾
 可以与Fe2+形成蓝色沉淀,常用于Fe2+检验。
可以与Fe2+形成蓝色沉淀,常用于Fe2+检验。
(1)实验室常用70%硫酸与亚硫酸钠固体制备SO2,写出反应的化学方程式
(2)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由黄色变成浅绿色,写出相关反应的离子方程式
(3)向试管B中溶液通入SO2至饱和,溶液变成红色,静置5min后,溶液的颜色从红色慢慢变回黄色。静置9h后,溶液慢慢由黄色变为浅绿色。
①甲同学认为溶液变红的原因是通入SO2后,Fe3+水解程度增大,形成Fe(OH)3胶体。乙同学根据SO2的性质否定了这一推论,原因是
②丙同学取上述5min后的黄色溶液,滴加盐酸酸化的BaCl2溶液,产生白色沉淀。该同学认为SO2与Fe3+发生氧化还原反应。丁同学认为该结论不严谨,重新设计并进行实验,证明两者发生了氧化还原反应,写出实验方案及现象
(4)查阅资料:Fe3+能与S(IV)微粒形成红色配合物。
该小组同学分析SO2水溶液成分,猜想可能是其中含S(IV)微粒SO2、H2SO3、
| 序号 | 实验 | 加入试剂 | 现象 |
| I |  | 2mL1mol/LNaHSO3溶液;再滴加几滴盐酸 | 溶液变成红色,比(3)中溶液红色深;滴加盐酸后,溶液颜色由红色变成黄色 |
| II | 2mL1mol/LNa2SO3溶液 | 溶液变成红色,比I中溶液红色深 |
②根据实验I现象,溶液中SO2、H2SO3浓度增大,红色消失,说明红色物质可能与SO2、H2SO3无关;
 有关。
有关。(5)通过上述实验可得结论:
①SO2与FeCl3溶液的反应,可以发生配位反应、氧化还原反应。
②
您最近一年使用:0次
名校
解题方法
5 . 硫酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物。一片药片所含铁元素60mg,一盒硫酸亚铁片含药100片。
(1)每盒硫酸亚铁中含铁元素的物质的量为_______ mol(结果保留小数点后一位);
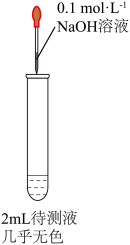
(2)甲同学为检验药片中 ,将硫酸亚铁片碾碎溶解后取上层清液进行实验(如图所示),预测观察到的现象是:
,将硫酸亚铁片碾碎溶解后取上层清液进行实验(如图所示),预测观察到的现象是:_______ ;
(3)乙同学认为药品有部分被氧化,将硫酸亚铁片碾碎溶解后取上层清液进行实验(如下图所示)
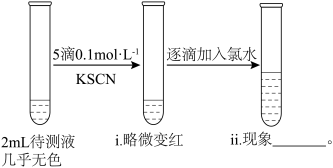
ⅱ中的现象是:_______ ;是由于 被氯水氧化,反应的离子方程式为
被氯水氧化,反应的离子方程式为_______ ;
(4)丙同学认为上述实验不能充分证明药品被部分氧化,应补充的实验是:_______ 。
(1)每盒硫酸亚铁中含铁元素的物质的量为
(2)甲同学为检验药片中
 ,将硫酸亚铁片碾碎溶解后取上层清液进行实验(如图所示),预测观察到的现象是:
,将硫酸亚铁片碾碎溶解后取上层清液进行实验(如图所示),预测观察到的现象是:
(3)乙同学认为药品有部分被氧化,将硫酸亚铁片碾碎溶解后取上层清液进行实验(如下图所示)

ⅱ中的现象是:
 被氯水氧化,反应的离子方程式为
被氯水氧化,反应的离子方程式为(4)丙同学认为上述实验不能充分证明药品被部分氧化,应补充的实验是:
您最近一年使用:0次
2022-12-29更新
|
103次组卷
|
2卷引用:北京市通州区2021-2022学年高一上学期期末测试化学试题
名校
6 . 长期放置的 溶液易被氧化而变质。某兴趣小组分别对新制和久置的两瓶
溶液易被氧化而变质。某兴趣小组分别对新制和久置的两瓶 溶液进行了如表实验。
溶液进行了如表实验。
I.分别取2mL新制的 溶液于三支试管中,进行如图实验。
溶液于三支试管中,进行如图实验。
(1)方案ii中,紫色褪去发生的离子方程式是_______ 。
(2)方案iii的实验现象是_______ ,写出氯水参与反应的离子方程式:__ 。
II.久置的 溶液。
溶液。
(3)将上述实验iv__ 和实验v中的实验现象__ ;操作__ 补充完整。
(4)小组同学查阅资料得知,“维生素C可将 转化为
转化为 ”。为了验证维生素C的作用,设计了如表实验vi。
”。为了验证维生素C的作用,设计了如表实验vi。
由实验vi能否得出“维生素C可将 转化为
转化为 ”的结论?请说明理由
”的结论?请说明理由_______ 。
 溶液易被氧化而变质。某兴趣小组分别对新制和久置的两瓶
溶液易被氧化而变质。某兴趣小组分别对新制和久置的两瓶 溶液进行了如表实验。
溶液进行了如表实验。I.分别取2mL新制的
 溶液于三支试管中,进行如图实验。
溶液于三支试管中,进行如图实验。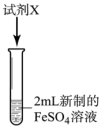 | 实验 | 试剂X | 实验现象 |
| 实验i | 1mL1mol/L NaOH溶液 | 现象a | |
| 实验ii | 5滴酸性 溶液 溶液 | 现象b:紫色褪去 | |
| 实验iii | 依次加入5滴KSCN溶液、5滴氯水 | 现象c |
(2)方案iii的实验现象是
II.久置的
 溶液。
溶液。| 实验操作 | 实验现象 | 实验结论 | |
| 实验iv | 取少量久置的 溶液于试管中,向其中滴加5滴KSCN溶液 溶液于试管中,向其中滴加5滴KSCN溶液 | _______ |  溶液部分变质 溶液部分变质 |
| 实验v | _______ | _______ | |
(4)小组同学查阅资料得知,“维生素C可将
 转化为
转化为 ”。为了验证维生素C的作用,设计了如表实验vi。
”。为了验证维生素C的作用,设计了如表实验vi。| 实验操作 | 实验现象 | |
| 实验vi | 取一定量 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性 溶液 溶液 | 紫色褪去 |
 转化为
转化为 ”的结论?请说明理由
”的结论?请说明理由
您最近一年使用:0次
2022-12-29更新
|
300次组卷
|
2卷引用:安徽省淮北市第一中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
7 . 下列除杂方式不可行的是
A. 溶液中混有 溶液中混有 :加入足量的铁粉 :加入足量的铁粉 |
B. 溶液中混有 溶液中混有 :应通入足量的 :应通入足量的 气体 气体 |
C. ( ( ):将混合气体通过足量的饱和食盐水 ):将混合气体通过足量的饱和食盐水 |
D. 中混有 中混有 :加入足量的 :加入足量的 溶液后,过滤、洗涤 溶液后,过滤、洗涤 |
您最近一年使用:0次
2022-12-29更新
|
206次组卷
|
2卷引用:甘肃省天水市第一中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
8 . 下图是物质间发生化学反应的颜色变化,下表选项中的物质对应正确的是
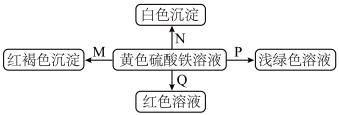

| 选项 | M | N | P | Q |
| A |  |  | 铜 | 石蕊溶液 |
| B | Na |  |  |  |
| C |  |  | 锌粉 |  |
| D |  |  | Fe | 石蕊溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-29更新
|
107次组卷
|
5卷引用:四川省天府新区太平中学2022-2023学年高一上学期期末考试化学试题
9 . 下列实验方案设计、现象与结论都正确的是
| 选项 | 目的 | 实验方案设计 | 现象与结论 |
| A | 检验溶液X中是否含有 | 向溶液X中滴加少量稀硝酸,然后滴入几滴 溶液,观察现象 溶液,观察现象 | 有白色沉淀产生,说明溶液中含 |
| B | 检验食品脱氧剂中的还原铁粉是否变质 | 取少量样品溶于盐酸,滴加KSCN溶液 | 溶液变红,说明已变质 |
| C | 验证压强对化学平衡的影响 | 先将密闭注射器内充满 气体,然后将活塞往里推压缩容积 气体,然后将活塞往里推压缩容积 | 观察到注射器内气体颜色加深,证明加压使平衡向生成 气体的方向移动 气体的方向移动 |
| D | 检验1-溴丁烷的消去产物 | 向圆底烧瓶中加2.0gNaOH和15mL无水乙醇,搅拌,再加5mL 1-溴丁烷和几片碎瓷片,微热,将产生的气体通入酸性高锰酸钾溶液中 | 酸性高锰酸钾溶液紫红色褪去,有1-丁烯生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 下列物质间的转化均能一步实现的是
A.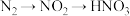 | B. |
C.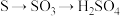 | D.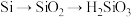 |
您最近一年使用:0次
2022-12-28更新
|
157次组卷
|
2卷引用:陕西省渭南市华阴市2021-2022学年高一上学期期末考试化学试题




