名校
解题方法
1 . 某澄清透明溶液中只可能含 、
、 、
、 、
、 、
、 和
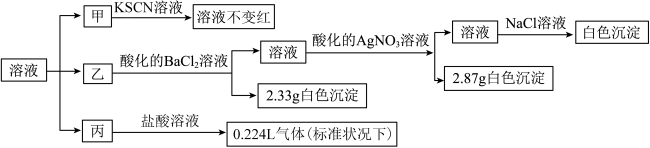
和 中的几种(忽略水解或水的电离)。取300mL溶液,平均分成甲、乙、丙三等份,设计如下实验。若往乙中加入的所有试剂均恰好完全反应,往丙中所加盐酸过量,且产生的气体全部逸出。下列说法正确的是
中的几种(忽略水解或水的电离)。取300mL溶液,平均分成甲、乙、丙三等份,设计如下实验。若往乙中加入的所有试剂均恰好完全反应,往丙中所加盐酸过量,且产生的气体全部逸出。下列说法正确的是
 、
、 、
、 、
、 、
、 和
和 中的几种(忽略水解或水的电离)。取300mL溶液,平均分成甲、乙、丙三等份,设计如下实验。若往乙中加入的所有试剂均恰好完全反应,往丙中所加盐酸过量,且产生的气体全部逸出。下列说法正确的是
中的几种(忽略水解或水的电离)。取300mL溶液,平均分成甲、乙、丙三等份,设计如下实验。若往乙中加入的所有试剂均恰好完全反应,往丙中所加盐酸过量,且产生的气体全部逸出。下列说法正确的是
A.溶液中一定含有 、 、 和 和 |
B.甲中含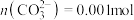 |
C.若100mL中含有0.04mol ,是否存在 ,是否存在 仍需要用焰色试验检验 仍需要用焰色试验检验 |
D.原溶液中 |
您最近一年使用:0次
名校
2 . 常温下,下列各组微粒在指定溶液中可能大量共存 的是
A.与铝粉反应放出氢气的溶液中:NO 、Mg2+、Na+、I- 、Mg2+、Na+、I- |
B.遇酚酞显红色的溶液中:Na+、Cl-、SO 、ClO- 、ClO- |
| C.含有大量Fe3+的溶液中:K+、Mg2+、S2-、SCN- |
D.常温下,pH<1的无色溶液中:Fe2+、Al3+、MnO 、 HSO 、 HSO |
您最近一年使用:0次
名校
3 . 对于某些物质或离子的检验及结论正确的是
A.向某溶液中滴加NaOH溶液后,加热,用湿润蓝色石蕊试纸检验发现变红,该溶液中一定含有NH |
| B.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,则原溶液一定含有Fe2+ |
C.向某溶液中加足量盐酸,产生无色无味气体能使澄清石灰水变浑浊,该溶液一定含有CO |
| D.某气体能使湿润淀粉碘化钾试纸变蓝,则该气体一定是氯气 |
您最近一年使用:0次
2024-02-22更新
|
310次组卷
|
3卷引用:河南省安阳市林州市第一中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
4 . 下列实验操作、现象及结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 取少量溶液X,向其中加入适量新制的氯水,再加几滴KSCN溶液 | 溶液颜色变红 | 溶液X含有Fe3+ |
| B | 向饱和的Na2CO3溶液通入CO2 | 产生白色沉淀 | 溶解度:NaHCO3<Na2CO3 |
| C | 向Fe2O3、CuO、Fe的混合粉末中加入过量稀盐酸 | 析出红色固体 | 反应后溶液中阳离子只有H+和Fe2+ |
| D | 取少量溶液Y,先滴加稀硝酸酸化,再滴加适量AgNO3溶液 | 生成白色沉淀 | Y溶液中有Cl- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-22更新
|
131次组卷
|
2卷引用:海南省白沙学校2023-2024学年高一上学期期末考试化学试题
解题方法
5 . 按要求完成下列问题。
(1)过氧化钠可用于呼吸面具中作为氧气的来源。完成下列化学方程式: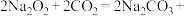
________ ;
(2)厨房中用的食盐和纯碱外观相似。某同学为区分这两种物质,各取少量置于玻璃杯中,滴加食醋,有气体产生的是___________ (填“食盐”或“纯碱”)。
(3)向盛有FeCl3溶液的试管中,滴加几滴KSCN溶液,溶液显___________ 色;
(4)Al2O3能溶于酸或强碱溶液生成盐和水,它是一种___________ (填“酸性”“碱性”或“两性”)氧化物;
(5)铁可以形成多种氧化物,其中常用作红色油漆和涂料的是___________ (填字母代号)。
A.FeO B.Fe2O3 C.Fe3O4
(1)过氧化钠可用于呼吸面具中作为氧气的来源。完成下列化学方程式:
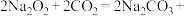
(2)厨房中用的食盐和纯碱外观相似。某同学为区分这两种物质,各取少量置于玻璃杯中,滴加食醋,有气体产生的是
(3)向盛有FeCl3溶液的试管中,滴加几滴KSCN溶液,溶液显
(4)Al2O3能溶于酸或强碱溶液生成盐和水,它是一种
(5)铁可以形成多种氧化物,其中常用作红色油漆和涂料的是
A.FeO B.Fe2O3 C.Fe3O4
您最近一年使用:0次
名校
6 . 高铁酸钾 是一种新型、高效、无毒的绿色环保水处理材料。
是一种新型、高效、无毒的绿色环保水处理材料。 为紫色固体,微溶于
为紫色固体,微溶于 溶液,具有强氧化性,在酸性或中性溶液中快速产生
溶液,具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
(1) 的制备。
的制备。 的制备装置如图,回答下列问题。
的制备装置如图,回答下列问题。
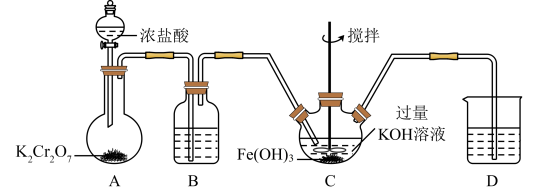
①A装置中盛放 的仪器为
的仪器为_____ (填仪器名称), 装置中反应的化学方程式为
装置中反应的化学方程式为_____ (提示:在酸性条件下, 常被还原为
常被还原为 )。
)。
②B装置中所盛试剂为_____ ;D装置的作用为_____ 。
③ 为制备
为制备 的主体装置,反应分两步进行,第一步为氯气与
的主体装置,反应分两步进行,第一步为氯气与 溶液的反应,第二步为第一步的产物之一氧化
溶液的反应,第二步为第一步的产物之一氧化 的过程。则第二步反应的离子方程式为
的过程。则第二步反应的离子方程式为_____ 。
(2)探究 的性质。取
的性质。取 中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液
中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液 ,经检验气体中含有
,经检验气体中含有 。为验证
。为验证 能否将
能否将 氧化从而产生
氧化从而产生 ,设计以下方案:
,设计以下方案:
①方案Ⅰ中溶液变红的原因为_____ (用离子方程式表示)。产生该现象_____ (填“能”或“不能”)判断一定是由 与
与 反应形成
反应形成 所致。如果不能,还可能因为
所致。如果不能,还可能因为_____ (填写离子方程式,如果上一空选“能”则本空不填)。
②方案Ⅱ得出氧化性:
_____  (填“>”或“<”)。
(填“>”或“<”)。
 是一种新型、高效、无毒的绿色环保水处理材料。
是一种新型、高效、无毒的绿色环保水处理材料。 为紫色固体,微溶于
为紫色固体,微溶于 溶液,具有强氧化性,在酸性或中性溶液中快速产生
溶液,具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。(1)
 的制备。
的制备。 的制备装置如图,回答下列问题。
的制备装置如图,回答下列问题。
①A装置中盛放
 的仪器为
的仪器为 装置中反应的化学方程式为
装置中反应的化学方程式为 常被还原为
常被还原为 )。
)。②B装置中所盛试剂为
③
 为制备
为制备 的主体装置,反应分两步进行,第一步为氯气与
的主体装置,反应分两步进行,第一步为氯气与 溶液的反应,第二步为第一步的产物之一氧化
溶液的反应,第二步为第一步的产物之一氧化 的过程。则第二步反应的离子方程式为
的过程。则第二步反应的离子方程式为(2)探究
 的性质。取
的性质。取 中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液
中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液 ,经检验气体中含有
,经检验气体中含有 。为验证
。为验证 能否将
能否将 氧化从而产生
氧化从而产生 ,设计以下方案:
,设计以下方案:| 方案Ⅰ | 取少量溶液 ,滴加 ,滴加 溶液至过量,溶液呈红色 溶液至过量,溶液呈红色 |
| 方案Ⅱ | 用 溶液充分洗涤 溶液充分洗涤 中所得固体,再用 中所得固体,再用 溶液将 溶液将 溶出 溶出得到紫色溶液  。取少量 。取少量 ,滴加盐酸,有 ,滴加盐酸,有 产生 产生 |
 与
与 反应形成
反应形成 所致。如果不能,还可能因为
所致。如果不能,还可能因为②方案Ⅱ得出氧化性:

 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
7 . 实验室用如下装置制取氯气,并进行氯气性质实验。回答下列问题:

已知:E中放置干燥红色布条,F中放置湿润红色布条。
(1)A中盛有浓盐酸,B中盛有 。加热时B中的化学方程式为
。加热时B中的化学方程式为___________ 。
(2)在实验室通过KMnO4与浓盐酸常温下反应也可制取氯气,据此推断KMnO4、Cl2、MnO2三种物质的氧化性由强到弱的顺序为___________ (用化学式表示)。
(3)D中盛放的试剂为___________ 。
(4)对比E和F中现象的差异可得出的结论是___________ 。
(5)实验后观察到G中溶液呈棕黄色,同学们猜测氧化产物可能有以下三种情况:
猜测1:只有Fe3+;
猜测2:只有I2;
猜测3:既有Fe3+又有I2。
于是取上述实验后G中的溶液进行如下实验:
①加入___________ 溶液,溶液未出现红色,证明猜测1和猜测3不正确;
②再加入___________ (填试剂和现象)证明猜测2正确。
由此得出离子的还原性Fe2+___________ I-(填“大于”,“等于”,“小于”)。
(6)H装置可用于模拟工业制造漂白粉的原理,实验后制得产品的有效成分是___________ (填化学式)。

已知:E中放置干燥红色布条,F中放置湿润红色布条。
(1)A中盛有浓盐酸,B中盛有
 。加热时B中的化学方程式为
。加热时B中的化学方程式为(2)在实验室通过KMnO4与浓盐酸常温下反应也可制取氯气,据此推断KMnO4、Cl2、MnO2三种物质的氧化性由强到弱的顺序为
(3)D中盛放的试剂为
(4)对比E和F中现象的差异可得出的结论是
(5)实验后观察到G中溶液呈棕黄色,同学们猜测氧化产物可能有以下三种情况:
猜测1:只有Fe3+;
猜测2:只有I2;
猜测3:既有Fe3+又有I2。
于是取上述实验后G中的溶液进行如下实验:
①加入
②再加入
由此得出离子的还原性Fe2+
(6)H装置可用于模拟工业制造漂白粉的原理,实验后制得产品的有效成分是
您最近一年使用:0次
8 . 现有A~G七种中学常见物质,它们之间能发生如下反应(图中部分反应物、产物及反应条件未标出)。
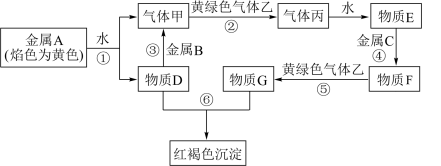
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:B___________ 、C___________ 、乙___________ 。
(2)借助KSCN溶液检验物质F中金属阳离子的方法是___________ 。
(3)写出反应③和⑤的离子方程式:___________ 、___________ 。
(4)将物质F少许,置于试管中,并加入NaOH溶液,其现象为___________ ,发生反应的化学方程式为___________ 、___________ 。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:B
(2)借助KSCN溶液检验物质F中金属阳离子的方法是
(3)写出反应③和⑤的离子方程式:
(4)将物质F少许,置于试管中,并加入NaOH溶液,其现象为
您最近一年使用:0次
解题方法
9 . 下列各组离子在对应条件下一定能大量共存的是
A.澄清溶液中: |
B.加入金属铝能放出氢气的溶液: |
C. 大量存在的溶液中: 大量存在的溶液中: |
D.遇石蕊变红的溶液: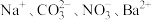 |
您最近一年使用:0次
名校
解题方法
10 . 下列转化必须加入氧化剂才能实现的是
A. | B.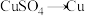 |
C.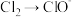 | D. |
您最近一年使用:0次



