解题方法
1 . 下列除去杂质的方法正确的是
A.用铁粉除去 溶液中含有的少量 溶液中含有的少量 |
B.用新制氯水除去 溶液中含有的少量 溶液中含有的少量 |
| C.铁粉中混有少量铝粉:加入烧碱溶液充分反应,过滤、洗涤、干燥 |
D. 溶液中混有少量 溶液中混有少量 :加入过量氨水充分反应,过滤、洗涤、干燥 :加入过量氨水充分反应,过滤、洗涤、干燥 |
您最近一年使用:0次
2 . 某工理师为了从使用过的腐蚀废液(主要含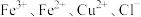 )中回收铜,并重新获得纯净的
)中回收铜,并重新获得纯净的 溶液,准备采用下列步骤:
溶液,准备采用下列步骤:

(1)请写出上述实验中加入的有关物质的化学式:
①______________ ,④______________ 。
(2)实验室收集制取出的黄绿色气体⑥的方法是______________ 。
(3)写出向②⑤的混合液中通入⑥的离子方程式______________ 。
(4)将铜片放入 溶液中,反应一段时间后取出铜片,溶液中
溶液中,反应一段时间后取出铜片,溶液中 ,则此时溶液中的
,则此时溶液中的 与
与 的物质的量之比为
的物质的量之比为______________ 。
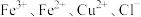 )中回收铜,并重新获得纯净的
)中回收铜,并重新获得纯净的 溶液,准备采用下列步骤:
溶液,准备采用下列步骤:
(1)请写出上述实验中加入的有关物质的化学式:
①
(2)实验室收集制取出的黄绿色气体⑥的方法是
(3)写出向②⑤的混合液中通入⑥的离子方程式
(4)将铜片放入
 溶液中,反应一段时间后取出铜片,溶液中
溶液中,反应一段时间后取出铜片,溶液中 ,则此时溶液中的
,则此时溶液中的 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
名校
3 . 某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)甲组同学研究pH对FeSO4稳定性的影响,得到如图所示结果,增强Fe2+稳定性的措施为___________ 。(写出一条即可)

(2)乙组同学为了探究Fe2(SO4)3与Cu的反应,做了如图所示实验:
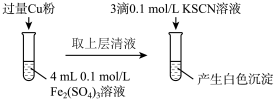
①Fe3+与Cu反应的离子方程式为___________ 。
②为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.SCN的化学性质与I-相似;
iii.2Cu2++4I-=2CuI↓+I2。
实验方案:
Cu2+与SCN-反应的离子方程式为 ___________ 。
(3)市售某种补铁口服液的主要成分是葡萄糖酸亚铁。根据名称猜测该糖浆中含有Fe2+,设计方案进行验证。
①方案ⅰ预期现象与实际现象相同,并不能证明补贴口服液中一定含有Fe2+,猜想理由是:___________ 。
②方案ⅱ中实验现象是___________ ,证明补铁口服液中含有Fe2+。
(1)甲组同学研究pH对FeSO4稳定性的影响,得到如图所示结果,增强Fe2+稳定性的措施为

(2)乙组同学为了探究Fe2(SO4)3与Cu的反应,做了如图所示实验:

①Fe3+与Cu反应的离子方程式为
②为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.SCN的化学性质与I-相似;
iii.2Cu2++4I-=2CuI↓+I2。
实验方案:
| 实验方案 | 现象 |
| 步骤1:取4mL0.2mol/L的FeSO4溶液,向其中滴加3滴0.1mol/L的KSCN溶液 | 无明显现象 |
| 步骤2:取4mL 0.1 mol/L的CuSO4溶液,向其中滴加3滴0.1mol/L的KSCN溶液 | 产生白色沉淀 |
(3)市售某种补铁口服液的主要成分是葡萄糖酸亚铁。根据名称猜测该糖浆中含有Fe2+,设计方案进行验证。
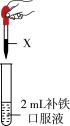 | 方案 | 试剂X |
| 方案ⅰ | 1mL 1mol/L酸性KMnO4溶液 | |
| 方案ⅱ | 依次加入5滴KSCN溶液、1mL新制氯水 |
②方案ⅱ中实验现象是
您最近一年使用:0次
解题方法
4 . 分别进行下列操作,由现象得出的结论正确的是
| 选项 | 操作 | 现象 | 结论 |
| A |  溶液加入 溶液加入 与 与 组成的悬浊液中 组成的悬浊液中 | 出现黑色沉淀 | 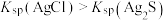 |
| B | 向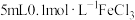 溶液中加入 溶液中加入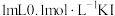 溶液,充分反应后,试管中滴加5~6滴 溶液,充分反应后,试管中滴加5~6滴 的 的 溶液,观察试管中溶液的颜色 溶液,观察试管中溶液的颜色 | 溶液变为血红色 | 证明 与 与 之间的反应属于可逆反应 之间的反应属于可逆反应 |
| C | 向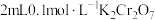 溶液中加入5滴98%的硫酸 溶液中加入5滴98%的硫酸 | 溶液颜色橙色变深 | 改变生成物的浓度,平衡移动 |
| D | 室温下,测定浓度均为 的 的 与 与 溶液的pH 溶液的pH |  溶液的pH大 溶液的pH大 | 结合 的能力: 的能力: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 教材中的实验有助于理论知识的学习,下列说法错误的是
| A | B | C | D |
 |  | 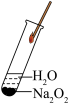 | 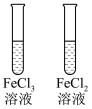 |
| 加热碳酸钠或碳酸氢钠 | 光照过程中氯水中氯离子的浓度变化 |  与水的反应 与水的反应 | 分别向 溶液和 溶液和 溶液中滴入 溶液中滴入 溶液 溶液 |
| 可以比较二者的热稳定性 | 氯离子浓度升高的原因是 分解 分解 | 带火星的木条复燃说明该反应生成氧气 | 此实验现象可应用于除去 溶液中的 溶液中的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 对于下列实验,能正确描述其反应的离子方程式是
A. 固体溶于氢碘酸: 固体溶于氢碘酸: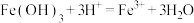 |
B.向 溶液中通入少量 溶液中通入少量 : :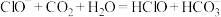 |
C.向 溶液中通入足量 溶液中通入足量 : : |
D.双氧水与酸性 溶液反应: 溶液反应: |
您最近一年使用:0次
7 . Ⅰ
(1)现有以下物质:① 固体②盐酸③
固体②盐酸③ 溶液④铜⑤
溶液④铜⑤ ⑥硫酸氢钾固体⑦乙醇
⑥硫酸氢钾固体⑦乙醇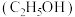 ⑧
⑧ 晶体⑨熔融态
晶体⑨熔融态 ⑩液氨。其中属于电解质的是
⑩液氨。其中属于电解质的是_____ 。(填序号)
Ⅱ、 都是中学化学中常见物质,其中均含有同一种元素,在一定条件下的相互转化关系如图所示(部分反应中的水已略去)根据题意回答下列问题:
都是中学化学中常见物质,其中均含有同一种元素,在一定条件下的相互转化关系如图所示(部分反应中的水已略去)根据题意回答下列问题:

(2)若 的焰色试验均为黄色,且
的焰色试验均为黄色,且 为强碱,
为强碱, 为绿色植物光合作用不可或缺的原料。
为绿色植物光合作用不可或缺的原料。
①除 固体中混有的
固体中混有的 固体的方法为
固体的方法为_____ (填除杂方法的名称),反应方程式为_____ 。
②反应Ⅲ的离子方程式为_____ 。
③ 的电子式为
的电子式为_____ , 的电子式为
的电子式为_____ 。
(3)若 为气体单质,
为气体单质, 为一种黑色金属单质。
为一种黑色金属单质。
①反应Ⅱ的离子方程式为_____ 。
②一定条件下, 能与水发生反应,该反应的化学方程式为
能与水发生反应,该反应的化学方程式为_____ 。
③检验 溶液中金属阳离子所用试剂名称
溶液中金属阳离子所用试剂名称_____ ,现象为_____ 。
(1)现有以下物质:①
 固体②盐酸③
固体②盐酸③ 溶液④铜⑤
溶液④铜⑤ ⑥硫酸氢钾固体⑦乙醇
⑥硫酸氢钾固体⑦乙醇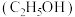 ⑧
⑧ 晶体⑨熔融态
晶体⑨熔融态 ⑩液氨。其中属于电解质的是
⑩液氨。其中属于电解质的是Ⅱ、
 都是中学化学中常见物质,其中均含有同一种元素,在一定条件下的相互转化关系如图所示(部分反应中的水已略去)根据题意回答下列问题:
都是中学化学中常见物质,其中均含有同一种元素,在一定条件下的相互转化关系如图所示(部分反应中的水已略去)根据题意回答下列问题:
(2)若
 的焰色试验均为黄色,且
的焰色试验均为黄色,且 为强碱,
为强碱, 为绿色植物光合作用不可或缺的原料。
为绿色植物光合作用不可或缺的原料。①除
 固体中混有的
固体中混有的 固体的方法为
固体的方法为②反应Ⅲ的离子方程式为
③
 的电子式为
的电子式为 的电子式为
的电子式为(3)若
 为气体单质,
为气体单质, 为一种黑色金属单质。
为一种黑色金属单质。①反应Ⅱ的离子方程式为
②一定条件下,
 能与水发生反应,该反应的化学方程式为
能与水发生反应,该反应的化学方程式为③检验
 溶液中金属阳离子所用试剂名称
溶液中金属阳离子所用试剂名称
您最近一年使用:0次
名校
解题方法
8 . 某变质的废铜屑主要成分为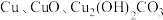 (其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是
(其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是

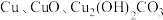 (其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是
(其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是
A.基态铜原子的价层电子排布式为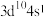 |
B.滤液1的溶质主要成分为 |
C.若分铜过程生成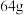 铜,则浸泡过程理论上有 铜,则浸泡过程理论上有 电子转移 电子转移 |
D.可用铁氰化钾溶液检验滤液2中 的存在 的存在 |
您最近一年使用:0次
名校
9 . 价类二维图是学习元素及其化合物知识的重要模型和工具。图甲为某常见金属单质及其部分化合物的价类二维图。下列推断不合理的是


| A.b、c、e、d均难溶于水 |
| B.可通过图乙装置制备物质e,且较长时间不易被氧化 |
| C.g具有强氧化性,可用于印刷电路板的刻蚀 |
| D.b、c均可与稀盐酸反应,且反应原理相同 |
您最近一年使用:0次
2024-02-24更新
|
102次组卷
|
2卷引用:云南省昭通市第一中学教研联盟2023-2024学年高一上学期期末质量检测化学(B卷)试题
名校
解题方法
10 . 除杂试剂的选择或除杂操作不正确的是
| 选项 | 括号内为杂质 | 除杂试剂 | 除杂操作 |
| A | 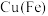 固体 固体 | 稀盐酸 | 充分反应后过滤 |
| B | 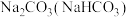 溶液 溶液 |  | 通入过量的 |
| C |  溶液 溶液 | 铁粉 | 充分反应后过滤 |
| D | 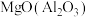 固体 固体 |  溶液 溶液 | 充分反应后过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



