1 . 已知:A、B、C、D、E、X是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。___________ 。
(2)若A为淡黄色粉末,X为非金属单质,通常为黑色粉末,则 与足量的
与足量的 充分反应时,转移电子总数为
充分反应时,转移电子总数为___________ ;若X为一种最常见的造成温室效应的气体。则鉴别等浓度的D、E两种溶液,可选择的试剂为___________ 。(填字母)
a. 溶液 b.氨水 c.澄清石灰水 d.
溶液 b.氨水 c.澄清石灰水 d. 溶液
溶液
(3)若A、B均为氮的常见氧化物,X是Fe,溶液D加入 溶液变红。
溶液变红。
①写出加热条件下C的浓溶液与X反应生成D的化学方程式___________ 。
②检验溶液D中还可能存在 的方法是
的方法是___________ 。
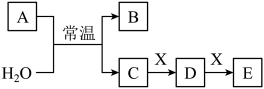
(2)若A为淡黄色粉末,X为非金属单质,通常为黑色粉末,则
 与足量的
与足量的 充分反应时,转移电子总数为
充分反应时,转移电子总数为a.
 溶液 b.氨水 c.澄清石灰水 d.
溶液 b.氨水 c.澄清石灰水 d. 溶液
溶液(3)若A、B均为氮的常见氧化物,X是Fe,溶液D加入
 溶液变红。
溶液变红。①写出加热条件下C的浓溶液与X反应生成D的化学方程式
②检验溶液D中还可能存在
 的方法是
的方法是
您最近一年使用:0次
2024-02-02更新
|
264次组卷
|
2卷引用:重庆市璧山来凤中学校2023-2024学年高一下学期3月月考化学试题
名校
解题方法
2 . 化学在医学上起到至关重要的作用。如:小苏打、氢氧化铝等可治疗胃酸(主要成分为稀盐酸)过多;硫酸亚铁可补铁、防治贫血;三价铬用于加强胰岛素的作用。试回答下列问题:
(1)写出小苏打与胃酸作用的离子方程式:_______ ,但该药剂缺点是易导致胃胀气,胃溃疡患者不能使用,而氢氧化铝很好的解决了这个问题,它在中和胃酸的同时,保护溃疡面,写出氢氧化铝与胃酸作用的化学方程式为_______ 。
(2)利用提供试剂设计实验证明补铁剂中铁元素都以+2存在(可选试剂:硫氰化钾、过氧化氢):_______ (填写实验操作、现象和结论)。
(3)三价铬是人体必需的微量元素,六价铬则严重危害人体健康,铬元素化合价循环示意图如下【已知: 可溶于水;
可溶于水; 难溶于水】:
难溶于水】:
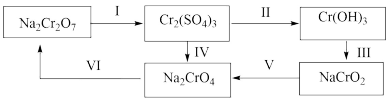
①步骤I所用的试剂是硫酸酸化的 ,请写出该反应的离子方程式;
,请写出该反应的离子方程式;_______
②现有含 和
和 的溶液,逐滴滴加NaOH溶液至过量,由上图信息可知,铁元素、铬元素的存在形态分别是
的溶液,逐滴滴加NaOH溶液至过量,由上图信息可知,铁元素、铬元素的存在形态分别是_______ 、_______ ;
③向50mL0.03mol/L的 溶液中,加入50mL0.2mol/L的NaOH溶液,写出相应离子反应方程式
溶液中,加入50mL0.2mol/L的NaOH溶液,写出相应离子反应方程式_______ 。
(1)写出小苏打与胃酸作用的离子方程式:
(2)利用提供试剂设计实验证明补铁剂中铁元素都以+2存在(可选试剂:硫氰化钾、过氧化氢):
(3)三价铬是人体必需的微量元素,六价铬则严重危害人体健康,铬元素化合价循环示意图如下【已知:
 可溶于水;
可溶于水; 难溶于水】:
难溶于水】:
①步骤I所用的试剂是硫酸酸化的
 ,请写出该反应的离子方程式;
,请写出该反应的离子方程式;②现有含
 和
和 的溶液,逐滴滴加NaOH溶液至过量,由上图信息可知,铁元素、铬元素的存在形态分别是
的溶液,逐滴滴加NaOH溶液至过量,由上图信息可知,铁元素、铬元素的存在形态分别是③向50mL0.03mol/L的
 溶液中,加入50mL0.2mol/L的NaOH溶液,写出相应离子反应方程式
溶液中,加入50mL0.2mol/L的NaOH溶液,写出相应离子反应方程式
您最近一年使用:0次
2023-01-12更新
|
417次组卷
|
2卷引用:重庆市南开中学2022-2023学年高一上期期末考试化学试题
名校
3 . 铁的化合物在实际中应用广泛,如氯化铁可用于五金蚀刻、污水处理及作催化剂、凝聚剂等,Na2FeO4可用作净水剂等。
(1)氯化铁溶液用于五金蚀刻时的反应产物是氯化亚铁,再通入氯气,又可将其转化为氯化铁,则通入氯气后反应的离子方程式为___________ 。
(2)氯化铁常用于净水,是因为铁离子转化为Fe(OH)3胶体,使水中悬浮物聚沉,Fe(OH)3胶体分散质微粒直径的范围是___________ 。实验室利用饱和氯化铁溶液制备Fe(OH)3胶体的离子方程式为: ___________ 。
(3)氯化铁还可以充当双氧水分解的催化剂,2个H2O2分子发生分解时反应中转移的电子数是___________ 。
(4)Na2FeO4是一种新型的净水消毒剂,可以通过下列反应制得:Fe(NO3)3+NaOH+Cl2 →Na2FeO4+ NaNO3+ NaCl+H2O(未配平)。上述反应中氧化产物为___________ 。
(1)氯化铁溶液用于五金蚀刻时的反应产物是氯化亚铁,再通入氯气,又可将其转化为氯化铁,则通入氯气后反应的离子方程式为
(2)氯化铁常用于净水,是因为铁离子转化为Fe(OH)3胶体,使水中悬浮物聚沉,Fe(OH)3胶体分散质微粒直径的范围是
(3)氯化铁还可以充当双氧水分解的催化剂,2个H2O2分子发生分解时反应中转移的电子数是
(4)Na2FeO4是一种新型的净水消毒剂,可以通过下列反应制得:Fe(NO3)3+NaOH+Cl2 →Na2FeO4+ NaNO3+ NaCl+H2O(未配平)。上述反应中氧化产物为
您最近一年使用:0次
2022-10-22更新
|
315次组卷
|
2卷引用:重庆市南开中学校2022-2023学年高一上学期10月月考化学试题
4 . 钠、铝、铁是三种非常重要的常见金属。根据所学知识完成下列填空。
(1)将一小块金属钠投入足量水中,发生反应的离子方程式为_______ 。
(2)足量的Fe在Cl2中点燃,所得产物的化学式是_______ 。将该产物溶于水配成溶液,分装在两支试管中。
a.若向其中一支试管中滴加KSCN溶液,则溶液变成_______ 色。
b.向另一支试管中滴加NaOH溶液,现象为_______ 。
(3)纯铝片投入氢氧化钠溶液中产生气泡的化学方程式为_______ 。若2.7g纯铝片投入足量盐酸中产生氢气的物质的量为_______ mol。
(1)将一小块金属钠投入足量水中,发生反应的离子方程式为
(2)足量的Fe在Cl2中点燃,所得产物的化学式是
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,现象为
(3)纯铝片投入氢氧化钠溶液中产生气泡的化学方程式为
您最近一年使用:0次
2021-04-02更新
|
122次组卷
|
2卷引用:重庆市巫山县官渡中学2020-2021学年高一下学期第一次月考化学试题
5 . 铁是人类最早使用的金属之一,人们在5000多年前就开始使用铁,如今它是应用最广泛的金属,被誉为“金属之王”。请回答下列问题:
(1)红热的铁与水蒸气发生反应生成的产物是_______ 。(填化学式)
(2)向盛有硫酸铁溶液的烧杯中滴加NaOH溶液,产生的现象是_______ 。
(3)氯化铁可用于五金蚀刻,不锈钢广告牌上的图形和文字就是用氯化铁溶液蚀刻而成,该过程发生的主要反应的离子方程式为_______ ,该反应说明_______ (填化学式)具有氧化性。
(4)某工业废水中含有大量FeSO4和较多Cu2+,为减少污染并变废为宝,向该废水中加入足量Fe并过滤以回收FeSO4和金属铜。
①加入Fe发生反应的离子方程式为_______ 。
②过滤后的固体中含有Cu和_______ (填化学式),可加入_______ (填试剂名称)再过滤,得到金属铜。
③若经过回收得到128g金属铜,则加入Fe的质量至少为_______ g。
(1)红热的铁与水蒸气发生反应生成的产物是
(2)向盛有硫酸铁溶液的烧杯中滴加NaOH溶液,产生的现象是
(3)氯化铁可用于五金蚀刻,不锈钢广告牌上的图形和文字就是用氯化铁溶液蚀刻而成,该过程发生的主要反应的离子方程式为
(4)某工业废水中含有大量FeSO4和较多Cu2+,为减少污染并变废为宝,向该废水中加入足量Fe并过滤以回收FeSO4和金属铜。
①加入Fe发生反应的离子方程式为
②过滤后的固体中含有Cu和
③若经过回收得到128g金属铜,则加入Fe的质量至少为
您最近一年使用:0次
名校
6 . (1)工业上将氯气通入NaOH溶液中制取“84”消毒液,其化学反应方程式为__ ;
(2)过氧化钠可用于呼吸面具或潜水艇中作为氧气的来源,请写出过氧化钠与CO2反应的化学方程式___ ;
(3)化学科学在药物的开发、合成和使用中起着至关重要的作用。如小苏打、氢氧化铝等可治疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
①写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:__ 。
②写出Al(OH)3与NaOH溶液反应的离子方程式__ 。
③在补铁剂中加入氯水可将Fe2+氧化成Fe3+,,写出相关的离子反应方程式:__ ,检验Fe3+常用的试剂除碱外,还可以用___ (填化学式),现象是__ 。
(2)过氧化钠可用于呼吸面具或潜水艇中作为氧气的来源,请写出过氧化钠与CO2反应的化学方程式
(3)化学科学在药物的开发、合成和使用中起着至关重要的作用。如小苏打、氢氧化铝等可治疗胃酸过多,硫酸亚铁可补铁、防治贫血。试回答下列问题:
①写出小苏打与胃酸(主要成分为稀盐酸)作用的离子方程式:
②写出Al(OH)3与NaOH溶液反应的离子方程式
③在补铁剂中加入氯水可将Fe2+氧化成Fe3+,,写出相关的离子反应方程式:
您最近一年使用:0次
名校
解题方法
7 . 铁是应用泛的金属之一,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)某课题小组采用离子交换和滴定的方法来测定铁的某氯化物 的化学式。实验中称取0.54g的
的化学式。实验中称取0.54g的 样品,溶解后先进行阳离子交换预处理,再通过含有饱和
样品,溶解后先进行阳离子交换预处理,再通过含有饱和 的阴离子交换柱,使
的阴离子交换柱,使 和
和 发生交换。交换完成后,流出溶液的
发生交换。交换完成后,流出溶液的 用
用 的盐酸滴定,滴定至终点时消耗盐酸25.00mL。通过计算求出
的盐酸滴定,滴定至终点时消耗盐酸25.00mL。通过计算求出 中x的值为
中x的值为_________ (取整数)。
(2)在实验室中,FeCl2可用铁粉和_________ 反应制备,FeCl3可用铁粉和_________ 反应制备。现有一瓶FeCl2溶液,某同学欲检验该溶液是否已经变质,首先取适量溶液于洁净的试管中,然后向溶液中滴加几滴______________ ,观察溶液是否变成红色即可得出结论。
(3)FeCl3与氢碘酸混合时有棕色物质生成,写出该反应的离子方程式:________ ;工业上还可以用FeCl3溶液来腐蚀印刷电路板上的铜,向反应所得的溶液中加入一定量的锌粉充分反应后,从理论上分析,下列说法合理的是____________ 。(填序号)。
A.若无固体剩余,则溶液中可能含有 、
、 、
、 、
、 四种离子
四种离子
B.若溶液中有 ,则体系中一定没有固体剩余
,则体系中一定没有固体剩余
C.若有固体剩余,则溶液中一定有反应 发生
发生
D.当溶液中有 存在时,则一定没有
存在时,则一定没有 析出
析出
(4)高铁酸钾( )是一种强氧化剂,可作为水处理剂和高容量电池的电极材料。在
)是一种强氧化剂,可作为水处理剂和高容量电池的电极材料。在 中铁元素的化合价为
中铁元素的化合价为_________ , 与
与 在强碱性条件下反应可制取
在强碱性条件下反应可制取 ,其反应的离子方程式为
,其反应的离子方程式为________ 。
(1)某课题小组采用离子交换和滴定的方法来测定铁的某氯化物
 的化学式。实验中称取0.54g的
的化学式。实验中称取0.54g的 样品,溶解后先进行阳离子交换预处理,再通过含有饱和
样品,溶解后先进行阳离子交换预处理,再通过含有饱和 的阴离子交换柱,使
的阴离子交换柱,使 和
和 发生交换。交换完成后,流出溶液的
发生交换。交换完成后,流出溶液的 用
用 的盐酸滴定,滴定至终点时消耗盐酸25.00mL。通过计算求出
的盐酸滴定,滴定至终点时消耗盐酸25.00mL。通过计算求出 中x的值为
中x的值为(2)在实验室中,FeCl2可用铁粉和
(3)FeCl3与氢碘酸混合时有棕色物质生成,写出该反应的离子方程式:
A.若无固体剩余,则溶液中可能含有
 、
、 、
、 、
、 四种离子
四种离子B.若溶液中有
 ,则体系中一定没有固体剩余
,则体系中一定没有固体剩余C.若有固体剩余,则溶液中一定有反应
 发生
发生D.当溶液中有
 存在时,则一定没有
存在时,则一定没有 析出
析出(4)高铁酸钾(
 )是一种强氧化剂,可作为水处理剂和高容量电池的电极材料。在
)是一种强氧化剂,可作为水处理剂和高容量电池的电极材料。在 中铁元素的化合价为
中铁元素的化合价为 与
与 在强碱性条件下反应可制取
在强碱性条件下反应可制取 ,其反应的离子方程式为
,其反应的离子方程式为
您最近一年使用:0次
8 . 国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:_______ 。
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:_________ 。
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_________ 。若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是________ (填字母)。
A.有铜无铁 B.有铁无铜
C.铁、铜都有 D.铁、铜都无
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:
(2)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
A.有铜无铁 B.有铁无铜
C.铁、铜都有 D.铁、铜都无
您最近一年使用:0次
9 . 按要求完成下列填空
(1)检验铁离子(Fe3+):试剂____________ (填化学式);现象______________ 。有铁离子(Fe3+)的环境下检验是否含有亚铁离子(Fe2+):试剂:_________ (填化学式),现象_______________ 。
(2)用小苏打片治疗胃酸过多的离子方程式为____________ 。
(3)镁带着火时,不能用液态CO2灭火剂来灭火的原因是_____________ 。(用化学方程式表示).
(4)除去混入Fe2O3粉末中少量Al2O3杂质离子方程式为______________ 。
(5)将AlCl3溶液蒸干,灼烧,得到的固体产物是__________ 。AlCl3溶液和NaHCO3溶液混合时发生反应的离子方程式为_________________ 。
(1)检验铁离子(Fe3+):试剂
(2)用小苏打片治疗胃酸过多的离子方程式为
(3)镁带着火时,不能用液态CO2灭火剂来灭火的原因是
(4)除去混入Fe2O3粉末中少量Al2O3杂质离子方程式为
(5)将AlCl3溶液蒸干,灼烧,得到的固体产物是
您最近一年使用:0次
10 . 铁是一种重要的金属材料,它的单质及化合物在生产生活中应用广泛。
(1)生铁含有C、Si、Mn、S、P等元素,其中属于金属元素的除Fe外,还有_______ 元素。
(2)铁元素有三种常见的氧化物,分别是FeO、Fe2O3、Fe3O4。其中具有磁性的是____________ ,可作为红色颜料的是____________ 。
(3)某补铁口服液中含有Fe2+,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为____________ 色,则说明其已变质。向该口服液中加入维生素C可防止其被氧化变质,此过程中利用了维生素C的____________ 性。
(4)FeCl3可作为铜电路板的腐蚀液,其反应原理为Cu与FeCl3溶液反应生成FeCl2和CuCl2,该反应的化学方程式为____________ 。向反应后的溶液中加入____________ ,可回收Cu,并得到FeCl2溶液。
(1)生铁含有C、Si、Mn、S、P等元素,其中属于金属元素的除Fe外,还有
(2)铁元素有三种常见的氧化物,分别是FeO、Fe2O3、Fe3O4。其中具有磁性的是
(3)某补铁口服液中含有Fe2+,为检验其是否被氧化变质,可取少量该口服液,向其中滴加KSCN溶液,若溶液变为
(4)FeCl3可作为铜电路板的腐蚀液,其反应原理为Cu与FeCl3溶液反应生成FeCl2和CuCl2,该反应的化学方程式为
您最近一年使用:0次
2019-10-31更新
|
339次组卷
|
2卷引用:重庆市2019年普通高中学业水平合格性模拟考试化学试题



