1 . 绿矾(FeSO4·7H2O)具有补血消积、燥湿杀虫功效。工业上用赤铁矿(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO等杂质)制备绿矾的工业流程如图所示:
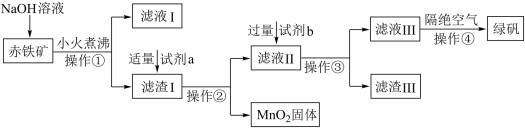
已知:Al2O3可溶于强碱溶液
(1)操作①的名称是___________ ,该操作要用到玻璃棒,其作用为___________ 。
(2)试剂a为稀硫酸,试剂b为铁粉,加入过量试剂b后金属元素之间发生反应的离子方程式为___________ 、___________ 。
(3)滤渣Ⅲ含有___________ ,将其快速分离的方法是___________ 。
(4)操作④隔绝空气的目的是___________ 。

已知:Al2O3可溶于强碱溶液
(1)操作①的名称是
(2)试剂a为稀硫酸,试剂b为铁粉,加入过量试剂b后金属元素之间发生反应的离子方程式为
(3)滤渣Ⅲ含有
(4)操作④隔绝空气的目的是
您最近一年使用:0次
2 . 实验室由硫铁矿烧渣(主要成分为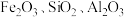 )制备软磁性材料
)制备软磁性材料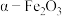 ,主要转化流程如下。
,主要转化流程如下。
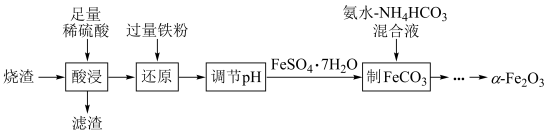
已知: 为酸性氧化物。
为酸性氧化物。
回答下列问题:
(1)“酸浸”时, 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为______________ ;“滤渣”中主要成分的化学式为______________ 。
(2)“还原”时,加入过量铁粉的主要目的是______________ ;该过程除生成 外,还会生成
外,还会生成_______ (填化学式)。
(3)根据表格信息,“调节 ”时的
”时的 范围为
范围为_______ 。
(4)“调节 ”后获得
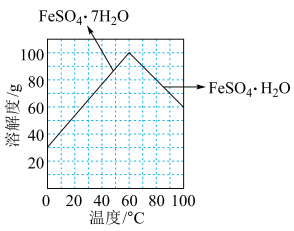
”后获得 晶体,根据如图所示的绿矾溶解度曲线,补充完整“调节
晶体,根据如图所示的绿矾溶解度曲线,补充完整“调节 ”后获得
”后获得 晶体的实验操作:向
晶体的实验操作:向 溶液中先加入稀硫酸酸化,在
溶液中先加入稀硫酸酸化,在 氛围中,
氛围中,_______ ,过滤,少量冰水洗涤,低温干燥,得到 晶体。
晶体。
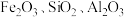 )制备软磁性材料
)制备软磁性材料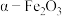 ,主要转化流程如下。
,主要转化流程如下。
离子 | 开始沉淀 | 完全沉淀 |
| 5.8 | 8.8 |
| 1.6 | 2.8 |
| 3.2 | 5.0 |
 为酸性氧化物。
为酸性氧化物。回答下列问题:
(1)“酸浸”时,
 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为(2)“还原”时,加入过量铁粉的主要目的是
 外,还会生成
外,还会生成(3)根据表格信息,“调节
 ”时的
”时的 范围为
范围为(4)“调节
 ”后获得
”后获得 晶体,根据如图所示的绿矾溶解度曲线,补充完整“调节
晶体,根据如图所示的绿矾溶解度曲线,补充完整“调节 ”后获得
”后获得 晶体的实验操作:向
晶体的实验操作:向 溶液中先加入稀硫酸酸化,在
溶液中先加入稀硫酸酸化,在 氛围中,
氛围中, 晶体。
晶体。
您最近一年使用:0次
名校
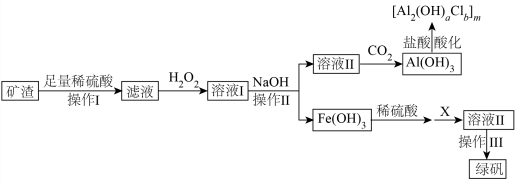
3 . 硫酸亚铁广泛应用于临床医疗,主要用于治疗各种因素导致的缺铁性贫血,如慢性失血、营养不良等,同时也可以治疗铁吸收障碍、儿童或婴儿期需铁量增加等因素引起的缺铁性贫血。絮凝剂聚合氯化铝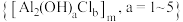 广泛用于废水处理。利用马矿的矿渣(成分为
广泛用于废水处理。利用马矿的矿渣(成分为 、
、 、
、 、
、 )制备绿矾(
)制备绿矾( )和聚合氯化铝的一种工艺流程如下:
)和聚合氯化铝的一种工艺流程如下:
已知: 不溶于稀硫酸;硫酸铝和过量
不溶于稀硫酸;硫酸铝和过量 溶液反应生成
溶液反应生成 ;
; 的絮凝效果可用盐基度(盐基度
的絮凝效果可用盐基度(盐基度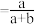 )衡量,当盐基度为0.60~0.85时,絮凝效果较好。
)衡量,当盐基度为0.60~0.85时,絮凝效果较好。
回答下列问题:
(1)操作I的名称是___________ ,需用到的玻璃仪器有___________ 。
(2)“滤液”中加入 发生的离子反应方程式是
发生的离子反应方程式是___________ ,发生该反应时可适当加热加快反应速率,但加热温度不宜过高,原因是___________ 。
(3)“溶液Ⅱ”若浓度较大,则通入过量 (
( 过量时,生成
过量时,生成 )不利于减少
)不利于减少 滤饼中的杂质,其原因是
滤饼中的杂质,其原因是___________ 。
(4)试剂“X”是___________ ,书写试剂“X”参与的化学反应方程式___________ 。
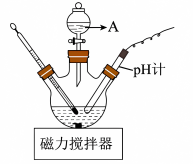
(5)“盐酸酸化”时的装置如图所示,仪器A的名称为___________ ,若要使产品盐基度为 ,则
,则
___________ 。
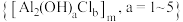 广泛用于废水处理。利用马矿的矿渣(成分为
广泛用于废水处理。利用马矿的矿渣(成分为 、
、 、
、 、
、 )制备绿矾(
)制备绿矾( )和聚合氯化铝的一种工艺流程如下:
)和聚合氯化铝的一种工艺流程如下:
已知:
 不溶于稀硫酸;硫酸铝和过量
不溶于稀硫酸;硫酸铝和过量 溶液反应生成
溶液反应生成 ;
; 的絮凝效果可用盐基度(盐基度
的絮凝效果可用盐基度(盐基度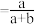 )衡量,当盐基度为0.60~0.85时,絮凝效果较好。
)衡量,当盐基度为0.60~0.85时,絮凝效果较好。回答下列问题:
(1)操作I的名称是
(2)“滤液”中加入
 发生的离子反应方程式是
发生的离子反应方程式是(3)“溶液Ⅱ”若浓度较大,则通入过量
 (
( 过量时,生成
过量时,生成 )不利于减少
)不利于减少 滤饼中的杂质,其原因是
滤饼中的杂质,其原因是(4)试剂“X”是
(5)“盐酸酸化”时的装置如图所示,仪器A的名称为
 ,则
,则

您最近一年使用:0次
名校
4 . 高铁酸钠( )是一种多功能绿色水处理剂,杀菌消毒的同时可生成氢氧化铁胶体。某工厂利用废金属屑(主要成分为Fe和Cu,含有少量
)是一种多功能绿色水处理剂,杀菌消毒的同时可生成氢氧化铁胶体。某工厂利用废金属屑(主要成分为Fe和Cu,含有少量 )制取
)制取 并回收金属Cu,工艺流程如下:
并回收金属Cu,工艺流程如下:
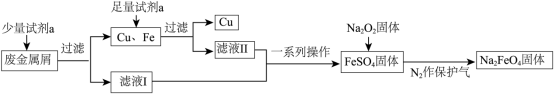
(1)试剂a为___________ (填化学式)。
(2)用离子方程式解释滤液I不含有 可能的原因
可能的原因___________ 。
(3)制备 的原理:
的原理: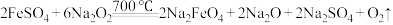 。反应中
。反应中___________ 作还原剂;每生成1mol 转移电子的物质的量为
转移电子的物质的量为___________ mol。
(4)高铁酸钠( )是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。
)是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。
①某兴趣小组欲用 固体配制100mL
固体配制100mL 的高铁酸钠溶液,需要高铁酸钠固体的质量为
的高铁酸钠溶液,需要高铁酸钠固体的质量为___________ g。配制所用的容量瓶上标有___________ 、___________ 、刻度线。
②下列操作导致浓度偏低的是___________ 。
A.容量瓶用蒸馏水洗净之后,直接用于溶液的配制
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.摇匀后,发现液面低于刻度线,又滴加蒸馏水至与刻度线相切
D.定容时,俯视刻度线
 )是一种多功能绿色水处理剂,杀菌消毒的同时可生成氢氧化铁胶体。某工厂利用废金属屑(主要成分为Fe和Cu,含有少量
)是一种多功能绿色水处理剂,杀菌消毒的同时可生成氢氧化铁胶体。某工厂利用废金属屑(主要成分为Fe和Cu,含有少量 )制取
)制取 并回收金属Cu,工艺流程如下:
并回收金属Cu,工艺流程如下:
(1)试剂a为
(2)用离子方程式解释滤液I不含有
 可能的原因
可能的原因(3)制备
 的原理:
的原理: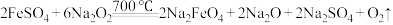 。反应中
。反应中 转移电子的物质的量为
转移电子的物质的量为(4)高铁酸钠(
 )是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。
)是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。①某兴趣小组欲用
 固体配制100mL
固体配制100mL 的高铁酸钠溶液,需要高铁酸钠固体的质量为
的高铁酸钠溶液,需要高铁酸钠固体的质量为②下列操作导致浓度偏低的是
A.容量瓶用蒸馏水洗净之后,直接用于溶液的配制
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.摇匀后,发现液面低于刻度线,又滴加蒸馏水至与刻度线相切
D.定容时,俯视刻度线
您最近一年使用:0次
名校
5 . 利用废旧铁铜粉可以制备补血剂原料碳酸亚铁和杀菌剂胆矾。流程如下图所示:
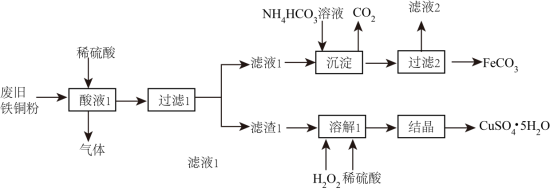
回答下列问题:
(1)“滤液1”中一定含有的金属阳离子___________ (填离子符号),写出检验该金属阳离子的方法___________ 。
(2)过滤用到的玻璃仪器是___________ 。
(3)“溶解1”过程温度不宜过高的原因是___________ 。
(4)向纯净的碳酸亚铁固体中加入足量乳酸溶液,在70℃下搅拌使其充分反应,可得到补铁剂乳酸亚铁。为防止乳酸亚铁变质,在反应体系中应加入少量铁粉,用离子方程式解释使用铁粉的原因___________ 。
(5)“结晶”的具体操作是___________ ,冷却结晶,过滤,洗涤,干燥。
(6)向 固体中加入蒸馏水,固体未见明显减少;一段时间后,难溶物上方出现红褐色氢氧化物并有气泡产生。试写出所发生的化学方程式
固体中加入蒸馏水,固体未见明显减少;一段时间后,难溶物上方出现红褐色氢氧化物并有气泡产生。试写出所发生的化学方程式___________ 。

回答下列问题:
(1)“滤液1”中一定含有的金属阳离子
(2)过滤用到的玻璃仪器是
(3)“溶解1”过程温度不宜过高的原因是
(4)向纯净的碳酸亚铁固体中加入足量乳酸溶液,在70℃下搅拌使其充分反应,可得到补铁剂乳酸亚铁。为防止乳酸亚铁变质,在反应体系中应加入少量铁粉,用离子方程式解释使用铁粉的原因
(5)“结晶”的具体操作是
(6)向
 固体中加入蒸馏水,固体未见明显减少;一段时间后,难溶物上方出现红褐色氢氧化物并有气泡产生。试写出所发生的化学方程式
固体中加入蒸馏水,固体未见明显减少;一段时间后,难溶物上方出现红褐色氢氧化物并有气泡产生。试写出所发生的化学方程式
您最近一年使用:0次
名校
6 .  是重要的化工产品,某小组设计如下实验装置制备氯化铁并探究其性质。
是重要的化工产品,某小组设计如下实验装置制备氯化铁并探究其性质。
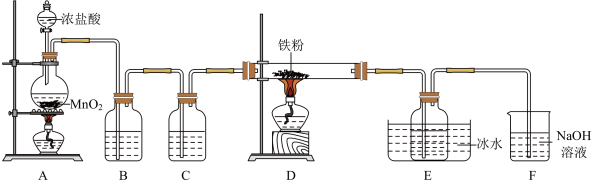
已知:① 易升华、遇水蒸气易潮解。
易升华、遇水蒸气易潮解。
②实验室用铁氰化钾{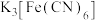 }溶液检验
}溶液检验 ,产生蓝色沉淀。
,产生蓝色沉淀。
回答下列问题:
(1)盛装浓盐酸的仪器是__________ (填名称),装置B中的试剂是__________ 。
(2)装置A中发生反应的化学方程式为__________ 。
(3)装置E中冰水浴的作用是__________ 。
(4)上述实验装置存在两处缺陷导致产品产率偏低,解决方案是:一是加租制备产品的导气管,防堵塞;二是__________ 。
(5)对实验装置进行改进后,继续完成实验。实验完毕后,取产品探究其性质:
根据上述实验现象,不能确定产品中是否剩余铁单质,理由是__________ (用离子方程式表示)。为了确认产品中是否剩余铁单质,取上述实验②所得溶液于试管中,__________ (补充步骤和现象),则证明产品中剩余铁单质。
 是重要的化工产品,某小组设计如下实验装置制备氯化铁并探究其性质。
是重要的化工产品,某小组设计如下实验装置制备氯化铁并探究其性质。
已知:①
 易升华、遇水蒸气易潮解。
易升华、遇水蒸气易潮解。②实验室用铁氰化钾{
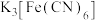 }溶液检验
}溶液检验 ,产生蓝色沉淀。
,产生蓝色沉淀。回答下列问题:
(1)盛装浓盐酸的仪器是
(2)装置A中发生反应的化学方程式为
(3)装置E中冰水浴的作用是
(4)上述实验装置存在两处缺陷导致产品产率偏低,解决方案是:一是加租制备产品的导气管,防堵塞;二是
(5)对实验装置进行改进后,继续完成实验。实验完毕后,取产品探究其性质:
实验 | 操作 | 现象 |
① | 取少量固体溶于蒸馏水,滴加KSCN溶液 | 溶液变红色 |
② | 取少量固体溶于稀硫酸 | 固体溶解,无气泡产生 |
您最近一年使用:0次
名校
解题方法
7 . 如图是硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2)为原料制备高纯氧化铁的生产流程示意图:

请回答下列问题:
(1)酸浸时,将硫铁矿烧渣粉碎的原因是___________ 。
(2)酸浸、过滤后滤液A中的金属阳离子是___________ 。
(3)煅烧FeCO3生成产品I的化学方程式为___________ 。
(4)产品Ⅱ的化学式为___________ 。
(5)写出步骤Ⅳ反应的离子方程式___________ 。

请回答下列问题:
(1)酸浸时,将硫铁矿烧渣粉碎的原因是
(2)酸浸、过滤后滤液A中的金属阳离子是
(3)煅烧FeCO3生成产品I的化学方程式为
(4)产品Ⅱ的化学式为
(5)写出步骤Ⅳ反应的离子方程式
您最近一年使用:0次
名校
解题方法
8 . 铁是人类较早使用的金属之一,运用所学知识,回答下列问题。
I.某学习小组研究 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
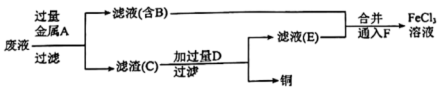
(1)滤渣C中所含物质的化学式为___________ ;通入F发生反应的离子方程式为___________ 。
(2)滤渣C与试剂D反应的离子方程式为_______ ,为测定滤渣中铜的质量分数,取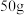 的滤渣与足量的试剂D反应,得到
的滤渣与足量的试剂D反应,得到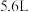 气体(标准状况下),试计算滤渣中铜的质量分数
气体(标准状况下),试计算滤渣中铜的质量分数______ 。
Ⅱ.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验
请回答:
(3)实验I中反应的化学方程式是___________ 。
(4)甲同学观察到实验Ⅰ中持续产生肥皂泡,但实验Ⅱ中溶液B未呈现红色,则溶液B未呈现红色的原因是___________ 。(写出反应的离子方程式)
(5)实验室在制备 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是___________ ;反应化学方程式为___________ 。
I.某学习小组研究
 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
(1)滤渣C中所含物质的化学式为
(2)滤渣C与试剂D反应的离子方程式为
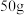 的滤渣与足量的试剂D反应,得到
的滤渣与足量的试剂D反应,得到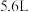 气体(标准状况下),试计算滤渣中铜的质量分数
气体(标准状况下),试计算滤渣中铜的质量分数Ⅱ.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验
| 实验I | 实验Ⅱ |
 | 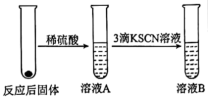 |
(3)实验I中反应的化学方程式是
(4)甲同学观察到实验Ⅰ中持续产生肥皂泡,但实验Ⅱ中溶液B未呈现红色,则溶液B未呈现红色的原因是
(5)实验室在制备
 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是
您最近一年使用:0次
名校
解题方法
9 . 单质A、B、C分别为固体、黄绿色气体和无色气体,在一定条件下它们的反应如下图所示。回答下列问题:
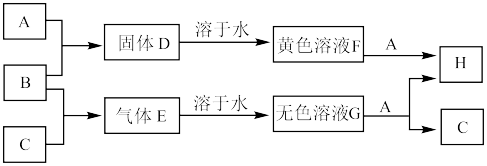
(1)C在充满B的集气瓶中燃烧时反应的现象是__________ 。
(2)A与B反应的化学方程式为__________ 。溶液G与A反应的离子方程式为__________ 。
(3)F、G、H三种溶液中所含相同的阴离子,检验该阴离子的方法是:__________ 。

(1)C在充满B的集气瓶中燃烧时反应的现象是
(2)A与B反应的化学方程式为
(3)F、G、H三种溶液中所含相同的阴离子,检验该阴离子的方法是:
您最近一年使用:0次
解题方法
10 . 纳米铁是一种黑色粉末,可用于制作高密度磁性材料。以铁屑(含少量 杂质)为原料制备纳米铁粉流程如下:
杂质)为原料制备纳米铁粉流程如下:
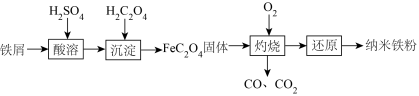
已知:草酸( )是一种二元酸
)是一种二元酸
(1)取少量产品分散于水中,___________ (填操作步骤),可验证所得铁粉直径是否为纳米级。
(2)写出“酸溶”时氧化还原反应的离子方程式:___________ 、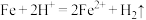 。
。
(3)若加入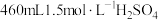 时,铁屑与
时,铁屑与 恰好完全反应,为了使
恰好完全反应,为了使 元素完全转化,则沉淀过程中加入
元素完全转化,则沉淀过程中加入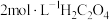 的体积至少为
的体积至少为___________  。
。
(4) 固体经灼烧后得到红棕色固体和
固体经灼烧后得到红棕色固体和 、
、 混合气体,若产物中
混合气体,若产物中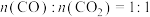 ,则“灼烧”过程中发生反应的化学方程式为
,则“灼烧”过程中发生反应的化学方程式为___________ 。
(5)纳米铁粉可用于处理含氧酸性废水中的 ,反应原理如图所示。
,反应原理如图所示。
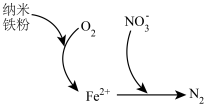
①该过程中体现了纳米铁粉的___________ 性(填“氧化”或“还原”)。
②在铁粉总量一定的条件下,废水中的溶解氧过多不利于 的去除,原因是
的去除,原因是___________ 。
 杂质)为原料制备纳米铁粉流程如下:
杂质)为原料制备纳米铁粉流程如下:
已知:草酸(
 )是一种二元酸
)是一种二元酸(1)取少量产品分散于水中,
(2)写出“酸溶”时氧化还原反应的离子方程式:
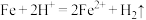 。
。(3)若加入
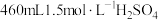 时,铁屑与
时,铁屑与 恰好完全反应,为了使
恰好完全反应,为了使 元素完全转化,则沉淀过程中加入
元素完全转化,则沉淀过程中加入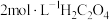 的体积至少为
的体积至少为 。
。(4)
 固体经灼烧后得到红棕色固体和
固体经灼烧后得到红棕色固体和 、
、 混合气体,若产物中
混合气体,若产物中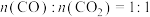 ,则“灼烧”过程中发生反应的化学方程式为
,则“灼烧”过程中发生反应的化学方程式为(5)纳米铁粉可用于处理含氧酸性废水中的
 ,反应原理如图所示。
,反应原理如图所示。
①该过程中体现了纳米铁粉的
②在铁粉总量一定的条件下,废水中的溶解氧过多不利于
 的去除,原因是
的去除,原因是
您最近一年使用:0次




