解题方法
1 . A~F是六种不同物质,A是单质,B和E都是酸,它们之间的反应关系如图所示(部分物质已略)分析辨识,解决问题:
(1)B和C反应的化学方程式是_____________ ,基本反应类型是________ 。
(2)D生成A的化学方程式是______________________________ (写一个即可)。
(3)若F与其他物质类别不同,E和F反应的微观实质是________________________

(1)B和C反应的化学方程式是
(2)D生成A的化学方程式是
(3)若F与其他物质类别不同,E和F反应的微观实质是

您最近一年使用:0次
名校
2 . 金属及金属材料在生产、生活中有广泛的应用。
(1)我省多地开展文明城市创建工作,垃圾分类回收是一项重要举措。某市街道垃圾桶如图所示,请回答下列问题:

①图中标识的物质,属于金属材料的是__________ (写出一种即可)。
②使用铝合金做内筒的优点是____ (写出一点即可)。某品牌饮料的空易拉罐应收入_____ (填“可回收”或“不可回收”)筒中。
③铁制品锈蚀的过程,实际上是铁跟空气中的________ 发生化学反应的过程:除去铁制品表面的铁锈可用稀盐酸,反应的化学方程式为________________________________
(2)将甲、乙、丙三种金属分别投入稀硫酸中,甲、丙表面有气泡产生,乙无明显现象:若将甲放入丙的硫酸盐溶液中,一段时间后,甲的表面有丙析出。由此推断这三种金属的活动性由强到弱的顺序是________________ 。
(3)将一定质量的铁粉加到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列说法正确的是________ (填字母)。
A.若滤液为蓝色,则滤渣中一定有银,可能有铜
B.若滤液中含有银、铜、铁,则滤液中一定含有Al3+、Fe3+、NO3-
C.若滤液为浅绿色,则滤渣中一定含银、铜、铝
D.若滤渣中加稀盐酸无气泡产生,则滤液中一定有Al3+、Fe2+、Cu2+,可能有Ag+
(1)我省多地开展文明城市创建工作,垃圾分类回收是一项重要举措。某市街道垃圾桶如图所示,请回答下列问题:

①图中标识的物质,属于金属材料的是
②使用铝合金做内筒的优点是
③铁制品锈蚀的过程,实际上是铁跟空气中的
(2)将甲、乙、丙三种金属分别投入稀硫酸中,甲、丙表面有气泡产生,乙无明显现象:若将甲放入丙的硫酸盐溶液中,一段时间后,甲的表面有丙析出。由此推断这三种金属的活动性由强到弱的顺序是
(3)将一定质量的铁粉加到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列说法正确的是
A.若滤液为蓝色,则滤渣中一定有银,可能有铜
B.若滤液中含有银、铜、铁,则滤液中一定含有Al3+、Fe3+、NO3-
C.若滤液为浅绿色,则滤渣中一定含银、铜、铝
D.若滤渣中加稀盐酸无气泡产生,则滤液中一定有Al3+、Fe2+、Cu2+,可能有Ag+
您最近一年使用:0次
2019-11-25更新
|
241次组卷
|
3卷引用:河北省张家口市2019-2020学年高一上学期文化课摸底考试化学试题
3 . 有关铁铜的说法正确的是
| A.用铜制容器可以运输浓硝酸和浓硫酸 |
| B.铜与过量的硫粉共热产物是Cu2S |
| C.Fe2O3与NaOH溶液反应可制取Fe(OH)3 |
| D.Fe在足量Cl2中燃烧生成FeCl3,在少量Cl2中燃烧生成FeCl2 |
您最近一年使用:0次
名校
4 . 以下几种类推结论中,正确的选项是
| A.由2Cu+O2==2CuO可推出同族的硫也有Cu+S==CuS |
| B.Fe3O4可表示为FeO·Fe2O3,那么Pb3O4可表示为PbO·Pb2O3 |
| C.Na能与水反应生成H2,K、Ca也能与水反应生成H2 |
| D.CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2反应只生成Na2SO3和O2 |
您最近一年使用:0次
解题方法
5 . 硫酸亚铁在空气中易被氧化,与硫酸铵反应生成硫酸亚铁铵[化学式为FeSO4·(NH4)2SO4·6H2O]后就不易被氧化。模拟工业制备硫酸亚铁铵晶体的实验装置如下图所示。请回答下列问题:
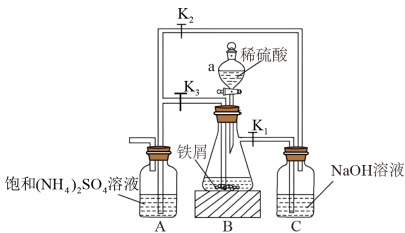
(1)仪器a的名称是______________________ 。
(2)铁屑中常含有Fe2O3、FeS等杂质,则装置C的作用是___________ ,装置B中发生反应的离子方程式可能是___________ (填序号)。
A. Fe+2H+=Fe2++H2↑
B.Fe2O3+6H+=2Fe3++3H2O
C.2Fe3++S2-=2Fe2++S↓
D.2Fe3++Fe=2Fe2+
(3)按上图连接好装置,经检验气密性良好后加入相应的药品,打开K1、K2,关闭K3,装置B中有气体产生,该气体的作用是___________ 。反应一段时间后,打开K3,关闭K1和K2。装置B中的溶液会流入装置A,其原因是______________________ 。
(4)按上图所示装置制备硫酸亚铁铵晶体的安全隐患是______________________ 。
(5)根据相关物质的溶解度判断,从装置A中分离出硫酸亚铁铵晶体,需采用的操作有___________ 、___________ 、洗涤、干燥。
三种盐的溶解度(单位为g/100gH2O)

(1)仪器a的名称是
(2)铁屑中常含有Fe2O3、FeS等杂质,则装置C的作用是
A. Fe+2H+=Fe2++H2↑
B.Fe2O3+6H+=2Fe3++3H2O
C.2Fe3++S2-=2Fe2++S↓
D.2Fe3++Fe=2Fe2+
(3)按上图连接好装置,经检验气密性良好后加入相应的药品,打开K1、K2,关闭K3,装置B中有气体产生,该气体的作用是
(4)按上图所示装置制备硫酸亚铁铵晶体的安全隐患是
(5)根据相关物质的溶解度判断,从装置A中分离出硫酸亚铁铵晶体,需采用的操作有
三种盐的溶解度(单位为g/100gH2O)
温度 | FeSO4 | (NH4)2SO4 | 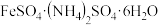 |
| 10 | 20.0 | 73 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78 | 28.1 |
您最近一年使用:0次
2018·河北·一模
6 . 实验室测定氧化物X(FexOy)的组成实验如下:

下列有关说法正确的是

下列有关说法正确的是
| A.步骤Ⅰ、Ⅱ中氯元素均被还原 |
| B.溶液Y中c(Fe2+)︰c(Fe3+)=1︰2 |
| C.溶液Z中的离子只有Fe3+和Cl- |
| D.步骤Ⅰ中消耗HCl的物质的量为0.28mol |
您最近一年使用:0次
7 . 在给定的条件下,下列选项所示的物质间转化均能一步实现的是
A.NaAlO2 (aq)  Al(OH)3 Al(OH)3 Al Al |
B.CaSO4(s) CaCO3(s) CaCO3(s) 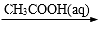 (CH3COO)2Ca(aq) (CH3COO)2Ca(aq) |
C.Fe2O3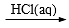 FeCl3(aq) FeCl3(aq)  无水FeCl3 无水FeCl3 |
D.NaCl(aq)  NaHCO3 NaHCO3 Na2CO3 Na2CO3 |
您最近一年使用:0次
名校
解题方法
8 . 某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:

据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是____________ 。
(2)根据上述框图反应关系,写出下列B、D、E所含物质的化学式:
B_________ ;D ___________ ;E__________ 。
(3)写出①、③反应方程式①_________________ ,③_____________________ 。

据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是
(2)根据上述框图反应关系,写出下列B、D、E所含物质的化学式:
B
(3)写出①、③反应方程式①
您最近一年使用:0次
名校
解题方法
9 . 黄铜矿(CuFeS2)是冶炼铜及制备铁的氧化物的重要矿藏,常含有微量的金、银等。如图是以黄铜矿为主要原料生产铜、铁红(氧化铁)颜料的工艺流程图:

(1)反应Ⅰ的离子方程式为_________________________________________ 。
(2)CuCl难溶于水,但可与过量的Cl-反应生成溶于水的[CuCl2]-。该反应的离子方程式为_________________________________________________ 。
(3)有大量Cl-存在时,Na2SO3可将CuCl2还原成[CuCl2]-。 Na2SO3要缓慢滴加到溶液中的原因是_________________________________________________ 。
(4)反应Ⅰ〜Ⅴ五个反应中属于非氧化还原反应的是反应____________ 。
(5)已知Cu+在反应Ⅴ中发生自身氧化还原反应,歧化为Cu2+和Cu,由此可推知溶液A中的溶质为_______________ (填化学式)。
(6)含AsO43-的废水对环境造成严重污染,常用新制的氢氧化铁沉淀与之作用形成FeAsO4沉淀而除去,相同温度下溶解度:Fe(OH)3__________ (填“<”“ >”或“=”)FeAsO4。
(7)在酸性、有氧条件下,一种叫Thibacillus ferroxidans的细菌能将黄铜矿转化成硫酸盐,该过程中发生反应的离子方程式为________________________________ 。
(8)将一定量的铁红溶于160 mL 5 mol • L-1盐酸中,再加入足量铁粉,待反应结束后共收集到气体2.24 L (标准状况),经检测,溶液中无 Fe3+,则参加反应的铁粉的质量为_____________ 。

(1)反应Ⅰ的离子方程式为
(2)CuCl难溶于水,但可与过量的Cl-反应生成溶于水的[CuCl2]-。该反应的离子方程式为
(3)有大量Cl-存在时,Na2SO3可将CuCl2还原成[CuCl2]-。 Na2SO3要缓慢滴加到溶液中的原因是
(4)反应Ⅰ〜Ⅴ五个反应中属于非氧化还原反应的是反应
(5)已知Cu+在反应Ⅴ中发生自身氧化还原反应,歧化为Cu2+和Cu,由此可推知溶液A中的溶质为
(6)含AsO43-的废水对环境造成严重污染,常用新制的氢氧化铁沉淀与之作用形成FeAsO4沉淀而除去,相同温度下溶解度:Fe(OH)3
(7)在酸性、有氧条件下,一种叫Thibacillus ferroxidans的细菌能将黄铜矿转化成硫酸盐,该过程中发生反应的离子方程式为
(8)将一定量的铁红溶于160 mL 5 mol • L-1盐酸中,再加入足量铁粉,待反应结束后共收集到气体2.24 L (标准状况),经检测,溶液中无 Fe3+,则参加反应的铁粉的质量为
您最近一年使用:0次
解题方法
10 . 有关物质转化关系如下图,已知A是一种常见金属,F是一种红褐色沉淀。回答下列问题。
(1)G的俗名为______________ ;它的一种用途是_______________ 。
(2)实验室保存C溶液时需加少量固体A,其原因是___________________________ 。
(3)检验C溶液中阳离子常用的方法是______________________________ 。
(4) B与盐酸反应的离子方程式为_____________________________ 。
(5)由D转化为C的化学方程式是________________________________ 。

(1)G的俗名为
(2)实验室保存C溶液时需加少量固体A,其原因是
(3)检验C溶液中阳离子常用的方法是
(4) B与盐酸反应的离子方程式为
(5)由D转化为C的化学方程式是
您最近一年使用:0次



