1 . A~L为中学常见物质,A为绿色矿石,C为无色常见液体,D为金属氧化物,E为光合作用原料之一,F为硫酸,K、H分别为黑色固体单质C、Fe,J为红色金属单质,I的水溶液呈绿色,它们之间的转化关系如图所示。
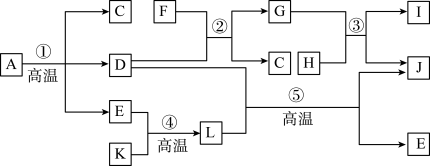
回答下列问题:
(1)A所含主要物质的化学式为__________ ,D 的化学式为__________ 。
(2)反应②的离子方程式为____________ 。
(3)写出反应③离子方程式并用单线桥法标明电子的转移:__________ 。
(4)反应⑤的现象为_______________ ,写出该反应的化学方程式并用双线桥法标明电子的转移且指出氧化剂、还原剂_________ 。

回答下列问题:
(1)A所含主要物质的化学式为
(2)反应②的离子方程式为
(3)写出反应③离子方程式并用单线桥法标明电子的转移:
(4)反应⑤的现象为
您最近一年使用:0次
2 . 有A、B、C、D、E、F六种化合物它们之间的反应关系如下。
①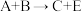
②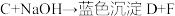
③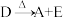
④
(1)写出A~F的化学式:A________ ;B________ ;C________ ;D________ ;E________ ;F________ 。
(2)写出反应①④的化学方程式。
①_______ ;
④_______ 。
①
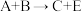
②
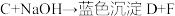
③
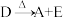
④

(1)写出A~F的化学式:A
(2)写出反应①④的化学方程式。
①
④
您最近一年使用:0次
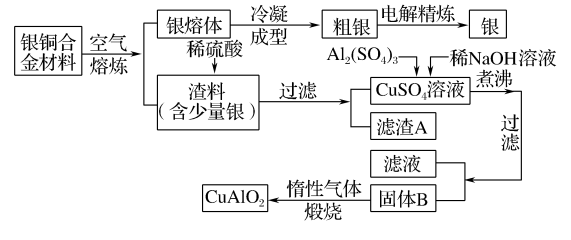
3 . 银铜合金广泛用于航空工业。从切割废料中回收银并制备铜化工产品的工艺流程如图所示:
【注: 和
和 ,开始分解的温度分别为
,开始分解的温度分别为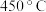 和
和 】
】
(1)固体B的组成为______ (填化学式);在生成固体B的过程中,需控制稀 溶液的加入量。若稀
溶液的加入量。若稀 溶液过量,则因过量引起的反应的离子方程式为
溶液过量,则因过量引起的反应的离子方程式为_____________ 。
(2)完成煅烧过程中一个反应的化学方程式:___ CuO+___ Al2O3
____ 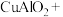
____  。
。
(3)若银铜合金中铜的质量分数为64%,理论上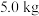 废料中的铜可完全转化为
废料中的铜可完全转化为_____ 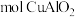 ,至少需要
,至少需要 的
的 溶液
溶液______ L。
(4) 溶液也可用于制备胆矾,其基本操作是
溶液也可用于制备胆矾,其基本操作是_____ 、_____ 、过滤、洗涤和干燥。

【注:
 和
和 ,开始分解的温度分别为
,开始分解的温度分别为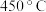 和
和 】
】(1)固体B的组成为
 溶液的加入量。若稀
溶液的加入量。若稀 溶液过量,则因过量引起的反应的离子方程式为
溶液过量,则因过量引起的反应的离子方程式为(2)完成煅烧过程中一个反应的化学方程式:

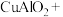
 。
。(3)若银铜合金中铜的质量分数为64%,理论上
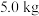 废料中的铜可完全转化为
废料中的铜可完全转化为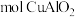 ,至少需要
,至少需要 的
的 溶液
溶液(4)
 溶液也可用于制备胆矾,其基本操作是
溶液也可用于制备胆矾,其基本操作是
您最近一年使用:0次
名校
解题方法
4 . 为探索工业上含铝、铁、铜的合金废料的再利用情况,某同学设计的回收利用方案如图所示:

(1)写出步骤①中涉及反应的离子方程式:___________ 。
(2)步骤②中通入过量 生成沉淀C的离子方程式为
生成沉淀C的离子方程式为___________ 。
(3)由滤渣 滤液
滤液 滤渣E,需加入的试剂的化学式为
滤渣E,需加入的试剂的化学式为_______ 反应的离子方程式为_____________ 。
(4)检验滤液D中是否含有 的最佳试剂为
的最佳试剂为___________ (填字母)。
A. 溶液 B.
溶液 B. 溶液 C.氯水 D.KSCN溶液
溶液 C.氯水 D.KSCN溶液
(5)试剂Y应是一种______ (填“氧化剂”或“还原剂”),它不可能是________ (填字母)。
A. B.铁单质 C.
B.铁单质 C.

(1)写出步骤①中涉及反应的离子方程式:
(2)步骤②中通入过量
 生成沉淀C的离子方程式为
生成沉淀C的离子方程式为(3)由滤渣
 滤液
滤液 滤渣E,需加入的试剂的化学式为
滤渣E,需加入的试剂的化学式为(4)检验滤液D中是否含有
 的最佳试剂为
的最佳试剂为A.
 溶液 B.
溶液 B. 溶液 C.氯水 D.KSCN溶液
溶液 C.氯水 D.KSCN溶液(5)试剂Y应是一种
A.
 B.铁单质 C.
B.铁单质 C.
您最近一年使用:0次
2020-10-02更新
|
590次组卷
|
4卷引用:人教版(2019)高一必修第一册 第三章 铁 金属材料 第二节 金属材料
20-21高一·全国·课时练习
解题方法
5 . 某课外小组对一些金属单质和化合物的性质进行研究。
(1)表为“铝与氯化铜溶液反应”实验报告的一部分:
①按反应类型写出实验中发生反应的化学方程式各一个(是离子反应的只写离子方程式):
置换反应________________________ ,化合反应________________________ .
②用石墨作电极,电解上述实验分离出的溶液,两极产生气泡,持续电解,在阴极附近的溶液中还可观察到的现象是________________________ ,解释此现象的离子方程式是____________________ 。
(2)探究氧化铜性质
①取A、B两支试管,向A中先加入适量CuO粉末,再分别向A和B中加入等体积的3% H2O2溶液,只观察到A中有大量气泡.实验结论是___________________ 。
②用收集气体并测定其体积的方法探究试管A中反应的速率,必需的实验仪器有:______________ 。
(1)表为“铝与氯化铜溶液反应”实验报告的一部分:
| 实验步骤 | 实验现象 |
| 将打磨过的铝片(过量)放入一定浓度的CuCl2溶液中 | 产生气泡,析出疏松的红色固体,溶液逐渐变为无色 |
| 反应结束后分离出溶液备用 | |
| 红色固体用蒸馏水洗涤后,置于潮湿空气中 | 一段时间后固体由红色变为绿色 |
置换反应
②用石墨作电极,电解上述实验分离出的溶液,两极产生气泡,持续电解,在阴极附近的溶液中还可观察到的现象是
(2)探究氧化铜性质
①取A、B两支试管,向A中先加入适量CuO粉末,再分别向A和B中加入等体积的3% H2O2溶液,只观察到A中有大量气泡.实验结论是
②用收集气体并测定其体积的方法探究试管A中反应的速率,必需的实验仪器有:
您最近一年使用:0次
6 . 已知A、B、D、E间的转化关系如图所示:
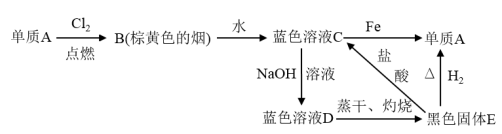
请回答下列问题。
(1)写出下列物质的化学式:A______ ,B______ ,E_______ 。
(2)写出下列反应的化学方程式:
①C→D__________ 。
②E→C__________ 。

请回答下列问题。
(1)写出下列物质的化学式:A
(2)写出下列反应的化学方程式:
①C→D
②E→C
您最近一年使用:0次
2020-09-12更新
|
112次组卷
|
2卷引用:鲁科版(2019)高一必修第一册第一章第2节 研究物质性质的方法和程序 课时2 研究物质性质的基本程序
20-21高一·全国·课时练习
解题方法
7 . 固体A由四种元素组成的化合物,为探究固体A的组成,设计并完成如下实验:
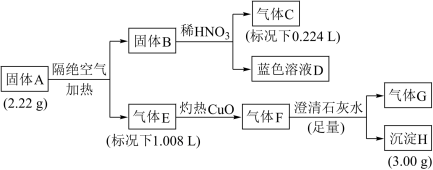
已知:固体B是一种单质,气体E、F都是G和另外一种气体组成。
请回答:
(1)组成A的四种元素是_____ ,气体E是____ 。
(2)固体A隔绝空气加热分解的化学方程式是______ 。
(3)蓝色溶液D和乙醇反应可获得固体A,同时还生成一种常见的温室气体,该反应的化学方程式为_____________________ 。

已知:固体B是一种单质,气体E、F都是G和另外一种气体组成。
请回答:
(1)组成A的四种元素是
(2)固体A隔绝空气加热分解的化学方程式是
(3)蓝色溶液D和乙醇反应可获得固体A,同时还生成一种常见的温室气体,该反应的化学方程式为
您最近一年使用:0次
解题方法
8 . 铝、铁、铜是生活中常见的金属。
(1)铝、铁、铜三种金属都能作导线,是因为它们都具有________ 。
(2)铝在空气中不易被锈蚀,是因为_____________ (用化学方程式表示)。
(3)铜锈的主要成分为碱式碳酸铜[Cu2(OH)2CO3],由此我们可以得到铜生锈是铜和氧气、水、____ 共同作用的结果。
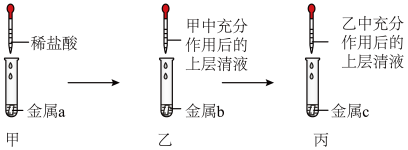
(4)某同学用如图所示装置,设计实验验证铝、铁、铜三种金属活动性强弱。(每步反应金属均有剩余)
若甲试管中无明显现象,乙试管中的金属b为______ 时可以验证三种金属活动性强弱,丙试管中反应的化学方程式为________________ 若金属a、b、c依次为铁、铝、铜时,则无法比较___ 和___ 的活动性强弱。

(1)铝、铁、铜三种金属都能作导线,是因为它们都具有
(2)铝在空气中不易被锈蚀,是因为
(3)铜锈的主要成分为碱式碳酸铜[Cu2(OH)2CO3],由此我们可以得到铜生锈是铜和氧气、水、
(4)某同学用如图所示装置,设计实验验证铝、铁、铜三种金属活动性强弱。(每步反应金属均有剩余)
若甲试管中无明显现象,乙试管中的金属b为
您最近一年使用:0次
2020-08-06更新
|
76次组卷
|
2卷引用:开学考试化学试卷03——2020年秋季高一新生入学分班考试化学试卷(全国通用)
9 . 加强废旧金属的回收和再利用,是合理开发和利用金属资源的主要途径之一。下图是从镀铜废电路板中回收金属铜的一种工艺流程(各过程需控制适宜条件)。
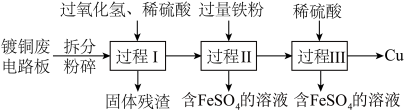
(1)上述流程中,为加快化学反应速率而采取的措施是______ 。
(2)过程Ⅰ中,Cu溶解,过氧化氢的作用是______ 。
(3)过程Ⅱ中,获得Cu的反应的离子方程式为______ 。
(4)过程Ⅲ的目的是______ 。

(1)上述流程中,为加快化学反应速率而采取的措施是
(2)过程Ⅰ中,Cu溶解,过氧化氢的作用是
(3)过程Ⅱ中,获得Cu的反应的离子方程式为
(4)过程Ⅲ的目的是
您最近一年使用:0次
2020-08-04更新
|
299次组卷
|
5卷引用:2020年北京市第一次普通高中学业水平合格性考试化学试题
名校
解题方法
10 . A、B、C、D 四种可溶性盐,其阳离子分别是 Na+、Ba2+、Cu2+、Ag+中的某一种, 阴离子分别是 Cl-、 、
、 、
、 中的某一种。现做以下实验:
中的某一种。现做以下实验:
①将四种盐各取少量,分别溶于盛有 5mL 蒸馏水的四支试管中,只有 B 盐溶液呈蓝色。
②分别向 4 支试管中加入 2mL 稀盐酸,发现 A 盐溶液中产生白色沉淀,C 盐溶液中有较多气泡产生,而 D 盐溶液无明显现象。
(1)根据上述事实,推断这四种盐的化学式分别为:A_____ 、B_____ 、C_____ 、D_____ 。
(2)写出下列反应的离子方程式:
①C+D_____ ;
②B+D_____ ;
③C+HCl→气体_____ 。
 、
、 、
、 中的某一种。现做以下实验:
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有 5mL 蒸馏水的四支试管中,只有 B 盐溶液呈蓝色。
②分别向 4 支试管中加入 2mL 稀盐酸,发现 A 盐溶液中产生白色沉淀,C 盐溶液中有较多气泡产生,而 D 盐溶液无明显现象。
(1)根据上述事实,推断这四种盐的化学式分别为:A
(2)写出下列反应的离子方程式:
①C+D
②B+D
③C+HCl→气体
您最近一年使用:0次
2020-11-22更新
|
197次组卷
|
7卷引用:成都龙泉第二中学2019-2020学年高二上学期入学考试化学试题



