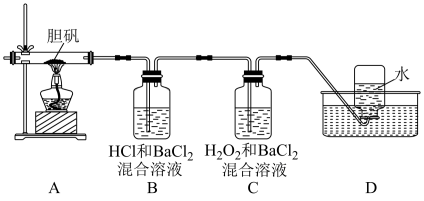
1 . 胆矾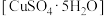 可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在
可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在 时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
(1)B装置中 的作用是
的作用是___________ 。
(2)实验中,观察到B中有白色沉淀生成,C中无明显变化,可确定产物中一定有___________ 气体产生,写出B中发生反应的离子方程式___________ 。
(3)推测D中收集到的气体是___________ ,其检验方法为___________ 。
(4)A中固体完全分解后变为红色粉末,某同学设计实验验证固体残留物仅为 ,而不含
,而不含 ,请帮他完成表中内容。已知:
,请帮他完成表中内容。已知: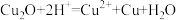 (试剂,仪器和用品自选)。
(试剂,仪器和用品自选)。
(5)结合上述实验现象,写出胆矾在 时隔绝空气加热完全分解的化学方程式
时隔绝空气加热完全分解的化学方程式____ 。
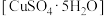 可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在
可做游泳池的消毒剂,其在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在 时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
时隔绝空气加热A,至胆矾分解完全,确定分解产物的成分(试剂均足量)。
(1)B装置中
 的作用是
的作用是(2)实验中,观察到B中有白色沉淀生成,C中无明显变化,可确定产物中一定有
(3)推测D中收集到的气体是
(4)A中固体完全分解后变为红色粉末,某同学设计实验验证固体残留物仅为
 ,而不含
,而不含 ,请帮他完成表中内容。已知:
,请帮他完成表中内容。已知: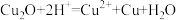 (试剂,仪器和用品自选)。
(试剂,仪器和用品自选)。| 实验步骤 | 实验预期 | 实验结论 |
准确称取 红色固体,加入足量 红色固体,加入足量 | 固体残留物仅为 |
 时隔绝空气加热完全分解的化学方程式
时隔绝空气加热完全分解的化学方程式
您最近一年使用:0次
名校
解题方法
2 . K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]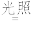 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为___ 。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按如图所示装置进行实验。

①通入氮气的目的是____ 。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有____ 、___ 。
③为防止倒吸,停止实验时应进行的操作是___ 。
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是____ 。
(1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3]
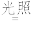 2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为
2FeC2O4+3K2C2O4+2CO2↑;显色反应的化学方程式为(2)某小组为探究三草酸合铁酸钾的热分解产物,按如图所示装置进行实验。

①通入氮气的目的是
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有
③为防止倒吸,停止实验时应进行的操作是
④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是
您最近一年使用:0次
2020-12-09更新
|
637次组卷
|
5卷引用:专题9 第一~三单元综合拔高练-高中化学必修第二册苏教版2019
专题9 第一~三单元综合拔高练-高中化学必修第二册苏教版2019(已下线)专题讲座(九) 热点实验综合探究 (精讲)-2021年高考化学一轮复习讲练测四川省绵阳市南山中学实验学校2022届高三上学学期开学考试化学试题四川省泸县第四中学2021-2022学年高三上学期第二次月考理综化学试题(已下线)专题讲座(十)化学实验设计与探究(练) — 2022年高考化学一轮复习讲练测(新教材新高考)
3 . 银铜合金广泛用于航空工业。从切割废料中回收银并制备铜化工产品的工艺流程如图所示:
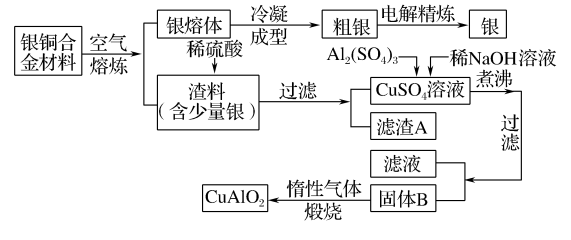
【注: 和
和 ,开始分解的温度分别为
,开始分解的温度分别为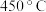 和
和 】
】
(1)固体B的组成为______ (填化学式);在生成固体B的过程中,需控制稀 溶液的加入量。若稀
溶液的加入量。若稀 溶液过量,则因过量引起的反应的离子方程式为
溶液过量,则因过量引起的反应的离子方程式为_____________ 。
(2)完成煅烧过程中一个反应的化学方程式:___ CuO+___ Al2O3
____ 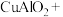
____  。
。
(3)若银铜合金中铜的质量分数为64%,理论上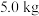 废料中的铜可完全转化为
废料中的铜可完全转化为_____ 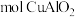 ,至少需要
,至少需要 的
的 溶液
溶液______ L。
(4) 溶液也可用于制备胆矾,其基本操作是
溶液也可用于制备胆矾,其基本操作是_____ 、_____ 、过滤、洗涤和干燥。

【注:
 和
和 ,开始分解的温度分别为
,开始分解的温度分别为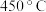 和
和 】
】(1)固体B的组成为
 溶液的加入量。若稀
溶液的加入量。若稀 溶液过量,则因过量引起的反应的离子方程式为
溶液过量,则因过量引起的反应的离子方程式为(2)完成煅烧过程中一个反应的化学方程式:

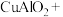
 。
。(3)若银铜合金中铜的质量分数为64%,理论上
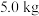 废料中的铜可完全转化为
废料中的铜可完全转化为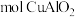 ,至少需要
,至少需要 的
的 溶液
溶液(4)
 溶液也可用于制备胆矾,其基本操作是
溶液也可用于制备胆矾,其基本操作是
您最近一年使用:0次
名校
解题方法
4 . 为探索工业上含铝、铁、铜的合金废料的再利用情况,某同学设计的回收利用方案如图所示:

(1)写出步骤①中涉及反应的离子方程式:___________ 。
(2)步骤②中通入过量 生成沉淀C的离子方程式为
生成沉淀C的离子方程式为___________ 。
(3)由滤渣 滤液
滤液 滤渣E,需加入的试剂的化学式为
滤渣E,需加入的试剂的化学式为_______ 反应的离子方程式为_____________ 。
(4)检验滤液D中是否含有 的最佳试剂为
的最佳试剂为___________ (填字母)。
A. 溶液 B.
溶液 B. 溶液 C.氯水 D.KSCN溶液
溶液 C.氯水 D.KSCN溶液
(5)试剂Y应是一种______ (填“氧化剂”或“还原剂”),它不可能是________ (填字母)。
A. B.铁单质 C.
B.铁单质 C.

(1)写出步骤①中涉及反应的离子方程式:
(2)步骤②中通入过量
 生成沉淀C的离子方程式为
生成沉淀C的离子方程式为(3)由滤渣
 滤液
滤液 滤渣E,需加入的试剂的化学式为
滤渣E,需加入的试剂的化学式为(4)检验滤液D中是否含有
 的最佳试剂为
的最佳试剂为A.
 溶液 B.
溶液 B. 溶液 C.氯水 D.KSCN溶液
溶液 C.氯水 D.KSCN溶液(5)试剂Y应是一种
A.
 B.铁单质 C.
B.铁单质 C.
您最近一年使用:0次
2020-10-02更新
|
588次组卷
|
4卷引用:人教版(2019)高一必修第一册 第三章 铁 金属材料 第二节 金属材料
名校
解题方法
5 . 三氧化二铁和氧化亚铜( )都是红色粉末,常用作颜料。某校一化学实验小组通过实验探究一红色粉末的成分。探究过程如下:
)都是红色粉末,常用作颜料。某校一化学实验小组通过实验探究一红色粉末的成分。探究过程如下:
【查阅资料】 溶于稀硫酸生成Cu、
溶于稀硫酸生成Cu、 和
和 ,在空气中加热生成
,在空气中加热生成 。
。
【提出假设】假设1:红色粉末是 ;
;
假设2:红色粉末是 ;
;
假设3:红色粉末是 和
和 的混合物。
的混合物。
【设计实验】取少量该红色粉末加入足量稀硫酸中,再向所得溶液中滴加KSCN溶液。
(1)若假设1成立,则实验现象是____________________________________________________________ 。
(2)若滴加KSCN溶液,溶液不变红,则证明原红色粉末中一定不含 。你认为这种说法
。你认为这种说法_________ (填“合理”或“不合理”),理由是______________________________________________________ 。
(3)若红色粉末完全溶解,滴加KSCN溶液,溶液不变红,则证明原红色粉末是_____________________ ,写出发生反应的离子方程式:_________________________________________________________ 。
【探究延伸】
(4)经实验分析,确定该红色粉末为 和
和 的混合物。某实验小组欲用加热法测定该红色粉末中
的混合物。某实验小组欲用加热法测定该红色粉末中 的质量分数。取
的质量分数。取 红色粉末在空气中充分加热,待质量不再变化时,称其质量为
红色粉末在空气中充分加热,待质量不再变化时,称其质量为 ,则该红色粉末中
,则该红色粉末中 的质量分数为
的质量分数为_____________________ 。
 )都是红色粉末,常用作颜料。某校一化学实验小组通过实验探究一红色粉末的成分。探究过程如下:
)都是红色粉末,常用作颜料。某校一化学实验小组通过实验探究一红色粉末的成分。探究过程如下:【查阅资料】
 溶于稀硫酸生成Cu、
溶于稀硫酸生成Cu、 和
和 ,在空气中加热生成
,在空气中加热生成 。
。【提出假设】假设1:红色粉末是
 ;
;假设2:红色粉末是
 ;
;假设3:红色粉末是
 和
和 的混合物。
的混合物。【设计实验】取少量该红色粉末加入足量稀硫酸中,再向所得溶液中滴加KSCN溶液。
(1)若假设1成立,则实验现象是
(2)若滴加KSCN溶液,溶液不变红,则证明原红色粉末中一定不含
 。你认为这种说法
。你认为这种说法(3)若红色粉末完全溶解,滴加KSCN溶液,溶液不变红,则证明原红色粉末是
【探究延伸】
(4)经实验分析,确定该红色粉末为
 和
和 的混合物。某实验小组欲用加热法测定该红色粉末中
的混合物。某实验小组欲用加热法测定该红色粉末中 的质量分数。取
的质量分数。取 红色粉末在空气中充分加热,待质量不再变化时,称其质量为
红色粉末在空气中充分加热,待质量不再变化时,称其质量为 ,则该红色粉末中
,则该红色粉末中 的质量分数为
的质量分数为
您最近一年使用:0次
2020-10-02更新
|
499次组卷
|
7卷引用:高一必修第一册(鲁科2019)第3章 第1节 铁的多样性 方法帮
高一必修第一册(鲁科2019)第3章 第1节 铁的多样性 方法帮人教版(2019)高一必修第一册 第三章 铁 金属材料 第一节 铁及其化合物 方法帮(已下线)2010年山西省山大附中高三上学期期中考试化学卷【全国百强校】河北省张家口市第一中学2018-2019学年高一(衔接班)下学期开学考试化学试题(已下线)第3章 章末检测-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)(已下线)2011届福建省泉州外国语中学高三上学期期中考试(理综)化学部分(已下线)2011-2012学年甘肃省天水一中高二第二学段测试化学试卷
6 . 有A、B、C、D、E、F六种化合物,它们之间的反应关系如下所示:
①A+B→C+E ②C + NaOH→蓝色沉淀D + F
③ D→A+E ④F + Ba(NO3)2 → 白色沉淀 + NaNO3
回答下列问题:
(1)写出它们的化学式:
A____________ ;B____________ ;C____________ ;
D____________ ;E____________ ;F____________ 。
(2)写出①④反应的离子方程式:
①_______ ;④_________ 。
①A+B→C+E ②C + NaOH→蓝色沉淀D + F
③ D→A+E ④F + Ba(NO3)2 → 白色沉淀 + NaNO3
回答下列问题:
(1)写出它们的化学式:
A
D
(2)写出①④反应的离子方程式:
①
您最近一年使用:0次
2020-09-23更新
|
1874次组卷
|
8卷引用:2012年鲁科版高中化学必修1 2.2电解质练习卷
20-21高一·全国·课时练习
解题方法
7 . 某课外小组对一些金属单质和化合物的性质进行研究。
(1)表为“铝与氯化铜溶液反应”实验报告的一部分:
①按反应类型写出实验中发生反应的化学方程式各一个(是离子反应的只写离子方程式):
置换反应________________________ ,化合反应________________________ .
②用石墨作电极,电解上述实验分离出的溶液,两极产生气泡,持续电解,在阴极附近的溶液中还可观察到的现象是________________________ ,解释此现象的离子方程式是____________________ 。
(2)探究氧化铜性质
①取A、B两支试管,向A中先加入适量CuO粉末,再分别向A和B中加入等体积的3% H2O2溶液,只观察到A中有大量气泡.实验结论是___________________ 。
②用收集气体并测定其体积的方法探究试管A中反应的速率,必需的实验仪器有:______________ 。
(1)表为“铝与氯化铜溶液反应”实验报告的一部分:
| 实验步骤 | 实验现象 |
| 将打磨过的铝片(过量)放入一定浓度的CuCl2溶液中 | 产生气泡,析出疏松的红色固体,溶液逐渐变为无色 |
| 反应结束后分离出溶液备用 | |
| 红色固体用蒸馏水洗涤后,置于潮湿空气中 | 一段时间后固体由红色变为绿色 |
置换反应
②用石墨作电极,电解上述实验分离出的溶液,两极产生气泡,持续电解,在阴极附近的溶液中还可观察到的现象是
(2)探究氧化铜性质
①取A、B两支试管,向A中先加入适量CuO粉末,再分别向A和B中加入等体积的3% H2O2溶液,只观察到A中有大量气泡.实验结论是
②用收集气体并测定其体积的方法探究试管A中反应的速率,必需的实验仪器有:
您最近一年使用:0次
8 . 已知A、B、D、E间的转化关系如图所示:
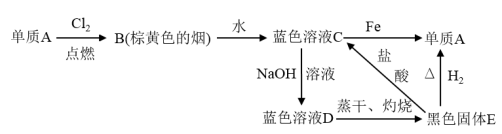
请回答下列问题。
(1)写出下列物质的化学式:A______ ,B______ ,E_______ 。
(2)写出下列反应的化学方程式:
①C→D__________ 。
②E→C__________ 。

请回答下列问题。
(1)写出下列物质的化学式:A
(2)写出下列反应的化学方程式:
①C→D
②E→C
您最近一年使用:0次
2020-09-12更新
|
111次组卷
|
2卷引用:鲁科版(2019)高一必修第一册第一章第2节 研究物质性质的方法和程序 课时2 研究物质性质的基本程序
解题方法
9 . 某工业废渣中主要含有 及少量杂质(
及少量杂质( 、
、 、
、 等),从该工业废渣中提取铜的工艺流程如图所示[已知
等),从该工业废渣中提取铜的工艺流程如图所示[已知 与足量
与足量 溶液反应生成
溶液反应生成 ,最终不会有
,最终不会有 ]:
]:
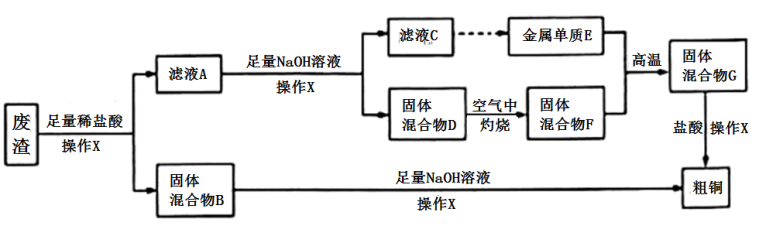
试回答下列问题。
(1)废渣中加入稀盐酸时, 发生
发生 元素自身的氧化还原反应,该反应的离子方程式为
元素自身的氧化还原反应,该反应的离子方程式为____________________________________ 。
(2)滤液 中的金属阳离子为
中的金属阳离子为 、
、 、
、___________ ,固体混合物 中含有的物质是
中含有的物质是____________ (写化学式)。
(3)操作 为常见的实验操作,其操作名称是
为常见的实验操作,其操作名称是_________________ ,在实验室,该操作中使用的玻璃仪器有________________________________________ 。
(4)金属单质 与固体混合物
与固体混合物 的反应常称为
的反应常称为________________ 反应,列举该反应的一种用途:____________________________________ 。
(5)上述方法制备的铜可用来制备铜合金,某铜合金中可能含有 、
、 中的一种,采用下列方法可测定该铜合金的组成。
中的一种,采用下列方法可测定该铜合金的组成。
实验方法:取 铜合金粉末样品放入烧杯中,将
铜合金粉末样品放入烧杯中,将 14.0%的稀硫酸(密度为
14.0%的稀硫酸(密度为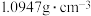 )平均分四次依次加入该烧杯中,每次均充分反应。
)平均分四次依次加入该烧杯中,每次均充分反应。
实验数据记录如下表:
①稀硫酸的物质的量浓度为_____________  。(结果保留两位小数)
。(结果保留两位小数)
②该铜合金中另一种金属是_____________ (填化学式)。
 及少量杂质(
及少量杂质( 、
、 、
、 等),从该工业废渣中提取铜的工艺流程如图所示[已知
等),从该工业废渣中提取铜的工艺流程如图所示[已知 与足量
与足量 溶液反应生成
溶液反应生成 ,最终不会有
,最终不会有 ]:
]:
试回答下列问题。
(1)废渣中加入稀盐酸时,
 发生
发生 元素自身的氧化还原反应,该反应的离子方程式为
元素自身的氧化还原反应,该反应的离子方程式为(2)滤液
 中的金属阳离子为
中的金属阳离子为 、
、 、
、 中含有的物质是
中含有的物质是(3)操作
 为常见的实验操作,其操作名称是
为常见的实验操作,其操作名称是(4)金属单质
 与固体混合物
与固体混合物 的反应常称为
的反应常称为(5)上述方法制备的铜可用来制备铜合金,某铜合金中可能含有
 、
、 中的一种,采用下列方法可测定该铜合金的组成。
中的一种,采用下列方法可测定该铜合金的组成。实验方法:取
 铜合金粉末样品放入烧杯中,将
铜合金粉末样品放入烧杯中,将 14.0%的稀硫酸(密度为
14.0%的稀硫酸(密度为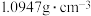 )平均分四次依次加入该烧杯中,每次均充分反应。
)平均分四次依次加入该烧杯中,每次均充分反应。实验数据记录如下表:
实验编号 |
|
|
|
|
加入稀硫酸的质量 | 14.0 | 14.0 | 14.0 | 14.0 |
剩余固体的质量 | 8.7 | 7.4 | 6.1 | 6.0 |
①稀硫酸的物质的量浓度为
 。(结果保留两位小数)
。(结果保留两位小数)②该铜合金中另一种金属是
您最近一年使用:0次
20-21高一·全国·课时练习
解题方法
10 . 固体A由四种元素组成的化合物,为探究固体A的组成,设计并完成如下实验:
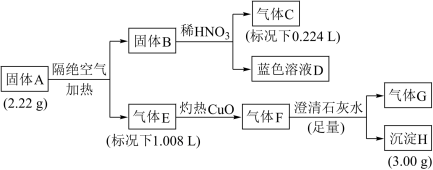
已知:固体B是一种单质,气体E、F都是G和另外一种气体组成。
请回答:
(1)组成A的四种元素是_____ ,气体E是____ 。
(2)固体A隔绝空气加热分解的化学方程式是______ 。
(3)蓝色溶液D和乙醇反应可获得固体A,同时还生成一种常见的温室气体,该反应的化学方程式为_____________________ 。

已知:固体B是一种单质,气体E、F都是G和另外一种气体组成。
请回答:
(1)组成A的四种元素是
(2)固体A隔绝空气加热分解的化学方程式是
(3)蓝色溶液D和乙醇反应可获得固体A,同时还生成一种常见的温室气体,该反应的化学方程式为
您最近一年使用:0次