1 . 以二氧化碳为碳源合成有机物,既能为有机合成提供廉价的原料,又有利于降低碳排放,实现“碳中和”。
回答下列问题:
(1) 催化加氢制备乙酸的过程中涉及如下反应:
催化加氢制备乙酸的过程中涉及如下反应:
Ⅰ.
 ;
;
Ⅱ.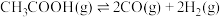
 ;
;
Ⅲ.
 。
。
则
______ ;已知反应Ⅲ中 、
、 的总键能分别为
的总键能分别为
 、
、 ,
, 键的键能为
键的键能为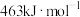 ,则
,则 中
中 键的键能为
键的键能为______  。
。
(2)已知
 。向某密闭容器中充入
。向某密闭容器中充入 ,
, ,控制适当的温度、压强使二者发生反应生成
,控制适当的温度、压强使二者发生反应生成 ,测得
,测得 的平衡转化率如图所示:
的平衡转化率如图所示: 表示
表示______ (填“温度”或“压强”),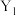
______  (填“>”或“<”)。
(填“>”或“<”)。
②若 点对应的压强为
点对应的压强为 ,反应从开始到平衡所用时间为
,反应从开始到平衡所用时间为 ,则
,则
______  ;平衡常数
;平衡常数
______ 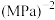 (保留两位有效数字)。
(保留两位有效数字)。
③该反应的速率常数 与反应温度
与反应温度 的关系为
的关系为 (其中
(其中 为活化能,
为活化能, 、
、 均为常数),则能使速率常数增大的措施是
均为常数),则能使速率常数增大的措施是______ (填选项字母)。
A.升高温度 B.压缩容器
C.增大 D.使用催化剂
D.使用催化剂
④上述容器中还存在两个副反应:
i.
 ;
;
ii.

研究表明,在温度较低时, 的平衡转化率开始时随着温度的升高而减小,当温度高于
的平衡转化率开始时随着温度的升高而减小,当温度高于 时,
时, 的平衡转化率却随着温度的升高而增大,其原因是
的平衡转化率却随着温度的升高而增大,其原因是______ 。
回答下列问题:
(1)
 催化加氢制备乙酸的过程中涉及如下反应:
催化加氢制备乙酸的过程中涉及如下反应:Ⅰ.

 ;
;Ⅱ.
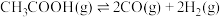
 ;
;Ⅲ.

 。
。则

 、
、 的总键能分别为
的总键能分别为
 、
、 ,
, 键的键能为
键的键能为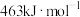 ,则
,则 中
中 键的键能为
键的键能为 。
。(2)已知

 。向某密闭容器中充入
。向某密闭容器中充入 ,
, ,控制适当的温度、压强使二者发生反应生成
,控制适当的温度、压强使二者发生反应生成 ,测得
,测得 的平衡转化率如图所示:
的平衡转化率如图所示: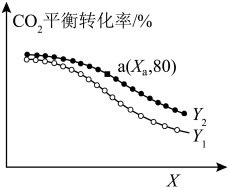
 表示
表示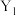
 (填“>”或“<”)。
(填“>”或“<”)。②若
 点对应的压强为
点对应的压强为 ,反应从开始到平衡所用时间为
,反应从开始到平衡所用时间为 ,则
,则
 ;平衡常数
;平衡常数
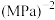 (保留两位有效数字)。
(保留两位有效数字)。③该反应的速率常数
 与反应温度
与反应温度 的关系为
的关系为 (其中
(其中 为活化能,
为活化能, 、
、 均为常数),则能使速率常数增大的措施是
均为常数),则能使速率常数增大的措施是A.升高温度 B.压缩容器
C.增大
 D.使用催化剂
D.使用催化剂④上述容器中还存在两个副反应:
i.

 ;
;ii.


研究表明,在温度较低时,
 的平衡转化率开始时随着温度的升高而减小,当温度高于
的平衡转化率开始时随着温度的升高而减小,当温度高于 时,
时, 的平衡转化率却随着温度的升高而增大,其原因是
的平衡转化率却随着温度的升高而增大,其原因是
您最近一年使用:0次
解题方法
2 . 如图所示,醇类物质在一种含 的配合物催化作用下可以转变成羧酸。下列说法错误的是
的配合物催化作用下可以转变成羧酸。下列说法错误的是
 的配合物催化作用下可以转变成羧酸。下列说法错误的是
的配合物催化作用下可以转变成羧酸。下列说法错误的是
| A.①→②,Rh元素被氧化 |
| B.增大催化剂的用量,甲醇的平衡转化率不变 |
C.CO作配体时,C原子的孤电子对与 的空轨道形成配位键 的空轨道形成配位键 |
| D.反应过程中③含量最少,其可能原因是③→④的反应活化能最大 |
您最近一年使用:0次
解题方法
3 . 氟化工被称为“黄金产业”,在国民经济和社会发展中占有重要地位。我国某公司利用萤石(主要成分为 ,及少量
,及少量 、
、 等)制备无水氟化铝的主要工艺流程如下所示。
等)制备无水氟化铝的主要工艺流程如下所示。 的熔点
的熔点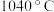 ,沸点
,沸点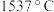 ;
;
③常温下, 。
。
请回答下列问题:
(1)在进入回转窑前,需要将萤石粉碎,其目的是_______ 。
(2)“回转窑反应”的温度控制在 之间,写出在回转窑获得
之间,写出在回转窑获得 的化学方程式:
的化学方程式:_______ 。
(3)在回转窑中的炉渣里还含有 ,将该物质在
,将该物质在 热分解,可获得两种气体(其中一种为
热分解,可获得两种气体(其中一种为 ),用多元醇选择性吸收产生的
),用多元醇选择性吸收产生的 气体,经过一系列工艺得到高纯
气体,经过一系列工艺得到高纯 。则多元醇能从两种气体中选择性吸收
。则多元醇能从两种气体中选择性吸收 的原理是
的原理是_______ 。
(4)经冷凝、精馏、脱气后的 与
与 在流化床、多级气流床中,在
在流化床、多级气流床中,在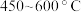 条件下进行一系列反应,由
条件下进行一系列反应,由 和
和 制备无水
制备无水 的反应的
的反应的 _______(填标号)。
_______(填标号)。
(5)常温下,向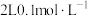 的
的 溶液中加入
溶液中加入 固体充分反应后可得
固体充分反应后可得 ,测得溶液中
,测得溶液中 的浓度为
的浓度为 ,则加入的
,则加入的 固体的物质的量为
固体的物质的量为_______ 。
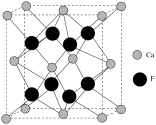
(6)已知萤石 立方晶胞参数
立方晶胞参数 ,结构如图所示,该
,结构如图所示,该 的晶体密度为
的晶体密度为_______  (列出计算式,设阿伏加德罗常数的值为
(列出计算式,设阿伏加德罗常数的值为 )。
)。
 ,及少量
,及少量 、
、 等)制备无水氟化铝的主要工艺流程如下所示。
等)制备无水氟化铝的主要工艺流程如下所示。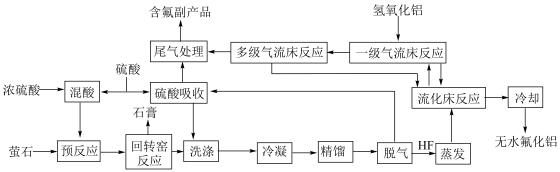
 的熔点
的熔点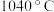 ,沸点
,沸点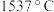 ;
;③常温下,
 。
。请回答下列问题:
(1)在进入回转窑前,需要将萤石粉碎,其目的是
(2)“回转窑反应”的温度控制在
 之间,写出在回转窑获得
之间,写出在回转窑获得 的化学方程式:
的化学方程式:(3)在回转窑中的炉渣里还含有
 ,将该物质在
,将该物质在 热分解,可获得两种气体(其中一种为
热分解,可获得两种气体(其中一种为 ),用多元醇选择性吸收产生的
),用多元醇选择性吸收产生的 气体,经过一系列工艺得到高纯
气体,经过一系列工艺得到高纯 。则多元醇能从两种气体中选择性吸收
。则多元醇能从两种气体中选择性吸收 的原理是
的原理是(4)经冷凝、精馏、脱气后的
 与
与 在流化床、多级气流床中,在
在流化床、多级气流床中,在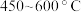 条件下进行一系列反应,由
条件下进行一系列反应,由 和
和 制备无水
制备无水 的反应的
的反应的 _______(填标号)。
_______(填标号)。| A.大于0 | B.小于0 | C.等于0 | D.无法确定 |
(5)常温下,向
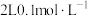 的
的 溶液中加入
溶液中加入 固体充分反应后可得
固体充分反应后可得 ,测得溶液中
,测得溶液中 的浓度为
的浓度为 ,则加入的
,则加入的 固体的物质的量为
固体的物质的量为(6)已知萤石
 立方晶胞参数
立方晶胞参数 ,结构如图所示,该
,结构如图所示,该 的晶体密度为
的晶体密度为 (列出计算式,设阿伏加德罗常数的值为
(列出计算式,设阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
4 . 回答下列问题:
(1)已知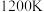 时在某恒容密闭容器中加入足量的
时在某恒容密闭容器中加入足量的 和
和 发生如下几个反应:
发生如下几个反应:






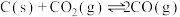


①写出基态 原子的价层电子排布图:
原子的价层电子排布图:_______ 。
②
_______ (用含 、
、 代数式表示)。
代数式表示)。
③若上述反应达到平衡后 的转化率为
的转化率为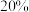 ,经检测体系中含有
,经检测体系中含有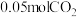 ,则得到
,则得到_______  金属铁。若再加入一定量的
金属铁。若再加入一定量的 ,再次达到平衡后,
,再次达到平衡后,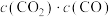 的值将
的值将_______ (填标号)。
A.增大 B.减小 C.不变 D.无法确定
(2)通过下列反应可实现 的再转化,合成
的再转化,合成 、
、 :
:
①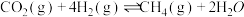

②

在密闭容器中通入一定量的 和
和 ,分别在压强为
,分别在压强为 和
和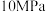 下进行反应。实验中对平衡体系的三种物质(
下进行反应。实验中对平衡体系的三种物质( 、
、 、
、 )进行分析,其中温度对
)进行分析,其中温度对 和
和 在三种物质中的体积分数影响如图所示。
在三种物质中的体积分数影响如图所示。 时
时 平衡体积分数随温度变化关系的曲线是
平衡体积分数随温度变化关系的曲线是_______ (填“a”“b”“o”或“d”中的一种)。简述理由:_______ 。
(3)有一个经验规则可以用于估算基元反应的活化能 :
:
(BE:反应中断掉的化学键的键能之和)
①反应中没有化学键断裂的反应;②自由基与分子的放热反应;③反应中化学键不完全断裂(如协同反应)的反应;④反应中化学键完全断裂的反应。
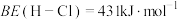
根据上述经验规则,估算氢气与氯气生成氯化氢的反应历程中第ⅱ步基元反应的活化能
_______ ,并与实验值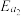 比较。
比较。
ⅰ.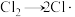
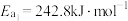
ⅱ.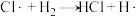
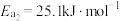
ⅲ.
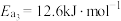
ⅳ.

 ;
; ;
;
上述反应历程中决定整个反应的速率是第_______ (填标号)步反应。
(1)已知
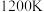 时在某恒容密闭容器中加入足量的
时在某恒容密闭容器中加入足量的 和
和 发生如下几个反应:
发生如下几个反应:





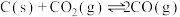


①写出基态
 原子的价层电子排布图:
原子的价层电子排布图:②

 、
、 代数式表示)。
代数式表示)。③若上述反应达到平衡后
 的转化率为
的转化率为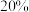 ,经检测体系中含有
,经检测体系中含有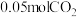 ,则得到
,则得到 金属铁。若再加入一定量的
金属铁。若再加入一定量的 ,再次达到平衡后,
,再次达到平衡后,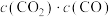 的值将
的值将A.增大 B.减小 C.不变 D.无法确定
(2)通过下列反应可实现
 的再转化,合成
的再转化,合成 、
、 :
:①
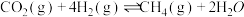

②


在密闭容器中通入一定量的
 和
和 ,分别在压强为
,分别在压强为 和
和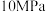 下进行反应。实验中对平衡体系的三种物质(
下进行反应。实验中对平衡体系的三种物质( 、
、 、
、 )进行分析,其中温度对
)进行分析,其中温度对 和
和 在三种物质中的体积分数影响如图所示。
在三种物质中的体积分数影响如图所示。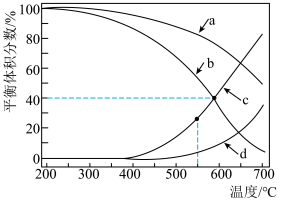
 时
时 平衡体积分数随温度变化关系的曲线是
平衡体积分数随温度变化关系的曲线是(3)有一个经验规则可以用于估算基元反应的活化能
 :
:反应类型 | ① | ② | ③ | ④ |
| 0 | 0.05 | 0.3 | 1 |
①反应中没有化学键断裂的反应;②自由基与分子的放热反应;③反应中化学键不完全断裂(如协同反应)的反应;④反应中化学键完全断裂的反应。
根据上述经验规则,估算氢气与氯气生成氯化氢的反应历程中第ⅱ步基元反应的活化能

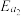 比较。
比较。ⅰ.
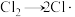
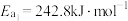
ⅱ.
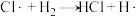
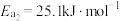
ⅲ.

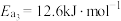
ⅳ.


 ;
; ;
;
上述反应历程中决定整个反应的速率是第
您最近一年使用:0次
解题方法
5 . 二甲醚 既是一种有机燃料,又是一种重要的有机化工原料。利用
既是一种有机燃料,又是一种重要的有机化工原料。利用 催化氢化制备二甲醚的反应原理如下:
催化氢化制备二甲醚的反应原理如下:
 .
.

 .
.

 .
.

回答下列问题:
(1)
___________ 。
(2)向初始温度为T℃的某恒容绝热容器中投入2mol 只发生反应
只发生反应 ,平衡时
,平衡时 的转化率为
的转化率为 。
。
①下列叙述能说明反应 已经达到平衡的是
已经达到平衡的是___________ (填选项字母)。
a.混合气体密度不再发生变化
b.容器内压强不再发生变化
c. 的消耗速率等于
的消耗速率等于 的消耗速率
的消耗速率
d. 的体积分数不再发生变化
的体积分数不再发生变化
②相同条件下,若向该容器中加入 和
和 各1mol,平衡时
各1mol,平衡时 的转化率为
的转化率为 。则
。则
___________ 1(填“>”“=”或“<”)。
③在催化剂条件下反应 的反应过程如图甲所示,“*”表示吸附在催化剂上。
的反应过程如图甲所示,“*”表示吸附在催化剂上。
该催化过程的决速步骤为___________ (填“第一步”或“第二步”),判断的理由是___________ 。
(3)向压强恒定为p kPa的某密闭容器中按 投入
投入 和
和 ,发生
,发生 催化氢化制备二甲醚系列反应
催化氢化制备二甲醚系列反应 和
和 。
。 平衡转化率
平衡转化率 随温度的变化情况如图乙。
随温度的变化情况如图乙。
①图中能表示 随温度变化的曲线是
随温度变化的曲线是___________ (填“ ”或“
”或“ ”),原因为
”),原因为___________ 。
② K时,
K时, 的平衡体积分数为10%。则平衡时
的平衡体积分数为10%。则平衡时 的体积分数为
的体积分数为___________ (保留3位有效数字); K时反应
K时反应 的压强平衡常数
的压强平衡常数
___________  (用含p的代数式表示,列出计算式即可)。
(用含p的代数式表示,列出计算式即可)。
 既是一种有机燃料,又是一种重要的有机化工原料。利用
既是一种有机燃料,又是一种重要的有机化工原料。利用 催化氢化制备二甲醚的反应原理如下:
催化氢化制备二甲醚的反应原理如下: .
.

 .
.

 .
.

回答下列问题:
(1)

(2)向初始温度为T℃的某恒容绝热容器中投入2mol
 只发生反应
只发生反应 ,平衡时
,平衡时 的转化率为
的转化率为 。
。①下列叙述能说明反应
 已经达到平衡的是
已经达到平衡的是a.混合气体密度不再发生变化
b.容器内压强不再发生变化
c.
 的消耗速率等于
的消耗速率等于 的消耗速率
的消耗速率d.
 的体积分数不再发生变化
的体积分数不再发生变化②相同条件下,若向该容器中加入
 和
和 各1mol,平衡时
各1mol,平衡时 的转化率为
的转化率为 。则
。则
③在催化剂条件下反应
 的反应过程如图甲所示,“*”表示吸附在催化剂上。
的反应过程如图甲所示,“*”表示吸附在催化剂上。
该催化过程的决速步骤为
(3)向压强恒定为p kPa的某密闭容器中按
 投入
投入 和
和 ,发生
,发生 催化氢化制备二甲醚系列反应
催化氢化制备二甲醚系列反应 和
和 。
。 平衡转化率
平衡转化率 随温度的变化情况如图乙。
随温度的变化情况如图乙。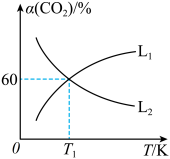
①图中能表示
 随温度变化的曲线是
随温度变化的曲线是 ”或“
”或“ ”),原因为
”),原因为②
 K时,
K时, 的平衡体积分数为10%。则平衡时
的平衡体积分数为10%。则平衡时 的体积分数为
的体积分数为 K时反应
K时反应 的压强平衡常数
的压强平衡常数
 (用含p的代数式表示,列出计算式即可)。
(用含p的代数式表示,列出计算式即可)。
您最近一年使用:0次
2024-05-19更新
|
136次组卷
|
4卷引用:2024届陕西省安康市汉滨区高三下学期联考模拟预测(四)理综试题-高中化学
2024届陕西省安康市汉滨区高三下学期联考模拟预测(四)理综试题-高中化学(已下线)押题卷01(14+4题型)-2024高考化学考点必杀300题(新高考通用)河南省青桐鸣联考2023-2024学年高二下学期3月月考化学试题(已下线)压轴题13?化学反应原理综合题(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
6 . 下列实验操作、现象及结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将铁锈溶于浓盐酸,再滴入KMnO4溶液 | 紫色褪去 | 铁锈中含有二价铁 |
| B | 向淀粉溶液中加入稀硫酸,加热一段时间后,再滴加银氨溶液,水浴加热 | 未产生银镜 | 淀粉未发生水解 |
| C | 向盛有10滴0.1mol/L AgNO3溶液的试管中滴加15滴0.1mol/L NaCl溶液,观察现象,再滴加2滴0.1mol/L KI溶液 | 先产生白色沉淀,后产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| D | 向一体积可变的密闭容器中充入NO2,发生反应:2NO2(g) N2O4(g),将容器体积压缩至原来的一半 N2O4(g),将容器体积压缩至原来的一半 | 相比压缩体积之前,气体颜色变浅 | 增大压强,平衡向气体分子数减小的方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-08更新
|
481次组卷
|
3卷引用:2024届内蒙古自治区赤峰市高三下学期三模理科综合试题-高中化学
2024届内蒙古自治区赤峰市高三下学期三模理科综合试题-高中化学(已下线)押题卷02(15+4题型) -2024高考化学考点必杀300题(新高考通用)内蒙古赤峰市2024届高三4月模拟考试(二模)理综-化学试题
2024·广东佛山·二模
解题方法
7 . 在恒容密闭容器中发生反应: ,Y的平衡转化率按不同投料比
,Y的平衡转化率按不同投料比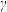 (
(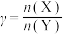 )随温度变化的曲线如图所示。下列说法正确的是
)随温度变化的曲线如图所示。下列说法正确的是
 ,Y的平衡转化率按不同投料比
,Y的平衡转化率按不同投料比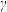 (
(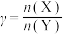 )随温度变化的曲线如图所示。下列说法正确的是
)随温度变化的曲线如图所示。下列说法正确的是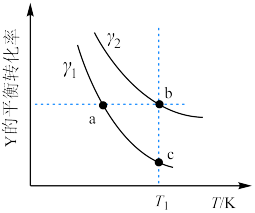
A.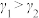 |
B.平衡常数: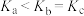 |
| C.当容器内气体密度不变时,反应达到平衡 |
D. 温度下增大压强,c点向a点方向移动 温度下增大压强,c点向a点方向移动 |
您最近一年使用:0次
2024·湖南·二模
解题方法
8 . 二氧化碳加氢制甲烷过程中的主要反应为
Ⅰ.

Ⅱ.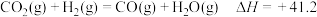

在密闭容器中, 时,
时, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如图所示。
实际转化率随温度的变化如图所示。 的选择性可表示为
的选择性可表示为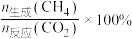 。下列说法正确的是
。下列说法正确的是
Ⅰ.


Ⅱ.
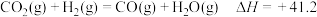

在密闭容器中,
 时,
时, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如图所示。
实际转化率随温度的变化如图所示。 的选择性可表示为
的选择性可表示为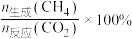 。下列说法正确的是
。下列说法正确的是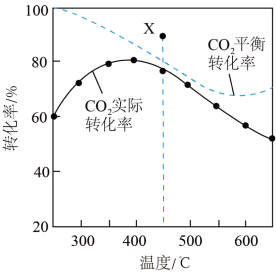
A.反应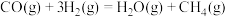 的焓变 的焓变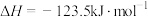 |
B.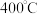 前 前 实际转化率增大的主要原因是:温度升高,反应Ⅱ平衡正移 实际转化率增大的主要原因是:温度升高,反应Ⅱ平衡正移 |
C.降低体系温度, 的平衡选择性增大 的平衡选择性增大 |
D.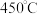 时,使用更高效催化剂,有可能使 时,使用更高效催化剂,有可能使 平衡转化率达到 平衡转化率达到 点 点 |
您最近一年使用:0次
9 . 第19届杭州亚运会上,“零碳”甲醇火炬彰显了“绿色亚运”的精神。“零碳”甲醇是利用焦炉气副产物 和工业尾气中的
和工业尾气中的 合成,涉及以下反应:
合成,涉及以下反应:
①
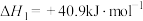
②

③

(1)反应③的 为
为___________  ;有利于反应②自发进行的条件是
;有利于反应②自发进行的条件是___________ (填“低温”或“高温”)。
(2)一定条件下,向容积为V L的恒容密闭容器中通入1mol 和2mol
和2mol 发生上述反应,反应20min时容器内反应达到平衡,容器中CO为
发生上述反应,反应20min时容器内反应达到平衡,容器中CO为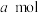 ,
, 为
为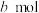 。
。
①以 表示的0~20min内平均反应速率
表示的0~20min内平均反应速率
___________  (用含a、b、V的代数式表示,下同),此时
(用含a、b、V的代数式表示,下同),此时 的浓度为
的浓度为___________  ,反应②的平衡常数为
,反应②的平衡常数为___________ 。
③下列叙述正确的有___________ (填字母)。
A.混合气体的密度不变能表明反应①达到化学平衡状态
B.增大压强,会增大反应②的平衡常数
C.适当提高氢碳比,有利于提高 的平衡产率
的平衡产率
D.适当升高温度,反应①②③的速率均会增大
(3) 优异的
优异的 催化加氢制甲醇性能逐渐受到科研工作者的关注,其晶体结构单元如图所示(
催化加氢制甲醇性能逐渐受到科研工作者的关注,其晶体结构单元如图所示( 之间紧密堆积,
之间紧密堆积, 位于
位于 形成的空隙中且未画出),其中
形成的空隙中且未画出),其中 半径为
半径为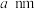 ,晶体结构单元的高为
,晶体结构单元的高为 ,该结构单元含
,该结构单元含 的个数是
的个数是___________ 。已知阿伏加德罗常数的值为 ,则
,则 晶体的摩尔体积
晶体的摩尔体积
___________ 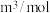 。
。
 和工业尾气中的
和工业尾气中的 合成,涉及以下反应:
合成,涉及以下反应:①

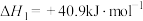
②


③


(1)反应③的
 为
为 ;有利于反应②自发进行的条件是
;有利于反应②自发进行的条件是(2)一定条件下,向容积为V L的恒容密闭容器中通入1mol
 和2mol
和2mol 发生上述反应,反应20min时容器内反应达到平衡,容器中CO为
发生上述反应,反应20min时容器内反应达到平衡,容器中CO为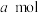 ,
, 为
为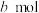 。
。①以
 表示的0~20min内平均反应速率
表示的0~20min内平均反应速率
 (用含a、b、V的代数式表示,下同),此时
(用含a、b、V的代数式表示,下同),此时 的浓度为
的浓度为 ,反应②的平衡常数为
,反应②的平衡常数为③下列叙述正确的有
A.混合气体的密度不变能表明反应①达到化学平衡状态
B.增大压强,会增大反应②的平衡常数
C.适当提高氢碳比,有利于提高
 的平衡产率
的平衡产率D.适当升高温度,反应①②③的速率均会增大
(3)
 优异的
优异的 催化加氢制甲醇性能逐渐受到科研工作者的关注,其晶体结构单元如图所示(
催化加氢制甲醇性能逐渐受到科研工作者的关注,其晶体结构单元如图所示( 之间紧密堆积,
之间紧密堆积, 位于
位于 形成的空隙中且未画出),其中
形成的空隙中且未画出),其中 半径为
半径为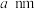 ,晶体结构单元的高为
,晶体结构单元的高为 ,该结构单元含
,该结构单元含 的个数是
的个数是 ,则
,则 晶体的摩尔体积
晶体的摩尔体积
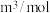 。
。
您最近一年使用:0次
解题方法
10 . 河南理工大学刘宝忠课题组以钌镍单原子合金(RuNiSAA)为催化剂研究了氨硼烷(NH3BH3)水解产生H2的催化反应机理(如图所示)。下列说法错误的是
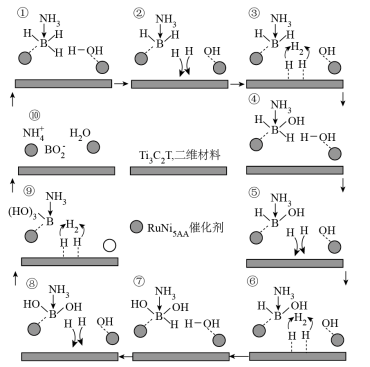
| A.NH3BH3分子中含极性共价键、配位键 |
| B.将NH3BH3替换为NH3BD3,得到气体HD |
| C.该反应机理中涉及O—H、B—H、N—H的断裂 |
D.该催化反应的总反应可以表示为 |
您最近一年使用:0次



