解题方法
1 . 氮及其化合物在化肥、医药、材料和国防工业中具有广泛应用。回答下列问题:
(1)自上个世纪德国建立了第一套合成氨装置,合成氨工业为解决人类的温饱问题作出了极大贡献。写出实验室制备氨气的方程式_________ 。
(2)有人设想寻求合适的催化剂和电极材料,以 、
、 为电极反应物,以
为电极反应物,以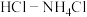 为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。
为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。

①a电极是该电池的_______ (填正极或者负极);该电池正极的电极反应式是___________ 。
②该电池在工作过程中 的浓度将不断
的浓度将不断_________ (填增大或减小),假设放电过程中电解质溶液的体积不变,当溶液中 的物质的量改变
的物质的量改变 时,理论上电池能为外电路提供
时,理论上电池能为外电路提供___________ mol电子。
(3)肼 又称为联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池以20%~30%的
又称为联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池以20%~30%的 溶液为电解质溶液,总反应方程式为:
溶液为电解质溶液,总反应方程式为: 。请写出该电池放电时,负极的电极反应式:
。请写出该电池放电时,负极的电极反应式:__________ 。
(4)为了监测空气中NOx的含量,科学家成功研制出了一种NOx传感器,其工作原理示意图如图:
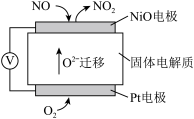
①固体电解质中 移向
移向___________ (填“正极”或“负极”)
②写出 电极发生的电极反应式:
电极发生的电极反应式:________ 。
(1)自上个世纪德国建立了第一套合成氨装置,合成氨工业为解决人类的温饱问题作出了极大贡献。写出实验室制备氨气的方程式
(2)有人设想寻求合适的催化剂和电极材料,以
 、
、 为电极反应物,以
为电极反应物,以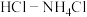 为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。
为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。
①a电极是该电池的
②该电池在工作过程中
 的浓度将不断
的浓度将不断 的物质的量改变
的物质的量改变 时,理论上电池能为外电路提供
时,理论上电池能为外电路提供(3)肼
 又称为联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池以20%~30%的
又称为联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池以20%~30%的 溶液为电解质溶液,总反应方程式为:
溶液为电解质溶液,总反应方程式为: 。请写出该电池放电时,负极的电极反应式:
。请写出该电池放电时,负极的电极反应式:(4)为了监测空气中NOx的含量,科学家成功研制出了一种NOx传感器,其工作原理示意图如图:

①固体电解质中
 移向
移向②写出
 电极发生的电极反应式:
电极发生的电极反应式:
您最近一年使用:0次
名校
解题方法
2 . 以NOx 为主要成分的雾霾的综合治理是当前重要的研究课题。
I.汽车尾气中的 NO(g)和 CO(g)在一定条件下可发生反应生成无毒的N2 和 CO2:
(1)已知:①N2(g)+O2(g) 2NO(g) △H1= +180.5 kJ·mol-1 ②CO 的燃烧热△H2 = - 283.0 kJ·mol-l,则反应③ 2NO(g)+2CO(g)
2NO(g) △H1= +180.5 kJ·mol-1 ②CO 的燃烧热△H2 = - 283.0 kJ·mol-l,则反应③ 2NO(g)+2CO(g) N2(g)+2CO2(g) △H3 =
N2(g)+2CO2(g) △H3 =_______ 。
(2)某研究小组在三个容积为 5 L 的恒容密闭容器中,分别充入 0.4mol NO 和 0.4 mol CO,发生反应③ 。在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示:
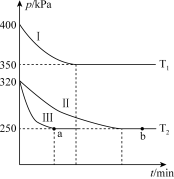
①温度:T1_____ T2(填“<”“=”或“>”)。
②CO 的平衡转化率:Ⅰ_____ Ⅱ_____ Ⅲ(填“<”“=”或“>”)。
③反应速率:a 点的 v逆_____ b 点的 v正 (填“<”“=”或“>”)。
④T2 时的平衡常数 Kc=_____ 。
(3)将 NO和 CO以一定的流速通过两种不同的催化剂(cat1、cat2)进行反应,相同时间内测量的脱氮率(脱氮率即 NO的转化率)如图所示。M 点_____ (填“是”或“不是”)对应温度下的平衡脱氮率, 说明理由_________ 。
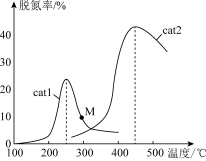
Ⅱ.N2O是一种强温室气体,且易形成颗粒性污染物,研究N2O的分解反应 2N2O=2N2+O2对环境保护有重要意义。
(4)碘蒸气存在能大幅度提高 N2O 的分解速率,反应历程为:
第一步 I2(g) 2I(g)快速平衡,平衡常数为K
2I(g)快速平衡,平衡常数为K
第二步 I(g)+N2O(g)→N2(g)+IO(g) v = k1·c(N2O)·c(I) 慢反应
第三步 IO(g)+N2O(g)→N2(g)+O2(g)+1/2I2(g) 快反应
其中可近似认为第二步反应不影响第一步的平衡。实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。
① k =_____ (用含 K 和 k1 的代数式表示)。
②下列表述正确的是_____ 。
a.IO 为反应的中间产物
b.碘蒸气的浓度大小不会影响 N2O的分解速率
c.第二步对总反应速率起决定作用
d.催化剂会降低反应的活化能,从而影响△H
(5)通过 N2O 传感器可监测环境中 N2O 的含量,其工作原理如图所示
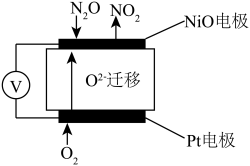
①NiO电极上的电极反应式为_____ 。
②N2O浓度越高,则电压表读数越_____ 。(填“高”或“低”)
I.汽车尾气中的 NO(g)和 CO(g)在一定条件下可发生反应生成无毒的N2 和 CO2:
(1)已知:①N2(g)+O2(g)
 2NO(g) △H1= +180.5 kJ·mol-1 ②CO 的燃烧热△H2 = - 283.0 kJ·mol-l,则反应③ 2NO(g)+2CO(g)
2NO(g) △H1= +180.5 kJ·mol-1 ②CO 的燃烧热△H2 = - 283.0 kJ·mol-l,则反应③ 2NO(g)+2CO(g) N2(g)+2CO2(g) △H3 =
N2(g)+2CO2(g) △H3 =(2)某研究小组在三个容积为 5 L 的恒容密闭容器中,分别充入 0.4mol NO 和 0.4 mol CO,发生反应③ 。在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示:

①温度:T1
②CO 的平衡转化率:Ⅰ
③反应速率:a 点的 v逆
④T2 时的平衡常数 Kc=
(3)将 NO和 CO以一定的流速通过两种不同的催化剂(cat1、cat2)进行反应,相同时间内测量的脱氮率(脱氮率即 NO的转化率)如图所示。M 点

Ⅱ.N2O是一种强温室气体,且易形成颗粒性污染物,研究N2O的分解反应 2N2O=2N2+O2对环境保护有重要意义。
(4)碘蒸气存在能大幅度提高 N2O 的分解速率,反应历程为:
第一步 I2(g)
 2I(g)快速平衡,平衡常数为K
2I(g)快速平衡,平衡常数为K第二步 I(g)+N2O(g)→N2(g)+IO(g) v = k1·c(N2O)·c(I) 慢反应
第三步 IO(g)+N2O(g)→N2(g)+O2(g)+1/2I2(g) 快反应
其中可近似认为第二步反应不影响第一步的平衡。实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。
① k =
②下列表述正确的是
a.IO 为反应的中间产物
b.碘蒸气的浓度大小不会影响 N2O的分解速率
c.第二步对总反应速率起决定作用
d.催化剂会降低反应的活化能,从而影响△H
(5)通过 N2O 传感器可监测环境中 N2O 的含量,其工作原理如图所示

①NiO电极上的电极反应式为
②N2O浓度越高,则电压表读数越
您最近一年使用:0次
名校
解题方法
3 . CO2的资源化利用能有效减少CO2的排放,充分利用碳资源。
(1)全球变暖现象很可能是大气中的温室气体(如CO2)聚集造成的。有科学家提出可以将CO2通过管道输送到海底,这样可减缓空气中CO2浓度的增加。下列有关说法正确的是__ (填字母)。
A.送到海底越深的地方,CO2溶解得越多,同时CO2可能液化甚至变成干冰
B.把CO2输送到海底,会使海水酸性增强,有利于海洋生态环境
C.把CO2输送到海底,这是人类减缓空气中CO2浓度增加速率的唯一办法
D.要减缓空气中CO2浓度的增加,最有效的措施是使用新能源和植树造林
(2)已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1
则反应CO2(g)+4H2(g)=CH4(g)+2H2O(l) ΔH=__ kJ·mol-1。
(3)CO2催化加氢合成二甲醚是CO2转化的一种方法,主要发生下列反应:
反应Ⅰ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+41.2kJ·mol-1
反应Ⅱ:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ΔH=-122.5kJ·mol-1
在一体积为1L的恒容密闭容器中,充入1molCO2与1molH2,CO2的平衡转化率和平衡时CH3OCH3的选择性随温度的变化曲线如图所示。其中:CH3OCH3的选择性= ×100%。
×100%。

①CH3OCH3的选择性随温度的升高而降低的原因是___ 。
②270℃时,测得平衡时CH3OCH3的物质的量为0.1mol,此时反应Ⅰ的化学平衡常数K=__ (保留2位有效数字)。
(4)多晶Cu是目前唯一被实验证实能高效催化CO2还原为烃类(如C2H4)的金属。电解装置中分别以多晶Cu和铂为电极材料,用阴离子交换膜分隔开阴、阳极室,阴、阳极室的KHCO3溶液的浓度(约0.1mol·L-1左右)基本保持不变。并向某极室内持续通入CO2,温度控制在10℃左右。通入CO2的电极为___ (填“阴极”或“阳极”),生成C2H4的电极反应式为__ 。
(1)全球变暖现象很可能是大气中的温室气体(如CO2)聚集造成的。有科学家提出可以将CO2通过管道输送到海底,这样可减缓空气中CO2浓度的增加。下列有关说法正确的是
A.送到海底越深的地方,CO2溶解得越多,同时CO2可能液化甚至变成干冰
B.把CO2输送到海底,会使海水酸性增强,有利于海洋生态环境
C.把CO2输送到海底,这是人类减缓空气中CO2浓度增加速率的唯一办法
D.要减缓空气中CO2浓度的增加,最有效的措施是使用新能源和植树造林
(2)已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1
则反应CO2(g)+4H2(g)=CH4(g)+2H2O(l) ΔH=
(3)CO2催化加氢合成二甲醚是CO2转化的一种方法,主要发生下列反应:
反应Ⅰ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+41.2kJ·mol-1
反应Ⅱ:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ΔH=-122.5kJ·mol-1
在一体积为1L的恒容密闭容器中,充入1molCO2与1molH2,CO2的平衡转化率和平衡时CH3OCH3的选择性随温度的变化曲线如图所示。其中:CH3OCH3的选择性=
 ×100%。
×100%。
①CH3OCH3的选择性随温度的升高而降低的原因是
②270℃时,测得平衡时CH3OCH3的物质的量为0.1mol,此时反应Ⅰ的化学平衡常数K=
(4)多晶Cu是目前唯一被实验证实能高效催化CO2还原为烃类(如C2H4)的金属。电解装置中分别以多晶Cu和铂为电极材料,用阴离子交换膜分隔开阴、阳极室,阴、阳极室的KHCO3溶液的浓度(约0.1mol·L-1左右)基本保持不变。并向某极室内持续通入CO2,温度控制在10℃左右。通入CO2的电极为
您最近一年使用:0次
2019-12-29更新
|
286次组卷
|
2卷引用:山东省菏泽市巨野县第一中学2020届高三上学期12月月考化学试题
名校
解题方法
4 . 醋酸和一水合氨是中学化学中常见的弱电解质。
(1)常温下,某研究性学习小组设计了如下方案证明醋酸为弱电解质,你认为方案可行的是_______ (填序号)
①配制一定量的0.10 mol/L CH3COOH溶液,然后测溶液的pH,若pH大于1,则证明醋酸为弱电解质。
②用醋酸溶液和盐酸做导电性实验,若醋酸溶液导电性弱,则证明醋酸为弱电解质。
③将pH=2的CH3COOH溶液加水稀释100倍后,若pH>4,则证明醋酸为弱电解质。
④配制一定量的CH3COONa溶液,测其pH,若pH大于7,则证明醋酸为弱电解质。
(2)若25℃时,0.10 mol/L的CH3COOH的电离度为1%,则该溶液的pH=________ ,由醋酸电离出的c(H+)约为水电离出的c(H+)的_________ 倍。
(3)已知在25℃时,醋酸的电离平衡常数为Ka=1.8×10-5。常温下,0.1mol/L NaOH溶液V1 mL和0.2mol/L CH3COOH溶液V2 mL混合后(忽略混合前后溶液体积的变化)溶液的pH=7。
①反应后溶液中离子浓度的大小关系为_________________________________________________ 。
②V1:V2__________ (填“>”、“<”或“=”)2:1
③c(CH3COO-):c(CH3COOH)=__________________ 。
(4)常温下,可用氨水吸收废气中的CO2得到NH4HCO3溶液,在该溶液中,c(NH4+)_______ (填“>”、“<”或“=”)c(HCO3-);反应NH4++HCO3-+H2O NH3·H2O+H2CO3的平衡常数K=
NH3·H2O+H2CO3的平衡常数K=_________ 。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数Ka1=4×10-7,Ka2=4×10-11)
(1)常温下,某研究性学习小组设计了如下方案证明醋酸为弱电解质,你认为方案可行的是
①配制一定量的0.10 mol/L CH3COOH溶液,然后测溶液的pH,若pH大于1,则证明醋酸为弱电解质。
②用醋酸溶液和盐酸做导电性实验,若醋酸溶液导电性弱,则证明醋酸为弱电解质。
③将pH=2的CH3COOH溶液加水稀释100倍后,若pH>4,则证明醋酸为弱电解质。
④配制一定量的CH3COONa溶液,测其pH,若pH大于7,则证明醋酸为弱电解质。
(2)若25℃时,0.10 mol/L的CH3COOH的电离度为1%,则该溶液的pH=
(3)已知在25℃时,醋酸的电离平衡常数为Ka=1.8×10-5。常温下,0.1mol/L NaOH溶液V1 mL和0.2mol/L CH3COOH溶液V2 mL混合后(忽略混合前后溶液体积的变化)溶液的pH=7。
①反应后溶液中离子浓度的大小关系为
②V1:V2
③c(CH3COO-):c(CH3COOH)=
(4)常温下,可用氨水吸收废气中的CO2得到NH4HCO3溶液,在该溶液中,c(NH4+)
 NH3·H2O+H2CO3的平衡常数K=
NH3·H2O+H2CO3的平衡常数K=
您最近一年使用:0次
名校
5 . 在容积为0.4L的容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g),升高温度,混合气体的颜色变深。回答下列问题:
2NO2(g),升高温度,混合气体的颜色变深。回答下列问题:
(1)该反应的△H_______ 0(填“>”或“<”下同)。
(2)100℃时,体系中各物质浓度随时间变化如图所示。

在0~60s时段,反应速率v(N2O4)为__________ ;反应的平衡常数K的值为_________ 。反应达平衡后,再向容器中充入0.4molN2O4。平衡向_________ (填“正反应”或“逆反应”)方向移动,再次达到平衡时,N2O4的转化率与原平衡相比_________ (填“变大”“变小”或“不变”)。
(3)100℃,相同容器中充入2.4molNO2与0.8molN2O4,则反应达平衡之前v正_____ v逆。
 2NO2(g),升高温度,混合气体的颜色变深。回答下列问题:
2NO2(g),升高温度,混合气体的颜色变深。回答下列问题:(1)该反应的△H
(2)100℃时,体系中各物质浓度随时间变化如图所示。

在0~60s时段,反应速率v(N2O4)为
(3)100℃,相同容器中充入2.4molNO2与0.8molN2O4,则反应达平衡之前v正
您最近一年使用:0次
名校
解题方法
6 . 下表是常温下,浓度为0.01mol/L的NaOH溶液与几种酸或盐混合后的情况:
回答下列问题:
(1)①组混合液中,HA、A-、Na+三种粒子浓度由大到小的顺序为________ ,若pH=8,则c(Na+)-c(A-)=________ mol/L(填具体数字)。
(2)由②组混合液pH=7可推知,V1____ V2。
(3)③组混合液中,pH>7的原因是______________________ 。
(4)0.01mol/LNaHD溶液中,水的电离度=_________ 。(已知:水的电离度=[已电离的水分子的个数/水分子总数]×100%)
(5)仅凭上述结果,一定能确定HA、HB、H2C、H2D四种酸中属于弱酸的是_________ 。
| 混合组别 | 混合前酸或盐的总浓度 | 混合比例及混合溶液性质 |
| ① | c(HA)=0.02mol/L | 等体积混合,pH>7 |
| ② | HB溶液的pH=2 | V1 mLNaOH溶液与V2mLHB溶液,pH=7 |
| ③ | c(H2C)=0.01mol/L | 等体积混合,pH>7 |
| ④ | c(NaHD)=0.01mol/L | 等体积混合,pH=7 |
(1)①组混合液中,HA、A-、Na+三种粒子浓度由大到小的顺序为
(2)由②组混合液pH=7可推知,V1
(3)③组混合液中,pH>7的原因是
(4)0.01mol/LNaHD溶液中,水的电离度=
(5)仅凭上述结果,一定能确定HA、HB、H2C、H2D四种酸中属于弱酸的是
您最近一年使用:0次
名校
7 . 蛋壳的主要成分是CaCO3,含有少量的SiO2、MgCO3及色素等杂质,测定蛋壳中钙含量的操作步骤如图所示:

已知:CaC2O4、MgC2O4都难溶于水。
回答下列问题:
(1)样品溶于盐酸后得到的滤渣主要是________________________________ 。
(2)①②操作时,加入饱和(NH4)2C2O4溶液和氨水的作用是_______________________ 。
(3)洗涤最好选用_____ (填“冰水”或“0.lmol/L草酸铵溶液”),其目的是____________________ 。
(4)在一定温度下,向2L的密闭容器中放入足量的草酸钙(固体所占体积忽略不计)发生反应:CaC204(s) CaO(s)+CO(g)+CO2(g),若前5min 内生成 CaO 的质量为11.2g,则该段时间内v(CO)=
CaO(s)+CO(g)+CO2(g),若前5min 内生成 CaO 的质量为11.2g,则该段时间内v(CO)=_______ 。
(5)滴定操作是用标准酸性高锰酸钾溶液滴定生成的草酸,通过钙与草酸的定量关系,可间接求出钙的含量。 步骤1:将溶液A加蒸馏水稀释至250mL。
步骤2:取稀释后的溶液25.00mL于锥形瓶中,加稀H2SO4酸化。
步骤3:用0.0190 mol·L-1KMnO4溶液滴定步骤2所得溶液至终点,消耗KMnO4溶液V1mL。
步骤4:重复步骤2、步骤3的操作3次,记录数据如下表:
①KMnO4溶液和草酸溶液在稀硫酸中反应的离子方程式为____________________ 。
②滴定终点的现象是________________________________________ 。
③该蛋壳中CaCO3的质量分数=_______ %,则此法求得的钙含量_________ 实际值(填“>”“=”或“<”)

已知:CaC2O4、MgC2O4都难溶于水。
回答下列问题:
(1)样品溶于盐酸后得到的滤渣主要是
(2)①②操作时,加入饱和(NH4)2C2O4溶液和氨水的作用是
(3)洗涤最好选用
(4)在一定温度下,向2L的密闭容器中放入足量的草酸钙(固体所占体积忽略不计)发生反应:CaC204(s)
 CaO(s)+CO(g)+CO2(g),若前5min 内生成 CaO 的质量为11.2g,则该段时间内v(CO)=
CaO(s)+CO(g)+CO2(g),若前5min 内生成 CaO 的质量为11.2g,则该段时间内v(CO)=(5)滴定操作是用标准酸性高锰酸钾溶液滴定生成的草酸,通过钙与草酸的定量关系,可间接求出钙的含量。 步骤1:将溶液A加蒸馏水稀释至250mL。
步骤2:取稀释后的溶液25.00mL于锥形瓶中,加稀H2SO4酸化。
步骤3:用0.0190 mol·L-1KMnO4溶液滴定步骤2所得溶液至终点,消耗KMnO4溶液V1mL。
步骤4:重复步骤2、步骤3的操作3次,记录数据如下表:
| 实验编号 | KMnO4溶液的浓度(mol /L) | KMnO4液滴入的体积(mL) |
| 1 | 0.0190 | V1=20.02 |
| 2 | 0.0190 | V2= 20.00 |
| 3 | 0.0190 | V3=19.98 |
| 4 | 0.0190 | V4 = 20.80 |
①KMnO4溶液和草酸溶液在稀硫酸中反应的离子方程式为
②滴定终点的现象是
③该蛋壳中CaCO3的质量分数=
您最近一年使用:0次
名校
8 . 乙二醛(OHC-CHO)是一种重要的精细化工产品。
Ⅰ.工业生产乙二醛
(1).乙醛(CH3CHO)液相硝酸氧化法
在Cu(NO3)2催化下,用稀硝酸氧化乙醛制取乙二醛,反应的化学方程式为______ 该法具有原料易得、反应条件温和等优点,但也存在比较明显的缺点是_______
(2).乙二醇(HOCH2CH2OH)气相氧化法
l).已知:OHC-CHO(g)+2H2(g) HOCH2CH2OH(g) ΔH=-78 kJ·mol-1 K1
HOCH2CH2OH(g) ΔH=-78 kJ·mol-1 K1
2H2(g)+O2(g) 2H2O(g) ΔH=-484 kJ·mol-1 K2
2H2O(g) ΔH=-484 kJ·mol-1 K2
乙二醇气相氧化反应HOCH2CH2OH(g)+O2(g) OHC—CHO(g)+2H2O(g)的ΔH=
OHC—CHO(g)+2H2O(g)的ΔH=________ kJ·mol-1。相同温度下,该反应的化学平衡常数K=________ (用含K1、K2的代数式表示)。
2).反应②在热力学上趋势很大,其原因是________
3).当原料气中氧醇比为1.35时,乙二醛和副产物CO2的产率与反应温度的关系如下图所示。反应温度在450~495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是_____________ 、_____________________
4).在恒温恒容下,如果从反应物出发建立平衡,能说明乙二醇气相氧化反应达到平衡状态的是_______ (填选项字母)。
A.体系压强不再变化 B.氧醇比保持不变
C.混合气体的密度保持不变 D.气体平均相对分子质量保持不变
Ⅱ.乙二醛被氧化可生成乙二酸即草酸,某些蔬菜中含有较多的草酸,如果人类不注意合理饮食容易形成草酸钙结石。某研究所利用SDT Q600热分析仪对草酸钙晶体(CaC2O4·H2O)进行热分解,获得相关数据,绘制成固体质量——分解温度的关系如下图。如果残留固体为11.12 克,求残留固体的成分和物质的量_________ 。
Ⅰ.工业生产乙二醛
(1).乙醛(CH3CHO)液相硝酸氧化法
在Cu(NO3)2催化下,用稀硝酸氧化乙醛制取乙二醛,反应的化学方程式为
(2).乙二醇(HOCH2CH2OH)气相氧化法
l).已知:OHC-CHO(g)+2H2(g)
 HOCH2CH2OH(g) ΔH=-78 kJ·mol-1 K1
HOCH2CH2OH(g) ΔH=-78 kJ·mol-1 K12H2(g)+O2(g)
 2H2O(g) ΔH=-484 kJ·mol-1 K2
2H2O(g) ΔH=-484 kJ·mol-1 K2乙二醇气相氧化反应HOCH2CH2OH(g)+O2(g)
 OHC—CHO(g)+2H2O(g)的ΔH=
OHC—CHO(g)+2H2O(g)的ΔH=2).反应②在热力学上趋势很大,其原因是
3).当原料气中氧醇比为1.35时,乙二醛和副产物CO2的产率与反应温度的关系如下图所示。反应温度在450~495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是

4).在恒温恒容下,如果从反应物出发建立平衡,能说明乙二醇气相氧化反应达到平衡状态的是
A.体系压强不再变化 B.氧醇比保持不变
C.混合气体的密度保持不变 D.气体平均相对分子质量保持不变
Ⅱ.乙二醛被氧化可生成乙二酸即草酸,某些蔬菜中含有较多的草酸,如果人类不注意合理饮食容易形成草酸钙结石。某研究所利用SDT Q600热分析仪对草酸钙晶体(CaC2O4·H2O)进行热分解,获得相关数据,绘制成固体质量——分解温度的关系如下图。如果残留固体为11.12 克,求残留固体的成分和物质的量

您最近一年使用:0次
9 . 乙醇可用来制取乙醛、乙醚、乙酸乙酯等化工原料,也是制取染料、涂料、洗涤剂等产品的原料。
(1)已知在常温常压下:
①CH3CH2OH(l)+3O2(g)=2CO2(g)+3H2O(g)△H1=-1366.8kJ/mol
②2CO+O2(g)=2CO2(g) △H2=-556kJ/mol
③H2O(g)=H2O(l) △H3=-44kJ/ mol
则CH3CH2OH(l)和O2生成CO和H2O(l)的热化学方程式是:_____________ 。
(2)在容积为2L的密闭容器中,由CO和H2合成由乙醇的反应为:2CO+4H2(g)=CH3CH2OH(l)+H2O(g),在其他条件不变的情况下,考查温度对反应的影响,CO转化率如图所示(注:T1、T2均大于280℃):
①图可推知T1______ T2(填“>”、“<”、“=”)。
②该反应△H______ 0(填“>”、“<”、“=”);升高温度,上述反应向______ (填“正”“逆”)反应方向移动。
③平衡常数表达式为_________ ,降低温度平衡常数将_______ (填“变大”、“变小”、“不变”下同),反应速率将___________ 。
④在T2温度时,将1mol CO和2mol H2充入一密闭恒容容器中,充分反应达到平衡后,若容器内的压强与起始压强之比为2:3,则CO转化率为a=________ 。
(1)已知在常温常压下:
①CH3CH2OH(l)+3O2(g)=2CO2(g)+3H2O(g)△H1=-1366.8kJ/mol
②2CO+O2(g)=2CO2(g) △H2=-556kJ/mol
③H2O(g)=H2O(l) △H3=-44kJ/ mol
则CH3CH2OH(l)和O2生成CO和H2O(l)的热化学方程式是:
(2)在容积为2L的密闭容器中,由CO和H2合成由乙醇的反应为:2CO+4H2(g)=CH3CH2OH(l)+H2O(g),在其他条件不变的情况下,考查温度对反应的影响,CO转化率如图所示(注:T1、T2均大于280℃):
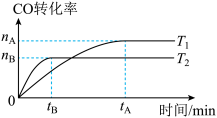
①图可推知T1
②该反应△H
③平衡常数表达式为
④在T2温度时,将1mol CO和2mol H2充入一密闭恒容容器中,充分反应达到平衡后,若容器内的压强与起始压强之比为2:3,则CO转化率为a=
您最近一年使用:0次
2017-05-23更新
|
452次组卷
|
2卷引用:江西省南昌市2017届高三第三次模拟考试理综化学试题
名校
10 . 碳、氮和铝的单质及其化合物在工农业生产和生活中有重要用途。
(1)真空碳热还原—氧化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)═3AlCl(g)+3CO(g) △H=akJ·mol-1
3AlCl(g)═2Al(l)+AlCl3(g) △H=bkJ·mol-1
反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=_________ kJ·mol-1(用含a、b的代数式表示);
(2)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g) N2(g)+CO2(g) △H=Q kJ·mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g) △H=Q kJ·mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
①0~10min内,NO的平均反应速率v(NO)=___________ ,T1℃时,该反应的平衡常数K=_______
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是__________ (填字母编号)。
a.通入一定量的NO b.通入一定量的N2
c.适当升高反应体系的温度 d.加入合适的催化剂
e.适当缩小容器的体积
③在恒容条件下,能判断该反应一定达到化学平衡状态的依据是_________ (填选项编号)。
a.单位时间内生成2nmolNO(g)的同时消耗nmolCO2(g)
b.反应体系的压强不再发生改变
c.混合气体的密度保持不变
d.混合气体的平均相对分子质量保持不变
④若保持与上述反应前30min的反应条件不变,起始时NO的浓度为2.50mol/L,则反应达平衡时c(NO)=_______ mol/L。NO的转化率_______ (填“增大”、“减小”或“不变”)。
(1)真空碳热还原—氧化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)═3AlCl(g)+3CO(g) △H=akJ·mol-1
3AlCl(g)═2Al(l)+AlCl3(g) △H=bkJ·mol-1
反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=
(2)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)
 N2(g)+CO2(g) △H=Q kJ·mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g) △H=Q kJ·mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:时间 物质 | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
①0~10min内,NO的平均反应速率v(NO)=
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是
a.通入一定量的NO b.通入一定量的N2
c.适当升高反应体系的温度 d.加入合适的催化剂
e.适当缩小容器的体积
③在恒容条件下,能判断该反应一定达到化学平衡状态的依据是
a.单位时间内生成2nmolNO(g)的同时消耗nmolCO2(g)
b.反应体系的压强不再发生改变
c.混合气体的密度保持不变
d.混合气体的平均相对分子质量保持不变
④若保持与上述反应前30min的反应条件不变,起始时NO的浓度为2.50mol/L,则反应达平衡时c(NO)=
您最近一年使用:0次
2017-03-04更新
|
197次组卷
|
3卷引用:【校级联考】重庆市西北狼教育联盟五校2019届高三上学期月考联考理综化学试题



