解题方法
1 . 现代化学反应中,非常多的反应都需要在分散系中完成,其中因为水的分散能力很强,所以大部分反应需要在水中完成,那么就避免不了需要研究水中的各种平衡以及原理,在水中,我们会有酸碱性,温度,电离与水解,这些都是高中学习探索的重点。可能使用到的数据Ksp(AgCl)=2×10-10,Ksp(AgI)=8.5×10-17,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8。
(1)下列叙述中,能证明CH3COOH是弱酸的是_______。
(2)大量的碘富集在海藻中,用水浸取后浓缩。浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中 =
=_______ 。
(3)已知25℃,若氨水的浓度为2.0 mol/L,溶液中的c(OH-)=_______ mol/L。在25℃下,将amol/L的氨水与0.01mol/L的盐酸等体积混合,反应平衡时溶液中 ,则溶液显
,则溶液显_______ 性(填“酸”或“碱”或“中”),计算出此时a的值_______ 。(保留两位有效数字)
(1)下列叙述中,能证明CH3COOH是弱酸的是_______。
| A.醋酸易溶于水 |
| B.醋酸溶液的导电能力比盐酸弱 |
| C.常温下,0.010 mol·L-1的醋酸溶液c(H+)=10-3.38 mol·L-1 |
| D.等体积、等浓度的醋酸溶液与NaOH溶液恰好完全反应 |
 =
=(3)已知25℃,若氨水的浓度为2.0 mol/L,溶液中的c(OH-)=
 ,则溶液显
,则溶液显
您最近一年使用:0次
解题方法
2 . Ⅰ.氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运。通过氨热分解法制取氢气,其反应的化学方程式如下: 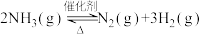
(1)根据下表数据,写出氨热分解法的热化学方程式___________ 。相关化学键的键能数据
(2)已知该反应的∆S=198.9×10-3kJ·mol-1·K-1,判断在300℃时反应是否能自发进行___________ (填“是”或“否”),理由是___________ 。
(3)在一定温度和催化剂的条件下,将0.1molNH3通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如下图所示。___________ mol·L-1·min-1(用含t1的代数式表示)。
②t2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是___________ (用图中a、b、c、d表示),理由是___________ 。
Ⅱ.氨气的催化氧化是工业制取硝酸的重要步骤,假设只会发生以下两个竞争反应Ⅰ、Ⅱ。
反应Ⅰ: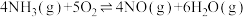
反应Ⅱ:
为分析某催化剂对该反应的选择性,将1moNH3和2molO2充入1L密闭容器中,在不同温度相同时间下,测得有关物质的量关系如图。___________ (填“Ⅰ”或“Ⅱ”)的选择性更好。
(5)高于840℃时,NO的产率降低的可能原因是___________。
(6)520℃时,反应4NH3(g)+3O2 2N2(g)+6H2O(g)的平衡常数K=
2N2(g)+6H2O(g)的平衡常数K=___________ (不要求得出计算结果,只需列出有具体数字的计算式)。
(7)请写出一种除了氨气以外的储氢载体及其生成氢气的化学方程式___________ 。
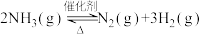
(1)根据下表数据,写出氨热分解法的热化学方程式
| 化学键 | N≡N | H-H | N-H |
| 键能E/(kJ·mol-1) | 946 | 436.0 | 390.8 |
(3)在一定温度和催化剂的条件下,将0.1molNH3通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如下图所示。
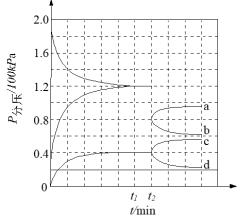
②t2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是
Ⅱ.氨气的催化氧化是工业制取硝酸的重要步骤,假设只会发生以下两个竞争反应Ⅰ、Ⅱ。
反应Ⅰ:
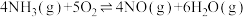
反应Ⅱ:

为分析某催化剂对该反应的选择性,将1moNH3和2molO2充入1L密闭容器中,在不同温度相同时间下,测得有关物质的量关系如图。
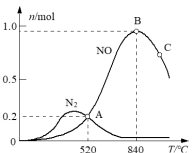
(5)高于840℃时,NO的产率降低的可能原因是___________。
| A.NH3溶于水 | B.反应活化能降低 |
| C.反应Ⅰ的平衡常数变小 | D.催化剂活性降低 |
 2N2(g)+6H2O(g)的平衡常数K=
2N2(g)+6H2O(g)的平衡常数K=(7)请写出一种除了氨气以外的储氢载体及其生成氢气的化学方程式
您最近一年使用:0次
名校
3 . Ⅰ.氢能的利用包括氢的制备、储存和应用三个环节。氢气制取是氢能利用经济性考量的重要环节。
(1)氯碱工业可获得纯度较高的副产物氢气;请写出“氯碱工业”对应离子方程式:___________ 。
(2)粒径在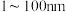 的纳米铝粉常温下能与水反应释氢;向水中加入下列物质,不能加快纳米铝粉释氢速率的是___________。
的纳米铝粉常温下能与水反应释氢;向水中加入下列物质,不能加快纳米铝粉释氢速率的是___________。
Ⅱ.甲烷重整是工业常用的制氢方法,包含水蒸气重整和氧化重整两种方法,原理如下:
水蒸气重整:

氧化重整:

(3)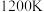 、
、 条件下进行水蒸气重整,起始
条件下进行水蒸气重整,起始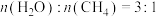 ,达到平衡时
,达到平衡时 的物质的量分数为0.3,
的物质的量分数为0.3, 的转化率为
的转化率为___________ 。
(4)理论上,按照甲烷、水蒸气、氧气体积比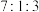 进料,可以将甲烷水蒸气重整和甲烷氧化重整两种方法结合,实现反应器中能量自给(不需要补充热量)。
进料,可以将甲烷水蒸气重整和甲烷氧化重整两种方法结合,实现反应器中能量自给(不需要补充热量)。
①甲烷氧化重整反应的焓变
___________ 。
②实际生产中,甲烷、水蒸气、氧气按约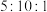 体积比进料。增加水蒸气有两个作用:一是
体积比进料。增加水蒸气有两个作用:一是___________ ,二是水蒸气还能发生___________ (用化学方程式表示)反应,从而获得更多的氢气。
Ⅲ.在新能源体系下,氢能被视为与电能互补的优质二次能源。氢燃料电池能量转换率远高于氢气直接燃烧。
(5)碱性氢氧燃料电池工作时,负极反应式为:___________ 。
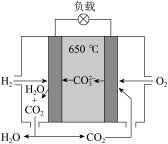
(6)氢氧熔融碳酸盐燃料电池是一种以熔融态碳酸盐为电解质的电池,其工作原理如图,有关该电池说法正确的是___________。
(1)氯碱工业可获得纯度较高的副产物氢气;请写出“氯碱工业”对应离子方程式:
(2)粒径在
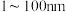 的纳米铝粉常温下能与水反应释氢;向水中加入下列物质,不能加快纳米铝粉释氢速率的是___________。
的纳米铝粉常温下能与水反应释氢;向水中加入下列物质,不能加快纳米铝粉释氢速率的是___________。A. | B. | C. | D. |
Ⅱ.甲烷重整是工业常用的制氢方法,包含水蒸气重整和氧化重整两种方法,原理如下:
水蒸气重整:


氧化重整:


(3)
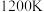 、
、 条件下进行水蒸气重整,起始
条件下进行水蒸气重整,起始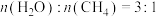 ,达到平衡时
,达到平衡时 的物质的量分数为0.3,
的物质的量分数为0.3, 的转化率为
的转化率为(4)理论上,按照甲烷、水蒸气、氧气体积比
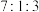 进料,可以将甲烷水蒸气重整和甲烷氧化重整两种方法结合,实现反应器中能量自给(不需要补充热量)。
进料,可以将甲烷水蒸气重整和甲烷氧化重整两种方法结合,实现反应器中能量自给(不需要补充热量)。①甲烷氧化重整反应的焓变

②实际生产中,甲烷、水蒸气、氧气按约
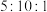 体积比进料。增加水蒸气有两个作用:一是
体积比进料。增加水蒸气有两个作用:一是Ⅲ.在新能源体系下,氢能被视为与电能互补的优质二次能源。氢燃料电池能量转换率远高于氢气直接燃烧。
(5)碱性氢氧燃料电池工作时,负极反应式为:
(6)氢氧熔融碳酸盐燃料电池是一种以熔融态碳酸盐为电解质的电池,其工作原理如图,有关该电池说法正确的是___________。

| A.电池工作时,熔融碳酸盐只起到导电的作用 |
B.该电池可利用工厂中排出的 ,减少温室气体的排放 ,减少温室气体的排放 |
| C.电子流向:氢电极-负载-氧电极-熔融碳酸盐-氢电极 |
D.电池工作时,外电路中流过 电子,消耗 电子,消耗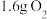 |
您最近一年使用:0次
名校
4 . Ⅰ.为实现碳达峰、碳中和,研发二氧化碳的利用技术,降低空气中二氧化碳的含量,成为研究热点。
(1) 由气体变成固体的过程中,下列判断正确的是___________。
由气体变成固体的过程中,下列判断正确的是___________。
Ⅱ.二氧化碳加氢制甲醇的总反应可表示为: ,该反应一般认为通过如下步骤来实现:
,该反应一般认为通过如下步骤来实现:
①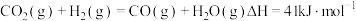
②
(2)总反应的
___________  。
。
(3)若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________。
(4)根据以上信息判断 与
与 制取甲醇的反应自发进行的条件是___________。
制取甲醇的反应自发进行的条件是___________。
Ⅲ.煤转化为水煤气的主要反应为: ,
,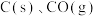 和
和 完全燃烧的热化学方程式分别为:
完全燃烧的热化学方程式分别为:
①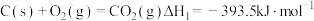 ;
;
②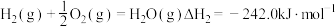 ;
;
③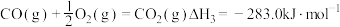 。
。
(5)请你根据以上数据,写出 与水蒸气反应生成
与水蒸气反应生成 和
和 的热化学方程式:
的热化学方程式:___________ 。
(6)比较反应热数据可知,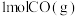 和
和 完全燃烧放出的热量之和,比
完全燃烧放出的热量之和,比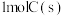 完全燃烧放出的热量
完全燃烧放出的热量___________ 。(填“多”或“少”)
(1)
 由气体变成固体的过程中,下列判断正确的是___________。
由气体变成固体的过程中,下列判断正确的是___________。A.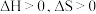 | B.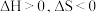 | C.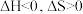 | D.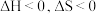 |
Ⅱ.二氧化碳加氢制甲醇的总反应可表示为:
 ,该反应一般认为通过如下步骤来实现:
,该反应一般认为通过如下步骤来实现:①
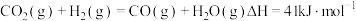
②

(2)总反应的

 。
。(3)若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________。
A.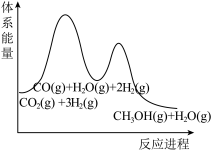 | B.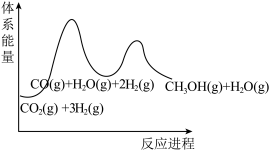 |
C.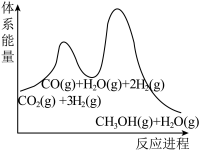 | D.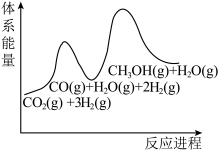 |
(4)根据以上信息判断
 与
与 制取甲醇的反应自发进行的条件是___________。
制取甲醇的反应自发进行的条件是___________。| A.高温 | B.低温 | C.任何温度 | D.任何条件下均不能自发 |
Ⅲ.煤转化为水煤气的主要反应为:
 ,
,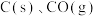 和
和 完全燃烧的热化学方程式分别为:
完全燃烧的热化学方程式分别为:①
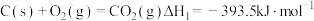 ;
;②
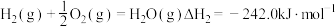 ;
;③
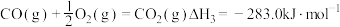 。
。(5)请你根据以上数据,写出
 与水蒸气反应生成
与水蒸气反应生成 和
和 的热化学方程式:
的热化学方程式:(6)比较反应热数据可知,
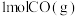 和
和 完全燃烧放出的热量之和,比
完全燃烧放出的热量之和,比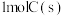 完全燃烧放出的热量
完全燃烧放出的热量
您最近一年使用:0次
2024-01-15更新
|
174次组卷
|
2卷引用:上海师范大学附属中学闵行分校2023-2024学年高二上学期期末考试 化学试卷(等级)
5 . 氧化还原反应原理在生产生活和科学研究中应用广泛,反应的发生往往伴随着能量的转变。
(1)某同学取10mL0.1mol•L﹣1KI溶液,加入6mL0.1mol•L﹣1FeCl3溶液混合。分别取2mL此溶液于3支试管中进行如下实验:
①第一支试管中加入1mLCCl4充分振荡静置,CCl4层显紫色。
②第二支试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀;(已知:3Fe2++2[Fe(CN)6]3﹣=Fe3[Fe(CN)6]2↓蓝色)。
③第三支试管中加入1滴KSCN溶液,溶液变红。
氯化铁溶液呈___ 色;实验②检验的离子是________ (填离子符号);通过3个实验能得出该反应的离子方程式___________ 。
(2)FeCl3溶液在工业上用于蚀刻铜箔电路板。从蚀刻后的废液中可回收铜并使蚀刻液再生,流程如图所示:

①写出FeCl3溶液蚀刻铜箔的反应的离子方程式___________ 。
②从固体中分离出铜,试剂X是什么物质?___________ 。
③若要使滤液再生为蚀刻液,可采用什么办法?___________ 。
人类利用化学反应不仅可以创造新物质,还可以实现不同形式能量之间的转化。
(3)下列反应中,生成物总能量低于反应物总能量的是_______。
(4)为探究反应过程中的能量变化,某小组同学用如下装置进行实验。

①装置Ⅰ中,正极的电极反应式为________ 。
②关于装置Ⅰ和Ⅱ,下列叙述正确的是_______ 。
A.装置Ⅰ和Ⅱ均为化学能转化为电能 B.Ⅱ中电流从Zn片经导线流向Cu片
C.Ⅰ和Ⅱ中的实验现象一样 D.Ⅰ和Ⅱ中的金属铜都参与了电极反应
(1)某同学取10mL0.1mol•L﹣1KI溶液,加入6mL0.1mol•L﹣1FeCl3溶液混合。分别取2mL此溶液于3支试管中进行如下实验:
①第一支试管中加入1mLCCl4充分振荡静置,CCl4层显紫色。
②第二支试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀;(已知:3Fe2++2[Fe(CN)6]3﹣=Fe3[Fe(CN)6]2↓蓝色)。
③第三支试管中加入1滴KSCN溶液,溶液变红。
氯化铁溶液呈
(2)FeCl3溶液在工业上用于蚀刻铜箔电路板。从蚀刻后的废液中可回收铜并使蚀刻液再生,流程如图所示:

①写出FeCl3溶液蚀刻铜箔的反应的离子方程式
②从固体中分离出铜,试剂X是什么物质?
③若要使滤液再生为蚀刻液,可采用什么办法?
人类利用化学反应不仅可以创造新物质,还可以实现不同形式能量之间的转化。
(3)下列反应中,生成物总能量低于反应物总能量的是_______。
| A.碳酸钙受热分解 | B.灼热的碳与二氧化碳反应 |
| C.酒精燃烧 | D.煤与高温下的水蒸气反应 |
(4)为探究反应过程中的能量变化,某小组同学用如下装置进行实验。

①装置Ⅰ中,正极的电极反应式为
②关于装置Ⅰ和Ⅱ,下列叙述正确的是
A.装置Ⅰ和Ⅱ均为化学能转化为电能 B.Ⅱ中电流从Zn片经导线流向Cu片
C.Ⅰ和Ⅱ中的实验现象一样 D.Ⅰ和Ⅱ中的金属铜都参与了电极反应
您最近一年使用:0次
名校
解题方法
6 . 石油化工、煤化工等行业的废气中普遍含有硫化氢, 的回收利用有重要意义。以下是
的回收利用有重要意义。以下是 处理的一些方法。
处理的一些方法。
Ⅰ.用氢氧化钠溶液吸收。
(1)写出用过量 吸收
吸收 的离子方程式
的离子方程式___________ ,尾气中是否含有 可用硫酸铜溶液检验,若尾气含有硫化氢,现象是
可用硫酸铜溶液检验,若尾气含有硫化氢,现象是___________ 。
Ⅱ.制取,其反应的能量示意如下图所示。

(2)写出由 、
、 、
、 生成
生成 的热化学方程式
的热化学方程式___________ 。
Ⅲ.高温分解: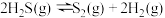
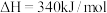
(3)能够判断上述反应到达平衡状态的是___________。(双选)
(4)在恒温恒压条件下,充入氩气,发现: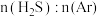 越小,
越小, 平衡转化率越大,请解释可能的原因。
平衡转化率越大,请解释可能的原因。___________
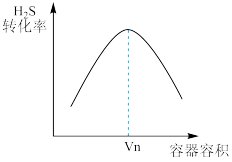
(5)某温度时,向体积不等的恒容容器中加入等量 ,反应相同时间后,测得各容器中
,反应相同时间后,测得各容器中 的转化率与容器体积关系如图所示。
的转化率与容器体积关系如图所示。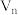 之后,
之后, 的转化率下降的原因是
的转化率下降的原因是___________ 。
Ⅳ.将 燃烧,产生的与剩余
燃烧,产生的与剩余 混合后反应,生成单质硫回收。
混合后反应,生成单质硫回收。
①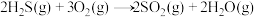
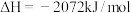
②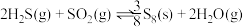

(6)②的平衡常数表达式为___________ ,某温度下,若只发生反应②,从反应开始到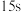 时,测得容器内的气体密度减小了
时,测得容器内的气体密度减小了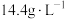 ,则
,则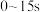 内,
内, 平均反应速率
平均反应速率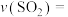
___________ 。
(7)在某温度下发生反应①和②,当②达到平衡,测得密闭系统中各组分浓度分别为: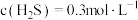 、
、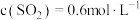 、
、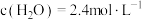 ,请计算开始时投料比
,请计算开始时投料比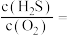
___________ 。
Ⅴ.活性炭吸附氧化法
可用表面喷淋水的活性炭吸附氧化 ,其反应原理如下图所示。
,其反应原理如下图所示。

(8)该方法的总反应方程式为___________ 。
 的回收利用有重要意义。以下是
的回收利用有重要意义。以下是 处理的一些方法。
处理的一些方法。Ⅰ.用氢氧化钠溶液吸收。
(1)写出用过量
 吸收
吸收 的离子方程式
的离子方程式 可用硫酸铜溶液检验,若尾气含有硫化氢,现象是
可用硫酸铜溶液检验,若尾气含有硫化氢,现象是Ⅱ.制取,其反应的能量示意如下图所示。

(2)写出由
 、
、 、
、 生成
生成 的热化学方程式
的热化学方程式Ⅲ.高温分解:
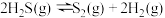
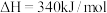
(3)能够判断上述反应到达平衡状态的是___________。(双选)
A. 的浓度保持不变 的浓度保持不变 | B.气体的质量保持不变 |
| C.恒容时,容器的压强保持不变 | D.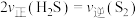 |
(4)在恒温恒压条件下,充入氩气,发现:
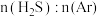 越小,
越小, 平衡转化率越大,请解释可能的原因。
平衡转化率越大,请解释可能的原因。(5)某温度时,向体积不等的恒容容器中加入等量
 ,反应相同时间后,测得各容器中
,反应相同时间后,测得各容器中 的转化率与容器体积关系如图所示。
的转化率与容器体积关系如图所示。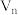 之后,
之后, 的转化率下降的原因是
的转化率下降的原因是
Ⅳ.将
 燃烧,产生的与剩余
燃烧,产生的与剩余 混合后反应,生成单质硫回收。
混合后反应,生成单质硫回收。①
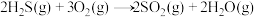
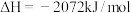
②
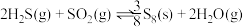

(6)②的平衡常数表达式为
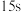 时,测得容器内的气体密度减小了
时,测得容器内的气体密度减小了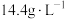 ,则
,则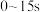 内,
内, 平均反应速率
平均反应速率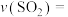
(7)在某温度下发生反应①和②,当②达到平衡,测得密闭系统中各组分浓度分别为:
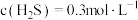 、
、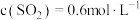 、
、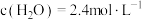 ,请计算开始时投料比
,请计算开始时投料比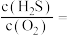
Ⅴ.活性炭吸附氧化法
可用表面喷淋水的活性炭吸附氧化
 ,其反应原理如下图所示。
,其反应原理如下图所示。
(8)该方法的总反应方程式为
您最近一年使用:0次
名校
7 . Ⅰ.一碳化学是指以分子中只含一个碳原子的化合物为原料,用化工的方法制造产品的化学体系的总称。甲烷、一氧化碳是常见的一碳化学的原料。已知反应:
①CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=206kJ•mol-1
CO(g)+3H2(g) ΔH=206kJ•mol-1
②C(s)+H2O(g) CO(g)+H2(g) ΔH=131kJ•mol-1
CO(g)+H2(g) ΔH=131kJ•mol-1
③CO(g)+2H2(g) CH3OH(g) ΔH=﹣124kJ•mol-1
CH3OH(g) ΔH=﹣124kJ•mol-1
(1)工业制取炭黑的方法之一是将甲烷隔绝空气加热到1300℃进行裂解。该反应的热化学方程式为___________ 。
(2)已知反应①中相关的化学键键能数据如表:
可知CO中C≡O键的键能为 ___________ kJ•mol-1。向恒容绝热的密闭容器中充入amolCH4与2amolH2O(g),进行反应①,下列能判断反应已达化学平衡状态的是 ___________ 。
a.容器中混合气体密度不变 b.混合气体中c(CO)与c(H2)之比不变
c.3v正(CH4)=v逆(H2) d.容器内温度不变
(3)反应②的正反应活化能为EakJ•mol-1,则逆反应的活化能为___________ kJ•mol-1。对反应②的自发性进行判断并说明理由___________ 。
Ⅱ.向容积固定为1L的密闭容器内充入2molCO和4molH2,保持250℃发生反应③,用压力计监测反应过程中容器内压强的变化如表:
(4)从开始到20min时,以CO浓度变化表示的平均反应速率v(CO)=___________ 。
(5)250℃时反应③平衡常数K3的值为___________ 。
(6)在容器容积不变的前提下,欲提高反应③中H2的平衡转化率,可采取的措施有___________ 、___________ (任写两项)。
Ⅲ.电喷雾电离等方法得到的M+(Fe+、Ni+、Co+等)与O3反应可得MO+。MO+与CH4反应能高选择性地生成甲醇,体系的能量随反应进程的变化如图所示。

(7)步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是___________ (填“Ⅰ”或“Ⅱ”)。
(8)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢。则MO+与CD4反应的能量变化应为图中曲线___________ (填“c”或“d”)。
(9)若MO+与CHD3反应,生成的氘代甲醇有___________ 种。
①CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH=206kJ•mol-1
CO(g)+3H2(g) ΔH=206kJ•mol-1②C(s)+H2O(g)
 CO(g)+H2(g) ΔH=131kJ•mol-1
CO(g)+H2(g) ΔH=131kJ•mol-1③CO(g)+2H2(g)
 CH3OH(g) ΔH=﹣124kJ•mol-1
CH3OH(g) ΔH=﹣124kJ•mol-1(1)工业制取炭黑的方法之一是将甲烷隔绝空气加热到1300℃进行裂解。该反应的热化学方程式为
(2)已知反应①中相关的化学键键能数据如表:
| 化学键 | C-H | O-H | H-H |
| 键能/kJ•mol﹣1 | 413 | 465 | 436 |
a.容器中混合气体密度不变 b.混合气体中c(CO)与c(H2)之比不变
c.3v正(CH4)=v逆(H2) d.容器内温度不变
(3)反应②的正反应活化能为EakJ•mol-1,则逆反应的活化能为
Ⅱ.向容积固定为1L的密闭容器内充入2molCO和4molH2,保持250℃发生反应③,用压力计监测反应过程中容器内压强的变化如表:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/MPa | p | 0.82p | 0.68p | 0.56p | 0.50p | 0.50p |
(4)从开始到20min时,以CO浓度变化表示的平均反应速率v(CO)=
(5)250℃时反应③平衡常数K3的值为
(6)在容器容积不变的前提下,欲提高反应③中H2的平衡转化率,可采取的措施有
Ⅲ.电喷雾电离等方法得到的M+(Fe+、Ni+、Co+等)与O3反应可得MO+。MO+与CH4反应能高选择性地生成甲醇,体系的能量随反应进程的变化如图所示。

(7)步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是
(8)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢。则MO+与CD4反应的能量变化应为图中曲线
(9)若MO+与CHD3反应,生成的氘代甲醇有
您最近一年使用:0次
名校
8 . CO 变换反应为:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41 kJ·mol⁻1。
(1)一定温度下,反应后测得各组分的平衡压强(即该组分的物质的量分数×总压): p(CO)=0.25 MPa、p(H2O)=0.25 MPa、p(CO2)=0.75 MPa 和 p(H2)=0.75 MPa,则该反应的平衡常数 Kp=___________ 。维持相同的温度和总压,提高水蒸气的投料比例,使 CO 的平衡转化率提高到 90%,则原料气中水蒸气和 CO 的物质的量之比为___________ 。
(2)生产过程中,为了提高变换反应的速率,下列措施中合适的是___________。
(3)以固体催化剂 M 催化 CO 变换反应,能量-反应过程关系如下图所示。步骤___________ 为决速步。(选填“I”或“II”)

用化学方程式表示该催化反应历程:
步骤 I: M(s)+H2O(g)=MO(s)+H2(g), 步骤 II:___________ 。
(1)一定温度下,反应后测得各组分的平衡压强(即该组分的物质的量分数×总压): p(CO)=0.25 MPa、p(H2O)=0.25 MPa、p(CO2)=0.75 MPa 和 p(H2)=0.75 MPa,则该反应的平衡常数 Kp=
(2)生产过程中,为了提高变换反应的速率,下列措施中合适的是___________。
| A.反应温度越高越好 | B.适当提高反应物压强 |
| C.选择合适的催化剂 | D.通入一定量的 N2 |

用化学方程式表示该催化反应历程:
步骤 I: M(s)+H2O(g)=MO(s)+H2(g), 步骤 II:
您最近一年使用:0次
名校
解题方法
9 . 合成氨是人类科学技术的一项重大突破。
(1)如图表示未用催化剂时,N2(g)和H2(g)反应生成1molNH3(g)时的能量变化。写出该反应的热化学方程式:______ 。
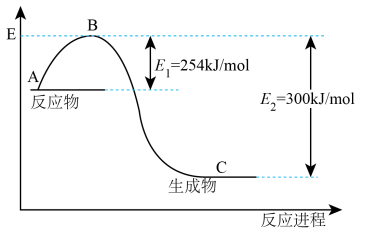
(2)若生成1molNH3(g)时反应的熵变△S=aJ•mol-1•K-1,则a______ 0,该反应能自发进行的温度(T)范围是______ (用含a的不等式表示)。
(3)恒温、恒容密闭容器中进行上述反应,一定能说明该反应达到平衡状态的是______ 。
(4)在温度分别为T1、T2时,固定N2的投入量,起始H2的物质的量与平衡时NH3的物质的量分数关系如图。
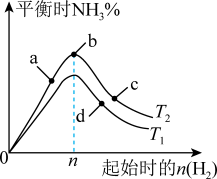
图像中T1和T2的关系是:T1______ T2(选填“>”、“<”或“=”)。a、b、c、d四点中,N2转化率最高的是:______ 。
(5)某温度下,向4L密闭容器中充入1.8molN2和4.2molH2。20min后,NH3浓度为0.3mol•L-1,用N2表示20min内平均反应速率为______ ,此时浓度商(Q)的数值为______ (保留3位有效数字)。若此时v正>v逆,则Q_____ K(K为该温度下平衡常数)。
(1)如图表示未用催化剂时,N2(g)和H2(g)反应生成1molNH3(g)时的能量变化。写出该反应的热化学方程式:

(2)若生成1molNH3(g)时反应的熵变△S=aJ•mol-1•K-1,则a
(3)恒温、恒容密闭容器中进行上述反应,一定能说明该反应达到平衡状态的是
| A.N2、H2、NH3的浓度之比为1∶3∶2 | B.N2质量分数保持不变 |
| C.容器内气体压强保持不变 | D.混合气体的密度保持不变 |

图像中T1和T2的关系是:T1
(5)某温度下,向4L密闭容器中充入1.8molN2和4.2molH2。20min后,NH3浓度为0.3mol•L-1,用N2表示20min内平均反应速率为
您最近一年使用:0次
名校
10 . 用活性炭还原处理氮氧化物,有关反应为C(s)+2NO(g)  N2(g)+CO2(g)。
N2(g)+CO2(g)。
(1)写出上述反应的平衡常数表达式:_______ 。
(2)在2 L恒容密闭容器中加入足量C与NO发生反应,所得数据如表,回答下列问题。
①结合表中数据,判断该反应的ΔH_______ (填“>”或“<”)0,理由是_______ 。
②判断该反应达到平衡状态的依据是_______ (填字母)。
A.容器内气体密度恒定 B.容器内各气体浓度恒定
C.容器内压强恒定 D.2v正(NO)=v逆(N2)
(3)700 ℃时,若向2 L体积恒定的密闭容器中充入一定量N2和CO2发生反应:N2(g)+CO2(g) C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。请回答下列问题。
C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。请回答下列问题。

①0~10 min内CO2的平均反应速率v=_______ 。
②图中A点v正_______ (填“>”“<”或“=”)v逆。
③第10 min时,外界改变的条件可能是_______ (填字母)。
A.加催化剂 B.增大C的物质的量
C.减小CO2的物质的量 D.升温 E.降温
(4)采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示。

容易得到的副产物有CO和CH2O,其中相对较多的副产物为_______ ;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中_______ (填字母)的能量变化。
A.*CO+*OH *CO+*H2O B.*CO
*CO+*H2O B.*CO *OCH
*OCH
C.*OCH2 *OCH3 D.*OCH3
*OCH3 D.*OCH3 *CH3OH
*CH3OH
 N2(g)+CO2(g)。
N2(g)+CO2(g)。(1)写出上述反应的平衡常数表达式:
(2)在2 L恒容密闭容器中加入足量C与NO发生反应,所得数据如表,回答下列问题。
| 实验编号 | 温度/℃ | 起始时NO的物质的量/mol | 平衡时N2的物质的量/mol |
| 1 | 700 | 0.40 | 0.09 |
| 2 | 800 | 0.24 | 0.08 |
②判断该反应达到平衡状态的依据是
A.容器内气体密度恒定 B.容器内各气体浓度恒定
C.容器内压强恒定 D.2v正(NO)=v逆(N2)
(3)700 ℃时,若向2 L体积恒定的密闭容器中充入一定量N2和CO2发生反应:N2(g)+CO2(g)
 C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。请回答下列问题。
C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。请回答下列问题。
①0~10 min内CO2的平均反应速率v=
②图中A点v正
③第10 min时,外界改变的条件可能是
A.加催化剂 B.增大C的物质的量
C.减小CO2的物质的量 D.升温 E.降温
(4)采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示。

容易得到的副产物有CO和CH2O,其中相对较多的副产物为
A.*CO+*OH
 *CO+*H2O B.*CO
*CO+*H2O B.*CO *OCH
*OCHC.*OCH2
 *OCH3 D.*OCH3
*OCH3 D.*OCH3 *CH3OH
*CH3OH
您最近一年使用:0次
2023-03-05更新
|
250次组卷
|
3卷引用:上海交通大学附属中学2022-2023学年高二下学期开学摸底考化学试题



