1 . 下列关于热化学反应的描述正确的是
| A.已知H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1,用含20.0gNaOH的稀溶液与稀盐酸反应测出的中和反应的反应热为28.65kJ·mol-1 |
| B.CO(g)的标准燃烧热△H=-283.0kJ·mol-1,则反应2CO2(g)=2CO(g)+O2(g)的△H=+(2×283.0) kJ·mol-1 |
| C.1mol甲烷燃烧生成气态水和二氧化碳时的焓变是甲烷的标准燃烧热 |
| D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
您最近一年使用:0次
名校
2 . 下列关于反应热的说法正确的是
| A.使用催化剂只改变可逆反应中正反应的活化能 |
| B.反应物的总键能小于生成物的总键能,则反应为吸热反应 |
C.已知红磷比白磷更稳定,  |
D.  ,则 ,则 燃烧热为 燃烧热为 |
您最近一年使用:0次
名校
解题方法
3 . 下列热化学方程式书写正确的是
A.甲烷的标准燃烧热为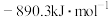 ,则甲烷燃烧的热化学方程式可表示为 ,则甲烷燃烧的热化学方程式可表示为 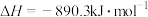 |
B.500℃、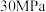 下,将 下,将 和 和 置于密闭容器中充分反应生成 置于密闭容器中充分反应生成 放热 放热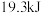 ,其热化学方程式为 ,其热化学方程式为 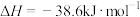 |
C.在 时, 时,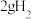 完全燃烧生成液态水,放出 完全燃烧生成液态水,放出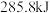 热量,氢气燃烧的热化学方程式表示为 热量,氢气燃烧的热化学方程式表示为 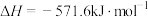 |
D.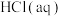 和 和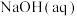 反应的中和热 反应的中和热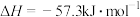 ,则稀 ,则稀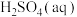 和 和 反应生成 反应生成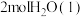 的反应热 的反应热 |
您最近一年使用:0次
名校
解题方法
4 . 下列说法正确的是
| A.0.5mol稀H2SO4与0.5mol稀Ba(OH)2溶液反应放出akJ热量,则中和热为-akJ/mol |
B. (标准燃烧热) (标准燃烧热) |
| C.测定中和热时,温度计测量盐酸的温度后,应用水冲洗干净并擦干再测量NaOH的温度 |
| D.进行中和热测定实验,在酸碱混合时,NaOH溶液应缓缓倒入小烧杯中,用玻璃棒搅拌 |
您最近一年使用:0次
名校
5 . 恒温恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图1所示。[已知:2SO2(g)+O2(g) 2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
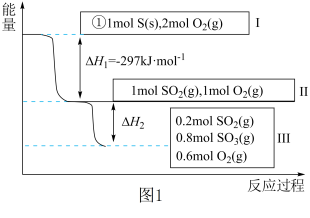
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:___________ 。
(2)恒容条件下,下列措施中能使n(SO3)/n(SO2)比图1所示情况增大的有___________。
(3)恒温恒容时,1mol SO2和2mol O2充分反应,放出热量的数值比|ΔH2|___________ (填“大”、“小”或“相等”)。
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是___________ ;图中表示平衡混合物中SO3的含量最高的一段时间是___________ 。

 2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
2SO3(g) ΔH=﹣196.9kJ•mol﹣1]
请回答下列问题:
(1)写出能表示硫的燃烧热的热化学方程式:
(2)恒容条件下,下列措施中能使n(SO3)/n(SO2)比图1所示情况增大的有___________。
| A.升高温度 | B.充入He | C.再充入1mol SO2(g)和1mol O2(g) | D.使用催化剂 |
(3)恒温恒容时,1mol SO2和2mol O2充分反应,放出热量的数值比|ΔH2|
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t4时引起平衡移动的条件可能是

您最近一年使用:0次
6 . 根据已知,回答下列问题。
(1)在 、
、 下,
下, 甲烷燃烧生成
甲烷燃烧生成 和液态水时放热
和液态水时放热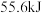 。则表示甲烷燃烧热的热化学方程式为
。则表示甲烷燃烧热的热化学方程式为______ 。
(2)常温常压下,断裂 (理想)气体分子化学键所吸收的能量或形成
(理想)气体分子化学键所吸收的能量或形成 (理想)气体分子化学键所放出的能量称为键能,下表是一些键能数
(理想)气体分子化学键所放出的能量称为键能,下表是一些键能数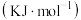
根据键能数据计算以下反应的反应热: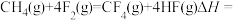
______ 。
(3)随着科学技术的进步,人们研制了多种甲醇质子交换膜燃料电池,以满足不同的需求。有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A.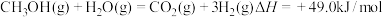
B.
由上述方程式可知, 的燃烧热
的燃烧热______ (填“大于”、“等于”或“小于”)
(4)火箭的常规燃料是液态四氧化二氮和液态肼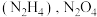 作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
已知:


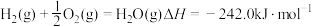
请写出肼和氟气反应的热化学方程式:______ 。
(1)在
 、
、 下,
下, 甲烷燃烧生成
甲烷燃烧生成 和液态水时放热
和液态水时放热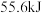 。则表示甲烷燃烧热的热化学方程式为
。则表示甲烷燃烧热的热化学方程式为(2)常温常压下,断裂
 (理想)气体分子化学键所吸收的能量或形成
(理想)气体分子化学键所吸收的能量或形成 (理想)气体分子化学键所放出的能量称为键能,下表是一些键能数
(理想)气体分子化学键所放出的能量称为键能,下表是一些键能数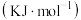
化学键 | 键能 | 化学键 | 键能 | 化学键 | 键能 |
C-H | 414 | C-F | 489 | H-F | 565 |
| 436 |
| 391 |
| 158 |
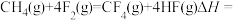
(3)随着科学技术的进步,人们研制了多种甲醇质子交换膜燃料电池,以满足不同的需求。有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A.
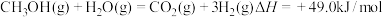
B.

由上述方程式可知,
 的燃烧热
的燃烧热
(4)火箭的常规燃料是液态四氧化二氮和液态肼
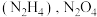 作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。已知:


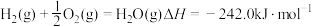
请写出肼和氟气反应的热化学方程式:
您最近一年使用:0次
7 . 下列叙述正确的是
A. 的燃烧热 的燃烧热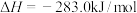 ,则 ,则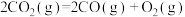 反应的 反应的 |
B.HCl和NaOH反应的中和热为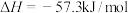 ,则 ,则 和 和 反应的中和热为 反应的中和热为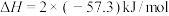 |
C.用等体积的 盐酸、 盐酸、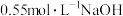 溶液进行中和热测定的实验,会使测得的中和热偏大 溶液进行中和热测定的实验,会使测得的中和热偏大 |
D.一定条件下,将 和 和 置于密闭容器中充分反应生成 置于密闭容器中充分反应生成 放热19.3kJ,其热化学方程式为 放热19.3kJ,其热化学方程式为 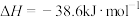 |
您最近一年使用:0次
8 . 已知反应:①101kPa时,2C(s)+O2(g)=2CO(g),ΔH=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O,ΔH=-57.3kJ/mol
下列结论正确的是
②稀溶液中,H+(aq)+OH-(aq)=H2O,ΔH=-57.3kJ/mol
下列结论正确的是
| A.碳的燃烧热大于110.5kJ/mol |
| B.①的反应热为221kJ/mol |
| C.稀硫酸与稀NaOH溶液反应的中和热为114.6kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
您最近一年使用:0次
2023-12-01更新
|
119次组卷
|
3卷引用:福建省福州格致中学2023-2024学年高二上学期10月期中考试化学试题
名校
解题方法
9 . 下列说法正确的是
A.已知:金刚石(s)=石墨(s)  ,则该条件下石墨比金刚石稳定 ,则该条件下石墨比金刚石稳定 |
B.若  ,则甲烷的燃烧热为812.3kJ/mol ,则甲烷的燃烧热为812.3kJ/mol |
C.若  ,则2mol ,则2mol 置于密闭容器中充分反应放出热量为56.9kJ 置于密闭容器中充分反应放出热量为56.9kJ |
D.若  ,则含0.5molNaOH的稀溶液与稀醋酸完全中和,放出的热量为28.7kJ ,则含0.5molNaOH的稀溶液与稀醋酸完全中和,放出的热量为28.7kJ |
您最近一年使用:0次
2023-11-16更新
|
212次组卷
|
4卷引用:福建省福州市八县(区市)协作校2023-2024学年高二上学期11月期中考试化学试题
名校
10 . 完成下列问题。
(1)实验测得16g甲醇 在氧气中充分燃烧生成二氧化碳气体和液态水时释放出363.25kJ的热量,试写出甲醇完全燃烧的热化学方程式:
在氧气中充分燃烧生成二氧化碳气体和液态水时释放出363.25kJ的热量,试写出甲醇完全燃烧的热化学方程式:___________ 。
(2)合成氨反应
 ,能量变化如图所示:
,能量变化如图所示:

①该反应通常用铁作催化剂,加催化剂会使图中
___________ (填“变大”“变小”或“不变”)。
②有关键能数据如下:
试根据表中所列键能数据计算a为___________ 。
(3)现根据下列的3个热化学反应方程式:
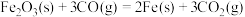

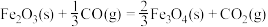
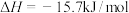

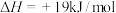
试写出CO气体还原FeO固体得到Fe固体和 气体的热化学反应方程式:
气体的热化学反应方程式:___________ 。
(1)实验测得16g甲醇
 在氧气中充分燃烧生成二氧化碳气体和液态水时释放出363.25kJ的热量,试写出甲醇完全燃烧的热化学方程式:
在氧气中充分燃烧生成二氧化碳气体和液态水时释放出363.25kJ的热量,试写出甲醇完全燃烧的热化学方程式:(2)合成氨反应

 ,能量变化如图所示:
,能量变化如图所示:
①该反应通常用铁作催化剂,加催化剂会使图中

②有关键能数据如下:
| 化学键 | H-H | N-H | N≡N |
键能( ) ) | 436 | 391 | 945 |
(3)现根据下列的3个热化学反应方程式:
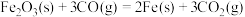

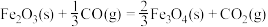
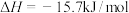

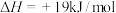
试写出CO气体还原FeO固体得到Fe固体和
 气体的热化学反应方程式:
气体的热化学反应方程式:
您最近一年使用:0次






