名校
解题方法
1 . 下列热化学方程式中ΔH代表燃烧热的是
| A.CH4(g)+3/2O2(g)=2H2O(l)+CO(g) ΔH1 |
| B.S(s)+3/2O2(g)=SO3(g) ΔH2 |
| C.C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l) ΔH3 |
| D.2CO(g)+O2(g)=2CO2(g) ΔH4 |
您最近一年使用:0次
2022-12-02更新
|
438次组卷
|
62卷引用:新疆巴音郭楞蒙古自治州第一中学2022-2023学年高三上学期期中化学试卷
新疆巴音郭楞蒙古自治州第一中学2022-2023学年高三上学期期中化学试卷(已下线)2010—2011学年内蒙古赤峰二中高一下学期期末考试化学试卷(已下线)河北省冀州中学10-11学年高一下学期期末考试(化学理)B卷(已下线)2011-2012年山东省莒南县三中高二上学期期中考试化学试卷(已下线)2011-2012学年黑龙江龙东地区高二第一学期高中教学联合体期末考试化学试卷(已下线)2011-2012学年湖南省蓝山二中高二上学期期末考试化学试卷(已下线)2011-2012学年江西上饶中学高一重点班下期末考试化学试卷2014-2015学年云南省富民县一中高二上学期期中化学试卷2014-2015学年云南省蒙自市蒙自一中高二上学期期中化学试卷2014-2015河北邢台一中高一3月月考化学试卷2015-2016学年广东省仲元中学高二上期中测试化学试卷2015-2016学年贵州省凯里一中高二上学期期末化学试卷2015-2016学年云南省开远四中高二下学期期中化学试卷2016-2017学年河北冀州中学高二上第一次月考化学试卷2016-2017学年黑龙江省大庆市杜蒙县高二上月考一化学卷2016-2017学年河北省张家口市第一中学高一3月月考(理)化学试卷【全国百强校】江苏省南菁高级中学2017-2018学年高二下学期期中考试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二上学期10月月考化学试题新疆维吾尔自治区兵团第二师华山中学2018-2019学年高二上学期第一次调研考试化学试题山西省阳泉二中2018-2019学年高二上学期期中考试化学试题辽宁省普兰店市第一中学2018-2019学年高二(理)上学期期中考试化学试题云南省玉溪市元江县第一中学2018-2019学年高二下学期开学考试化学试题安徽省六安市二中2018-2019学年高二第一学期10月月考化学试题湖南省邵东县创新实验学校2019-2020学年高二上学期期中考试化学(理)试题辽宁省葫芦岛市第八高级中学2019-2020学年高二上学期期中考试化学试题福建2020届高三化学总复习专题训练——选修四化学反应原理测试2020届高三化学二轮复习———燃烧热的综合2020年春季人教版高中化学选修4第一章《化学反应与能量》测试卷【懂做原理题】2020届高三化学选修4二轮专题练——燃烧热【选择精编25题】2020届高三化学二轮复习—— 化学能与热能【精编选择25题】内蒙古包头市第六中学2019-2020学年高二上学期期中考试化学试题云南省曲靖市罗平县第三中学2020届高二下学期开学考试化学试题人教版(2019)高二选择性必修第一册 第一章 化学反应的热效应 第一节 反应热2湖南省宁乡县第七中学2020-2021学年高二10月月考化学试题吉林省榆树市第一高级中学2020-2021学年高二上学期期中考试化学试题天津市静海瀛海学校2020-2021学年高二上学期11月联考化学试题河南省新乡市长垣县第十中学2020-2021学年高二上学期期中考试化学试题广西南宁市第四中学2020-2021学年高二下学期开学考试化学试题河北省石家庄市第二十三中学2020-2021学年高一第二学期5月月考化学试题青海省海南州贵德高级中学2020-2021学年高二下学期期中化学试题安徽省淮北市树人高级中学2020-2021学年高一下学期第四次阶段考试化学试题(已下线)第二节 燃烧热 能源(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)河南省南阳市第五完全中学2020-2021学年高二上学期开学考试化学试题青海省西宁市北外附属新华联国际学校2021-2022学年高二上学期第一次月考化学(理)试题重庆市长寿中学校2021-2022学年高二10月月考化学试题山西省太原市第五十六中学2021-2022学年高二上学期10月月考化学试题(已下线)第1章基础巩固测评卷-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)1.3 燃料的合理利用-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)1.3 燃料的合理利用-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第24练 反应热-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第02讲 热化学方程式与燃烧热(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)宁夏永宁县永宁中学2021-2022学年高二上学期期中考试化学试题天津市第九十五中学益中学校2022-2023学年高二上学期期中考试化学试题山西省太原市第五十六中学2022-2023学年高二上学期10月联考化学试题陕西省西安市周至县第四中学2021-2022学年高二上学期期中考试化学(理科)试题广东省连平县忠信中学2020-2021学年高二下学期第二次段考化学试题云南昆明市昆明行知中学2021-2022学年高二上学期期中考试化学试题新疆乌鲁木齐市第八中学2022-2023学年高二上学期期末考试化学试题6.2.2燃料燃烧释放的能量(课后)-2019苏教版必修2课前课中课后甘肃省天水市秦安县第一中学2022-2023学年高二上学期期末考试化学试题新疆喀什市2023-2024学年高二上学期期中考试化学试题新疆兵团第三师图木舒克市鸿德实验学校2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
2 . 在25℃和101 kPa下,1 g H2燃烧生成液态水放出142.9 kJ的热量,则下列属于H2的燃烧热的热化学方程式的是
A. 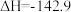 kJ/mol kJ/mol |
B. 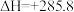 kJ/mol kJ/mol |
C.  kJ/mol kJ/mol |
D.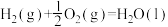 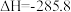 kJ/mol kJ/mol |
您最近一年使用:0次
2022-11-21更新
|
1388次组卷
|
19卷引用:新疆巴州第一中学2022-2023学年高二上学期10月月考化学试题
新疆巴州第一中学2022-2023学年高二上学期10月月考化学试题湖南省长沙市长郡中学2021-2022学年高二上学期期中考试化学试题北京市大兴区2021-2022学年高二上学期期中考试化学试题人教2019版选择性必修一第一章 化学反应的热效应 复习与提高浙江省山河联盟2021-2022学年高二上学期12月考试化学试题内蒙古呼和浩特市2021-2022学年高二上学期期末考试化学试题天津市部分区2021-2022学年高二上学期期末(下学期期初)考试化学试题吉林省吉化第一高级中学校2021-2022学年高一下学期复课检测化学试题浙江省金华市江南中学2021-2022学年高二上学期期中考试化学试题海南省儋州市鑫源中学2021-2022学年高二上学期期末考试化学试题湖南省宁远县第一中学2022-2023学年高二上学期第一次适应性考试化学试题广东省茂名市电白区2022-2023学年高二上学期期中选择性考试化学试题广东省深圳市罗湖区翠园中学2022-2023高二上学期期中考试化学试题广东省深圳市翠园中学2022-2023学年高二上学期期中考试化学试题浙江省龙泉浙大中学2022-2023学年高二上学期12月教学质量检测化学试题山西省大同市第一中学校2023-2024学年高二上学期10月月考化学试题(已下线)专题01 化学反应的热效应-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(天津专用)四川省射洪中学校2023-2024学年高二上学期第三次月考化学试题江西省上饶市2023-2024学年高二上学期期末教学质量测试化学试卷
名校
解题方法
3 . 下列热化学方程式中,正确的是
| A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1 |
B.500℃、30MPa下,将0.5molN2(g)和1.5molH2(g)置于密闭容器中充分反应生成NH3(g)放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H=-38.6kJ·mol-1 2NH3(g) △H=-38.6kJ·mol-1 |
| C.HCl和NaOH反应的中和热△H=-57.3kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ·mol-1 |
| D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1 |
您最近一年使用:0次
2022-05-14更新
|
371次组卷
|
17卷引用:新疆巴音郭楞蒙古自治州第一中学2022-2023学年高二上学期期末考试化学试题
新疆巴音郭楞蒙古自治州第一中学2022-2023学年高二上学期期末考试化学试题辽宁省营口市第二高级中学2020届高三上学期第一次月考化学试题安徽省安庆市怀宁县第二中学2019-2020学年高二下学期期中线上检测化学试题(已下线)专题07 化学反应中的能量变化-2020年高考真题和模拟题化学分项汇编黑龙江省大庆市第四中学2019-2020学年高二上学期第一次检测化学试题(已下线)1.1.2 反应热的测量和计算(重点练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)黑龙江省哈尔滨市第一中学校2019-2020学年高一下学期期末考试化学试题西藏自治区拉萨市拉萨中学2020-2021学年高二第一次月考理综化学试题甘肃省武威第八中学2020-2021学年高二上学期月考化学试题黑龙江省伊春市伊美区第二中学2020-2021学年高二上学期开学考试化学试题(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记福建省南安市柳城中学2020-2021学年高一下学期期中考试化学试题四川省成都市蒲江县蒲江中学2019-2020学年高二上学期10月月考化学试题江苏省海安市南莫中学2021-2022学年高二上学期第一次月考备考金卷B卷化学试题湖南省益阳市箴言中学2021-2022学年高二上学期10月月考化学试题(已下线)第04讲 燃料燃烧释放的能量与氢燃料的发展前景-【寒假自学课】2022年高一化学寒假精品课(苏教版必修第二册)辽宁省沈阳市第一二〇中学2020-2021学年高一下学期期中化学试题
名校
4 . 习近平总书记提出:绿水青山就是金山银山,为了更好的解决能源问题,人们一方面研究如何提高燃料的燃烧效率,另一方面寻找能源,以下做法不能提高燃料效率的是
| A.煤的气化与液化 | B.液体燃料呈雾状喷出 |
| C.通入大大过量的空气 | D.将煤粉碎 |
您最近一年使用:0次
2020-11-19更新
|
269次组卷
|
14卷引用:新疆生产建设兵团第二师八一中学2021-2022学年高二上学期期中考试化学试题
新疆生产建设兵团第二师八一中学2021-2022学年高二上学期期中考试化学试题(已下线)2012年人教版高中化学选修4 2.2影响化学反应速率的因素练习卷(已下线)2012年苏教版高中化学必修2 2.4太阳能、生物能和氢能的利用练习卷(已下线)2012-2013学年云南省大理州宾川县第四高级中学高二4月月考化学卷(已下线)2014年高二化学人教版选修二 2.3 石油煤天然气利用练习卷2015-2016学年甘肃省嘉峪关一中高一下学期期末化学试卷2016-2017学年福建省宁德市部分中学高二上期中化学试卷江苏省东台市创新高级中学2018-2019学年高二下学期3月月考化学试题2020届人教版高中化学高三专题基础复习专题13《化学与技术》测试卷2020届高中化学第一轮复习第十三章《化学与技术》测试卷(已下线)江苏省沭阳县修远中学2018-2019学年高一下学期第二次月考化学试题湖北省襄阳市五校(宜城一中、枣阳一中、襄州一中、曾都一中、南漳一中)2020-2021学年高二上学期期中联考化学试题湖北省枣阳一中2021-2022学年高二上学期10月月考化学试题青海省海南州贵德高级中学2022-2023学年高二下学期期末考试化学试卷
解题方法
5 . 写出下列反应的热化学方程式。
(1) 葡萄糖晶体在氧气中完全氧化生成二氧化碳气体和液态水时放出
葡萄糖晶体在氧气中完全氧化生成二氧化碳气体和液态水时放出 热量:
热量:_______ 。
(2)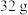 铜粉在足量氧气中反应生成氧化铜固体时放出
铜粉在足量氧气中反应生成氧化铜固体时放出 热量:
热量:_________ 。
(3)标准状况下,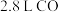 气体在氧气中完全燃烧生成二氧化碳气体时放出
气体在氧气中完全燃烧生成二氧化碳气体时放出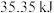 热量:
热量:_________ 。
(4)一氧化碳气体还原磁铁矿得到 单质铁时放出
单质铁时放出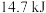 热量:
热量:_______________ 。
(1)
 葡萄糖晶体在氧气中完全氧化生成二氧化碳气体和液态水时放出
葡萄糖晶体在氧气中完全氧化生成二氧化碳气体和液态水时放出 热量:
热量:(2)
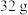 铜粉在足量氧气中反应生成氧化铜固体时放出
铜粉在足量氧气中反应生成氧化铜固体时放出 热量:
热量:(3)标准状况下,
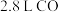 气体在氧气中完全燃烧生成二氧化碳气体时放出
气体在氧气中完全燃烧生成二氧化碳气体时放出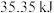 热量:
热量:(4)一氧化碳气体还原磁铁矿得到
 单质铁时放出
单质铁时放出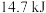 热量:
热量:
您最近一年使用:0次
2020-10-07更新
|
520次组卷
|
5卷引用:新疆巴州第一中学2022-2023学年高二上学期10月月考化学试题
名校
6 . 已知:101 kPa时,1molH2完全燃烧生成液态水,放出285.8 kJ的热量;1molCH4完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列能表示燃烧热的热化学方程式是
A.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH=−890.3 kJ CO2(g)+2H2O(l) ΔH=−890.3 kJ |
B.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH=+890.3 kJ·mol−1 CO2(g)+2H2O(l) ΔH=+890.3 kJ·mol−1 |
C.CH4(g)+2O2(g) CO2(g)+2H2O(g) ΔH=−890.3 kJ·mol−1 CO2(g)+2H2O(g) ΔH=−890.3 kJ·mol−1 |
D.H2(g)+ O2(g) O2(g) H2O(l) ΔH=−285.8 kJ·mol−1 H2O(l) ΔH=−285.8 kJ·mol−1 |
您最近一年使用:0次
2020-02-02更新
|
134次组卷
|
3卷引用:新疆生产建设兵团第二师八一中学2021-2022学年高二上学期期中考试化学试题
名校
7 . 甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时放出222.5kJ热量,则下列热化学方程式中正确的是
| A.2CH4(g) + 4O2(g) =2CO2(g) + 4H2O(l)ΔH= +890 kJ·mol-1 |
| B.CH4(g) + 2O2(g) = CO2(g) +2H2O(l)ΔH= +890 kJ·mol-1 |
| C.CH4(g) + 2O2(g) = CO2(g) +2H2O(l)ΔH=-890 kJ·mol-1 |
| D.2CH4(g) + 4O2(g) = 2CO2(g) + 4H2O(l)ΔH= -890 kJ·mol-1 |
您最近一年使用:0次
2019-01-30更新
|
1148次组卷
|
34卷引用:新疆巴州第一中学2022-2023学年高二上学期10月月考化学试题
新疆巴州第一中学2022-2023学年高二上学期10月月考化学试题(已下线)2010—2011学年甘肃省天水一中高二下学期期末考试化学试卷(已下线)2011-2012学年山东省鲁北中学高二上学期期中考试化学试卷(已下线)2011-2012学年山东省济宁市邹城二中高二上学期期中质量检测化学试卷(已下线)2011-2012学年贵州省凯里一中高二上学期期中考试化学试卷(已下线)2011-2012学年云南省玉溪一中高二下学期期中考试化学试卷(已下线)2011-2012贵州省凯里一中第一学期期末考试高二化学试卷2014-2015学年甘肃省民乐一中高二上学期第一次月考化学试卷2015-2016学年湖南宁远一中、祁阳一中高二上第二次联考化学试卷2015-2016学年江苏省射阳县第二中学高二上学期期末选修化学试卷甘肃省天水市第一中学2016-2017学年高一下学期期末(第三次)考试(理)化学试题河南省信阳市商城县高级中学2017-2018学年高二上学期第一次月考化学试题陕西省渭南市尚德中学2017-2018学年高二上学期期中考试化学试卷陕西省蓝田县焦岱中学2018-2019学年高二上学期第一次月考化学试题河北省邢台市第八中学2018-2019学年高二上学期期中考试化学试题内蒙古集宁一中(西校区)2018-2019学年高一下学期期末考试化学试题黑龙江省龙东南联合体2018-2019学年高一下学期期末考试化学试题河南省周口中英文学校2019-2020学年高二上学期第一次月考化学试题吉林省榆树市第一高级中学2019-2020学年高二上学期期中考试化学试题宁夏青铜峡市高级中学2019-2020学年高二上学期期中考试化学试题山东省微山县第二中学2019-2020学年高二上学期第二学段质量检测化学试题甘肃省古浪县第二中学2019-2020学年高二上学期基础知识竞赛化学试题黑龙江省哈尔滨市延寿县第二中学2020-2021学年高二上学期9月月考化学试题福建省永安市第三中学2020-2021学年高二10月月考化学(选考班)试题吉林省梅河口市朝鲜族中学2019-2020学年高二上学期期末考试化学试题天津市第八中学2020-2021学年高二上学期第三次统练化学试题安徽省六安市城南中学2020-2021学年高二上学期期中考试化学试题吉林省通化县综合高级中学2021-2022学年高二上学期期中考试化学试题宁夏青铜峡市高级中学2021-2022学年高二上学期期中考试化学试题广东省揭阳华侨高级中学2021-2022学年高二上学期第一次阶段考试化学试题甘肃省临夏州临夏县中学2022-2023学年高二上学期9月月考化学试题广西柳州市第三中学2022-2023学年高二上学期10月月考化学试题吉林省白城市第十四中学2021-2022学年高二上学期期中考试化学试卷题海南省临高县新盈中学2021-2022学年高二上学期(1-4班)期中考试化学试题
名校
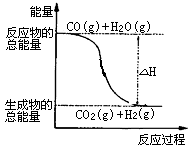
8 . 已知热化学方程式:
①CO(g)+1/2O2(g)=CO2(g)ΔH=-283.0kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1
则下列说法正确的是( )
①CO(g)+1/2O2(g)=CO2(g)ΔH=-283.0kJ·mol-1
②H2(g)+1/2O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1
则下列说法正确的是( )

| A.H2的燃烧热为241.8kJ·mol-1 |
| B.由反应①、②可知上图所示的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g)ΔH=-41.2 kJ·mol-1 |
| C.H2(g)转变成H2O(g)的化学反应一定要放出能量 |
| D.根据②推知反应H2(g)+1/2O2(g)=H2O(l)ΔH>-241.8 kJ·mol-1 |
您最近一年使用:0次
2016-12-05更新
|
262次组卷
|
6卷引用:新疆维吾尔自治区且末县第二中学2018-2019学年高二上学期期末考试化学试题



