名校
解题方法
1 . 下列关于热化学方程式的说法正确的是
A.若 的燃烧热为a kJ⋅mol 的燃烧热为a kJ⋅mol ,则热化学方程式为 ,则热化学方程式为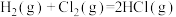  kJ⋅mol kJ⋅mol |
B.若1 mol  和0.5 mol 和0.5 mol  完全反应放热98.3 kJ,则热化学方程式为 完全反应放热98.3 kJ,则热化学方程式为  kJ⋅mol kJ⋅mol |
C.若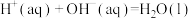 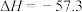 kJ⋅mol kJ⋅mol ,则稀硫酸与稀 ,则稀硫酸与稀 反应的热化学方程式为 反应的热化学方程式为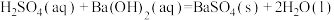  kJ⋅mol kJ⋅mol |
D.若3l g白磷的能量比3l g红磷多b kJ,则白磷转化为红磷的热化学方程式为 (白磷,s) (白磷,s) (红磷,s) (红磷,s)  kJ⋅mol kJ⋅mol |
您最近一年使用:0次
2023-10-12更新
|
317次组卷
|
65卷引用:重庆市重庆实验外国语学校2021-2022学年高二上学期9月月考化学试题
重庆市重庆实验外国语学校2021-2022学年高二上学期9月月考化学试题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)模块七 化学反应与能量(模块检测)-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)江苏省海安市南莫中学2021-2022学年高二上学期第一次月考备考金卷A卷化学试题福建省武平县第一中学2021-2022学年高二上学期10月月考化学试题江苏省泰州中学2021-2022学年高二上学期第一次月度检测化学试题(已下线)专题18 化学反应与能量(限时精练)-2022年高三毕业班化学常考点归纳与变式演练安徽省合肥市第六中学2021-2022学年高二上学期月考化学试题福建省泉州现代中学2021-2022学年高二上学期9月月考化学试题山东省济钢高级中学2021-2022学年高二上学期第二次教学检测化学试题山东省济南市第一中学2021-2022学年高二上学期期中考试化学试题(已下线)必考点01 化学反应与能量-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版)湖北省部分省级示范高中2021-2022学年高二上学期期中测试化学试题(已下线)专题09 化学反应与能量变化-备战2022年高考化学学霸纠错(全国通用)北京理工大学附属中学2021-2022学年高二上学期期中练习化学试题黑龙江省牡丹江市第三中学2021-2022学年高二上学期第一次月考化学(理)试题广东省广雅中学2021-2022学年高二上学期期中考试化学试题辽宁省丹东市东港第二高级中学2021-2022学年高二上学期11月第二次教学检测化学试题宁夏石嘴山市第三中学2021-2022学年高三上学期第二次月考化学试题宁夏永宁县永宁中学2021-2022学年高二上学期期中考试化学试题重庆市永川北山中学校2022-2023学年高三上学期期中质量监测化学试题广东省广州真光中学2021-2022学年高二上学期期中考试化学试题(已下线)2018年9月10日 《每日一题》一轮复习-热化学方程式的书写(已下线)2018年12月20日 《每日一题》人教选修4-热化学方程式的书写与判断百所名校联考-化学反应与能量(已下线)2019年9月9日《每日一题》2020年一轮复习—— 热化学方程式的书写(已下线)考点08 化学反应中的能量变化——《备战2020年高考精选考点专项突破题集》宁夏石嘴山市第三中学2019-2020学年高二下学期期中考试化学试题黑龙江省牡丹江市第一高级中学2020-2021学年高二上学期8月开学考试化学试题(已下线)1.1.2 热化学方程式 燃烧热(练习)——2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)(已下线)第一章 化学反应的热效应(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)辽宁省盘锦市第二高级中学2020-2021学年高二上学期第一次阶段性考试化学试题山东省济宁市实验中学2020-2021学年高二上学期10月月考化学试题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)湖北省鄂州市2021-2022学年高二上学期期末质量监测化学试题(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)第一节 反应热 第2课时 热化学方程式 燃烧热黑龙江省双鸭山市第一中学2022-2023学年高二上学期开学考试化学试题 (已下线)专题六 化学反应与能量 能力提升检测卷(测)-2023年高考化学一轮复习讲练测(新教材新高考)湖北省红安县第一中学2022-2023学年高二上学期9月考试化学试题湖北省襄阳市第五中学2022-2023学年高二上学期9月化学试题山东省青岛第二中学2022-2023学年高二上学期10月月考化学试题安徽省舒城中学2022-2023学年高二上学期第二次月考化学试题黑龙江省牡丹江市第一高级中学2022-2023学年高二上学期期中考试化学试题福建省石狮市第一中学2022-2023学年高二上学期第一次月考化学试题甘肃省兰州市第二中学2022-2023学年高二上学期期中考试化学试题广东省广州市育才中学2022-2023学年高二上学期期中考试化学试题新疆喀什地区疏附县第一中学2022-2023学年高二上学期期末考试化学试题(已下线)专题15 反应热计算的几种类型-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)黑龙江省双鸭山市第一中学2022-2023学年高二下学期开学考试化学试题湖南省长沙市芙蓉高级中学2022-2023学年高二上学期期中考试化学试题广东省广州市从化区从化中学2022-2023学年高二上学期期中考试化学试题(已下线)查补易混易错04 化学反应原理部分-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)广东省广州市第八十六中学2022-2023学年高二上学期期中考试化学试题(已下线)专题突破卷07 化学反应与能量?-2024年高考化学一轮复习考点通关卷(新教材新高考)(已下线)考点17 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)宁夏回族自治区中宁县第一中学2022-2023学年高二上学期10月月考化学试题四川省成都外国语学校2023-2024学年高二上学期10月月考化学试题福建省福州市连江尚德中学2023-2024学年高二上学期第一次诊断性测试化学试题广东省梅州市大埔县虎山中学2023-2024学年高二上学期10月期中考试化学试题四川省成都市成华区某校2023-2024学年高一上学期期中考试化学试题陕西省西安中学2023-2024学年高三上学期实验班11月练考理科综合能力测试题
名校
2 . 自热化学链重整制氢 CLR(a)工艺的原理如图所示:
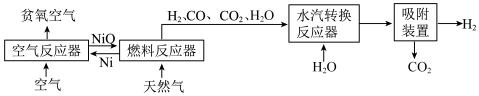
回答下列问题:
(1)25℃、101kPa 时,5.9gNi 与足量 O2反应生成 NiO 放出 47.2kJ 的热量,则在“空气反应器” 中发生反应的热化学方程式为___________ 。
(2)“燃料反应器”中发生的部分反应有:
(I)CO(g)+NiO(s)=CO2(g)+Ni(s) ΔH1=-47.0kJ/mol 平衡常数 K1
(II)CH4(g)+4NiO(s)=CO2(g)+2H2O(g)+4Ni(s) ΔH2=+137.7kJ/mol 平衡常数 K2
(III) CH4(g)+3CO2(g)=4CO(g)+2H2O(g) ΔH3=akJ/mol 平衡常数 K3
①CO2的电子式:___________ 。
②K1、K2、K3之间的关系是:___________ ;
③在___________ (填“高温”或“低温”)情况下有利于反应Ⅲ的自发进行。
(3)“水汽转换反应器”中发生的反应为CO(g)+ H2O(g)=CO2(g)+H2(g),将天然气看作是纯净的CH4(假定向水汽转换反应器中补充的水的物质的量等于甲烷的物质的量),若在 t℃时进行转换,水汽转换反应器中达平衡时 CO、H2O、H2、CO2浓度之比为1:x:3:1,则该反应的平衡常数 K=___________ 。
(4)甲烷制氢传统工艺有水蒸气重整部分氧化重整以及联合重整等,CLR(a)工艺重整是一种联合重整,涉及反应的热化学方程式如下:
CH4(g)+2H2O(g)=CO2(g)+4H2(g) ΔH=+192kJ/mol
CH4(g)+O2(g)=CO2(g)+2H2(g) ΔH=-768kJ/mol
水蒸气重整反应: 部分氧化重整反应:
①采用水蒸气重整的优点是:___________ ;
②上述两个反应的缺点之一是在制取氢气的同时产生大量温室气体 CO2,若用 NaOH 溶液来吸收 CO2,写出反应的离子方程式:___________ ;
③若上述两个反应在保持自热条件下(假设无热量损失),理论上 2 molCH4至多可获得 H2的物质的量为___________ (结果保留 1 位小数)。

回答下列问题:
(1)25℃、101kPa 时,5.9gNi 与足量 O2反应生成 NiO 放出 47.2kJ 的热量,则在“空气反应器” 中发生反应的热化学方程式为
(2)“燃料反应器”中发生的部分反应有:
(I)CO(g)+NiO(s)=CO2(g)+Ni(s) ΔH1=-47.0kJ/mol 平衡常数 K1
(II)CH4(g)+4NiO(s)=CO2(g)+2H2O(g)+4Ni(s) ΔH2=+137.7kJ/mol 平衡常数 K2
(III) CH4(g)+3CO2(g)=4CO(g)+2H2O(g) ΔH3=akJ/mol 平衡常数 K3
①CO2的电子式:
②K1、K2、K3之间的关系是:
③在
(3)“水汽转换反应器”中发生的反应为CO(g)+ H2O(g)=CO2(g)+H2(g),将天然气看作是纯净的CH4(假定向水汽转换反应器中补充的水的物质的量等于甲烷的物质的量),若在 t℃时进行转换,水汽转换反应器中达平衡时 CO、H2O、H2、CO2浓度之比为1:x:3:1,则该反应的平衡常数 K=
(4)甲烷制氢传统工艺有水蒸气重整部分氧化重整以及联合重整等,CLR(a)工艺重整是一种联合重整,涉及反应的热化学方程式如下:
CH4(g)+2H2O(g)=CO2(g)+4H2(g) ΔH=+192kJ/mol
CH4(g)+O2(g)=CO2(g)+2H2(g) ΔH=-768kJ/mol
水蒸气重整反应: 部分氧化重整反应:
①采用水蒸气重整的优点是:
②上述两个反应的缺点之一是在制取氢气的同时产生大量温室气体 CO2,若用 NaOH 溶液来吸收 CO2,写出反应的离子方程式:
③若上述两个反应在保持自热条件下(假设无热量损失),理论上 2 molCH4至多可获得 H2的物质的量为
您最近一年使用:0次
名校
3 . 下列说法不正确的是
| A.CH4 的燃烧热是890.3kJ·mol-1,则表示 CH4 的燃烧热的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
| B.由C(金刚石)=C(石墨) ΔH=-1.9 kJ·mol-1可知,石墨比金刚石稳定 |
| C.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,若将含 1mol HNO3 的稀溶液与含 1mol Ba(OH)2 的稀溶液混合,放出的热量为 57.3 kJ |
| D.1mol 钠蒸气与 2 mol 钠蒸气完全燃烧时,燃烧热相同 |
您最近一年使用:0次
2023-08-19更新
|
371次组卷
|
2卷引用:重庆市大足中学2021-2022学年高二上学期第一次月考化学试题
4 . 下列有关说法正确的是
A.已知HI(g)  H2(g)+ H2(g)+ I2(s) ΔH=-26.5 kJ·mol-1,由此可知1 mol HI气体在密闭容器中充分分解后可以放出26.5 kJ的热量 I2(s) ΔH=-26.5 kJ·mol-1,由此可知1 mol HI气体在密闭容器中充分分解后可以放出26.5 kJ的热量 |
| B.已知2H2(g)+O2(g)=2H2O(g) ΔH= -571.6 kJ·mol-1,则氢气的燃烧热为ΔH= -285.8 kJ·mol-1 |
| C.已知2C(s)+2O2(g)=2CO2(g) ΔH1,2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1<ΔH2 |
| D.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) ΔH=-57.4 kJ·mol-1 |
您最近一年使用:0次
2023-06-06更新
|
1849次组卷
|
31卷引用:重庆市朝阳中学2021-2022学年高二10月月考化学试题
重庆市朝阳中学2021-2022学年高二10月月考化学试题辽宁省大连市一0三中学2020-2021学年高一4月月考化学试题四川省南充市李渡中学2020-2021学年高一下学期期中考试化学试题广西贵港市江南中学2021-2022学年高二上学期12月月考化学(理科)试题甘肃省甘南藏族自治州舟曲县第一中学2021-2022学年高二上学期期中考试化学试题吉林省汪清县第六中学2021-2022学年高二12月月考化学试题内蒙古赤峰市第四中学分校2021-2022学年高二上学期9月月考化学试题【全国百强校】四川省成都市石室中学2018-2019学年高二上学期期中考试化学试题湖南省长沙市明德中学2019-2020学年高二下学期第一次月考化学试题湖北省武汉市第十一中学2019-2020学年高一下学期期中测试化学试题河南省南阳市第一中学2019-2020学年高二下学期第三次月考(6月)化学试题广东省广州大学附属中学2019-2020学年高一下学期期末考试化学试题(已下线)1.1.2 热化学方程式 燃烧热(练习)——2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)(已下线)1.3.2 反应热的计算(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)广东省广州大学附属中学等三校2019~2020学年高一下学期期末联考化学试题(已下线)第一章 化学反应与能量(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)(已下线)1.3.1+盖斯定律-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)山东省德州市夏津第一中学2020-2021学年高二上学期9月月考化学试题江西省南昌县莲塘第三中学2020-2021学年高二上学期期中考试化学试题江西省赣州市会昌县第五中学2020-2021学年高二上学期第一次月考化学试题吉林省延边第二中学2020-2021学年高二上学期第二次考试月考化学试题云南省富源县第一中学2020-2021学年高二上学期第一次统测化学试题黑龙江省大兴安岭呼玛县高级中学2021-2022学年高二上学期期末考试化学试题黑龙江省大庆铁人中学2022-2023学年高一下学期期中考试化学试题(已下线)考点巩固卷07 化学反应与能量(3大考点45题)-2024年高考化学一轮复习考点通关卷(新高考通用)陕西省宝鸡市金台区2022-2023学年高一下学期期末考试化学试题黑龙江省佳木斯市第一中学2023-2024学年高二上学期10月月考化学试题河南省商丘市第一高级中学2023-2024学年高三上学期10月份月考化学试题江西省宜春市上高二中2023-2024学年高二上学期第一次月考化学试题陕西省汉中市乡县第一中学2023-2024学年高二上学期10月月考化学试题广东省深圳市罗湖外语学校2023-2024学年高二上学期期中考试化学试题
名校
解题方法
5 . 下列热化学方程式中ΔH代表燃烧热的是
| A.CH4(g)+3/2O2(g)=2H2O(l)+CO(g) ΔH1 |
| B.S(s)+3/2O2(g)=SO3(g) ΔH2 |
| C.C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l) ΔH3 |
| D.2CO(g)+O2(g)=2CO2(g) ΔH4 |
您最近一年使用:0次
2022-12-02更新
|
437次组卷
|
62卷引用:重庆市长寿中学校2021-2022学年高二10月月考化学试题
重庆市长寿中学校2021-2022学年高二10月月考化学试题广西南宁市第四中学2020-2021学年高二下学期开学考试化学试题河北省石家庄市第二十三中学2020-2021学年高一第二学期5月月考化学试题青海省海南州贵德高级中学2020-2021学年高二下学期期中化学试题安徽省淮北市树人高级中学2020-2021学年高一下学期第四次阶段考试化学试题(已下线)第二节 燃烧热 能源(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)青海省西宁市北外附属新华联国际学校2021-2022学年高二上学期第一次月考化学(理)试题山西省太原市第五十六中学2021-2022学年高二上学期10月月考化学试题宁夏永宁县永宁中学2021-2022学年高二上学期期中考试化学试题陕西省西安市周至县第四中学2021-2022学年高二上学期期中考试化学(理科)试题广东省连平县忠信中学2020-2021学年高二下学期第二次段考化学试题云南昆明市昆明行知中学2021-2022学年高二上学期期中考试化学试题(已下线)2010—2011学年内蒙古赤峰二中高一下学期期末考试化学试卷(已下线)河北省冀州中学10-11学年高一下学期期末考试(化学理)B卷(已下线)2011-2012年山东省莒南县三中高二上学期期中考试化学试卷(已下线)2011-2012学年黑龙江龙东地区高二第一学期高中教学联合体期末考试化学试卷(已下线)2011-2012学年湖南省蓝山二中高二上学期期末考试化学试卷(已下线)2011-2012学年江西上饶中学高一重点班下期末考试化学试卷2014-2015学年云南省富民县一中高二上学期期中化学试卷2014-2015学年云南省蒙自市蒙自一中高二上学期期中化学试卷2014-2015河北邢台一中高一3月月考化学试卷2015-2016学年广东省仲元中学高二上期中测试化学试卷2015-2016学年贵州省凯里一中高二上学期期末化学试卷2015-2016学年云南省开远四中高二下学期期中化学试卷2016-2017学年河北冀州中学高二上第一次月考化学试卷2016-2017学年黑龙江省大庆市杜蒙县高二上月考一化学卷2016-2017学年河北省张家口市第一中学高一3月月考(理)化学试卷【全国百强校】江苏省南菁高级中学2017-2018学年高二下学期期中考试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二上学期10月月考化学试题新疆维吾尔自治区兵团第二师华山中学2018-2019学年高二上学期第一次调研考试化学试题山西省阳泉二中2018-2019学年高二上学期期中考试化学试题辽宁省普兰店市第一中学2018-2019学年高二(理)上学期期中考试化学试题云南省玉溪市元江县第一中学2018-2019学年高二下学期开学考试化学试题安徽省六安市二中2018-2019学年高二第一学期10月月考化学试题湖南省邵东县创新实验学校2019-2020学年高二上学期期中考试化学(理)试题辽宁省葫芦岛市第八高级中学2019-2020学年高二上学期期中考试化学试题福建2020届高三化学总复习专题训练——选修四化学反应原理测试2020届高三化学二轮复习———燃烧热的综合2020年春季人教版高中化学选修4第一章《化学反应与能量》测试卷【懂做原理题】2020届高三化学选修4二轮专题练——燃烧热【选择精编25题】2020届高三化学二轮复习—— 化学能与热能【精编选择25题】内蒙古包头市第六中学2019-2020学年高二上学期期中考试化学试题云南省曲靖市罗平县第三中学2020届高二下学期开学考试化学试题人教版(2019)高二选择性必修第一册 第一章 化学反应的热效应 第一节 反应热2湖南省宁乡县第七中学2020-2021学年高二10月月考化学试题吉林省榆树市第一高级中学2020-2021学年高二上学期期中考试化学试题天津市静海瀛海学校2020-2021学年高二上学期11月联考化学试题河南省新乡市长垣县第十中学2020-2021学年高二上学期期中考试化学试题河南省南阳市第五完全中学2020-2021学年高二上学期开学考试化学试题(已下线)第1章基础巩固测评卷-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)1.3 燃料的合理利用-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)1.3 燃料的合理利用-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第24练 反应热-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第02讲 热化学方程式与燃烧热(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)天津市第九十五中学益中学校2022-2023学年高二上学期期中考试化学试题新疆巴音郭楞蒙古自治州第一中学2022-2023学年高三上学期期中化学试卷山西省太原市第五十六中学2022-2023学年高二上学期10月联考化学试题新疆乌鲁木齐市第八中学2022-2023学年高二上学期期末考试化学试题6.2.2燃料燃烧释放的能量(课后)-2019苏教版必修2课前课中课后甘肃省天水市秦安县第一中学2022-2023学年高二上学期期末考试化学试题新疆喀什市2023-2024学年高二上学期期中考试化学试题新疆兵团第三师图木舒克市鸿德实验学校2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
6 . 在25℃、 下,1 g甲醇燃烧生成
下,1 g甲醇燃烧生成 和液态水时放热
和液态水时放热 ,下列热化学方程式正确的是
,下列热化学方程式正确的是
 下,1 g甲醇燃烧生成
下,1 g甲醇燃烧生成 和液态水时放热
和液态水时放热 ,下列热化学方程式正确的是
,下列热化学方程式正确的是A. 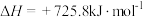 |
B.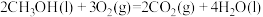 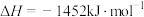 |
C.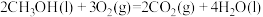  |
D.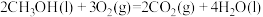 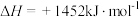 |
您最近一年使用:0次
2022-11-18更新
|
910次组卷
|
90卷引用:重庆市清华中学校2021—2022学年上学期高二10月月考化学试题
重庆市清华中学校2021—2022学年上学期高二10月月考化学试题新疆伊犁奎屯市第一高级中学2020-2021学年高二上学期期末考试化学试题青海省北外附属西宁新华联国际学校2020-2021学年高二上学期期末考试化学试题高中化学苏教2019版必修第二册-专题6 第二单元 第1课时 放热反应与吸热反应(已下线)专题08 化学反应与能量-备战2021届高考化学二轮复习题型专练河北省临漳县第一中学2020-2021学年高一下学期3月份月考化学试题(已下线)第一章 第三节 化学反应热的计算(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)山西省太原市第五十六中学2021-2022学年高二上学期10月月考化学试题江苏省泰州中学2021-2022学年高二上学期第二次质量检测化学试题江苏省扬州市江都区邵伯高级中学2020-2021学年高一下学期期中考试化学试题宁夏吴忠市吴忠中学2021-2022学年高二上学期月考化学试题广东省深圳市第七高级中学2021-2022学年高二上学期期中考试化学试题河南省许昌市鄢陵县职业教育中心2021-2022学年高二上学期第一次月考化学试题云南省玉龙纳西族自治县田家炳民族中学2021-2022学年高二上学期期中考试化学试题黑龙江省佳木斯市第八中学2021-2022学年高二上学期期中考试化学试题(已下线)浙江省临海市白云中学2009—2010学年度高二下学期第一次月考化学试题(已下线)2010年安徽师大附中高二第二学期期中考查(已下线)2011-2012年河北省灵寿中学高二上学期第一次月考化学试卷(已下线)2011-2012学年江苏省江阴市一中高二上学期期中考试化学(选修)试卷(已下线)2011-2012学年河南省焦作市修武一中分校高二上学期期中考试化学试卷(已下线)2012届甘肃省西北师大附中高三第一学期期中考试化学试卷(已下线)2011-2012学年浙江杭州萧山九中高二下学期第一次质量检测化学试卷(已下线)2011-2012学年广西北海合浦县教育局高二下学期期中理科化学试卷(已下线)2011-2012学年浙江东阳中学、兰溪一中高一下学期期中考试化学卷 (已下线)2011-2012年呼伦贝尔市牙克石林业一中高一下学期期末考试化学试卷(已下线)2011-2012学年福建省安溪一中高一下学期期末联考化学试卷(已下线)2012-2013学年福建龙岩一中高二上第一学段模块考试化学试卷(已下线)2012年苏教版高中化学选修4 1.1化学反应中的热效应(已下线)2012-2013年江苏南京学大教育专修学校高二3月月考化学试卷(已下线)2012-2013学年江西省赣州市十一县(市)高二上学期期中联考化学试卷(已下线)2012-2013学年福建省漳州市芗城中学高二上学期期末考试化学试卷(已下线)2014届江苏省常州市某重点中学学初学业水平测试化学试卷(已下线)2012届西北师大附中高三第一学期期中考试化学试卷(已下线)2014-2015学年河南省汝州市高二上学期第一次月考化学试卷(已下线)2014-2015学年辽宁师范大学附中高二10月模考化学试卷2014-2015学年宁夏育才中学高二上学期期中化学试卷2014-2015学年河北省正定中学高一下学期期中化学试卷2015-2016学年山西省右玉一中高二上学期第一次月考化学试卷2015-2016学年江西省南昌市湾里区一中高二上学期期中测试化学试卷2015-2016学年西藏日喀则中学高二上12月月考化学试卷2015-2016学年广东省深圳市明德外语学校高二上学期期中理化学试卷2015-2016学年安徽省亳州市高二上学期期末质检化学试卷2015-2016学年湖南省常德一中高二下第一次月考化学试卷2015-2016学年河北省唐山市开滦一中高一下期末理科化学试卷2015-2016学年福建省福州市文博中学高二上期中化学试卷2016-2017学年贵州省思南中学高二上半期考试化学卷2016-2017学年甘肃省嘉峪关市酒钢三中高二上学期期末考试化学试卷2017届河北省定州中学高三下学期开学考试化学试卷2016-2017学年山东省烟台第二中学高二下学期开学考试化学试卷河北省唐山市曹妃甸区第一中学2016-2017学年高一下学期期中考试化学试题河北省大名县第一中学2017-2018学年高二上学期第一次月考化学试题福建省长泰县第一中学2017-2018学年高二上学期期中考试(理)化学试题新疆昌吉市2017-2018学年高二上学期期末考试化学试题河北省深州中学2017-2018高一下学期期中考试化学试题人教版高二化学选修四专题:化学反应与能量变化同步练习题吉林省辽源市田家炳高级中学2018-2019学年高二9月月考化学试题新疆自治区北京大学附属中学新疆分校2018-2019学年高二上学期10月月考化学试题甘肃省宁县二中2018-2019学年高二上学期期中考试化学试题云南省育能高级中学2018-2019学年高二上学期期中考试化学试题江西省奉新县第一中学2018-2019学年高二上学期第三次月考化学试题陕西省黄陵中学高新部2018-2019学年高一第二学期期中考试化学试题浙江省丽水四校联考2019年6月高二阶段性考试化学试题陕西省黄陵县中学2018-2019学年高一(重点班)下学期期中考试化学试题吉林省白城市通榆县第一中学2019-2020学年高二上学期第一次月考化学试题山东省淄博市淄川区般阳中学2019-2020学年高二10月月考化学试题河北省唐山市第十一中学2019-2020学年高二上学期期中考试化学(理)试题河北省石家庄市六校2019-2020学年高二上学期期中考试化学试题陕西省西安电子科技大学附属中学2019-2020学年高二上学期期中考试化学(理)试题广东省惠来县葵潭中学2019-2020学年高二上学期第二次月考化学试题新疆哈密市第十五中学2019-2020学年高一上学期期末考试化学试题云南省昆明市寻甸县民族中学2019-2020学年高二下学期第一次月考化学试题陕西省咸阳市实验中学2020-2021学年高二上学期第一次月考化学试题贵州省遵义市航天高级中学2020-2021学年高二上学期第一次月考化学(理)试题内蒙古赤峰学院附属中学2020-2021学年高二上学期期中考试化学试题西藏拉萨市第二高级中学2019-2020学年高二上学期期中考试化学试题河北省石家庄市元氏县第四中学2020-2021学年高二上学期期中考试化学试题云南省保山第九中学2019-2020学年高二下学期期末考试化学试题(苏教版2019)必修第二册专题6 化学反应与能量变化 第二单元 化学反应中的热 课时1 化学反应中的能量变化湖南省长沙市第一中学2020-2021学年高二上学期入学考试化学试题福建省诏安县桥东中学2021-2022学年高一下学期期中考试化学试题天津市第三中学2022-2023学年高二上学期期中考试化学试题江苏省马坝高级中学2022-2023学年高二上学期期中考试化学试题山西省太原市第五十六中学2022-2023学年高二上学期10月联考化学试题广东省珠海市斗门第一中学2022-2023学年高二上学期期中考试化学试题福建省福州市外国语学校2022-2023学年高二上学期12月阶段性测试化学试题湖南省常德市西洞庭管理区第一中学2022-2023学年高二上学期第二次月考化学试题山东烟台2022-2023学年高一下学期3月月考化学试题(已下线)专题01 化学反应的热效应-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)新疆维吾尔自治区阿克苏地区第一中学2023-2024学年高二上学期期末考试化学试卷北京市中国人民大学附属中学2023-2024学年高一下学期期中考试化学试题
名校
7 . 已知H+(aq)+OH-(aq)=H2O(l)ΔH1=-57.3kJ·mol-1,下列说法正确的是
| A.1mol强酸与1mol强碱完全反应放出的热量均为57.3kJ |
| B.在稀溶液中,酸与碱发生中和反应放出的热量均为57.3kJ |
| C.氢气的燃烧热ΔH=-285.8kJ·mol-1,则表示燃烧热的热化学方程式为2H2(g)+O2(g)=2H2O(l) ΔH=-285.8kJ·mol-1 |
| D.C(石墨,s)=C(金刚石,s) ΔH=+1.9kJ·mol-1,则由石墨制取金刚石的反应是吸热反应,石墨比金刚石稳定 |
您最近一年使用:0次
名校
解题方法
8 . 在101kPa时,一定量H2在O2中完全燃烧生成2.00mol液态H2O。放出571.6kJ的热量,写出H2燃烧热的热化学方程式:___________ 。计算10gH2完全燃烧生成液态水时放出热量为:___________ 。
您最近一年使用:0次
9 . 通过以下反应均可获取H2,下列有关说法正确的是
①太阳光催化分解水制氢:2H2O(l) = 2H2(g) + O2(g) ΔH1=+571.6 kJ·mol-1
②焦炭与水反应制氢:C(s) + H2O(g) = CO(g) + H2(g) ΔH2=+131.3 kJ·mol-1
③甲烷与水反应制氢:CH4(g) + H2O(g) = CO(g) + 3H2(g) ΔH3=+206.1 kJ·mol-1
①太阳光催化分解水制氢:2H2O(l) = 2H2(g) + O2(g) ΔH1=+571.6 kJ·mol-1
②焦炭与水反应制氢:C(s) + H2O(g) = CO(g) + H2(g) ΔH2=+131.3 kJ·mol-1
③甲烷与水反应制氢:CH4(g) + H2O(g) = CO(g) + 3H2(g) ΔH3=+206.1 kJ·mol-1
| A.反应①可知,氢气的燃烧热为571.6kJ·mol-1 |
| B.反应②为吸热反应,不能自发进行 |
| C.反应③使用催化剂,∆H3减小 |
| D.反应CH4(g) = C(s) + 2H2(g) 的∆H=+74.8 kJ·mol-1 |
您最近一年使用:0次
2022-08-16更新
|
290次组卷
|
2卷引用:重庆市第七中学校2021-2022学年高二上学期第二次月考化学试题
名校
解题方法
10 . 重庆火锅、重庆小面都离不开辣椒,而辣椒的味道主要来自于辣椒素.兴趣小组探究其组成和性质,获得如下信息:
①元素分析仪测得该物质有C、H、O、N四种元素,其中氧元素含量为
②质谱仪测定该物质相对分子质量为305
③取 辣椒素完全燃烧,测得有
辣椒素完全燃烧,测得有 和
和 ,放出的热量可以使
,放出的热量可以使 水上升9.2℃(水的比热容为
水上升9.2℃(水的比热容为 )
)
④能与 反应放出
反应放出 ,但不能与
,但不能与 反应
反应
⑤能在强酸和强碱条件下水解
下列对辣椒素推测错误的是
①元素分析仪测得该物质有C、H、O、N四种元素,其中氧元素含量为

②质谱仪测定该物质相对分子质量为305
③取
 辣椒素完全燃烧,测得有
辣椒素完全燃烧,测得有 和
和 ,放出的热量可以使
,放出的热量可以使 水上升9.2℃(水的比热容为
水上升9.2℃(水的比热容为 )
)④能与
 反应放出
反应放出 ,但不能与
,但不能与 反应
反应⑤能在强酸和强碱条件下水解
下列对辣椒素推测错误的是
A.它的分子式为 |
B.它的燃烧热为 |
| C.它完全燃烧的产物可以不进行尾气处理 |
| D.它的结构中有多种含氧官能团 |
您最近一年使用:0次
2022-04-03更新
|
161次组卷
|
2卷引用:重庆市第一中学2021-2022学年高三上学期第三次月考化学试题



