2022·江苏南通·模拟预测
名校
解题方法
1 . 有效去除烟气中的 是环境保护的重要课题。
是环境保护的重要课题。
(1)O3能将NO和NO2转化成绿色硝化剂N2O5。已知下列热化学方程式:
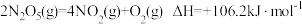
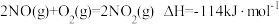

则反应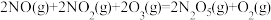 的
的
_______ 。
(2)一种通过 和
和 的相互转化脱除
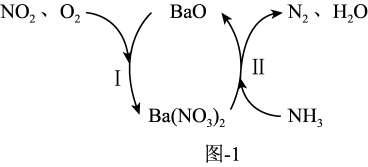
的相互转化脱除 的原理如图1所示。脱除
的原理如图1所示。脱除 的总反应为
的总反应为_______ 。
(3)NH3在催化剂作用下能与烟气(主要为空气,含少量NOx)中的NOx反应,实现NOx的脱除。常见的催化剂有V2O5等。反应的催化剂附在载体的表面,该载体为Ti的氧化物,其有两种晶体类型,分别如图2(a)、(b)所示,其中晶体a比表面积大,附着能力强,可用作载体,一定温度下可转化为晶体b。在V2O5催化下,NOx的脱除机理如图3所示。
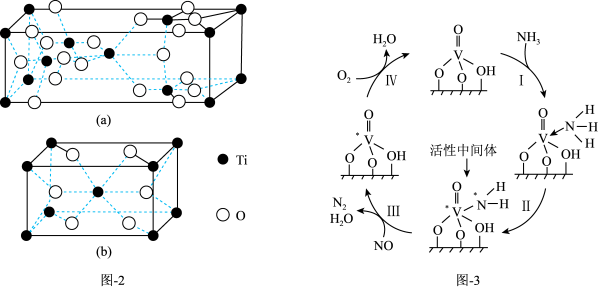
①晶体b的化学式为_______ 。
②转化IV中,V元素化合价的变化为_______ 。
③脱除NOx时须控制反应的温度,实验发现,其他条件一定,当温度过高时,NOx的脱除率会降低,原因除高温下不利于NH3的吸附、催化剂本身活性降低外,还可能的原因是_______ 和_______ 。
 是环境保护的重要课题。
是环境保护的重要课题。(1)O3能将NO和NO2转化成绿色硝化剂N2O5。已知下列热化学方程式:
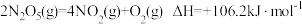
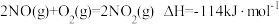

则反应
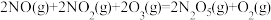 的
的
(2)一种通过
 和
和 的相互转化脱除
的相互转化脱除 的原理如图1所示。脱除
的原理如图1所示。脱除 的总反应为
的总反应为
(3)NH3在催化剂作用下能与烟气(主要为空气,含少量NOx)中的NOx反应,实现NOx的脱除。常见的催化剂有V2O5等。反应的催化剂附在载体的表面,该载体为Ti的氧化物,其有两种晶体类型,分别如图2(a)、(b)所示,其中晶体a比表面积大,附着能力强,可用作载体,一定温度下可转化为晶体b。在V2O5催化下,NOx的脱除机理如图3所示。

①晶体b的化学式为
②转化IV中,V元素化合价的变化为
③脱除NOx时须控制反应的温度,实验发现,其他条件一定,当温度过高时,NOx的脱除率会降低,原因除高温下不利于NH3的吸附、催化剂本身活性降低外,还可能的原因是
您最近一年使用:0次
2022-04-21更新
|
954次组卷
|
6卷引用:山西省晋中市祁县中学2022-2023学年高三上学期10月月考化学试题
山西省晋中市祁县中学2022-2023学年高三上学期10月月考化学试题(已下线)江苏省南通市如皋市2021-2022学年高三下学期 4月适应性考试(二)化学试题(已下线)化学-2022年高考押题预测卷02(江苏卷)江苏省响水中学2021-2022学年高二下学期第二次学情分析考试化学试题(已下线)2022年江苏卷高考真题变式题14-17河南省周口恒大中学2023-2024学年高二下学期3月月考化学试题
名校
2 . 清洁能源的综合利用可有效降低碳排放,是实现“碳中和、碳达峰”的重要途径。
(1)以环己烷为原料通过芳构化反应生产苯,同时可获取氢气。图甲是该反应过程中几种物质间的能量关系。
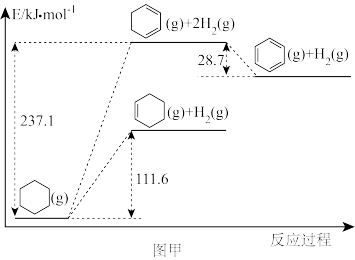
芳构化反应: (g)→
(g)→ (g)+3H2(g)
(g)+3H2(g) 
_______ kJ/mol。
(2) 和
和 合成乙醇反应为:
合成乙醇反应为: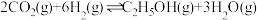 。将等物质的量的
。将等物质的量的 和
和 充入一刚性容器中,测得平衡时
充入一刚性容器中,测得平衡时 的体积分数随温度和压强的关系如图乙。
的体积分数随温度和压强的关系如图乙。
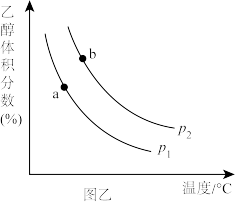
①压强P1_______ P2(填“>”“=”或“<”,下同),a、b两点的平衡常数Ka_______ Kb。
②已知Arrhenius经验公式为 (
( 为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效能,进行了实验探究,依据实验数据获得图丙曲线。
为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效能,进行了实验探究,依据实验数据获得图丙曲线。
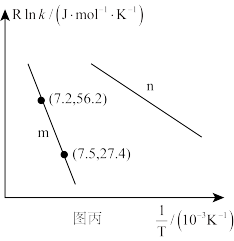
在m催化剂作用下,该反应的活化能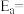
_______ J/mol。从图中信息获知催化效能较高的催化剂是_______ (填“m”或“n”),判断理由是_______ 。
(3) 和CO合成甲烷反应为:
和CO合成甲烷反应为: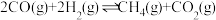 。T℃将等物质的量CO和H2充入恒压(200KPa)的密闭容器中。已知逆反应速率
。T℃将等物质的量CO和H2充入恒压(200KPa)的密闭容器中。已知逆反应速率 ,其中p为分压,该温度下
,其中p为分压,该温度下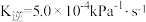 。反应达平衡时测得v正=
。反应达平衡时测得v正=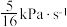 。CO的平衡转化率为
。CO的平衡转化率为_______ ,该温度下反应的Kp=_______ 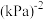 (用组分的分压计算的平衡常数)。
(用组分的分压计算的平衡常数)。
(1)以环己烷为原料通过芳构化反应生产苯,同时可获取氢气。图甲是该反应过程中几种物质间的能量关系。

芳构化反应:
 (g)→
(g)→ (g)+3H2(g)
(g)+3H2(g) 
(2)
 和
和 合成乙醇反应为:
合成乙醇反应为: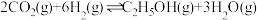 。将等物质的量的
。将等物质的量的 和
和 充入一刚性容器中,测得平衡时
充入一刚性容器中,测得平衡时 的体积分数随温度和压强的关系如图乙。
的体积分数随温度和压强的关系如图乙。
①压强P1
②已知Arrhenius经验公式为
 (
( 为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效能,进行了实验探究,依据实验数据获得图丙曲线。
为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效能,进行了实验探究,依据实验数据获得图丙曲线。
在m催化剂作用下,该反应的活化能
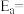
(3)
 和CO合成甲烷反应为:
和CO合成甲烷反应为: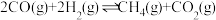 。T℃将等物质的量CO和H2充入恒压(200KPa)的密闭容器中。已知逆反应速率
。T℃将等物质的量CO和H2充入恒压(200KPa)的密闭容器中。已知逆反应速率 ,其中p为分压,该温度下
,其中p为分压,该温度下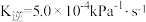 。反应达平衡时测得v正=
。反应达平衡时测得v正=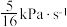 。CO的平衡转化率为
。CO的平衡转化率为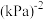 (用组分的分压计算的平衡常数)。
(用组分的分压计算的平衡常数)。
您最近一年使用:0次
2022-04-14更新
|
1515次组卷
|
10卷引用:山西省晋中市平遥县第二中学校2021-2022学年高二下学期升级化学试题
山西省晋中市平遥县第二中学校2021-2022学年高二下学期升级化学试题山东省青岛市2021-2022学年高三下学期第一次模拟考试化学试题(已下线)化学-2022年高考押题预测卷02(辽宁卷)(已下线)押江苏卷第18题 化学反应原理综合题 -备战2022年高考化学临考题号押题(江苏卷)山东省泰安市2022届高三下学期三轮验收考试化学试题(已下线)化学-2022年高考考前押题密卷(湖北卷)广东省珠海市实验中学、东莞市第六高级中学、河源高级中学、中山市实验中学2021-2022学年下学期高三第五次联考化学试题山东省滨州市2023届高三上学期期末综合测试化学试题(已下线)山东省济南市2022届高三3月高考模拟考试(一模)(原理综合题)湖南省醴陵市第一中学2023届高三下学期第七次月考化学试题
3 . 2021年11月2日,第四届世界顶尖科学家碳大会——通往“双碳目标”的科技之路论坛在上海召开。我国科学家刘科提到了绿色甲醇技术,将CO2转化为甲醇是实现碳达峰、碳中和的一种非常重要的路径。回答下列问题:
(1)已知H2(g)和CH3OH(l)的燃烧热分别为285.8kJ·mol-1、726.5kJ·mol-1,则CO2与H2反应生成液态甲醇和液态水的热化学方程式为_____ 。
(2)最近科学家采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,反应历程如图所示:
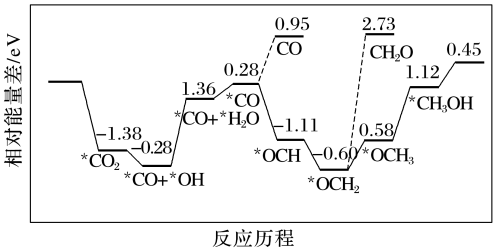
①反应容易得到的副产物有CO和CH2O,其中相对较少的副产物为_____ 。
②上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中_____ (填字母)的能量变化。
A.*CO+*OH→*CO+*H2O B.*CO+*H2O→*CO
C.*OCH2→*OCH3 D.*OCH3→*CH3OH
(3)一定条件下,在1L恒容密闭容器中充入1molCO2和3molH2发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),温度对CO2平衡转化率及催化剂的催化效率影响如图所示:
CH3OH(g)+H2O(g),温度对CO2平衡转化率及催化剂的催化效率影响如图所示:
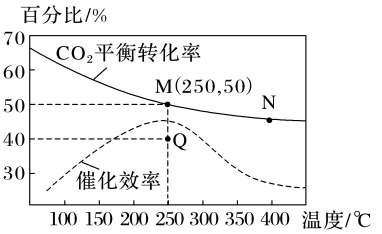
①下列说法能说明该反应达到化学平衡状态的是_____ (填字母)。
A.混合气体的密度不再变化
B.混合气体的平均相对分子质量不再变化
C.CO2、H2、CH3OH、H2O的物质的量之比为1∶3∶1∶1
D.H2O(g)和CO2(g)的生成速率之比为1∶1
②反应速率:v正(M)_____ (填“大于”“小于”“等于”或“无法判断”,下同)v逆(N),化学平衡常数:KM_____ KN。
③M点甲醇的体积分数为_____ ,该温度下,反应的平衡常数K=_____ 。
④已知:反应速率v=v正-v逆=k正c(CO2)·c3(H2)-k逆c(CH3OH)·c(H2O),k正、k逆分别为正、逆反应速率常数,则Q点时 =
=_____ (保留2位小数)。
(1)已知H2(g)和CH3OH(l)的燃烧热分别为285.8kJ·mol-1、726.5kJ·mol-1,则CO2与H2反应生成液态甲醇和液态水的热化学方程式为
(2)最近科学家采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,反应历程如图所示:

①反应容易得到的副产物有CO和CH2O,其中相对较少的副产物为
②上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中
A.*CO+*OH→*CO+*H2O B.*CO+*H2O→*CO
C.*OCH2→*OCH3 D.*OCH3→*CH3OH
(3)一定条件下,在1L恒容密闭容器中充入1molCO2和3molH2发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),温度对CO2平衡转化率及催化剂的催化效率影响如图所示:
CH3OH(g)+H2O(g),温度对CO2平衡转化率及催化剂的催化效率影响如图所示:
①下列说法能说明该反应达到化学平衡状态的是
A.混合气体的密度不再变化
B.混合气体的平均相对分子质量不再变化
C.CO2、H2、CH3OH、H2O的物质的量之比为1∶3∶1∶1
D.H2O(g)和CO2(g)的生成速率之比为1∶1
②反应速率:v正(M)
③M点甲醇的体积分数为
④已知:反应速率v=v正-v逆=k正c(CO2)·c3(H2)-k逆c(CH3OH)·c(H2O),k正、k逆分别为正、逆反应速率常数,则Q点时
 =
=
您最近一年使用:0次
解题方法
4 . 利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A:
已知:
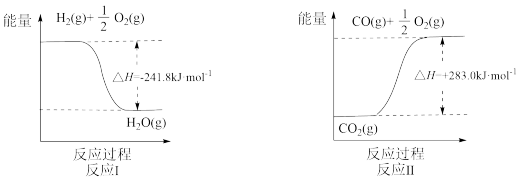
(1)反应Ⅱ是___________ 反应(填“吸热”或“放热”),其原因是___________ 。
(2)反应A的热化学方程式是___________ 。
反应A:

已知:

(1)反应Ⅱ是
(2)反应A的热化学方程式是
您最近一年使用:0次
2022-01-28更新
|
98次组卷
|
2卷引用:山西省晋中市平遥县第二中学2021-2022学年高二上学期12月考试化学试题
解题方法
5 . 我国提出争取在2030年前实现碳峰值,2060年实现碳中和,这对改善环境、实现绿色发展至关重要。以含碳物质为原料的“碳-化学”将处于化学产业的核心,成为科学家研究的重要课题。请回答下列问题:
(1)已知CO、H2、 的燃烧热分别为:
的燃烧热分别为: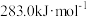 、
、 、
、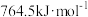 。则反应:
。则反应:
_______ 。
(2)在一容积可变的密闭容器中充入 和
和 ,发生反应
,发生反应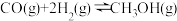 ,CO的平衡转化率(
,CO的平衡转化率( )与温度(T)、压强(p)的关系如图所示。
)与温度(T)、压强(p)的关系如图所示。
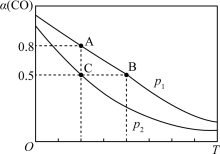
则压强
_______ (填“<”“=”或“>”) ;A、B、C三点的平衡常数
;A、B、C三点的平衡常数 、
、 、
、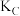 的大小关系为
的大小关系为_______ (用“<”“=”或“>”表示)。
(3) 经催化加氢可合成低碳烯烃:
经催化加氢可合成低碳烯烃: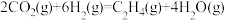 。在
。在 时,按
时,按 投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
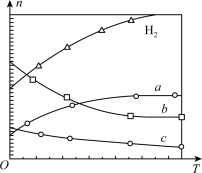
则:
①该反应的
_______ (填“>”或“<”)0。
②曲线c表示的物质为_______ 。
(4)在 、
、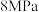 下,将
下,将 和
和 按物质的量之比1∶3通入一密闭容器中发生反应:
按物质的量之比1∶3通入一密闭容器中发生反应: ,达到平衡时,测得
,达到平衡时,测得 的平衡转化率为50%,则该反应条件下的平衡常数
的平衡转化率为50%,则该反应条件下的平衡常数
_______ 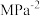 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)已知CO、H2、
 的燃烧热分别为:
的燃烧热分别为: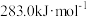 、
、 、
、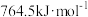 。则反应:
。则反应:
(2)在一容积可变的密闭容器中充入
 和
和 ,发生反应
,发生反应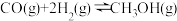 ,CO的平衡转化率(
,CO的平衡转化率( )与温度(T)、压强(p)的关系如图所示。
)与温度(T)、压强(p)的关系如图所示。
则压强

 ;A、B、C三点的平衡常数
;A、B、C三点的平衡常数 、
、 、
、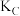 的大小关系为
的大小关系为(3)
 经催化加氢可合成低碳烯烃:
经催化加氢可合成低碳烯烃: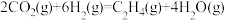 。在
。在 时,按
时,按 投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
则:
①该反应的

②曲线c表示的物质为
(4)在
 、
、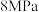 下,将
下,将 和
和 按物质的量之比1∶3通入一密闭容器中发生反应:
按物质的量之比1∶3通入一密闭容器中发生反应: ,达到平衡时,测得
,达到平衡时,测得 的平衡转化率为50%,则该反应条件下的平衡常数
的平衡转化率为50%,则该反应条件下的平衡常数
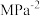 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
您最近一年使用:0次
名校
解题方法
6 .  捕获技术用于去除气流中的
捕获技术用于去除气流中的 或者分离出
或者分离出 作为气体产物,其中
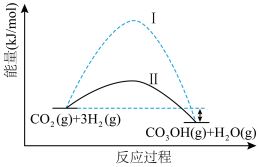
作为气体产物,其中 催化合成甲醇是一种很有前景的方法。如图所示为该反应在无催化剂及有正催化剂时的能量变化(该反应为可逆反应)。
催化合成甲醇是一种很有前景的方法。如图所示为该反应在无催化剂及有正催化剂时的能量变化(该反应为可逆反应)。
(1)温度为523 K时,测得上述反应中生成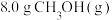 放出的热量为12.3 kJ。反应的热化学方程式为
放出的热量为12.3 kJ。反应的热化学方程式为___________ 。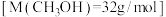
(2)从图可知,有催化剂存在的是过程___________ (填“Ⅰ”或“Ⅱ”)。
(3)一定温度下(各物质均为气态),向体积为2 L的恒容密闭容器中充入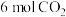 和
和 ,加入合适催化剂进行反应。某时刻测得
,加入合适催化剂进行反应。某时刻测得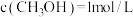 ,此时反应
,此时反应___________ (填“正向移动”、“逆向移动”或“达到平衡)。已知该温度下反应的化学平衡常数值为1/40.
(4)关于 催化合成甲醇的反应,下列说法中合理的是___________(填字母序号)。
催化合成甲醇的反应,下列说法中合理的是___________(填字母序号)。
(5)制备过程中存在副反应: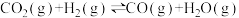
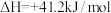 将混合气按进料比
将混合气按进料比 通入反应装置,选择合适催化剂发生反应。不同温度和压强下,
通入反应装置,选择合适催化剂发生反应。不同温度和压强下, 平衡产率和
平衡产率和 平衡转化率分别如图1、图2。
平衡转化率分别如图1、图2。
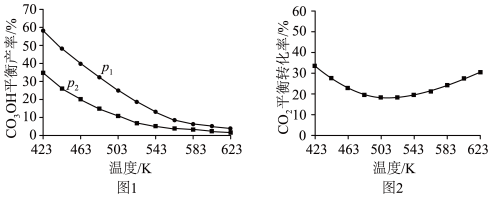
①图1中,压强
___________  (填“>”“=”或“<”),推断的依据是
(填“>”“=”或“<”),推断的依据是___________ 。
②图2中,压强为 ,温度高于503 K后,
,温度高于503 K后, 平衡转化率随温度升高而增大的原因是
平衡转化率随温度升高而增大的原因是___________ 。
 捕获技术用于去除气流中的
捕获技术用于去除气流中的 或者分离出
或者分离出 作为气体产物,其中
作为气体产物,其中 催化合成甲醇是一种很有前景的方法。如图所示为该反应在无催化剂及有正催化剂时的能量变化(该反应为可逆反应)。
催化合成甲醇是一种很有前景的方法。如图所示为该反应在无催化剂及有正催化剂时的能量变化(该反应为可逆反应)。
(1)温度为523 K时,测得上述反应中生成
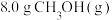 放出的热量为12.3 kJ。反应的热化学方程式为
放出的热量为12.3 kJ。反应的热化学方程式为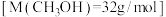
(2)从图可知,有催化剂存在的是过程
(3)一定温度下(各物质均为气态),向体积为2 L的恒容密闭容器中充入
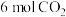 和
和 ,加入合适催化剂进行反应。某时刻测得
,加入合适催化剂进行反应。某时刻测得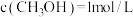 ,此时反应
,此时反应(4)关于
 催化合成甲醇的反应,下列说法中合理的是___________(填字母序号)。
催化合成甲醇的反应,下列说法中合理的是___________(填字母序号)。| A.该反应原子转化率为100% |
B.该反应可用于 的转化,有助于缓解温室效应 的转化,有助于缓解温室效应 |
C.使用催化剂可以降低该反应的 ,从而使反应放出更多热量 ,从而使反应放出更多热量 |
D.降温分离液态甲醇和水,将剩余气体重新通入反应器,可提高 与 与 的利用率 的利用率 |
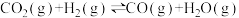
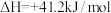 将混合气按进料比
将混合气按进料比 通入反应装置,选择合适催化剂发生反应。不同温度和压强下,
通入反应装置,选择合适催化剂发生反应。不同温度和压强下, 平衡产率和
平衡产率和 平衡转化率分别如图1、图2。
平衡转化率分别如图1、图2。
①图1中,压强

 (填“>”“=”或“<”),推断的依据是
(填“>”“=”或“<”),推断的依据是②图2中,压强为
 ,温度高于503 K后,
,温度高于503 K后, 平衡转化率随温度升高而增大的原因是
平衡转化率随温度升高而增大的原因是
您最近一年使用:0次
2021-11-15更新
|
181次组卷
|
2卷引用:山西省介休市第十中学2022-2023学年高二上学期 期中考试化学试题
7 . 李克强总理在十三届全国人民代表大会第四次会议上作政府工作报告时指出:优化产业结构和能源结构,扎实做好碳达峰、碳中和各项工作。碳中和是指一个组织在一年内的二氧化碳排放通过二氧化碳去除技术达到平衡。
(1)科研人员借助太阳能用二氧化碳制备甲醇等燃料的催化转化是迄今为止最接近光合作用的方法,并且实现了二氧化碳的循环(如图所示),下列说法错误的是___________ (填字母)。
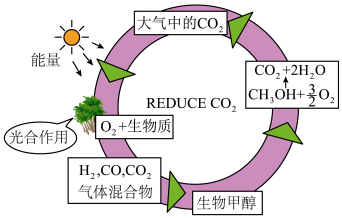
A.图中能量转化形式有两种
B.使用催化剂可以提高单位时间内反应物的转化率
C.利用太阳能开发甲醇等液态燃料有利于环境保护
D.该工艺中的H2目前只能由电解水获得
(2)CO2加氢还可制备甲酸(HCOOH)。
①工业上利用甲酸的能量关系转换图如图所示:
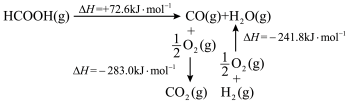
反应CO2(g)+H2(g) HCOOH(g)的焓变△H=
HCOOH(g)的焓变△H=___________ kJ·mol-1。
②温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g) HCOOH(g) K=2。
HCOOH(g) K=2。
实验测得:v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=___________ k正。
③温度为T2℃时,k正=1.9k逆,则T2℃时平衡压强___________ (填“>”“<”或“=”)T1℃时平衡压强,理由是___________ 。
(3)工业上常用氨水吸收含碳燃料燃烧时产生的温室气体CO2,其产物之一是NH4HCO3。已知常温下碳酸的电离常数Ka1=4.4×10-7、Ka2=4.7×10-11,NH3·H2O的电离常数Kb=1.8×10-5,写出NH4HCO3水解反应的化学方程式:___________ ,选用上述数据计算该反应的平衡常数Kh=___________ (保留三位有效数字)。
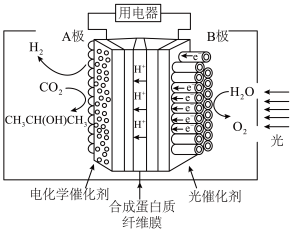
(4)某光电催化反应器如图所示,A极是Pt/CNT电极,B极是TiO2电极。写出A极由CO2制异丙醇的电极反应式:___________ 。
(1)科研人员借助太阳能用二氧化碳制备甲醇等燃料的催化转化是迄今为止最接近光合作用的方法,并且实现了二氧化碳的循环(如图所示),下列说法错误的是

A.图中能量转化形式有两种
B.使用催化剂可以提高单位时间内反应物的转化率
C.利用太阳能开发甲醇等液态燃料有利于环境保护
D.该工艺中的H2目前只能由电解水获得
(2)CO2加氢还可制备甲酸(HCOOH)。
①工业上利用甲酸的能量关系转换图如图所示:

反应CO2(g)+H2(g)
 HCOOH(g)的焓变△H=
HCOOH(g)的焓变△H=②温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g)
 HCOOH(g) K=2。
HCOOH(g) K=2。实验测得:v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=
③温度为T2℃时,k正=1.9k逆,则T2℃时平衡压强
(3)工业上常用氨水吸收含碳燃料燃烧时产生的温室气体CO2,其产物之一是NH4HCO3。已知常温下碳酸的电离常数Ka1=4.4×10-7、Ka2=4.7×10-11,NH3·H2O的电离常数Kb=1.8×10-5,写出NH4HCO3水解反应的化学方程式:
(4)某光电催化反应器如图所示,A极是Pt/CNT电极,B极是TiO2电极。写出A极由CO2制异丙醇的电极反应式:

您最近一年使用:0次



