名校
1 . 在催化剂作用下,以 和
和 为原料进行合成
为原料进行合成 的实验。保持压强一定,将起始
的实验。保持压强一定,将起始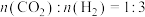 的混合气体通过装有催化剂的反应管,测得出口处
的混合气体通过装有催化剂的反应管,测得出口处 的转化率和
的转化率和 的选择性
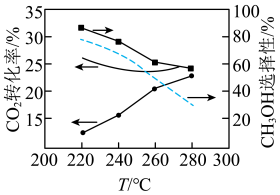
的选择性 与温度的关系如图所示(图中虚线表示平衡时
与温度的关系如图所示(图中虚线表示平衡时 的转化率或
的转化率或 的选择性)。已知反应管内发生的反应为:
的选择性)。已知反应管内发生的反应为:
反应1:

反应2:

下列说法正确的是
 和
和 为原料进行合成
为原料进行合成 的实验。保持压强一定,将起始
的实验。保持压强一定,将起始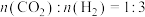 的混合气体通过装有催化剂的反应管,测得出口处
的混合气体通过装有催化剂的反应管,测得出口处 的转化率和
的转化率和 的选择性
的选择性 与温度的关系如图所示(图中虚线表示平衡时
与温度的关系如图所示(图中虚线表示平衡时 的转化率或
的转化率或 的选择性)。已知反应管内发生的反应为:
的选择性)。已知反应管内发生的反应为:反应1:


反应2:


下列说法正确的是

A.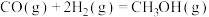 的 的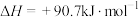 |
B.220℃~240℃时, 转化率随温度升高而升高,主要原因是温度升高,促进反应2平衡正向移动 转化率随温度升高而升高,主要原因是温度升高,促进反应2平衡正向移动 |
| C.220℃~280℃时,反应1的速率高于反应2的速率 |
D.为提高 的产率,应研发高温下催化活性更强的催化剂 的产率,应研发高温下催化活性更强的催化剂 |
您最近一年使用:0次
2023-10-21更新
|
267次组卷
|
2卷引用:江苏省海安高级中学2023-2024学年高二上学期10月月考化学试题
名校
2 . 氮氧化物污染指数是衡量空气质量的重要标准,氮氧化物的治理刻不容缓。回答下列问题:
(1)已知:①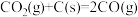 ΔH1
ΔH1
②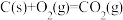 ΔH2
ΔH2
③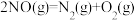 ΔH3
ΔH3
则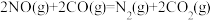 的ΔH=
的ΔH=___________ 。
(2)SCR(选择性催化还原)脱硝法是工业上消除氮氧化物的常用方法,反应原理为 ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
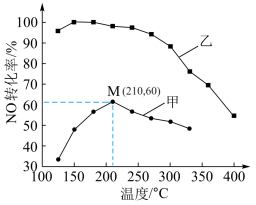
①工业上选择催化剂___________ (填“甲”或“乙”)。
②在催化剂甲作用下,图中M点NO的转化率___________ (填“是”或“不是”)该温度下的平衡转化率。高于210℃时,NO转化率降低的原因可能是___________ 。
(3)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的NO ,其工作原理如下图所示。
,其工作原理如下图所示。
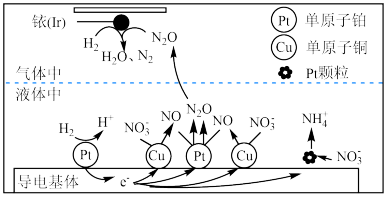
①导电基体Pt颗粒 上NO
上NO 发生的电极反应式为
发生的电极反应式为___________ 。
②在单原子铜、铂催化作用下,H2转化NO 为N2的过程可描述为
为N2的过程可描述为___________ 。
(1)已知:①
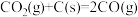 ΔH1
ΔH1②
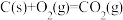 ΔH2
ΔH2③
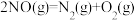 ΔH3
ΔH3则
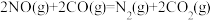 的ΔH=
的ΔH=(2)SCR(选择性催化还原)脱硝法是工业上消除氮氧化物的常用方法,反应原理为
 ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
①工业上选择催化剂
②在催化剂甲作用下,图中M点NO的转化率
(3)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的NO
 ,其工作原理如下图所示。
,其工作原理如下图所示。
①导电基体Pt颗粒
 上NO
上NO 发生的电极反应式为
发生的电极反应式为②在单原子铜、铂催化作用下,H2转化NO
 为N2的过程可描述为
为N2的过程可描述为
您最近一年使用:0次
名校
3 .  是空气的主要污染物之一,有效去除大气中的
是空气的主要污染物之一,有效去除大气中的 可以保护大气环境。含氮废水氨氮(以
可以保护大气环境。含氮废水氨氮(以 、
、 存在)和态硝氮(以
存在)和态硝氮(以 、
、 存在)引起水体富营养化,需经处理后才能排放。
存在)引起水体富营养化,需经处理后才能排放。
Ⅰ.空气中污染物NO可在催化剂作用下用 还原。
还原。
已知:
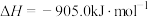


(1)有氧条件下, 与NO反应生成
与NO反应生成 ,相关热化学方程式为
,相关热化学方程式为

_____  。
。
Ⅱ.工业上含氮化合物污染物处理
(2)以 、
、 、熔融
、熔融 组成的燃料电池装置如图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,则该电池的正极反应式为
组成的燃料电池装置如图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,则该电池的正极反应式为_____ 。

(3)纳米铁粉可用于处理含氮废水。
①一定条件下,向 溶液中滴加碱性
溶液中滴加碱性 溶液,溶液中
溶液,溶液中 (B元素的化合价为+3)与
(B元素的化合价为+3)与 反应生成纳米铁粉、
反应生成纳米铁粉、 和
和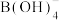 ,其离子方程式为
,其离子方程式为_____ 。
②铁粉与水中 反应的离子方程式为
反应的离子方程式为 。研究发现,若pH偏低将会导致
。研究发现,若pH偏低将会导致 的去除率下降,其原因是
的去除率下降,其原因是_____ 。
③相同条件下,纳米铁粉去除不同水样中 的速率有较大差异(如图所示),产生该差异的可能原因是
的速率有较大差异(如图所示),产生该差异的可能原因是_____ 。

(4)电极生物膜法也能有效去除水体中的 ,进行生物的反硝化反应。其可能反应机理如图所示。以必要的
,进行生物的反硝化反应。其可能反应机理如图所示。以必要的化学用语及文字 来描述此过程为_____ 。

 是空气的主要污染物之一,有效去除大气中的
是空气的主要污染物之一,有效去除大气中的 可以保护大气环境。含氮废水氨氮(以
可以保护大气环境。含氮废水氨氮(以 、
、 存在)和态硝氮(以
存在)和态硝氮(以 、
、 存在)引起水体富营养化,需经处理后才能排放。
存在)引起水体富营养化,需经处理后才能排放。Ⅰ.空气中污染物NO可在催化剂作用下用
 还原。
还原。已知:

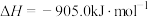


(1)有氧条件下,
 与NO反应生成
与NO反应生成 ,相关热化学方程式为
,相关热化学方程式为

 。
。Ⅱ.工业上含氮化合物污染物处理
(2)以
 、
、 、熔融
、熔融 组成的燃料电池装置如图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,则该电池的正极反应式为
组成的燃料电池装置如图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,则该电池的正极反应式为
(3)纳米铁粉可用于处理含氮废水。
①一定条件下,向
 溶液中滴加碱性
溶液中滴加碱性 溶液,溶液中
溶液,溶液中 (B元素的化合价为+3)与
(B元素的化合价为+3)与 反应生成纳米铁粉、
反应生成纳米铁粉、 和
和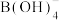 ,其离子方程式为
,其离子方程式为②铁粉与水中
 反应的离子方程式为
反应的离子方程式为 。研究发现,若pH偏低将会导致
。研究发现,若pH偏低将会导致 的去除率下降,其原因是
的去除率下降,其原因是③相同条件下,纳米铁粉去除不同水样中
 的速率有较大差异(如图所示),产生该差异的可能原因是
的速率有较大差异(如图所示),产生该差异的可能原因是
(4)电极生物膜法也能有效去除水体中的
 ,进行生物的反硝化反应。其可能反应机理如图所示。以必要的
,进行生物的反硝化反应。其可能反应机理如图所示。以必要的
您最近一年使用:0次
9-10高一下·福建福州·阶段练习
名校
解题方法
4 . 已知H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6 kJ·mol-1,则反应HCl(g)=  H2(g)+
H2(g)+ Cl2(g)的ΔH为
Cl2(g)的ΔH为
 H2(g)+
H2(g)+ Cl2(g)的ΔH为
Cl2(g)的ΔH为| A.+184.6 kJ·mol-1 | B.-92.3 kJ·mol-1 |
| C.-369.2 kJ·mol-1 | D.+92.3 kJ·mol-1 |
您最近一年使用:0次
2023-08-26更新
|
1492次组卷
|
86卷引用:2013届江苏省淮阴中学高一下学期期初考试化学试卷
(已下线)2013届江苏省淮阴中学高一下学期期初考试化学试卷江苏省东台市创新高级中学2018-2019学年高二下学期3月月考化学试题江苏省沭阳县2018-2019学年高二下学期期中调研测试化学试题江苏省盐城市实验高级中学(新洋高级中学)2020-2021学年高二下学期期中考试化学试题(已下线)09-10年福州格致中学高一下学期第三学段质量检查化学卷(已下线)2010年内蒙古赤峰市田家炳中学高二上学期期中考试化学试卷(已下线)2010-2011学年广东省中山市桂山中学高二下期中考试化学试卷(已下线)2010—2011学年吉林省长春外国语学校高一下学期期末考试化学试卷理(已下线)2011-2012年河南省长葛市第三实验高中高二上学期第一次月考化学试卷(已下线)2011-2012年广东省广雅中学高二上学期期中考试化学(理)试卷(已下线)2011-2012学年山东省济南外国语学校高二上学期期中考试化学(理)试卷(已下线)2011-2012学年福建泉州晋江市季延中学高二下学期期中化学试卷(已下线)2012-2013学年福建省晋江市季延中学高二下学期期中考试化学试卷2014-2015学年内蒙古巴市一中高二10月月考化学试卷2014-2015学年甘肃省民乐一中高二上学期第一次月考化学试卷2015-2016学年青海省高级中学高二上9月质检化学试卷2015-2016学年贵州省遵义航天中学高二上期末化学试卷2015-2016学年浙江省温州市瑞安市龙翔中学高二上第三次月考化学卷2016-2017学年北大附中河南分校高二上第一次月考化学卷2016-2017学年贵州省贵阳六中高二上10月月考化学卷(已下线)1.3.1 盖斯定律吉林省汪清县第六中学2017-2018学年高二9月月考化学试题陕西省西安市电子科技中学2017-2018学年高二上学期第一次月考化学试题广东省阳东广雅学校2017-2018学年高二9月月考化学试题河北省邢台第三中学2017-2018学年高二9月月考化学试题天津市杨柳青一中2017-2018第一学期高二第一次化学月考高中化学人教版 选修四 第一章 化学反应与能量 第三节 化学反应热的计算 化学反应热的计算第一课时(盖斯定律)安徽省滁州市(九校)2017-2018学年高二上学期期末考试化学试题四川省成都七中实验学校2018-2019学年高二上学期10月月考化学试题黑龙江省伊春市第二中学2018-2019学年高二(理)上学期期中考试化学试题陕西省黄陵中学2018-2019学年高二(普通班)上学期期末考试化学试题【区级联考】北京市西城区2018-2019学年高二上学期期末考试化学试题【校级联考】河北省鸡泽县第一中学2018-2019学年高一下学期3月月考化学试题步步为赢 高二化学暑假作业:作业七 化学反应与能量陕西省吴起高级中学2018-2019学年高一下学期第二次月考基础卷化学试题吉林省吉林地区普通高中友好学校联合体第三十一届2019-2020学年高二上学期期中考试化学试题河北省邢台市第八中学2019-2020学年高二上学期第一次月考化学试题甘肃省白银市会宁县第四中学2019-2020学年高二上学期期中考试化学试题内蒙古呼和浩特开来中学2019-2020学年高二上学期期中考试化学试题湖南省永州市双牌县第二中学2019-2020学年高二上学期期中考试化学试题(选考)安徽省黄山市“八校联盟”2019-2020学年高二上学期期中考试化学试题河北省保定市易县中学2019-2020学年高一(B部)下学期3月月考化学试题辽宁省大连市普兰店市第一中学2019-2020学年高二上学期期末考试化学试题湖南省长沙市雨花区2018-2019学年高二上学期期末考试化学(理)试题福建省永安市第三中学2020-2021学年高二10月月考化学(学考班)试题吉林省松原市乾安县第七中学2020-2021学年高二上学期第一次教学质量检测化学试题吉林省通化县综合高级中学2020-2021学年高二上学期期中考试化学试题甘肃省兰州市第四片区2020-2021学年高二上学期期中考试化学(理)试题宁夏长庆高级中学2020-2021学年高二上学期第一次月考化学试题福建省三明市三地三校2020-2021学年高二上学期期中联考化学试题北京市第四十三中学2020-2021学年高二上学期12月月考化学试题河南正阳县高级中学2020-2021学年高二上学期第三次素质检测化学试题陕西省咸阳百灵中学2020-2021学年高二上学期期中考试化学试题广东省东莞市二中2020-2021学年上学期高二10月考试化学试题海南省海南鑫源高级中学2019-2020学年高二上学期期末考试化学试题安徽省安庆市九一六学校2020-2021学年高二下学期开学考试化学试题山西省沁源县第一中学2020-2021学年高二下学期开学考试化学试题河北省石家庄市2019~2020学年高二上学期期末考试化学试题贵州省龙里县九八五实验学校2020-2021学年高二上学期1月月考化学试题辽宁省恒仁满族自治县第二高级中学2020-2021学年高二上学期期末考试化学试题(已下线)1.1.2 反应热的测量与计算(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)云南省玉溪第一中学2021-2022学年高二上学期第一次月考化学试题湖南省郴州市湘南中学2019-2020学年高二上学期期中考试化学试题(高考班)吉林省通化县综合高级中学2021-2022学年高二上学期期中考试化学试题安徽省宣城市六校2021-2022学年高二上学期期中联考化学试题河南省中原名校2021-2022学年高二上学期12月联考化学试题福建省三明第一中学2021-2022学年高二上学期第二次月考化学试题云南省曲靖市宣威市第七中学2021-2022学年高二下学期2月考试化学试题河南省温县第一高级中学2021-2022学年高二上学期1月月考化学试题福建省莆田华侨中学2021-2022学年高二上学期期中考试化学试题福建省莆田华侨中学2021-2022学年高二上学期期中考试化学试题北京市第七中学2022-2023学年高二上学期期中化学试题海南省白沙中学2021-2022学年高二上学期第一次月考化学试题广东省广州市从化区从化中学2022-2023学年高二上学期期中考试化学试题第3课时 反应焓变的计算【定心卷】1.1.3 热化学方程式随堂练习-人教版2023-2024学年选择性必修1江西省抚州市乐安县第二中学2023-2024学年高二上学期11月期中化学试题(已下线)BBWYhjhx1102陕西省西安市鄠邑区2023-2024学年高二上学期期中质量检测化学试题北京市大兴区兴华中学2023-2024学年高二上学期期中考试化学试题四川省泸州市泸县第五中学2023-2024学年高二上学期12月月考化学试题云南省宣威市第三中学2023-2024学年高二上学期第四次月考化学试题江西省金溪县第一中学、广昌一中、南丰一中2023-2024学年高二上学期第一次月考化学试题新疆乌鲁木齐市六校联考2023-2024学年高二上学期期末考试化学试题河北省石家庄康福外国语学校2023-2024学年高二上学期期中考试化学试题宁夏开元学校2023-2024学年高二学年下学期开学收心测试化学试题
名校
5 . 含氯化合物在生产生活中应用广泛。舍勒发现将软锰矿和浓盐酸混合加热可产生氯气,该方法仍是当今实验室制备氯气的主要方法之一,工业上以 为原料可制得
为原料可制得 、
、 、
、 、
、 和
和 等。在催化剂
等。在催化剂 作用下,通过氧气直接氧化氯化氢制备氯气。该反应为可逆反应,热化学方程式为
作用下,通过氧气直接氧化氯化氢制备氯气。该反应为可逆反应,热化学方程式为
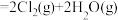
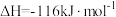 。下列化学反应表示正确的是
。下列化学反应表示正确的是
 为原料可制得
为原料可制得 、
、 、
、 、
、 和
和 等。在催化剂
等。在催化剂 作用下,通过氧气直接氧化氯化氢制备氯气。该反应为可逆反应,热化学方程式为
作用下,通过氧气直接氧化氯化氢制备氯气。该反应为可逆反应,热化学方程式为
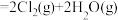
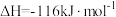 。下列化学反应表示正确的是
。下列化学反应表示正确的是A.实验室制氯气: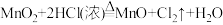 |
B.电解饱和 溶液的阴极反应: 溶液的阴极反应: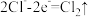 |
C.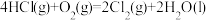 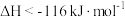 |
D.氯气溶于水具有漂白性: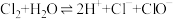 |
您最近一年使用:0次
名校
解题方法
6 . 页岩气中含有CH4、CO2、H2S等气体,是蕴藏于页岩层可供开采的天然气资源。页岩气的有效利用需要处理其中所含的CO2和H2S。
Ⅰ.CO2的处理:
(1)CO2和CH4重整可制合成气(主要成分为CO、H2)。
已知下列热化学反应方程式:C(s)+2H2(g)=CH4(g);ΔH=-74.5kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g);ΔH=-40.0kJ·mol-1
C(s)+H2O(g)=CO(g)+H2(g);ΔH=+132.0kJ·mol-1
反应CO2(g)+CH4(g)=2CO(g)+2H2(g)的ΔH=_______ kJ·mol-1。
(2)Ni催化CO2加H2形成CH4,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中CH4的百分含量及CO2的转化率随温度的变化如图2所示。

①260℃时生成主要产物所发生反应的化学方程式为_______ 。
②温度高于320℃,CO2的转化率下降的原因是_______ 。
Ⅱ.H2S的处理:Fe2O3可用作脱除H2S气体的脱硫剂。Fe2O3脱硫和Fe2O3再生的可能反应机理如图3所示。

(3)Fe2O3脱硫和Fe2O3再生过程可以描述为_______ 。
(4)再生时需控制通入O2的浓度和温度。400℃条件下,氧气浓度较大时,会出现脱硫剂再生时质量增大,且所得再生脱硫剂脱硫效果差,原因是_______ 。
Ⅰ.CO2的处理:
(1)CO2和CH4重整可制合成气(主要成分为CO、H2)。
已知下列热化学反应方程式:C(s)+2H2(g)=CH4(g);ΔH=-74.5kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g);ΔH=-40.0kJ·mol-1
C(s)+H2O(g)=CO(g)+H2(g);ΔH=+132.0kJ·mol-1
反应CO2(g)+CH4(g)=2CO(g)+2H2(g)的ΔH=
(2)Ni催化CO2加H2形成CH4,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中CH4的百分含量及CO2的转化率随温度的变化如图2所示。

①260℃时生成主要产物所发生反应的化学方程式为
②温度高于320℃,CO2的转化率下降的原因是
Ⅱ.H2S的处理:Fe2O3可用作脱除H2S气体的脱硫剂。Fe2O3脱硫和Fe2O3再生的可能反应机理如图3所示。

(3)Fe2O3脱硫和Fe2O3再生过程可以描述为
(4)再生时需控制通入O2的浓度和温度。400℃条件下,氧气浓度较大时,会出现脱硫剂再生时质量增大,且所得再生脱硫剂脱硫效果差,原因是
您最近一年使用:0次
7 . 二氧化碳加氢制甲烷过程中的主要反应为

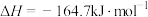

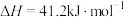
在密闭容器中, 、
、 时,
时, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如题图所示。
实际转化率随温度的变化如题图所示。 的选择性可表示为
的选择性可表示为 。下列说法正确的是
。下列说法正确的是

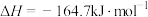

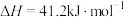
在密闭容器中,
 、
、 时,
时, 平衡转化率、在催化剂作用下反应相同时间所测得的
平衡转化率、在催化剂作用下反应相同时间所测得的 实际转化率随温度的变化如题图所示。
实际转化率随温度的变化如题图所示。 的选择性可表示为
的选择性可表示为 。下列说法正确的是
。下列说法正确的是
A.反应 的焓变 的焓变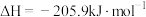 |
B. 的平衡选择性随着温度的升高而增加 的平衡选择性随着温度的升高而增加 |
| C.用该催化剂催化二氧化碳反应的最佳温度范围约为480~530℃ |
D.450℃时,提高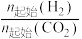 的值或增大压强,均能使 的值或增大压强,均能使 平衡转化率达到X点的值 平衡转化率达到X点的值 |
您最近一年使用:0次
2023-08-07更新
|
6844次组卷
|
13卷引用:2023年高考江苏卷化学真题
2023年高考江苏卷化学真题(已下线)选择题11-13江苏省扬州大学附属中学2023-2024学年高二上学期12月月考化学试题江苏省南通市海安市实验中学2023-2024学年高二上学期12月月考化学试题(已下线)江苏省南京师范大学附属中学2024届高三下学期三模考试化学试题(已下线)第28讲化化学平衡的移动及反应进行的方向河南省宜阳县第一高级中学2023-2024学年高二上学期能力达标测试化学试题北京市首都师范大学附属中学2023-2024学年高三上学期12月阶段练习化学试题安徽省淮南第二中学2024届高三上学期第四次段考化学试题(已下线)专题01 化学反应的热效应-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题03 化学平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)(已下线)FHgkyldyjhx08
真题
解题方法
8 . 氢元素及其化合物在自然界广泛存在且具有重要应用。 、
、 、
、 是氢元素的3种核素,基态H原子
是氢元素的3种核素,基态H原子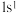 的核外电子排布,使得H既可以形成
的核外电子排布,使得H既可以形成 又可以形成
又可以形成 ,还能形成
,还能形成 、
、 、
、 、
、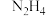 、
、 等重要化合物;水煤气法、电解水、光催化分解水都能获得
等重要化合物;水煤气法、电解水、光催化分解水都能获得 ,如水煤气法制氢反应中,
,如水煤气法制氢反应中, 与足量
与足量 反应生成
反应生成 和
和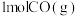 吸收131.3kJ的热量。
吸收131.3kJ的热量。 在金属冶炼、新能源开发、碳中和等方面具有重要应用,如
在金属冶炼、新能源开发、碳中和等方面具有重要应用,如 在催化剂作用下与
在催化剂作用下与 反应可得到
反应可得到 。我国科学家在氢气的制备和应用等方面都取得了重大成果。下列化学反应表示正确的是
。我国科学家在氢气的制备和应用等方面都取得了重大成果。下列化学反应表示正确的是
 、
、 、
、 是氢元素的3种核素,基态H原子
是氢元素的3种核素,基态H原子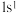 的核外电子排布,使得H既可以形成
的核外电子排布,使得H既可以形成 又可以形成
又可以形成 ,还能形成
,还能形成 、
、 、
、 、
、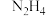 、
、 等重要化合物;水煤气法、电解水、光催化分解水都能获得
等重要化合物;水煤气法、电解水、光催化分解水都能获得 ,如水煤气法制氢反应中,
,如水煤气法制氢反应中, 与足量
与足量 反应生成
反应生成 和
和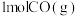 吸收131.3kJ的热量。
吸收131.3kJ的热量。 在金属冶炼、新能源开发、碳中和等方面具有重要应用,如
在金属冶炼、新能源开发、碳中和等方面具有重要应用,如 在催化剂作用下与
在催化剂作用下与 反应可得到
反应可得到 。我国科学家在氢气的制备和应用等方面都取得了重大成果。下列化学反应表示正确的是
。我国科学家在氢气的制备和应用等方面都取得了重大成果。下列化学反应表示正确的是A.水煤气法制氢: 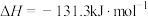 |
B. 催化加氢生成 催化加氢生成 的反应: 的反应: |
C.电解水制氢的阳极反应: |
D. 与水反应: 与水反应: |
您最近一年使用:0次
2023-08-07更新
|
4233次组卷
|
5卷引用:2023年高考江苏卷化学真题
2023年高考江苏卷化学真题(已下线)选择题6-10(已下线)考点1 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)专题01 化学反应的热效应-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)湖南省长沙市弘益高级中学2023-2024学年高三上学期第四次月考化学试卷
名校
9 .  的资源化利用和转化已成为当今科学研究的热点。
的资源化利用和转化已成为当今科学研究的热点。
(1)1902年,PaulSabatier首次报道了 的甲烷化。在一定的温度和压力条件下,将按一定比例混合的
的甲烷化。在一定的温度和压力条件下,将按一定比例混合的 和
和 通过装有金属Ni的反应器可得到
通过装有金属Ni的反应器可得到 。已知:
。已知: 和
和 的标准燃烧热分别为
的标准燃烧热分别为 、
、 。
。 甲烷化反应
甲烷化反应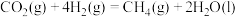 的
的
___________  。
。
(2)近年来,生物电催化技术运用微生物电解池实现了 的甲烷化,其工作原理如图所示。微生物电解池实现
的甲烷化,其工作原理如图所示。微生物电解池实现 甲烷化的阴极电极反应式为
甲烷化的阴极电极反应式为___________ 。

(3)325℃时,水在Mn粉表面产生的 可将
可将 转化成甲酸,同时生成MnO。直接加热
转化成甲酸,同时生成MnO。直接加热 与
与 难以生成甲酸,该条件下能较快生成甲酸的原因是
难以生成甲酸,该条件下能较快生成甲酸的原因是___________ 。
(4) 和环氧乙烷在MgO作催化剂的条件下合成碳酸乙烯酯。
和环氧乙烷在MgO作催化剂的条件下合成碳酸乙烯酯。
① 溶液中加入尿素
溶液中加入尿素 生成
生成 沉淀,同时有
沉淀,同时有 气体产生。该反应的离子方程式为
气体产生。该反应的离子方程式为___________ 。
② 与沉淀剂(尿素、氢氧化钠)反应生成沉淀,过滤后将沉淀焙烧得到MgO。与氢氧化钠作沉淀剂相比,用尿素作沉淀剂焙烧生成的MgO作催化剂效果更好,其原因是
与沉淀剂(尿素、氢氧化钠)反应生成沉淀,过滤后将沉淀焙烧得到MgO。与氢氧化钠作沉淀剂相比,用尿素作沉淀剂焙烧生成的MgO作催化剂效果更好,其原因是___________ 。
③MgO催化 合成碳酸乙烯酯(
合成碳酸乙烯酯( )可能的反应机理如图所示。根据元素电负性的变化规律,步骤I、II的过程可描述为
)可能的反应机理如图所示。根据元素电负性的变化规律,步骤I、II的过程可描述为___________ 。

 的资源化利用和转化已成为当今科学研究的热点。
的资源化利用和转化已成为当今科学研究的热点。(1)1902年,PaulSabatier首次报道了
 的甲烷化。在一定的温度和压力条件下,将按一定比例混合的
的甲烷化。在一定的温度和压力条件下,将按一定比例混合的 和
和 通过装有金属Ni的反应器可得到
通过装有金属Ni的反应器可得到 。已知:
。已知: 和
和 的标准燃烧热分别为
的标准燃烧热分别为 、
、 。
。 甲烷化反应
甲烷化反应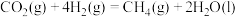 的
的
 。
。(2)近年来,生物电催化技术运用微生物电解池实现了
 的甲烷化,其工作原理如图所示。微生物电解池实现
的甲烷化,其工作原理如图所示。微生物电解池实现 甲烷化的阴极电极反应式为
甲烷化的阴极电极反应式为
(3)325℃时,水在Mn粉表面产生的
 可将
可将 转化成甲酸,同时生成MnO。直接加热
转化成甲酸,同时生成MnO。直接加热 与
与 难以生成甲酸,该条件下能较快生成甲酸的原因是
难以生成甲酸,该条件下能较快生成甲酸的原因是(4)
 和环氧乙烷在MgO作催化剂的条件下合成碳酸乙烯酯。
和环氧乙烷在MgO作催化剂的条件下合成碳酸乙烯酯。①
 溶液中加入尿素
溶液中加入尿素 生成
生成 沉淀,同时有
沉淀,同时有 气体产生。该反应的离子方程式为
气体产生。该反应的离子方程式为②
 与沉淀剂(尿素、氢氧化钠)反应生成沉淀,过滤后将沉淀焙烧得到MgO。与氢氧化钠作沉淀剂相比,用尿素作沉淀剂焙烧生成的MgO作催化剂效果更好,其原因是
与沉淀剂(尿素、氢氧化钠)反应生成沉淀,过滤后将沉淀焙烧得到MgO。与氢氧化钠作沉淀剂相比,用尿素作沉淀剂焙烧生成的MgO作催化剂效果更好,其原因是③MgO催化
 合成碳酸乙烯酯(
合成碳酸乙烯酯( )可能的反应机理如图所示。根据元素电负性的变化规律,步骤I、II的过程可描述为
)可能的反应机理如图所示。根据元素电负性的变化规律,步骤I、II的过程可描述为
您最近一年使用:0次
10 . 将TiO2、C、Cl2以一定的物质的量之比加入密闭容器中反应可生成TiCl4。可能发生的反应如下:
反应Ⅰ:TiO2(s)+2Cl2(g) TiCl4(g)+O2(g) ΔH1 =+172 kJ·mol−1
TiCl4(g)+O2(g) ΔH1 =+172 kJ·mol−1
反应Ⅱ:C(s)+O2(g)=CO2(g) ΔH2 =-393.5 kJ·mol−1
反应Ⅲ:2CO2(g)=2CO(g)+O2(g) ΔH3 = +564 kJ·mol−1
平衡时容器中气体的物质的量分数随温度变化如图所示(曲线a、b表示生成的CO2或CO)。下列说法不正确 的是

反应Ⅰ:TiO2(s)+2Cl2(g)
 TiCl4(g)+O2(g) ΔH1 =+172 kJ·mol−1
TiCl4(g)+O2(g) ΔH1 =+172 kJ·mol−1反应Ⅱ:C(s)+O2(g)=CO2(g) ΔH2 =-393.5 kJ·mol−1
反应Ⅲ:2CO2(g)=2CO(g)+O2(g) ΔH3 = +564 kJ·mol−1
平衡时容器中气体的物质的量分数随温度变化如图所示(曲线a、b表示生成的CO2或CO)。下列说法

| A.曲线a为CO |
| B.与仅加入TiO2、Cl2相比,碳的加入可提高TiCl4的产率 |
| C.TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) ΔH=-51 kJ·mol-1 |
| D.其他条件不变,增大压强,TiCl4的平衡产率增大 |
您最近一年使用:0次



