2024·陕西西安·二模
名校
解题方法
1 . 乙醇是燃料,也是重要的有机化工原料,二氧化碳加氢还原制乙醇已成为研究热点,相关的反应如下:
反应i:
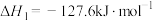
反应ii: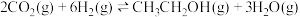
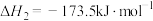
反应iii: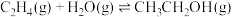
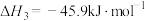
请回答下列问题:
(1)已知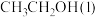 的燃烧热(
的燃烧热( )为
)为 ,表示
,表示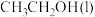 燃烧热的热化学方程式为
燃烧热的热化学方程式为________ 。
(2)在一定温度下,向2L恒容密闭容器中充入 和
和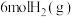 ,在某催化剂作用下发生上述反应,测得含碳元素物质占比[如
,在某催化剂作用下发生上述反应,测得含碳元素物质占比[如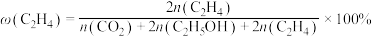 ]与时间的关系如图所示。
]与时间的关系如图所示。
①表示乙烯占比的曲线是________ (填“a”“b”或“c”)。
②若选择对反应i催化效果更好的催化剂,则A点可能移向________ (填“E”“E点上方”或“E点下方”)。
③已知C点、D点均为平衡点,则反应iii的平衡常数K=________ (保留小数点后一位)。
④设反应i和反应ii的化学平衡常数分别为 、
、 ,适当升温后,
,适当升温后,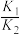
________ (填“增大”“减小”或“无法判断”),理由是________ 。
(3)近日,中国科学技术大学某课题组以Pd掺杂的 原子层为原型,在温和条件下,通过
原子层为原型,在温和条件下,通过 光还原合成乙酸,获得选择性近100%的好成绩。草酸钴是制备钻的氧化物的重要原料,二水合草酸钴(
光还原合成乙酸,获得选择性近100%的好成绩。草酸钴是制备钻的氧化物的重要原料,二水合草酸钴( )(
)(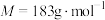 )在空气中受热时固体质量随温度变化的曲线如图所示。
)在空气中受热时固体质量随温度变化的曲线如图所示。________ ,CD段发生反应的化学方程式为________ 。
反应i:

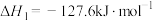
反应ii:
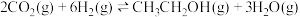
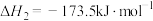
反应iii:
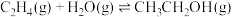
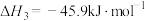
请回答下列问题:
(1)已知
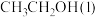 的燃烧热(
的燃烧热( )为
)为 ,表示
,表示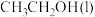 燃烧热的热化学方程式为
燃烧热的热化学方程式为(2)在一定温度下,向2L恒容密闭容器中充入
 和
和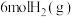 ,在某催化剂作用下发生上述反应,测得含碳元素物质占比[如
,在某催化剂作用下发生上述反应,测得含碳元素物质占比[如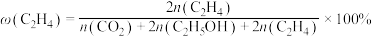 ]与时间的关系如图所示。
]与时间的关系如图所示。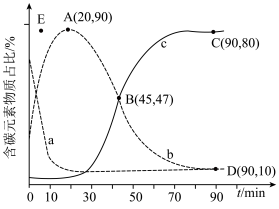
①表示乙烯占比的曲线是
②若选择对反应i催化效果更好的催化剂,则A点可能移向
③已知C点、D点均为平衡点,则反应iii的平衡常数K=
④设反应i和反应ii的化学平衡常数分别为
 、
、 ,适当升温后,
,适当升温后,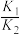
(3)近日,中国科学技术大学某课题组以Pd掺杂的
 原子层为原型,在温和条件下,通过
原子层为原型,在温和条件下,通过 光还原合成乙酸,获得选择性近100%的好成绩。草酸钴是制备钻的氧化物的重要原料,二水合草酸钴(
光还原合成乙酸,获得选择性近100%的好成绩。草酸钴是制备钻的氧化物的重要原料,二水合草酸钴( )(
)( )在空气中受热时固体质量随温度变化的曲线如图所示。
)在空气中受热时固体质量随温度变化的曲线如图所示。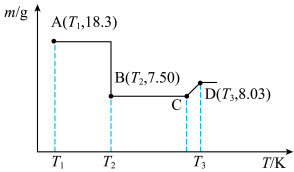
您最近一年使用:0次
名校
2 . 第三周期元素的单质及其化合物具有重要用途。在熔融状态下,可用金属钠制备金属钾;MgCl2可制备多种镁产品;铝—空气电池具有较高的比能量,在碱性电解液中总反应为4Al+3O2+4OH-+6H2O=4[Al(OH)4]-。高纯硅广泛用于信息技术领域,高温条件下,将粗硅转化为三氯硅烷(SiHCl3),再经氢气还原得到高纯硅。硫有多种单质,如斜方硫(燃烧热为297kJ·mol–1)、单斜硫等。H2S可除去废水中Hg2+等重金属离子,H2S水溶液在空气中会缓慢氧化生成S而变浑浊。SO2催化氧化是工业制硫酸的重要反应之一,常用V2O5作催化剂。下列化学反应表示正确的是
| A.斜方硫燃烧:S(s,斜方硫)+O2(g)=SO2(g) ∆H=297kJ·mol–1 |
| B.CuSO4溶液中加入小粒金属钠:2Na+Cu2+=Cu+2Na+ |
C.SiHCl3转化为高纯硅:SiHCl3+H2 Si+3HCl Si+3HCl |
| D.铝—空气电池放电时的负极反应:Al+4H2O-3e−=[Al(OH)4]-+4H+ |
您最近一年使用:0次
名校
3 . 乙苯被吸附在催化剂表面发生脱氢可生成苯乙烯、苯甲醛等,生成苯乙烯的相关反应如下。
反应1: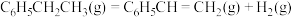
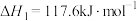
反应2:

反应3:
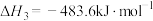
(1)反应4:
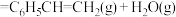

___________  。
。
(2)较低温度下,向乙苯脱氢的反应体系中加入少量 ,乙苯平衡转化率较高而苯乙烯的选择性较低,其原因可能是
,乙苯平衡转化率较高而苯乙烯的选择性较低,其原因可能是___________ 。
(3)向乙苯脱氢反应体系中加入 ,乙苯转化率与体系中
,乙苯转化率与体系中 分压强的关系如图1所示。随
分压强的关系如图1所示。随 的增加,乙苯转化率先增大后减小的可能原因为
的增加,乙苯转化率先增大后减小的可能原因为___________ 。 ,MgO催化剂表面进行
,MgO催化剂表面进行 的乙苯脱氢反应中,V(+5价)是反应的活性中心,转化过程如图2所示。
的乙苯脱氢反应中,V(+5价)是反应的活性中心,转化过程如图2所示。___________ ,反应一段时间后,催化剂活性有所下降,原因可能有反应过程产生的积碳覆盖在活性中心表面和___________ 。
②简述转化II的作用___________ 。
反应1:
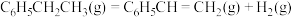
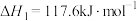
反应2:


反应3:

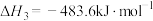
(1)反应4:

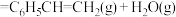

 。
。(2)较低温度下,向乙苯脱氢的反应体系中加入少量
 ,乙苯平衡转化率较高而苯乙烯的选择性较低,其原因可能是
,乙苯平衡转化率较高而苯乙烯的选择性较低,其原因可能是(3)向乙苯脱氢反应体系中加入
 ,乙苯转化率与体系中
,乙苯转化率与体系中 分压强的关系如图1所示。随
分压强的关系如图1所示。随 的增加,乙苯转化率先增大后减小的可能原因为
的增加,乙苯转化率先增大后减小的可能原因为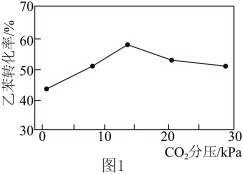
 ,MgO催化剂表面进行
,MgO催化剂表面进行 的乙苯脱氢反应中,V(+5价)是反应的活性中心,转化过程如图2所示。
的乙苯脱氢反应中,V(+5价)是反应的活性中心,转化过程如图2所示。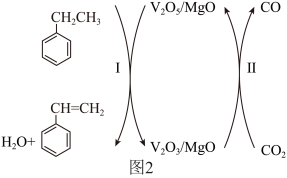
②简述转化II的作用
您最近一年使用:0次
4 . 已知: 与不足量的
与不足量的 反应时,生成S和
反应时,生成S和 。根据以下三个热化学方程式:
。根据以下三个热化学方程式:
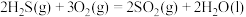
 ①
①

 ②
②

 ③
③
 、
、 、
、 三者大小关系正确的是
三者大小关系正确的是
 与不足量的
与不足量的 反应时,生成S和
反应时,生成S和 。根据以下三个热化学方程式:
。根据以下三个热化学方程式: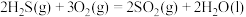
 ①
①
 ②
②
 ③
③ 、
、 、
、 三者大小关系正确的是
三者大小关系正确的是A.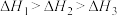 | B.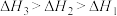 |
C.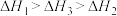 | D.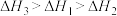 |
您最近一年使用:0次
2023-12-03更新
|
460次组卷
|
24卷引用:江苏省淮安市涟水县第一中学2020届高三上学期第二次月考化学试题
江苏省淮安市涟水县第一中学2020届高三上学期第二次月考化学试题江西省上饶县中学2017-2018学年高二上学期补考化学试题重庆市第三十中学2018-2019学年高二上学期第三次月考化学试题甘肃省古浪县第二中学2019-2020学年高二上学期基础知识竞赛化学试题福建省福州格致中学2021-2022学年高二上学期第一阶段测试化学试题(10月)山西省怀仁市2021-2022学年高二上学期期中化学试题广西钦州市2021-2022学年高二上学期期末考试化学试题第二节 反应热的计算 第2课时 反应热的计算甘肃省甘南藏族自治州合作第一中学2021-2022学年高二上学期期中考试化学试题(理)河南省濮阳市元龙高级中学2021-2022学年高二上学期期中考试化学试题贵州省部分学校2022-2023学年高二上学期10月联考化学试题贵州省“三新”改革联盟校联考2022-2023学年高二上学期期中考试化学试题陕西省咸阳市实验中学2021-2022学年高二上学期第三次月考化学试题湖南省怀化市雅礼实验学校2022-2023学年高二上学期第一次月考化学试题河南省洛阳市第一中学2022-2023学年高二上学期期末检测化学试题章末检测卷(一) 化学反应的热效应广东省广州市执信中学2023-2024学年高二上学期10月选考化学试题安徽省无为襄安中学2022-2023学年高二下学期开学考试化学试题山东省聊城市2023-2024学年高二上学期11月期中考试化学试题天津市南开区2023-2024学年高二上学期11月期中考试化学试题陕西省咸阳市兴平市西郊高级中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假作业01 化学反应的热效应-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)江西省抚州市资溪县第一中学2023-2024学年高二上学期11月期中化学试题安徽省淮北市第一中学2023-2024学年高二下学期寒假自主学习质量评估化学试题
名校
5 . 氮氧化物污染指数是衡量空气质量的重要标准,氮氧化物的治理刻不容缓。回答下列问题:
(1)已知:①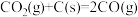 ΔH1
ΔH1
②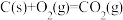 ΔH2
ΔH2
③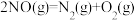 ΔH3
ΔH3
则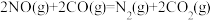 的ΔH=
的ΔH=___________ 。
(2)SCR(选择性催化还原)脱硝法是工业上消除氮氧化物的常用方法,反应原理为 ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
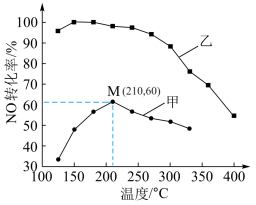
①工业上选择催化剂___________ (填“甲”或“乙”)。
②在催化剂甲作用下,图中M点NO的转化率___________ (填“是”或“不是”)该温度下的平衡转化率。高于210℃时,NO转化率降低的原因可能是___________ 。
(3)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的NO ,其工作原理如下图所示。
,其工作原理如下图所示。
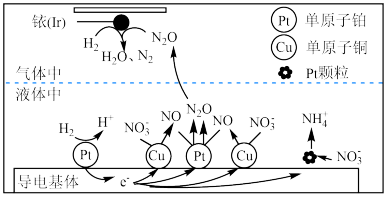
①导电基体Pt颗粒 上NO
上NO 发生的电极反应式为
发生的电极反应式为___________ 。
②在单原子铜、铂催化作用下,H2转化NO 为N2的过程可描述为
为N2的过程可描述为___________ 。
(1)已知:①
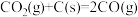 ΔH1
ΔH1②
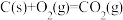 ΔH2
ΔH2③
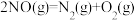 ΔH3
ΔH3则
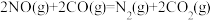 的ΔH=
的ΔH=(2)SCR(选择性催化还原)脱硝法是工业上消除氮氧化物的常用方法,反应原理为
 ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
①工业上选择催化剂
②在催化剂甲作用下,图中M点NO的转化率
(3)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的NO
 ,其工作原理如下图所示。
,其工作原理如下图所示。
①导电基体Pt颗粒
 上NO
上NO 发生的电极反应式为
发生的电极反应式为②在单原子铜、铂催化作用下,H2转化NO
 为N2的过程可描述为
为N2的过程可描述为
您最近一年使用:0次
9-10高一下·福建福州·阶段练习
名校
解题方法
6 . 已知H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6 kJ·mol-1,则反应HCl(g)=  H2(g)+
H2(g)+ Cl2(g)的ΔH为
Cl2(g)的ΔH为
 H2(g)+
H2(g)+ Cl2(g)的ΔH为
Cl2(g)的ΔH为| A.+184.6 kJ·mol-1 | B.-92.3 kJ·mol-1 |
| C.-369.2 kJ·mol-1 | D.+92.3 kJ·mol-1 |
您最近一年使用:0次
2023-08-26更新
|
1492次组卷
|
86卷引用:2013届江苏省淮阴中学高一下学期期初考试化学试卷
(已下线)2013届江苏省淮阴中学高一下学期期初考试化学试卷(已下线)09-10年福州格致中学高一下学期第三学段质量检查化学卷(已下线)2010年内蒙古赤峰市田家炳中学高二上学期期中考试化学试卷(已下线)2010-2011学年广东省中山市桂山中学高二下期中考试化学试卷(已下线)2010—2011学年吉林省长春外国语学校高一下学期期末考试化学试卷理(已下线)2011-2012年河南省长葛市第三实验高中高二上学期第一次月考化学试卷(已下线)2011-2012年广东省广雅中学高二上学期期中考试化学(理)试卷(已下线)2011-2012学年山东省济南外国语学校高二上学期期中考试化学(理)试卷(已下线)2011-2012学年福建泉州晋江市季延中学高二下学期期中化学试卷(已下线)2012-2013学年福建省晋江市季延中学高二下学期期中考试化学试卷2014-2015学年内蒙古巴市一中高二10月月考化学试卷2014-2015学年甘肃省民乐一中高二上学期第一次月考化学试卷2015-2016学年青海省高级中学高二上9月质检化学试卷2015-2016学年贵州省遵义航天中学高二上期末化学试卷2015-2016学年浙江省温州市瑞安市龙翔中学高二上第三次月考化学卷2016-2017学年北大附中河南分校高二上第一次月考化学卷2016-2017学年贵州省贵阳六中高二上10月月考化学卷(已下线)1.3.1 盖斯定律吉林省汪清县第六中学2017-2018学年高二9月月考化学试题陕西省西安市电子科技中学2017-2018学年高二上学期第一次月考化学试题广东省阳东广雅学校2017-2018学年高二9月月考化学试题河北省邢台第三中学2017-2018学年高二9月月考化学试题天津市杨柳青一中2017-2018第一学期高二第一次化学月考高中化学人教版 选修四 第一章 化学反应与能量 第三节 化学反应热的计算 化学反应热的计算第一课时(盖斯定律)安徽省滁州市(九校)2017-2018学年高二上学期期末考试化学试题四川省成都七中实验学校2018-2019学年高二上学期10月月考化学试题黑龙江省伊春市第二中学2018-2019学年高二(理)上学期期中考试化学试题陕西省黄陵中学2018-2019学年高二(普通班)上学期期末考试化学试题【区级联考】北京市西城区2018-2019学年高二上学期期末考试化学试题【校级联考】河北省鸡泽县第一中学2018-2019学年高一下学期3月月考化学试题江苏省东台市创新高级中学2018-2019学年高二下学期3月月考化学试题步步为赢 高二化学暑假作业:作业七 化学反应与能量江苏省沭阳县2018-2019学年高二下学期期中调研测试化学试题陕西省吴起高级中学2018-2019学年高一下学期第二次月考基础卷化学试题吉林省吉林地区普通高中友好学校联合体第三十一届2019-2020学年高二上学期期中考试化学试题河北省邢台市第八中学2019-2020学年高二上学期第一次月考化学试题甘肃省白银市会宁县第四中学2019-2020学年高二上学期期中考试化学试题内蒙古呼和浩特开来中学2019-2020学年高二上学期期中考试化学试题湖南省永州市双牌县第二中学2019-2020学年高二上学期期中考试化学试题(选考)安徽省黄山市“八校联盟”2019-2020学年高二上学期期中考试化学试题河北省保定市易县中学2019-2020学年高一(B部)下学期3月月考化学试题辽宁省大连市普兰店市第一中学2019-2020学年高二上学期期末考试化学试题湖南省长沙市雨花区2018-2019学年高二上学期期末考试化学(理)试题福建省永安市第三中学2020-2021学年高二10月月考化学(学考班)试题吉林省松原市乾安县第七中学2020-2021学年高二上学期第一次教学质量检测化学试题吉林省通化县综合高级中学2020-2021学年高二上学期期中考试化学试题甘肃省兰州市第四片区2020-2021学年高二上学期期中考试化学(理)试题宁夏长庆高级中学2020-2021学年高二上学期第一次月考化学试题福建省三明市三地三校2020-2021学年高二上学期期中联考化学试题北京市第四十三中学2020-2021学年高二上学期12月月考化学试题河南正阳县高级中学2020-2021学年高二上学期第三次素质检测化学试题陕西省咸阳百灵中学2020-2021学年高二上学期期中考试化学试题广东省东莞市二中2020-2021学年上学期高二10月考试化学试题海南省海南鑫源高级中学2019-2020学年高二上学期期末考试化学试题安徽省安庆市九一六学校2020-2021学年高二下学期开学考试化学试题山西省沁源县第一中学2020-2021学年高二下学期开学考试化学试题河北省石家庄市2019~2020学年高二上学期期末考试化学试题贵州省龙里县九八五实验学校2020-2021学年高二上学期1月月考化学试题辽宁省恒仁满族自治县第二高级中学2020-2021学年高二上学期期末考试化学试题(已下线)1.1.2 反应热的测量与计算(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)云南省玉溪第一中学2021-2022学年高二上学期第一次月考化学试题湖南省郴州市湘南中学2019-2020学年高二上学期期中考试化学试题(高考班)吉林省通化县综合高级中学2021-2022学年高二上学期期中考试化学试题安徽省宣城市六校2021-2022学年高二上学期期中联考化学试题河南省中原名校2021-2022学年高二上学期12月联考化学试题江苏省盐城市实验高级中学(新洋高级中学)2020-2021学年高二下学期期中考试化学试题福建省三明第一中学2021-2022学年高二上学期第二次月考化学试题云南省曲靖市宣威市第七中学2021-2022学年高二下学期2月考试化学试题河南省温县第一高级中学2021-2022学年高二上学期1月月考化学试题福建省莆田华侨中学2021-2022学年高二上学期期中考试化学试题福建省莆田华侨中学2021-2022学年高二上学期期中考试化学试题北京市第七中学2022-2023学年高二上学期期中化学试题海南省白沙中学2021-2022学年高二上学期第一次月考化学试题广东省广州市从化区从化中学2022-2023学年高二上学期期中考试化学试题第3课时 反应焓变的计算【定心卷】1.1.3 热化学方程式随堂练习-人教版2023-2024学年选择性必修1江西省抚州市乐安县第二中学2023-2024学年高二上学期11月期中化学试题(已下线)BBWYhjhx1102陕西省西安市鄠邑区2023-2024学年高二上学期期中质量检测化学试题北京市大兴区兴华中学2023-2024学年高二上学期期中考试化学试题四川省泸州市泸县第五中学2023-2024学年高二上学期12月月考化学试题云南省宣威市第三中学2023-2024学年高二上学期第四次月考化学试题江西省金溪县第一中学、广昌一中、南丰一中2023-2024学年高二上学期第一次月考化学试题新疆乌鲁木齐市六校联考2023-2024学年高二上学期期末考试化学试题河北省石家庄康福外国语学校2023-2024学年高二上学期期中考试化学试题宁夏开元学校2023-2024学年高二学年下学期开学收心测试化学试题
7 . CO2循环再利用制备甲烷、甲醇等有机燃料,变废为宝历来是化学重要的研究领域。为了减少CO2的排放,可用下列方法把CO2转化成燃料,试回答下列问题:
反应I:

反应II:
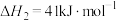
反应III:

(1)计算可知
___________  。
。
(2)某温度下,在固定容积为2.0L的密闭容器中充入0.8mol的CO2和2.4mol的H2,按反应I进行反应,测得CO2和CH3OH的物质的量随时间变化如图1:

①0~2min内,用CH3OH表示的反应速率为___________ ,该反应达到最大限度时H2的转化率为___________ ,此时CH3OH在平衡混合物中的体积分数为___________ 。
②下列措施可以提高该化学反应速率的是___________ (填选项序号)。
A.升高温度 B.容器体积不变,充入He
C.增大容器的体积 D.容器体积不变,充入更多的H2(g)
③下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.反应中CO2与CH3OH的物质的量之比为1:1
B.
C.混合气体的压强不随时间的变化而变化
D.混合气体的密度不再改变
(3)H2还原CO电化学法制备甲醇(见反应III)的工作原理如图2所示:电池工作过程中H+通过质子膜向___________ (填“左”或者“右”)移动,通入CO的一端发生的电极反应式为___________ 。

反应I:


反应II:

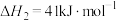
反应III:


(1)计算可知

 。
。(2)某温度下,在固定容积为2.0L的密闭容器中充入0.8mol的CO2和2.4mol的H2,按反应I进行反应,测得CO2和CH3OH的物质的量随时间变化如图1:

①0~2min内,用CH3OH表示的反应速率为
②下列措施可以提高该化学反应速率的是
A.升高温度 B.容器体积不变,充入He
C.增大容器的体积 D.容器体积不变,充入更多的H2(g)
③下列叙述中能说明上述反应达到平衡状态的是
A.反应中CO2与CH3OH的物质的量之比为1:1
B.

C.混合气体的压强不随时间的变化而变化
D.混合气体的密度不再改变
(3)H2还原CO电化学法制备甲醇(见反应III)的工作原理如图2所示:电池工作过程中H+通过质子膜向

您最近一年使用:0次
8 . γ-丁内酯为无色油状液体,高温时易分解,是重要的化工原料和医药中间体。工业利用1,4-丁二醇生产γ-丁内酯的主、副反应的化学方程式如下:
主反应: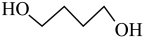 (g)
(g)
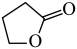 (g)( γ-丁内酯)+2H2(g) △H1=akJ•mol-1
(g)( γ-丁内酯)+2H2(g) △H1=akJ•mol-1
副反应: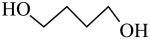 (g)
(g)
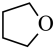 (g)(四氢呋喃)+H2O(g) △H2=bkJ•mol-1
(g)(四氢呋喃)+H2O(g) △H2=bkJ•mol-1
(1)反应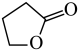 (g)+2H2(g)
(g)+2H2(g)
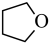 (g)+H2O(g)的△H=
(g)+H2O(g)的△H=_______ kJ•mol-1。
(2)由1,4-丁二醇合成γ-丁内酯的一种机理如图所示(“★”表示此微粒吸附在催化剂表面)
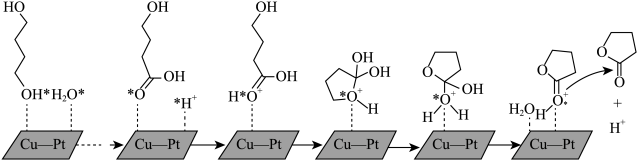
①步骤Ⅱ历程是质子化的过程,H+和氧原子间形成的作用力是______ 。
②H+在上述合成γ-丁内酯过程中的作用是_______ 。
③γ-丁内酯分子中σ键与π键数目之比为_______ 。
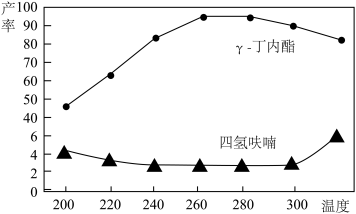
(3)将1,4-丁二醇与H2的混合气体以一定流速通过填充有催化剂的反应器,反应相同时间,测得γ-丁内酯和四氢呋喃的产率如图所示。
已知:1,4-丁二醇的沸点为228℃。
①当温度低于220℃,1,4-丁二醇的转化率较低,可能的原因是_______ 。
②当温度高于260℃,γ-丁内酯的产率下降,可能的原因是_______ 。
(4)铜基催化剂(Cu/Pt)能高效加快由1.4-丁二醇合成γ-丁内酯的合成速率,但因原料中的杂质或发生副反应生成的物质会使催化剂失活。
①1,4-丁二醇中混有少量的1,4-丁二硫醇(HSCH2CH2CH2CH2SH)。合成时加入ZnO可有效避免铜基催化剂失活,其原理用化学反应方程式表示为_______ 。
②将失活的铜基催化剂分为两份,第一份直接在氢气下进行还原,第二份先在空气中高温煅烧后再进行氢气还原,结果只有第二份催化剂活性恢复。说明催化剂失活的另外可能的原因是______ 。
(5)含有1,4-丁二醇的强酸性污水可用“铁碳微电池”法处理,过程中两电极分别产生的Fe2+和活性氢原子(H•)都具有较高的化学活性,在厌氧条件下将1,4-丁二醇转化为甲烷,假设两电极只生成Fe2+和H•,且全部参与该转化过程,写出该过程的离子方程式:_______ 。
主反应:
 (g)
(g)
 (g)( γ-丁内酯)+2H2(g) △H1=akJ•mol-1
(g)( γ-丁内酯)+2H2(g) △H1=akJ•mol-1副反应:
 (g)
(g)
 (g)(四氢呋喃)+H2O(g) △H2=bkJ•mol-1
(g)(四氢呋喃)+H2O(g) △H2=bkJ•mol-1(1)反应
 (g)+2H2(g)
(g)+2H2(g)
 (g)+H2O(g)的△H=
(g)+H2O(g)的△H=(2)由1,4-丁二醇合成γ-丁内酯的一种机理如图所示(“★”表示此微粒吸附在催化剂表面)

①步骤Ⅱ历程是质子化的过程,H+和氧原子间形成的作用力是
②H+在上述合成γ-丁内酯过程中的作用是
③γ-丁内酯分子中σ键与π键数目之比为
(3)将1,4-丁二醇与H2的混合气体以一定流速通过填充有催化剂的反应器,反应相同时间,测得γ-丁内酯和四氢呋喃的产率如图所示。
已知:1,4-丁二醇的沸点为228℃。
①当温度低于220℃,1,4-丁二醇的转化率较低,可能的原因是
②当温度高于260℃,γ-丁内酯的产率下降,可能的原因是

(4)铜基催化剂(Cu/Pt)能高效加快由1.4-丁二醇合成γ-丁内酯的合成速率,但因原料中的杂质或发生副反应生成的物质会使催化剂失活。
①1,4-丁二醇中混有少量的1,4-丁二硫醇(HSCH2CH2CH2CH2SH)。合成时加入ZnO可有效避免铜基催化剂失活,其原理用化学反应方程式表示为
②将失活的铜基催化剂分为两份,第一份直接在氢气下进行还原,第二份先在空气中高温煅烧后再进行氢气还原,结果只有第二份催化剂活性恢复。说明催化剂失活的另外可能的原因是
(5)含有1,4-丁二醇的强酸性污水可用“铁碳微电池”法处理,过程中两电极分别产生的Fe2+和活性氢原子(H•)都具有较高的化学活性,在厌氧条件下将1,4-丁二醇转化为甲烷,假设两电极只生成Fe2+和H•,且全部参与该转化过程,写出该过程的离子方程式:
您最近一年使用:0次
解题方法
9 . 通过反应Ⅰ:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g),可将有机氯化工业的副产品HCl转化为Cl2。在0.2MPa、反应物起始物质的量比 =2条件下,不同温度时HCl转化率如图所示(图中虚线表示相同条件下HCl的平衡转化率随温度的变化)。向反应体系中加入CuCl2,能加快反应速率。
=2条件下,不同温度时HCl转化率如图所示(图中虚线表示相同条件下HCl的平衡转化率随温度的变化)。向反应体系中加入CuCl2,能加快反应速率。
反应Ⅱ:2CuCl2(s)+O2(g)=2CuO(s)+2Cl2(g) △H=125.6kJ•mol-1
反应Ⅲ:CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) △H=-120.0kJ•mol-1

下列说法正确的是
 =2条件下,不同温度时HCl转化率如图所示(图中虚线表示相同条件下HCl的平衡转化率随温度的变化)。向反应体系中加入CuCl2,能加快反应速率。
=2条件下,不同温度时HCl转化率如图所示(图中虚线表示相同条件下HCl的平衡转化率随温度的变化)。向反应体系中加入CuCl2,能加快反应速率。反应Ⅱ:2CuCl2(s)+O2(g)=2CuO(s)+2Cl2(g) △H=125.6kJ•mol-1
反应Ⅲ:CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) △H=-120.0kJ•mol-1

下列说法正确的是
| A.反应Ⅰ的△H=5.6kJ•mol-1 |
| B.230至300℃时,HCl转化率降低是因为温度升高,平衡向逆反应方向移动 |
| C.保持其他条件不变,400℃时,使用CuCl2,能使HCl转化率从X点的值升至Y点的值 |
D.在0.2MPa、400℃条件下,若起始 <2条件下,HCl的转化率可能达到Y点的值 <2条件下,HCl的转化率可能达到Y点的值 |
您最近一年使用:0次
名校
10 . 含氮化合物( 、
、 、
、 等)是环境污染物,可用以下方法消除其污染。
等)是环境污染物,可用以下方法消除其污染。
Ⅰ.苯酚( )是一种广泛使用、易氧化的化工产品。一种在
)是一种广泛使用、易氧化的化工产品。一种在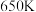 下用
下用 废气催化氧化苯制备苯酚的新方法为:
废气催化氧化苯制备苯酚的新方法为: 。
。
(1)已知



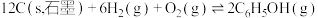
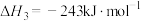
则

___________ 。
Ⅱ.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的 可高效转化酸性溶液中的硝态氮(
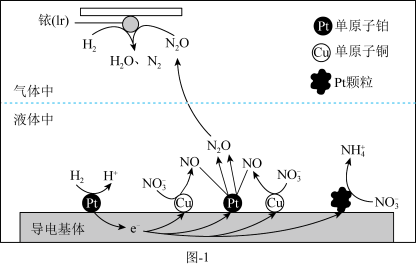
可高效转化酸性溶液中的硝态氮( ),以达到消除污染的目的,其工作原理如图-1所示。
),以达到消除污染的目的,其工作原理如图-1所示。
(2) 被
被 还原为
还原为 的过程可描述为:液体中,
的过程可描述为:液体中, 在导电基体的单原子铂上失去电子生成
在导电基体的单原子铂上失去电子生成 ,电子进入导电基体中进行传导,
,电子进入导电基体中进行传导,___________ 。
(3)若导电基体上的Pt颗粒增多,造成的后果是___________ 。
(4)单原子铂催化剂相比于Pt颗粒催化剂,优点有___________ 。
Ⅲ.三维电极法:它是在传统的电解槽两电极之间填充粒状或碎屑状材料,填充的粒子电极表面能带电,成为新的一极(第三极)。如图2为用三维电极法处理氨氮废水的原理图,石墨板作为阴、阳极,自制活性炭为填充材料,电解一定浓度的 、
、 与NaCl的酸性混合溶液来进行模拟。
与NaCl的酸性混合溶液来进行模拟。

(5)该装置可以生成大量氧化性更强的 ,
, 去除
去除 的离子方程式为
的离子方程式为___________ 。
(6)相比于传统的二维电极反应系统,三维电极的优点有___________ 。
 、
、 、
、 等)是环境污染物,可用以下方法消除其污染。
等)是环境污染物,可用以下方法消除其污染。Ⅰ.苯酚(
 )是一种广泛使用、易氧化的化工产品。一种在
)是一种广泛使用、易氧化的化工产品。一种在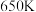 下用
下用 废气催化氧化苯制备苯酚的新方法为:
废气催化氧化苯制备苯酚的新方法为: 。
。(1)已知




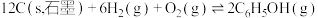
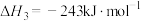
则


Ⅱ.在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的
 可高效转化酸性溶液中的硝态氮(
可高效转化酸性溶液中的硝态氮( ),以达到消除污染的目的,其工作原理如图-1所示。
),以达到消除污染的目的,其工作原理如图-1所示。
(2)
 被
被 还原为
还原为 的过程可描述为:液体中,
的过程可描述为:液体中, 在导电基体的单原子铂上失去电子生成
在导电基体的单原子铂上失去电子生成 ,电子进入导电基体中进行传导,
,电子进入导电基体中进行传导,(3)若导电基体上的Pt颗粒增多,造成的后果是
(4)单原子铂催化剂相比于Pt颗粒催化剂,优点有
Ⅲ.三维电极法:它是在传统的电解槽两电极之间填充粒状或碎屑状材料,填充的粒子电极表面能带电,成为新的一极(第三极)。如图2为用三维电极法处理氨氮废水的原理图,石墨板作为阴、阳极,自制活性炭为填充材料,电解一定浓度的
 、
、 与NaCl的酸性混合溶液来进行模拟。
与NaCl的酸性混合溶液来进行模拟。
(5)该装置可以生成大量氧化性更强的
 ,
, 去除
去除 的离子方程式为
的离子方程式为(6)相比于传统的二维电极反应系统,三维电极的优点有
您最近一年使用:0次



