名校
解题方法
1 . 有效去除大气中的NOx和水体中的氮,并且转化为可利用的资源是重要课题。
(1)在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下: (aq)+2O2(g)=
(aq)+2O2(g)= (aq)+2H+(aq)+H2O(l) ΔH=
(aq)+2H+(aq)+H2O(l) ΔH=_______ kJ·mol-1
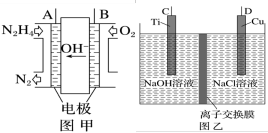
(2)近年来,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中的c(OH-)制备纳米Cu2O备受关注,其模拟装置如图甲、乙。_______ (请填“C”或“D”)极相连。
②该电解池的阳极反应式为_______ 。
③该电解池(图乙)中离子交换膜为_______ (请填“阴”或“阳”)离子交换膜。
④理论上,每生产144g纳米Cu2O,需要消耗肼(N2H4)_______ mol。
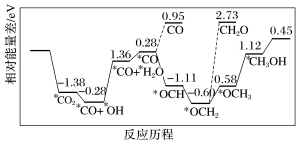
(3)纳米颗粒在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示。_______ 。
②上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中_______ (填字母)的活化能。
A.*CO+*OH→*CO+*H2O
B.*CO→*OCH
C.*OCH2→*OCH3
D.*OCH3→*CH3OH
(4)磷酸铵镁(MgNH4PO4)沉淀法可去除水体中的氨氮( 和NH3)。实验室中模拟氨氮处理:1 L的模拟氨氮废水(主要含
和NH3)。实验室中模拟氨氮处理:1 L的模拟氨氮废水(主要含 ),置于搅拌器上,设定反应温度为25 ℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30 min后,取液面下2 cm处清液测定氨氮质量浓度。已知:常温下,磷酸铵镁(MgNH4PO4)微溶于水;H3PO4的Ka1=6.9×10-3, Ka2=6.2×10-8 ,Ka3=4.8×10-13。
),置于搅拌器上,设定反应温度为25 ℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30 min后,取液面下2 cm处清液测定氨氮质量浓度。已知:常温下,磷酸铵镁(MgNH4PO4)微溶于水;H3PO4的Ka1=6.9×10-3, Ka2=6.2×10-8 ,Ka3=4.8×10-13。_______ 。
②当反应pH为9.0时,该沉淀法对氨氮的去除率达到最高,当pH继续增至10.0时,氨氮的去除率下降,原因是_______ 。
(1)在微生物作用的条件下,
 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下: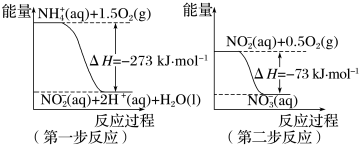
 (aq)+2O2(g)=
(aq)+2O2(g)= (aq)+2H+(aq)+H2O(l) ΔH=
(aq)+2H+(aq)+H2O(l) ΔH=(2)近年来,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中的c(OH-)制备纳米Cu2O备受关注,其模拟装置如图甲、乙。
②该电解池的阳极反应式为
③该电解池(图乙)中离子交换膜为
④理论上,每生产144g纳米Cu2O,需要消耗肼(N2H4)
(3)纳米颗粒在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示。
②上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中
A.*CO+*OH→*CO+*H2O
B.*CO→*OCH
C.*OCH2→*OCH3
D.*OCH3→*CH3OH
(4)磷酸铵镁(MgNH4PO4)沉淀法可去除水体中的氨氮(
 和NH3)。实验室中模拟氨氮处理:1 L的模拟氨氮废水(主要含
和NH3)。实验室中模拟氨氮处理:1 L的模拟氨氮废水(主要含 ),置于搅拌器上,设定反应温度为25 ℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30 min后,取液面下2 cm处清液测定氨氮质量浓度。已知:常温下,磷酸铵镁(MgNH4PO4)微溶于水;H3PO4的Ka1=6.9×10-3, Ka2=6.2×10-8 ,Ka3=4.8×10-13。
),置于搅拌器上,设定反应温度为25 ℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30 min后,取液面下2 cm处清液测定氨氮质量浓度。已知:常温下,磷酸铵镁(MgNH4PO4)微溶于水;H3PO4的Ka1=6.9×10-3, Ka2=6.2×10-8 ,Ka3=4.8×10-13。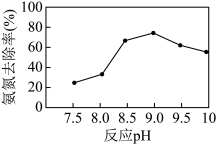
②当反应pH为9.0时,该沉淀法对氨氮的去除率达到最高,当pH继续增至10.0时,氨氮的去除率下降,原因是
您最近一年使用:0次
2 . 研发二氧化碳的利用技术具有重要意义。
(1) 还原
还原 是实现“双碳”经济的有效途径之一,相关反应有:
是实现“双碳”经济的有效途径之一,相关反应有:
反应Ⅰ:


反应Ⅱ:


反应Ⅲ:


则反应 的
的
___________ 。
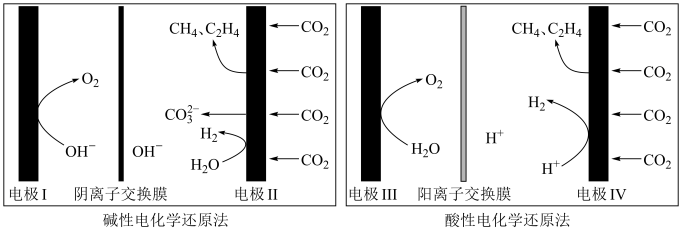
(2)利用电解法在碱性或酸性条件下将 还原为
还原为 和
和 的原理如下图所示:
的原理如下图所示:
已知:选择性(S)和法拉第效率(FE)的定义(X代表 或
或 )如下:
)如下:
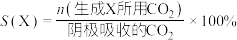
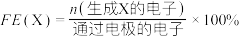
①写出碱性条件下 生成
生成 的电极反应式:
的电极反应式:___________ 。
②实验测得,碱性条件生成 、
、 总的选择性小于酸性条件,原因是
总的选择性小于酸性条件,原因是___________ 。
③实验测得,酸性条件生成 、
、 总的法拉第效率小于碱性条件,原因是
总的法拉第效率小于碱性条件,原因是___________ 。
④碱性条件下反应一段时间,实验测得 、
、 的选择性及
的选择性及 的法拉第效率如下表所示。则
的法拉第效率如下表所示。则 的法拉第效率
的法拉第效率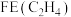 为
为___________ 。
(1)
 还原
还原 是实现“双碳”经济的有效途径之一,相关反应有:
是实现“双碳”经济的有效途径之一,相关反应有:反应Ⅰ:



反应Ⅱ:



反应Ⅲ:



则反应
 的
的
(2)利用电解法在碱性或酸性条件下将
 还原为
还原为 和
和 的原理如下图所示:
的原理如下图所示:
已知:选择性(S)和法拉第效率(FE)的定义(X代表
 或
或 )如下:
)如下: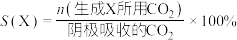
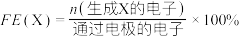
①写出碱性条件下
 生成
生成 的电极反应式:
的电极反应式:②实验测得,碱性条件生成
 、
、 总的选择性小于酸性条件,原因是
总的选择性小于酸性条件,原因是③实验测得,酸性条件生成
 、
、 总的法拉第效率小于碱性条件,原因是
总的法拉第效率小于碱性条件,原因是④碱性条件下反应一段时间,实验测得
 、
、 的选择性及
的选择性及 的法拉第效率如下表所示。则
的法拉第效率如下表所示。则 的法拉第效率
的法拉第效率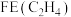 为
为 |  | |
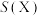 | 2% | 8% |
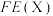 | 12.5% |
您最近一年使用:0次
2024-02-24更新
|
252次组卷
|
2卷引用:江苏省 徐州市第七中学2023-2024学年高三上学期12月月考化学试题
3 . 氢能是一种绿色能源,也是重要的还原剂。目前有多种方法可以制氢并储氢。催化加氢反应可以用于重要化工原料的转化。
Ⅰ.电解法制氢
(1)甲醇电解可制得 ,其原理如图所示。
,其原理如图所示。___________ 。
Ⅱ.催化重整法制氢
(2)已知:反应1:

反应2:
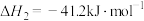
则反应3: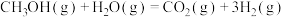
 =
=______ 
(3)以 催化剂进行甲醇重整制氢时,固定其它条件不变,改变水、甲醇的物质的量比,甲醇平衡转化率及
催化剂进行甲醇重整制氢时,固定其它条件不变,改变水、甲醇的物质的量比,甲醇平衡转化率及 选择性的影响如图所示。
选择性的影响如图所示。 的选择性=
的选择性=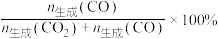
当水、甲醇比大于0.8时, 选择性下降的原因是
选择性下降的原因是___________ 。
(4)铜基催化剂(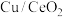 )能高效进行甲醇重整制氢,但因原料中的杂质或发生副反应生成的物质会使催化剂失活。甲醇中混有少量的甲硫醇(
)能高效进行甲醇重整制氢,但因原料中的杂质或发生副反应生成的物质会使催化剂失活。甲醇中混有少量的甲硫醇(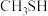 ),重整制氢时加入
),重整制氢时加入 可有效避免铜基催化剂失活且平衡产率略有上升,其原理用化学反应方程式表示为
可有效避免铜基催化剂失活且平衡产率略有上升,其原理用化学反应方程式表示为___________ 。
Ⅲ.催化加氢还原反应的应用 单原子位点对4-硝基苯乙烯有较好吸附效果。
单原子位点对4-硝基苯乙烯有较好吸附效果。
①使用双单原子催化剂可以大大提高4-乙烯基苯胺的产率,原因是_______ 。
Ⅰ.电解法制氢
(1)甲醇电解可制得
 ,其原理如图所示。
,其原理如图所示。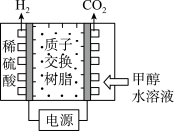
Ⅱ.催化重整法制氢
(2)已知:反应1:


反应2:

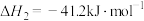
则反应3:
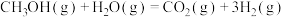
 =
=
(3)以
 催化剂进行甲醇重整制氢时,固定其它条件不变,改变水、甲醇的物质的量比,甲醇平衡转化率及
催化剂进行甲醇重整制氢时,固定其它条件不变,改变水、甲醇的物质的量比,甲醇平衡转化率及 选择性的影响如图所示。
选择性的影响如图所示。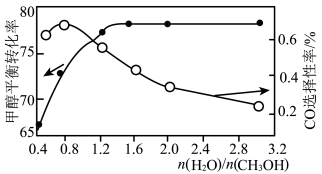
 的选择性=
的选择性=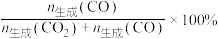
当水、甲醇比大于0.8时,
 选择性下降的原因是
选择性下降的原因是(4)铜基催化剂(
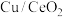 )能高效进行甲醇重整制氢,但因原料中的杂质或发生副反应生成的物质会使催化剂失活。甲醇中混有少量的甲硫醇(
)能高效进行甲醇重整制氢,但因原料中的杂质或发生副反应生成的物质会使催化剂失活。甲醇中混有少量的甲硫醇(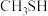 ),重整制氢时加入
),重整制氢时加入 可有效避免铜基催化剂失活且平衡产率略有上升,其原理用化学反应方程式表示为
可有效避免铜基催化剂失活且平衡产率略有上升,其原理用化学反应方程式表示为Ⅲ.催化加氢还原反应的应用
 能将
能将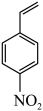 在特定条件下转化为4-乙烯基苯胺
在特定条件下转化为4-乙烯基苯胺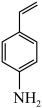 。两种不同催化剂将4-硝基苯乙烯还原加氢的过程如图所示。
。两种不同催化剂将4-硝基苯乙烯还原加氢的过程如图所示。

 单原子位点对4-硝基苯乙烯有较好吸附效果。
单原子位点对4-硝基苯乙烯有较好吸附效果。①使用双单原子催化剂可以大大提高4-乙烯基苯胺的产率,原因是
②请描述4-硝基苯乙烯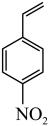 在单原子催化剂下与
在单原子催化剂下与 发生反应的过程
发生反应的过程
您最近一年使用:0次
解题方法
4 . 工业废水和废渣中会产生含硫(-2价)污染物,需经处理后排放。
Ⅰ.含硫废水(硫元素的主要存在形式为 ),需要回收处理并加以利用。
),需要回收处理并加以利用。
(1)用 、
、 处理含硫废水有关反应如下:
处理含硫废水有关反应如下:
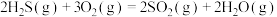





则 热分解反应
热分解反应 的△H=
的△H=_______ (用含 、
、 、
、 的式子表示)。
的式子表示)。
(2)用 处理含硫废水,硫元素易被氧化为S或
处理含硫废水,硫元素易被氧化为S或 。已知:
。已知: 溶液中含硫微粒的物质的量分数随pH变化情况如图所示。
溶液中含硫微粒的物质的量分数随pH变化情况如图所示。
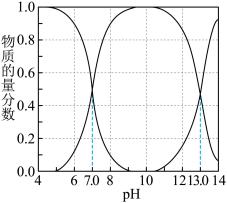
①向含硫废水中加入稀 调节溶液的pH为6,废水中
调节溶液的pH为6,废水中
_______ 。
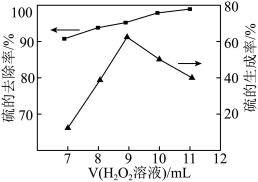
②向含硫废水中加入 溶液,其他条件一定,测得硫(-2价)的去除率、硫(单质)的生成率与加入
溶液,其他条件一定,测得硫(-2价)的去除率、硫(单质)的生成率与加入 溶液体积的关系如图所示。当加入
溶液体积的关系如图所示。当加入 溶液体积大于9mL时,硫的生成率随
溶液体积大于9mL时,硫的生成率随 溶液加入而降低,可能的原因是
溶液加入而降低,可能的原因是_______ 。
(3)催化氧化法。 可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如图所示。
可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如图所示。
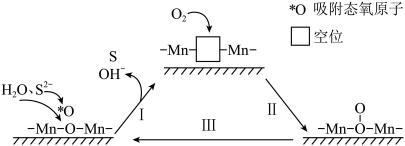
①该反应过程Ⅰ、Ⅱ可描述为_______ 。
②催化剂使用一段时间后催化效率会下降,处理的方法是用氯仿( )浸取催化剂,再将催化剂干燥即可,催化剂使用一段时间后催化效率降低的原因是
)浸取催化剂,再将催化剂干燥即可,催化剂使用一段时间后催化效率降低的原因是_______ 。
Ⅱ.含硫废渣(硫元素的主要存在形式为 ),可以回收处理并加以利用。
),可以回收处理并加以利用。
(4)沉积物-微生物燃料电池可以将沉积物中的化学能直接转化为电能,同时加速沉积物中污染物的去除,燃料电池处理含硫废水的工作原理如图所示。
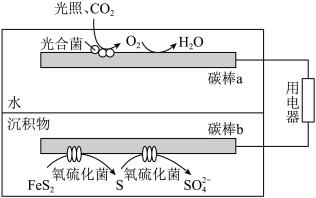
①碳棒b处S生成 的电极反应式为
的电极反应式为_______ 。
②工作一段时间后,电池效率降低的可能原因为_______ 。
Ⅰ.含硫废水(硫元素的主要存在形式为
 ),需要回收处理并加以利用。
),需要回收处理并加以利用。(1)用
 、
、 处理含硫废水有关反应如下:
处理含硫废水有关反应如下: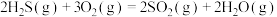





则
 热分解反应
热分解反应 的△H=
的△H= 、
、 、
、 的式子表示)。
的式子表示)。(2)用
 处理含硫废水,硫元素易被氧化为S或
处理含硫废水,硫元素易被氧化为S或 。已知:
。已知: 溶液中含硫微粒的物质的量分数随pH变化情况如图所示。
溶液中含硫微粒的物质的量分数随pH变化情况如图所示。
①向含硫废水中加入稀
 调节溶液的pH为6,废水中
调节溶液的pH为6,废水中
②向含硫废水中加入
 溶液,其他条件一定,测得硫(-2价)的去除率、硫(单质)的生成率与加入
溶液,其他条件一定,测得硫(-2价)的去除率、硫(单质)的生成率与加入 溶液体积的关系如图所示。当加入
溶液体积的关系如图所示。当加入 溶液体积大于9mL时,硫的生成率随
溶液体积大于9mL时,硫的生成率随 溶液加入而降低,可能的原因是
溶液加入而降低,可能的原因是
(3)催化氧化法。
 可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如图所示。
可用作空气氧化含硫(-2价)废水的催化剂。碱性条件下,催化氧化废水的机理如图所示。
①该反应过程Ⅰ、Ⅱ可描述为
②催化剂使用一段时间后催化效率会下降,处理的方法是用氯仿(
 )浸取催化剂,再将催化剂干燥即可,催化剂使用一段时间后催化效率降低的原因是
)浸取催化剂,再将催化剂干燥即可,催化剂使用一段时间后催化效率降低的原因是Ⅱ.含硫废渣(硫元素的主要存在形式为
 ),可以回收处理并加以利用。
),可以回收处理并加以利用。(4)沉积物-微生物燃料电池可以将沉积物中的化学能直接转化为电能,同时加速沉积物中污染物的去除,燃料电池处理含硫废水的工作原理如图所示。

①碳棒b处S生成
 的电极反应式为
的电极反应式为②工作一段时间后,电池效率降低的可能原因为
您最近一年使用:0次
解题方法
5 . 回收利用含硫化合物有利于节约资源、保护环境。
(1)一种由含 的烟气回收硫磺的工艺为:将一部分含
的烟气回收硫磺的工艺为:将一部分含 的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到单质硫
的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到单质硫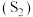 ,该工艺中涉及反应为:
,该工艺中涉及反应为:
反应1: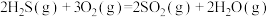

反应2: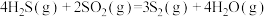
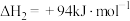
反应3: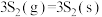
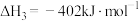
①反应
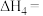
________ 。
②如果上述反应均能完全进行,为提高硫磺的产率,该工艺中需要控制反应1和反应2的烟气的体积比是________ 。
(2)一种以 为原料,循环吸收烟气中
为原料,循环吸收烟气中 的物质转化关系如下,写出转化中由
的物质转化关系如下,写出转化中由 制
制 同时生成硫酸铵的化学反应方程式:
同时生成硫酸铵的化学反应方程式:________ 。

(3)一种以 为催化剂载体、
为催化剂载体、 为催化剂的
为催化剂的 还原烟气中
还原烟气中 制S的反应机理如题图1和题图2所示:
制S的反应机理如题图1和题图2所示:
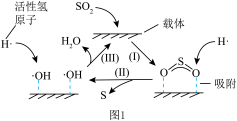
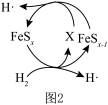
①图1中所示转化可以描述为 分解为活性氢原子,
分解为活性氢原子,________ 。
②图2中X的电子式为________ 。
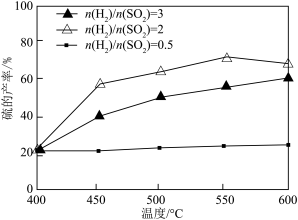
③其他条件一定,改变起始时 与
与 的比例,反应相同时间,测得S的产率与温度和
的比例,反应相同时间,测得S的产率与温度和 比值的关系如题图所示,500℃时,
比值的关系如题图所示,500℃时, 比值为3时硫的产率小于比值为2时的原因是
比值为3时硫的产率小于比值为2时的原因是________ 。
(1)一种由含
 的烟气回收硫磺的工艺为:将一部分含
的烟气回收硫磺的工艺为:将一部分含 的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到单质硫
的烟气在空气中燃烧,将燃烧所得产物与剩余烟气混合,冷却后可回收得到单质硫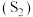 ,该工艺中涉及反应为:
,该工艺中涉及反应为:反应1:
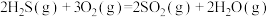

反应2:
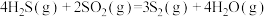
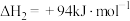
反应3:
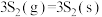
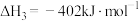
①反应

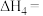
②如果上述反应均能完全进行,为提高硫磺的产率,该工艺中需要控制反应1和反应2的烟气的体积比是
(2)一种以
 为原料,循环吸收烟气中
为原料,循环吸收烟气中 的物质转化关系如下,写出转化中由
的物质转化关系如下,写出转化中由 制
制 同时生成硫酸铵的化学反应方程式:
同时生成硫酸铵的化学反应方程式:
(3)一种以
 为催化剂载体、
为催化剂载体、 为催化剂的
为催化剂的 还原烟气中
还原烟气中 制S的反应机理如题图1和题图2所示:
制S的反应机理如题图1和题图2所示:

①图1中所示转化可以描述为
 分解为活性氢原子,
分解为活性氢原子,②图2中X的电子式为
③其他条件一定,改变起始时
 与
与 的比例,反应相同时间,测得S的产率与温度和
的比例,反应相同时间,测得S的产率与温度和 比值的关系如题图所示,500℃时,
比值的关系如题图所示,500℃时, 比值为3时硫的产率小于比值为2时的原因是
比值为3时硫的产率小于比值为2时的原因是
您最近一年使用:0次
6 . 页岩气中含有CH4、CO2、H2S等气体,是可供开采天然气资源。页岩气的有效利用需要处理其中所含的CO2和H2S。
Ⅰ.CO2的处理:
(1)CO2和CH4重整可制合成气(主要成分为CO、H2),已知下列热化学反应方程式:
①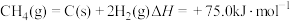
②
③
则反应 的
的
___________ 。
(2)Ni催化CO2加H2形成CH4,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中CH4的百分含量及CO2的转化率随温度的变化如图2所示。
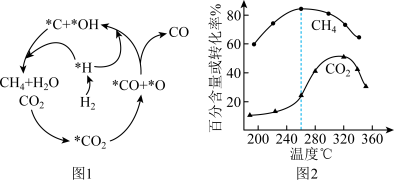
①260℃时生成主要产物所发生反应的化学方程式为___________ 。
②温度高于320℃,CO2的转化率下降的原因是___________ 。
Ⅱ.H2S的处理:
方法一:工业上常采用如图3电解装置电解: 和KHCO3混合溶液,电解一段时间后,通入H2S加以处理。利用生成的铁的化合物
和KHCO3混合溶液,电解一段时间后,通入H2S加以处理。利用生成的铁的化合物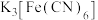 将气态废弃物中的H2S转化为可利用的硫单质,自身转化为
将气态废弃物中的H2S转化为可利用的硫单质,自身转化为 。已知:水溶液中电离方程式:
。已知:水溶液中电离方程式:
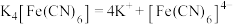
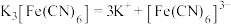
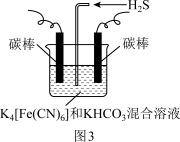
(3)电解时,阳极的电极反应式为___________ 。
方法二:表面喷淋水的活性炭可用于吸附氧化H2S,其原理可用如图4表示。

(4)其它条件不变时,水膜的酸碱性与厚度会影响H2S的去除率。适当增大活性炭表面的水膜pH,H2S的氧化去除率增大的原因是___________ 。
方法三:Fe2O3可用作脱除H2S气体的脱硫剂。Fe2O3脱硫和Fe2O3再生的可能反应机理如图5所示。
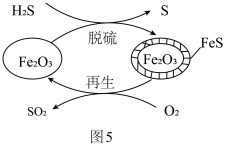
(5)Fe2O3脱硫剂的脱硫和再生过程可以描述为___________ 。
(6)再生时需控制通入O2的浓度和温度。400℃条件下,氧气浓度较大时,会出现脱硫剂再生时质量增大,且所得再生脱硫剂脱硫效果差,原因是___________ 。
Ⅰ.CO2的处理:
(1)CO2和CH4重整可制合成气(主要成分为CO、H2),已知下列热化学反应方程式:
①
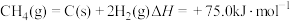
②

③

则反应
 的
的
(2)Ni催化CO2加H2形成CH4,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中CH4的百分含量及CO2的转化率随温度的变化如图2所示。

①260℃时生成主要产物所发生反应的化学方程式为
②温度高于320℃,CO2的转化率下降的原因是
Ⅱ.H2S的处理:
方法一:工业上常采用如图3电解装置电解:
 和KHCO3混合溶液,电解一段时间后,通入H2S加以处理。利用生成的铁的化合物
和KHCO3混合溶液,电解一段时间后,通入H2S加以处理。利用生成的铁的化合物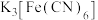 将气态废弃物中的H2S转化为可利用的硫单质,自身转化为
将气态废弃物中的H2S转化为可利用的硫单质,自身转化为 。已知:水溶液中电离方程式:
。已知:水溶液中电离方程式: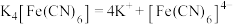
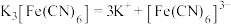

(3)电解时,阳极的电极反应式为
方法二:表面喷淋水的活性炭可用于吸附氧化H2S,其原理可用如图4表示。

(4)其它条件不变时,水膜的酸碱性与厚度会影响H2S的去除率。适当增大活性炭表面的水膜pH,H2S的氧化去除率增大的原因是
方法三:Fe2O3可用作脱除H2S气体的脱硫剂。Fe2O3脱硫和Fe2O3再生的可能反应机理如图5所示。

(5)Fe2O3脱硫剂的脱硫和再生过程可以描述为
(6)再生时需控制通入O2的浓度和温度。400℃条件下,氧气浓度较大时,会出现脱硫剂再生时质量增大,且所得再生脱硫剂脱硫效果差,原因是
您最近一年使用:0次
名校
7 .  和
和 均是洁净的能源和重要的化工原料。
均是洁净的能源和重要的化工原料。
Ⅰ.甲烷高温分解可制碳黑,设计成燃料电池可提高能量的利用效率。
(1)已知25℃、101kPa时,1g甲烷完全燃烧生成液态水放出55.64kJ热量。则该条件下 完全燃烧的热化学方程式为
完全燃烧的热化学方程式为___________ 。
(2)甲烷高温分解生成氢气和碳。在密闭容器中进行此反应时要通入适量空气使部分甲烷燃烧,其目的是___________ 。
(3)已知某甲烷燃料电池的总反应为 ,则电池负极的电极反应为
,则电池负极的电极反应为___________ ,随着电池不断放电,负极附近溶液的pH___________ 。(填“增大”、“减小”或“不变”)
Ⅱ.利用工业废气或大气捕获的 制备甲醇(
制备甲醇( ),可减轻对化石燃料的依赖。
),可减轻对化石燃料的依赖。
实验室在体积为2L的密闭容器中充入1mol 和3mol
和3mol 在催化剂作用下通过反应
在催化剂作用下通过反应
 制备甲醇,实验测得
制备甲醇,实验测得 和
和 的物质的量随时间的变化关系如图所示。
的物质的量随时间的变化关系如图所示。
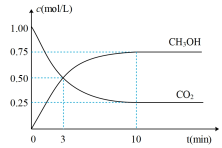
(4)由图可知,当反应进行到___________ (填“3min”或“10min”)时,正反应速率和逆反应速率恰好相等。
(5)下列情况能说明该反应达到化学平衡状态的是___________ (填字母)。
a.单位时间内消耗1mol 的同时生成1mol
的同时生成1mol
b. 与
与 的物质的量之比不再发生变化
的物质的量之比不再发生变化
c.混合气体的密度不再发生变化
(6)若上述反应中生成水的总物质的量不变,但水为液态,则反应过程中放出的热量___________ (填“增多”“减少”或“不变”)。
 和
和 均是洁净的能源和重要的化工原料。
均是洁净的能源和重要的化工原料。Ⅰ.甲烷高温分解可制碳黑,设计成燃料电池可提高能量的利用效率。
(1)已知25℃、101kPa时,1g甲烷完全燃烧生成液态水放出55.64kJ热量。则该条件下
 完全燃烧的热化学方程式为
完全燃烧的热化学方程式为(2)甲烷高温分解生成氢气和碳。在密闭容器中进行此反应时要通入适量空气使部分甲烷燃烧,其目的是
(3)已知某甲烷燃料电池的总反应为
 ,则电池负极的电极反应为
,则电池负极的电极反应为Ⅱ.利用工业废气或大气捕获的
 制备甲醇(
制备甲醇( ),可减轻对化石燃料的依赖。
),可减轻对化石燃料的依赖。实验室在体积为2L的密闭容器中充入1mol
 和3mol
和3mol 在催化剂作用下通过反应
在催化剂作用下通过反应
 制备甲醇,实验测得
制备甲醇,实验测得 和
和 的物质的量随时间的变化关系如图所示。
的物质的量随时间的变化关系如图所示。
(4)由图可知,当反应进行到
(5)下列情况能说明该反应达到化学平衡状态的是
a.单位时间内消耗1mol
 的同时生成1mol
的同时生成1mol
b.
 与
与 的物质的量之比不再发生变化
的物质的量之比不再发生变化c.混合气体的密度不再发生变化
(6)若上述反应中生成水的总物质的量不变,但水为液态,则反应过程中放出的热量
您最近一年使用:0次
2023-05-16更新
|
81次组卷
|
2卷引用:江苏省徐州市铜山区2022-2023学年高一下学期期中化学(选择考)试题
解题方法
8 . CO2的转化和重整受到越来越多的关注,它是有效应对全球气候变化、促进低碳社会构建的重要方法。
(1)工业生产中可利用H2还原CO2制备清洁能源甲醇。
①已知2CO(g)+O2(g)=2CO2(g) ∆H=-566.0kJ/mol
2H2(g)+O2(g)=2H2O(l) ∆H=-571.6kJ/mol
CO与H2合成甲醇的能量变化如图1所示,则用CO2和H2制备甲醇和液态水的热化学方程式为___________ 。

②一定物质的量之比的 和
和 在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图2所示。温度为
在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图2所示。温度为 时,图中P点
时,图中P点___________ (填“处于”或“不处于”)平衡状态。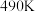 之后,甲醇产率下降的原因是
之后,甲醇产率下降的原因是___________ 。

(2)基于新材料及3D打印技术,科学家研制出一种微胶囊吸收剂能将工厂排放的 以更加安全、廉价和高效的方式处理技术,在球形微胶囊内部充入
以更加安全、廉价和高效的方式处理技术,在球形微胶囊内部充入 溶液,原理如图3所示。
溶液,原理如图3所示。

①这种微胶囊吸收 的原理是
的原理是___________ (写离子方程式)。
②在吸收过程中关于胶囊内溶液下列说法正确的是___________ 。
a.吸收前溶液中
b.吸收过程中,体系中的含碳微粒有
c.当 时,溶液中
时,溶液中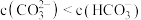
d.溶液中始终有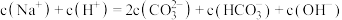
(3) 循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
①在催化剂作用下, 分解生成
分解生成 和
和 可能的反应机理如图4所示。
可能的反应机理如图4所示。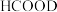 催化释氢反应除生成
催化释氢反应除生成 外,还生成
外,还生成___________ (填化学式)。

② 电催化加氢合成甲酸的工作原理如图5所示。
电催化加氢合成甲酸的工作原理如图5所示。

电极表面积对 转化率和
转化率和 选择性
选择性 的影响如图6所示。控制其他条件不变,电极表面积越大,生成
的影响如图6所示。控制其他条件不变,电极表面积越大,生成 的量
的量___________ (填“越多”或“越少”或“无影响”);随者电极表面积的增大, 转化率增大且
转化率增大且 选择性下降的原因是
选择性下降的原因是___________ 。

(1)工业生产中可利用H2还原CO2制备清洁能源甲醇。
①已知2CO(g)+O2(g)=2CO2(g) ∆H=-566.0kJ/mol
2H2(g)+O2(g)=2H2O(l) ∆H=-571.6kJ/mol
CO与H2合成甲醇的能量变化如图1所示,则用CO2和H2制备甲醇和液态水的热化学方程式为

②一定物质的量之比的
 和
和 在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图2所示。温度为
在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图2所示。温度为 时,图中P点
时,图中P点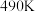 之后,甲醇产率下降的原因是
之后,甲醇产率下降的原因是
(2)基于新材料及3D打印技术,科学家研制出一种微胶囊吸收剂能将工厂排放的
 以更加安全、廉价和高效的方式处理技术,在球形微胶囊内部充入
以更加安全、廉价和高效的方式处理技术,在球形微胶囊内部充入 溶液,原理如图3所示。
溶液,原理如图3所示。
①这种微胶囊吸收
 的原理是
的原理是②在吸收过程中关于胶囊内溶液下列说法正确的是
a.吸收前溶液中

b.吸收过程中,体系中的含碳微粒有

c.当
 时,溶液中
时,溶液中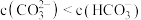
d.溶液中始终有
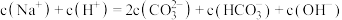
(3)
 循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
循环在氢能的贮存/释放、燃料电池等方面具有重要应用。①在催化剂作用下,
 分解生成
分解生成 和
和 可能的反应机理如图4所示。
可能的反应机理如图4所示。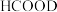 催化释氢反应除生成
催化释氢反应除生成 外,还生成
外,还生成
②
 电催化加氢合成甲酸的工作原理如图5所示。
电催化加氢合成甲酸的工作原理如图5所示。
电极表面积对
 转化率和
转化率和 选择性
选择性 的影响如图6所示。控制其他条件不变,电极表面积越大,生成
的影响如图6所示。控制其他条件不变,电极表面积越大,生成 的量
的量 转化率增大且
转化率增大且 选择性下降的原因是
选择性下降的原因是
您最近一年使用:0次
名校
解题方法
9 .  催化加氢合成甲醇是重要的碳捕获利用与封存技术。
催化加氢合成甲醇是重要的碳捕获利用与封存技术。 催化加氢主要反应有:
催化加氢主要反应有:
反应I.
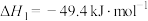
反应II.

压强分别为 、
、 时,将
时,将 的混合气体置于密闭容器中反应,不同温度下体系中
的混合气体置于密闭容器中反应,不同温度下体系中 的平衡转化率和
的平衡转化率和 、CO的选择性如图所示。
、CO的选择性如图所示。
 (或CO)的选择性
(或CO)的选择性
 催化加氢合成甲醇是重要的碳捕获利用与封存技术。
催化加氢合成甲醇是重要的碳捕获利用与封存技术。 催化加氢主要反应有:
催化加氢主要反应有:反应I.

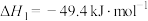
反应II.


压强分别为
 、
、 时,将
时,将 的混合气体置于密闭容器中反应,不同温度下体系中
的混合气体置于密闭容器中反应,不同温度下体系中 的平衡转化率和
的平衡转化率和 、CO的选择性如图所示。
、CO的选择性如图所示。 (或CO)的选择性
(或CO)的选择性

A.反应 为吸热反应 为吸热反应 |
B.曲线③、④表示CO的选择性,且 |
C.相同温度下,反应I、II的平衡常数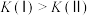 |
D.一定温度下,调整 ,可提高 ,可提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次
2023-01-16更新
|
785次组卷
|
7卷引用:江苏省徐州市沛县第二中学2023-2024学年高三下学期开学化学试题
江苏省徐州市沛县第二中学2023-2024学年高三下学期开学化学试题江苏省南通市2022-2023学年高二上学期1月期末考试化学试题(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(选择题11-14)江苏省海安高级中学2022-2023学年高三下学期3月月考化学试题江苏省盐城市五校2022-2023学年高二下学期5月联考化学试题(已下线)专题07 化学能与热能、电能-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(江苏专用)江苏省锡东高级中学2023-2024学年高二下学期3月月考化学试题
10 . 已知:C(s)+H2O(g)=CO(g)+H2(g) ΔH=a kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-220 kJ·mol-1
H-H、O=O和O-H的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,则a为
2C(s)+O2(g)=2CO(g) ΔH=-220 kJ·mol-1
H-H、O=O和O-H的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,则a为
| A.-332 | B.-118 | C.+350 | D.+130 |
您最近一年使用:0次
2022-10-12更新
|
2056次组卷
|
130卷引用:江苏省徐州市2020-2021学年高二上学期期初检测化学试题
江苏省徐州市2020-2021学年高二上学期期初检测化学试题2014年全国普通高等学校招生统一考试理科综合能力测试化学(重庆卷)(已下线)2015届河南省实验中学高二上学期期中考试化学试卷(已下线)2014秋河北省唐山一中高二上学期期中化学试卷2015届河北省衡水冀州中学高三12月月考化学试卷2015届福建省养正中学高三上学期第二次月考化学试卷2014-2015辽宁省沈阳二中高一下学期4月月考化学试卷2014-2015学年河北省正定中学高二下第三次月考化学试卷2016届西藏日喀则地区一中高三10月月考理综化学试卷2015-2016学年河南洛阳高级中学高二上9月月考化学试卷2015-2016学年湖南常德市第一中学高二12月月考化学卷2015-2016学年广西钦州市钦南区高二上学期期中测试化学试卷2015-2016学年湖北荆州中学高二上期中测试化学试卷2015-2016学年浙江省湖州中学高二上学期期中化学试卷2015-2016学年湖北省宜昌金东方高级中学高二上学期期末化学试卷2016-2017学年河北冀州市中学高二上开学调研化学卷2016-2017学年河南郑州外国语学校高二上开学考试化学2016-2017学年陕西省西安中学高二上10月月考化学试卷2016-2017学年山东省枣庄二中高二第二次月考化学试卷2016-2017学年广东省湛江一中高二上第一次大考化学卷2016-2017学年河南省漯河中学高二上第一次月考化学卷2016-2017学年安徽师大附中高二上10月月考化学卷2016-2017学年安徽省宣城市郎溪中学等四校高二上期中化学卷2016-2017学年四川省达州市年高二上学期期末检测化学试卷重庆市第十八中学2016-2017学年高一下学期期中考试化学试题天津市南开区2017届高三基础训练化学试题2018版化学(苏教版)高考总复习专题六课时跟踪训练--化学反应的热效应河南省林州市第一中学2017-2018学年高二上学期开学考试化学试题河北省大名县第一中学2017-2018学年高二上学期第一次月考化学试题河北省邯郸市成安县第一中学2017-2018学年高二9月月考化学试题甘肃省兰州第一中学2017-2018学年高二上学期第一次月考(9月)化学试题安徽省铜陵市第一中学2017-2018学年高二10月月考化学试题黑龙江省饶河县高级中学2017-2018学年高二上学期第一次月考化学试题内蒙古巴彦淖尔市第一中学2017-2018学年高二9月月考化学试题A内蒙古巴彦淖尔市第一中学2017-2018学年高二9月月考化学试题B浙江省温州中学2017-2018学年高二上学期期中考试化学试题河北省衡水市安平中学2018届高三上学期期中考试化学试题安徽省淮北市第一中学2017--2018学年度第一学期期中考试高二年级化学试题宁夏长庆高级中学2018届高三第四次月考理综化学试卷(已下线)黄金30题系列 高二化学(选修4) 小题好拿分【提升版】湖北省监利县实验高中2017-2018学年高二上学期期中考试化学试题山西省大同市第一中学2017-2018学年高二上学期期末考试化学试题福建省厦门双十中学2017-2018学年高二下学期期中考试化学试题【全国校级联考】内蒙古赤峰市重点高中(赤峰二中,平煤高级中学等)2017-2018学年高二下学期期末联考(A)化学试题辽宁省实验中学2017-2018学年高一下学期期中考试理科化学试题甘肃省岷县二中2018-2019学年高二上学期第一次月考化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2019届高三上学期10月月考化学试题【市级联考】内蒙古鄂尔多斯市2019届高三上学期期中考试化学试题【全国百强校】湖北省武汉市华中师范大学第一附属中学2018-2019学年高二上学期期中检测化学试题河北省衡水市安平县安平中学2019届高三上学期期中考试化学试题河北省唐山市玉田县2018-2019学年高二上学期期中考试化学试题(已下线)2019高考备考二轮复习精品资料-专题8 化学反应中与能量变化(教学案)新疆维吾尔自治区昌吉市第九中学2018-2019学年高二上学期期末考试化学试题浙江省东阳中学2018-2019学年高一下学期期中考试化学试题甘肃省天水市第一中学2017-2018学年高二暑假作业检测考试化学试题安徽省怀宁中学2019-2020学年高二上学期开学考试化学试题甘肃省兰州市第一中学2019-2020学年高二9月月考化学试题河北省唐山一中2019-2020学年高二上学期10月月考化学试题安徽省青阳县第一中学2019-2020学年高二10月月考化学试题宁夏吴忠中学2019-2020学年高二上学期期中考试化学试题湖南省益阳市第六中学2019-2020学年高二上学期期中考试化学试题四川省绵阳市南山中学实验学校2019-2020学年高二12月月考化学试题四川省蓬溪县蓬南中学2019-2020学年高二上学期第四次月考化学试题宁夏海原县第一中学2019-2020学年高二上学期期末考试化学试题江西省南昌市八一中学、洪都中学等六校2019-2020学年高二上学期期末联考化学试题广东省深圳实验学校2019-2020学年高二上学期期末考试化学试题云南省楚雄市实验中学2018—2019学年高二上学期11月月考化学试题甘肃省酒泉市敦煌中学2020届高三上学期第二次调研考试化学试题【懂做原理题】2020届高三化学选修4二轮专题练——盖斯定律的应用【选择提升24题】2020届高三化学选修4二轮专题练——盖斯定律的应用【选择精编25题】广西壮族自治区贺州市桂梧高中2019-2020学年高二上学期第一次月考化学试题河南省平顶山市鲁山县第一高级中学2019-2020高一下学期5月考试化学试题广东省湛江市第二十一中学2019-2020学年高二上学期期中考试化学试题黑龙江省大庆市第四中学2020届高三下学期4月月考理综化学试题广东省广州大学附属中学2019-2020学年高一下学期期末考试化学试题(已下线)1.1.3 反应焓变的计算 练习——【高中新教材同步备课】鲁科版高中化学选择性必修1吉林省长春实验中学2019-2020学年高一6月月考化学试题江苏省启东中学2020-2021学年高二上学期期初考试化学试题(已下线)1.3.2 反应热的计算(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)广东省广州大学附属中学等三校2019~2020学年高一下学期期末联考化学试题江苏省泰州中学2020-2021学年高二上学期期初检测化学试题(已下线)第01章 化学反应的热效应(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)(已下线)第一章 化学反应的热效应(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)(已下线)第01章 化学反应与能量转化(B卷能力提升篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)黑龙江省双鸭山市第一中学2021届高三上学期第一次月考化学试题河北省邢台市第七中学2019-2020学年高二上学期10月月考化学试题安徽省安庆市宜秀区白泽湖中学2020-2021学年高二上学期第一次月考化学试题河南省安阳市第一中学2020-2021学年高二上学期第一次阶段考试化学试题辽宁省盘锦市第二高级中学2020-2021学年高二上学期第一次阶段性考试化学试题山东省济宁市曲阜市第一中学2020-2021学年高二上学期阶段性检测(9月月考)化学试题宁夏回族自治区海原县第一中学2020-2021学年高二上学期第一次月考化学试题福建省福清西山学校高中部2020-2021学年高二上学期期中考试化学试题内蒙古自治区通辽市科左后旗甘旗卡第二高级中学2020-2021学年高二上学期期中考试化学试题山东省德州市第一中学2020-2021学年高二上学期期中检测化学试题黑龙江省哈尔滨市南岗区哈尔滨师范大学附属中学2021届高三上学期期中考试化学试题宁夏银川一中2020-2021学年高二上学期期末考试化学试题黑龙江省龙东南六校2020-2021学年高二上学期期末联考化学试题黑龙江省七台河市勃利县高级中学2020-2021学年高二3月月考化学试题(已下线)【镇江新东方】高二上第二次月考黑龙江省大庆市铁人中学2020-2021学年高一下学期期末考试化学试题黑龙江省哈尔滨师范大学附属中学2020-2021学年高一下学期期末考试化学(理)试题新疆乌鲁木齐市第八中学2018-2019学年高二上学期期中考试化学试题(已下线)课时29 盖斯定律及反应热计算-2022年高考化学一轮复习小题多维练(全国通用)甘肃省民勤县第一中学2021-2022学年高二上学期第一次月考化学试题安徽省合肥市第六中学2021-2022学年高二上学期月考化学试题青海省西宁市北外附属新华联国际学校2021-2022学年高二上学期第一次月考化学(理)试题甘肃省庆阳市第六中学2021-2022学年高二上学期第一次月考化学(理)试题黑龙江省海林市朝鲜族中学2020届高三上学期第二次月考化学试题山西省乡宁县第一中学2021-2022高二上学期第一次月考化学试题浙江省绍兴市诸暨中学2021-2022学年高一上学期期中考试(实验班)化学试题新疆昌吉州2021-2022学年高二上学期期末考试化学试题江西省新余市2021-2022学年高二上学期期末检测化学试题安徽省亳州市第一中学2021-2022学年高二上学期第二次月考化学试题浙江省宁波市九校2021-2022学年高一下学期6月联考化学试题广西桂林市第十八中学2021-2022学年高二下学期开学考试化学试题山东省济南市莱芜第四中学2021-2022学年高二上学期第一次质量检测化学试题 黑龙江省密山市牡丹江管理局高级中学2021-2022学年高二上学期期末考试化学试题北京市顺义区第一中学2022-2023学年高二上学期10月月考化学试题湖北省黄州中学2022--2023学年高二上学期10月月考化学试题湖北省武汉市东湖中学2022-2023学年高二上学期期中考试化学试题湖北省黄冈市麻城第二中学2021-2022学年高一下学期4月月考化学试题浙江省浙江大学附属中学(玉泉校区)2022-2023学年高二上学期期中考试 高二化学试卷(已下线)【2022】【高二化学】【期中考】-180(已下线)【知识图鉴】单元讲练测选择性必修1第1单元03巩固练安徽省安庆二中2022-2023学年高一下学期5月月考化学试题第二节 反应热的计算河北省新乐市第一中学2022-2023学年高二上学期11月期中考试化学试题山东省鄄城县第一中学2022-2023学年高一下学期3月月考化学试题江西省永修县第一中学2023-2024学年高二上学期10月月考化学试题陕西省渭南市瑞泉中学2023-2024学年高二上学期第一次质量检测化学试题



