名校
解题方法
1 . 化学链燃烧是利用载氧体将空气中的氧传输至燃料的新技术,基于CuO/Cu2O载氧体的丙烷(C3H8)化学链燃烧技术原理如图所示。
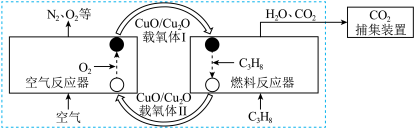
空气反应器与燃料反应器中发生的反应分别如下:
反应1:2Cu2O(s)+O2(g) 4CuO(s) ΔH1
4CuO(s) ΔH1
反应2:20CuO(s)+C3H8(g) 10Cu2O(s)+3CO2(g)+4H2O(g) ΔH2
10Cu2O(s)+3CO2(g)+4H2O(g) ΔH2
反应3:C3H8(g)+5O2(g) 3CO2(g)+4H2O(g) ΔH3
3CO2(g)+4H2O(g) ΔH3
回答下列问题:
(1)ΔH2 =___________ (用含ΔH1、ΔH3的代数式表示)。
(2)一定温度下,在容积可变的密闭容器中加入足量Cu2O(s)和适量的O2发生反应1。
①当Cu2O的质量不变时,___________ (填“能”或“不能”)说明该反应达到平衡状态。
②若达到平衡之后,保持恒温恒容条件下再充入少量O2,达到新平衡之后,O2的平衡转化率___________ (填“增大”、“减小”或“不变”)。
(3)在一定温度下,总压强恒定为68kPa,在密闭容器中加入丙烷和氮气的混合气体以及足量CuO,只发生上述反应2(氮气不参与反应),测得丙烷平衡转化率与投料比[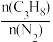 ]的关系如图所示:
]的关系如图所示:

该温度下,平衡常数Kp的计算式 为___________ (以分压表示,分压=总压×物质的量分数;只列式,不计算出最后结果)。

空气反应器与燃料反应器中发生的反应分别如下:
反应1:2Cu2O(s)+O2(g)
 4CuO(s) ΔH1
4CuO(s) ΔH1反应2:20CuO(s)+C3H8(g)
 10Cu2O(s)+3CO2(g)+4H2O(g) ΔH2
10Cu2O(s)+3CO2(g)+4H2O(g) ΔH2 反应3:C3H8(g)+5O2(g)
 3CO2(g)+4H2O(g) ΔH3
3CO2(g)+4H2O(g) ΔH3回答下列问题:
(1)ΔH2 =
(2)一定温度下,在容积可变的密闭容器中加入足量Cu2O(s)和适量的O2发生反应1。
①当Cu2O的质量不变时,
②若达到平衡之后,保持恒温恒容条件下再充入少量O2,达到新平衡之后,O2的平衡转化率
(3)在一定温度下,总压强恒定为68kPa,在密闭容器中加入丙烷和氮气的混合气体以及足量CuO,只发生上述反应2(氮气不参与反应),测得丙烷平衡转化率与投料比[
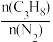 ]的关系如图所示:
]的关系如图所示:
该温度下,平衡常数Kp的
您最近一年使用:0次
名校
2 . 用H2O2和H2SO4的混合溶液可溶出印刷电路板中的铜,其热化学方程式为:Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l) △H。
已知:①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H1=+64kJ•mol-1
②2H2O2(1)=2H2O(1)+O2(g) △H2=-196kJ•mol-1
③H2(g)+ O2(g)=H2O(1) △H3=-286kJ•mol-1
O2(g)=H2O(1) △H3=-286kJ•mol-1
下列说法不正确的是
已知:①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) △H1=+64kJ•mol-1
②2H2O2(1)=2H2O(1)+O2(g) △H2=-196kJ•mol-1
③H2(g)+
 O2(g)=H2O(1) △H3=-286kJ•mol-1
O2(g)=H2O(1) △H3=-286kJ•mol-1下列说法不正确的是
| A.△H=-320kJ•mol-1 |
| B.反应①可通过铜作电极电解稀硫酸的方法实现 |
| C.已知2H2(g)+O2(g)=2H2O(g) △H4,则△H4>2△H3 |
| D.使用MnO2作催化剂时因改变反应②的焓变△H2,从而加快反应的速率 |
您最近一年使用:0次
名校
3 . 下列有关说法不正确的是
A.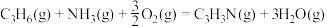 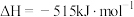 和 和 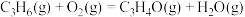 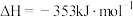 ,两个反应在热力学上趋势均很大 ,两个反应在热力学上趋势均很大 |
B. 与 与 的反应是熵增加的放热反应,该反应能正向自发进行 的反应是熵增加的放热反应,该反应能正向自发进行 |
C.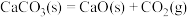 在室温下不能自发进行,说明该反应 在室温下不能自发进行,说明该反应 |
D. 在室温下能自发进行,则该反应 在室温下能自发进行,则该反应 |
您最近一年使用:0次
4 . 下图为两种途径制备硫酸的过程,反应条件略。下列说法不正确的是
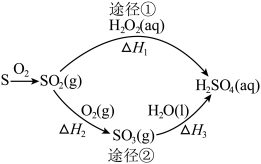

A.若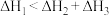 ,则 ,则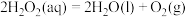 为放热反应 为放热反应 |
B.若将途径①设计为原电池反应,负极区溶液 会变小 会变小 |
C.途径②增大 浓度可提高 浓度可提高 转化率 转化率 |
D.含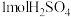 的浓溶液与足量 的浓溶液与足量 反应,放出的热量即为中和热 反应,放出的热量即为中和热 |
您最近一年使用:0次
名校
解题方法
5 . 下列叙述中错误的是
| A.物质发生化学变化一定伴随能量的变化 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同 |
| D.水凝结成冰的过程中,ΔH<0,ΔS<0 |
您最近一年使用:0次
名校
解题方法
6 . 化石燃料的综合利用既能减少污染,又能提高资源利用率。回答下列问题:
(1)煤气化过程如下:
反应1
反应2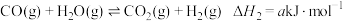
反应3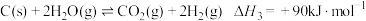
①a=___________ 。
②反应2在催化剂作用下的反应历程如图(TS表示过渡态,*表示吸附态),历程中决速步的方程式为___________ 。

(2)在一定温度下,向某恒容容器中充入2molCO2(g)和2molH2(g),仅发生反应: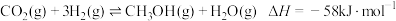 。
。
①下列情况表明反应已达到平衡状态的是___________ (填标号)。
A.CO2的体积分数保持不变 B.混合气体的平均摩尔质量保持不变
C.CO2的转化率保持不变 D.CH3OH与H2O的物质的量之比不再改变
②该反应能在___________ (填“高温”、“低温”或“任何温度”)下自发。
(3)向2L的恒容密闭容器中充入1molCH3OH(g),发生反应: 。其他条件不变时,CH3OH的平衡转化率随着温度(T)的变化如图所示。
。其他条件不变时,CH3OH的平衡转化率随着温度(T)的变化如图所示。

①欲提高CH3OH的平衡转化率且加快反应速率,下列措施可能有效的是___________ (填标号)。
a.降低温度并及时分离出产物
b.加入合适的催化剂并分离出产物
c.再向容器中充入1molCH3OH(g)
d.适当降温并加入合适的催化剂
②T1K时,反应经过20min达到平衡,用C2H4表示的该段时间内的平均速率为___________  ,该温度下,改变投料,某时刻容器内
,该温度下,改变投料,某时刻容器内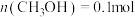 、
、 、
、 ,则此时
,则此时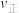
___________ (填“>”、“<”或“=”) 。
。
(1)煤气化过程如下:
反应1

反应2
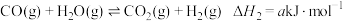
反应3
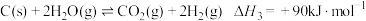
①a=
②反应2在催化剂作用下的反应历程如图(TS表示过渡态,*表示吸附态),历程中决速步的方程式为

(2)在一定温度下,向某恒容容器中充入2molCO2(g)和2molH2(g),仅发生反应:
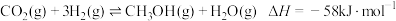 。
。①下列情况表明反应已达到平衡状态的是
A.CO2的体积分数保持不变 B.混合气体的平均摩尔质量保持不变
C.CO2的转化率保持不变 D.CH3OH与H2O的物质的量之比不再改变
②该反应能在
(3)向2L的恒容密闭容器中充入1molCH3OH(g),发生反应:
 。其他条件不变时,CH3OH的平衡转化率随着温度(T)的变化如图所示。
。其他条件不变时,CH3OH的平衡转化率随着温度(T)的变化如图所示。
①欲提高CH3OH的平衡转化率且加快反应速率,下列措施可能有效的是
a.降低温度并及时分离出产物
b.加入合适的催化剂并分离出产物
c.再向容器中充入1molCH3OH(g)
d.适当降温并加入合适的催化剂
②T1K时,反应经过20min达到平衡,用C2H4表示的该段时间内的平均速率为
 ,该温度下,改变投料,某时刻容器内
,该温度下,改变投料,某时刻容器内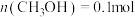 、
、 、
、 ,则此时
,则此时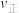
 。
。
您最近一年使用:0次
名校
7 . 热化学硫碘循环制氢是目前最有前景的制氢方法之一,以太阳能为热源的一种制氢方法流程如图,相关反应的热化学方程式为:
反应Ⅰ: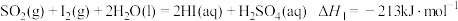
反应Ⅱ: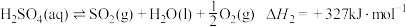
反应Ⅲ: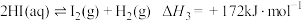
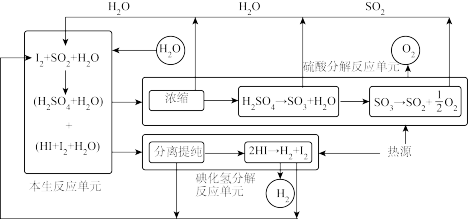
下列说法错误的是
反应Ⅰ:
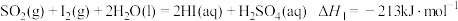
反应Ⅱ:
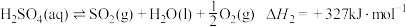
反应Ⅲ:
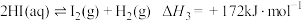

下列说法错误的是
| A.为了提高H2SO4和HI的平衡转化率,研究者往往会利用高压条件进行分解转化 |
| B.碘化氢分解反应单元产生的I2可以进入本生反应单元循环利用 |
| C.整个设备不宜采用铁质材料,原因是H2SO4及HI对铁质设备有很强的腐蚀性 |
D.总反应的热化学方程式为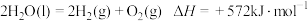 |
您最近一年使用:0次
名校
8 . i.某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线如图所示。已知:达平衡后,若其他条件不变将容器体积扩大为原来的2倍,其气体平均摩尔质量不变。

(1)反应开始时,容器中加入X的物质的量为___________ 。
(2)下列条件的改变能加快其反应速率的是___________ (填序号)。
①升高温度
②增加X的物质的量
③保持压强不变,充入He使容器的体积增大
④保持容积不变,充入He使体系压强增大
ii.
(3)将CO2转化为乙醇可以实现降碳,过程中发生的反应如下:
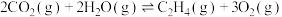

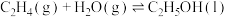



则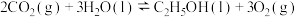

___________ 。
(4)将CO2转化为甲醇也可以实现降碳。
一定条件下,发生反应 。往2L恒容密闭容器中充入1molCO2和3molH2,在甲、乙不同催化剂作用下,反应时间均为tmin时,测得甲醇的物质的量分数随温度变化如图所示:
。往2L恒容密闭容器中充入1molCO2和3molH2,在甲、乙不同催化剂作用下,反应时间均为tmin时,测得甲醇的物质的量分数随温度变化如图所示:

①相同温度下催化剂效果更好的催化剂是___________ (填“甲”或“乙”)。 温度下,b点时甲醇的平均反应速率
温度下,b点时甲醇的平均反应速率
___________ 。
②在甲催化作用下,甲醇的物质的量分数随温度的升高呈现如图变化的原因是___________ 。
③在 和
和 温度下,平衡常数
温度下,平衡常数
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
④已知气体分压=气体总压×气体的物质的量分数。 温度下,反应开始时容器中的总压为
温度下,反应开始时容器中的总压为 ,该温度下反应的平衡常数
,该温度下反应的平衡常数
___________ 。

(1)反应开始时,容器中加入X的物质的量为
(2)下列条件的改变能加快其反应速率的是
①升高温度
②增加X的物质的量
③保持压强不变,充入He使容器的体积增大
④保持容积不变,充入He使体系压强增大
ii.
(3)将CO2转化为乙醇可以实现降碳,过程中发生的反应如下:
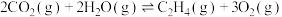

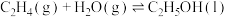



则
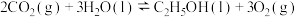

(4)将CO2转化为甲醇也可以实现降碳。
一定条件下,发生反应
 。往2L恒容密闭容器中充入1molCO2和3molH2,在甲、乙不同催化剂作用下,反应时间均为tmin时,测得甲醇的物质的量分数随温度变化如图所示:
。往2L恒容密闭容器中充入1molCO2和3molH2,在甲、乙不同催化剂作用下,反应时间均为tmin时,测得甲醇的物质的量分数随温度变化如图所示:
①相同温度下催化剂效果更好的催化剂是
 温度下,b点时甲醇的平均反应速率
温度下,b点时甲醇的平均反应速率
②在甲催化作用下,甲醇的物质的量分数随温度的升高呈现如图变化的原因是
③在
 和
和 温度下,平衡常数
温度下,平衡常数
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。④已知气体分压=气体总压×气体的物质的量分数。
 温度下,反应开始时容器中的总压为
温度下,反应开始时容器中的总压为 ,该温度下反应的平衡常数
,该温度下反应的平衡常数
您最近一年使用:0次
9 . 我国力争2060年前实现碳中和。CH,与CO2催化重整是实现碳中和的热点研究课题。该催化重整反应体系主要涉及以下反应:
反应I:主反应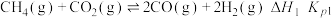
反应II:副反应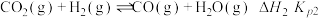
反应III:积碳反应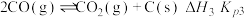
反应IV:积碳反应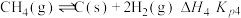
(1)已知H2(g)、CO(g)的燃烧热 分别为-285.8kJ⋅mol-1、﹣283.01kJ⋅mol-1,
分别为-285.8kJ⋅mol-1、﹣283.01kJ⋅mol-1,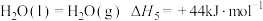 ,则反应II的
,则反应II的
___________  。
。
(2)下列关于该重整反应体系的说法正确的是___________。
(3)对于反应I:主反应 在pMPa时,将CO2和CH4按物质的量之比为1:1充入密闭容器中,分别在无催化剂及ZrO2催化下反应相同时间,测得CO2的转化率与温度的关系如图所示:
在pMPa时,将CO2和CH4按物质的量之比为1:1充入密闭容器中,分别在无催化剂及ZrO2催化下反应相同时间,测得CO2的转化率与温度的关系如图所示:

①a点CO2转化率相等的原因是___________ 。
②在pMPa、900℃、ZrO2催化条件下,将CO2、CH4、H2O按物质的量之比为1:1:n充入催化剂密闭容器,CO2的平衡转化率α大于50%,解释说明原因________ ,此时平衡常数
_________ (以分压表示,分压=总压×物质的量分数:写出含α、n、p的计算表达式)。
(4)以NaCl饱和溶液为电解质溶液,利用如图所示的装置将CO2转化为燃料CO。则电极II接电源的___________ 极,阴极上电极反应式为___________ 。

反应I:主反应
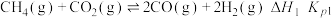
反应II:副反应
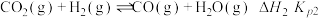
反应III:积碳反应
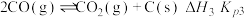
反应IV:积碳反应
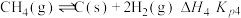
(1)已知H2(g)、CO(g)的燃烧热
 分别为-285.8kJ⋅mol-1、﹣283.01kJ⋅mol-1,
分别为-285.8kJ⋅mol-1、﹣283.01kJ⋅mol-1,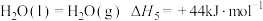 ,则反应II的
,则反应II的
 。
。(2)下列关于该重整反应体系的说法正确的是___________。
A.在投料时适当增大 的值,有利于减少积碳 的值,有利于减少积碳 |
| B.在一定条件下建立平衡后,移去部分积碳,反应Ⅲ和反应Ⅳ平衡均向右移 |
C.随着投料比 的增大,达到平衡时 的增大,达到平衡时 的转化率增大 的转化率增大 |
| D.降低反应温度,反应I、II、IV的正反应速率减小,逆反应速率增大;反应III的正反应速率增大,逆反应速率减小 |
(3)对于反应I:主反应
 在pMPa时,将CO2和CH4按物质的量之比为1:1充入密闭容器中,分别在无催化剂及ZrO2催化下反应相同时间,测得CO2的转化率与温度的关系如图所示:
在pMPa时,将CO2和CH4按物质的量之比为1:1充入密闭容器中,分别在无催化剂及ZrO2催化下反应相同时间,测得CO2的转化率与温度的关系如图所示:
①a点CO2转化率相等的原因是
②在pMPa、900℃、ZrO2催化条件下,将CO2、CH4、H2O按物质的量之比为1:1:n充入催化剂密闭容器,CO2的平衡转化率α大于50%,解释说明原因

(4)以NaCl饱和溶液为电解质溶液,利用如图所示的装置将CO2转化为燃料CO。则电极II接电源的

您最近一年使用:0次
10 . 氮及其化合物与人类生产生活息息相关。
(1)氮气在雷电的作用下,生成氮的氧化物,再经复杂变化形成能供给植物营养的硝酸盐。
涉及的部分反应:
I.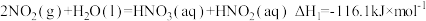 ;
;
II.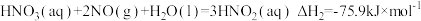 ;
;
III. ;
;
①
___________  。
。
②将两个充有等量NO2的A、B烧瓶,分别放入两个盛有等量的水的烧杯中,待气体颜色稳定后,若向右边的烧杯中加入5.0g硝酸铵晶体,实验装置如图所示(略去铁架台等),则观察到B烧瓶中气体颜色___________ (填“变深”、“不变”或“变浅”),其原因是___________ 。

(2)氮气是生产氮肥的主要原料。
①实验室可用氯化铵与消石灰反应制备少量NH3.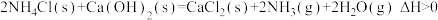 ,该反应在
,该反应在___________ (填“高温”、“低温”或“任何温度”)下能自发进行。
②已知 ,工业合成氨通常选择30MPa左右,700K左右,以铁触媒为催化剂,分析工业合成氨时不选用更高的压强或更高的温度的可能原因
,工业合成氨通常选择30MPa左右,700K左右,以铁触媒为催化剂,分析工业合成氨时不选用更高的压强或更高的温度的可能原因_______ 。
(3)CO和NO是汽车尾气中的主要污染物,将它们转化为无害物质是重要的研究课题。
已知:在25℃时,
IV.
V.
25℃时,反应: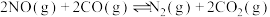 的平衡常数K6=
的平衡常数K6=___________ (填含K4、K5的代数式)。
(1)氮气在雷电的作用下,生成氮的氧化物,再经复杂变化形成能供给植物营养的硝酸盐。
涉及的部分反应:
I.
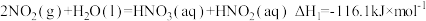 ;
;II.
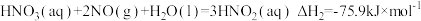 ;
;III.
 ;
;①

 。
。②将两个充有等量NO2的A、B烧瓶,分别放入两个盛有等量的水的烧杯中,待气体颜色稳定后,若向右边的烧杯中加入5.0g硝酸铵晶体,实验装置如图所示(略去铁架台等),则观察到B烧瓶中气体颜色

(2)氮气是生产氮肥的主要原料。
①实验室可用氯化铵与消石灰反应制备少量NH3.
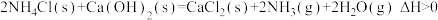 ,该反应在
,该反应在②已知
 ,工业合成氨通常选择30MPa左右,700K左右,以铁触媒为催化剂,分析工业合成氨时不选用更高的压强或更高的温度的可能原因
,工业合成氨通常选择30MPa左右,700K左右,以铁触媒为催化剂,分析工业合成氨时不选用更高的压强或更高的温度的可能原因(3)CO和NO是汽车尾气中的主要污染物,将它们转化为无害物质是重要的研究课题。
已知:在25℃时,
IV.

V.

25℃时,反应:
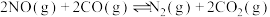 的平衡常数K6=
的平衡常数K6=
您最近一年使用:0次



