1 . 我国力争于2030年前做到碳达峰,2060年前实现碳中和。
(1)CH4与CO2重整是CO2利用的研究热点之一、该重整反应体系主要涉及以下反应:
a)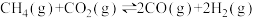

b)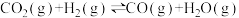

c)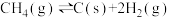

d)

e)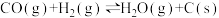

①根据盖斯定律,反应a的
___________ (写出一个代数式即可)。
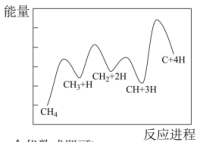
②一定条件下,CH4分解形成碳的反应历程如图所示。该历程分___________ 步进行,其中,第___________ 步的反应最慢。
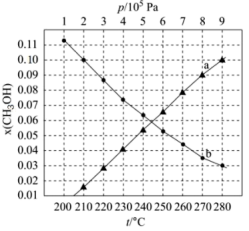
(2)二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。反应可表示为: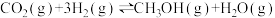 。在起始物
。在起始物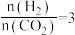 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为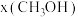 ,在
,在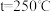 下的
下的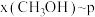 、在
、在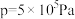 下的
下的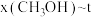 如图所示。
如图所示。
①用各物质的平衡分压[如 的分压可表示为
的分压可表示为 ]表示该反应平衡常数,表达式
]表示该反应平衡常数,表达式
___________ ;
②图中对应等温过程的曲线是___________ ,判断的理由是___________ ;
③当 时,
时, 的平衡转化率
的平衡转化率
___________ ,反应条件可能为___________ 或___________ 。
(1)CH4与CO2重整是CO2利用的研究热点之一、该重整反应体系主要涉及以下反应:
a)
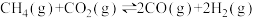

b)
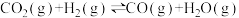

c)
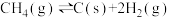

d)


e)
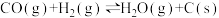

①根据盖斯定律,反应a的

②一定条件下,CH4分解形成碳的反应历程如图所示。该历程分

(2)二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。反应可表示为:
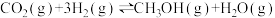 。在起始物
。在起始物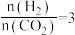 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为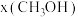 ,在
,在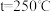 下的
下的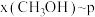 、在
、在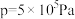 下的
下的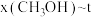 如图所示。
如图所示。
①用各物质的平衡分压[如
 的分压可表示为
的分压可表示为 ]表示该反应平衡常数,表达式
]表示该反应平衡常数,表达式
②图中对应等温过程的曲线是
③当
 时,
时, 的平衡转化率
的平衡转化率
您最近一年使用:0次
2 . 回答下列问题:
(1)将5mL0.005mol/L的 溶液与5mL0.01mol/L的KSCN溶液混合,建立平衡。
溶液与5mL0.01mol/L的KSCN溶液混合,建立平衡。
①若滴加1mol/LKSCN溶液4滴,平衡___________ (填“正向”“不”或“逆向”,②同)移动,溶液红色___________ 。
②若滴加3滴浓KCl溶液,则平衡___________ 移动。
(2)火箭发射时可以用肼( ,液态)为燃料,过氧化氢(液态)作氧化剂,两者反应生成氮气和水蒸气,已知0.05 mol
,液态)为燃料,过氧化氢(液态)作氧化剂,两者反应生成氮气和水蒸气,已知0.05 mol 在上述反应中放出64.22kJ的热量,该反应的热化学方程式为
在上述反应中放出64.22kJ的热量,该反应的热化学方程式为___________ 。
(3)在探究温度对化学平衡影响的实验中。已知,绿色 水溶液中存在如下平衡:
水溶液中存在如下平衡: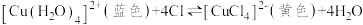
 ,加热的实验现象是溶液变为
,加热的实验现象是溶液变为___________ 色,由此得出的结论是___________ 。
(4)1909年化学家哈伯在实验室首次合成了氨,2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得了诺贝尔化学奖。
①工业上合成氨反应的化学方程式为___________ 。
②用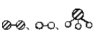 分别表示N2、H2、NH3。观察下图,写出符合在催化剂表面合成氨反应过程的顺序 (将下面五张图按反应过程顺序用序号排列)
分别表示N2、H2、NH3。观察下图,写出符合在催化剂表面合成氨反应过程的顺序 (将下面五张图按反应过程顺序用序号排列) ___________
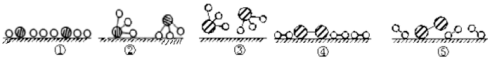
状态①、②、④中,能量最高的状态是___________ 。
(1)将5mL0.005mol/L的
 溶液与5mL0.01mol/L的KSCN溶液混合,建立平衡。
溶液与5mL0.01mol/L的KSCN溶液混合,建立平衡。①若滴加1mol/LKSCN溶液4滴,平衡
②若滴加3滴浓KCl溶液,则平衡
(2)火箭发射时可以用肼(
 ,液态)为燃料,过氧化氢(液态)作氧化剂,两者反应生成氮气和水蒸气,已知0.05 mol
,液态)为燃料,过氧化氢(液态)作氧化剂,两者反应生成氮气和水蒸气,已知0.05 mol 在上述反应中放出64.22kJ的热量,该反应的热化学方程式为
在上述反应中放出64.22kJ的热量,该反应的热化学方程式为(3)在探究温度对化学平衡影响的实验中。已知,绿色
 水溶液中存在如下平衡:
水溶液中存在如下平衡: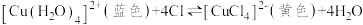
 ,加热的实验现象是溶液变为
,加热的实验现象是溶液变为(4)1909年化学家哈伯在实验室首次合成了氨,2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得了诺贝尔化学奖。
①工业上合成氨反应的化学方程式为
②用
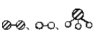 分别表示N2、H2、NH3。观察下图,写出符合在催化剂表面合成氨反应过程的顺序 (将下面五张图按反应过程顺序用序号排列)
分别表示N2、H2、NH3。观察下图,写出符合在催化剂表面合成氨反应过程的顺序 (将下面五张图按反应过程顺序用序号排列) 
状态①、②、④中,能量最高的状态是
您最近一年使用:0次
3 .  (Ⅲ)晶面铁原子簇是合成氨工业的一种新型高效催化剂,N2和H2在其表面首先变为活化分子,反应机理为:①
(Ⅲ)晶面铁原子簇是合成氨工业的一种新型高效催化剂,N2和H2在其表面首先变为活化分子,反应机理为:①

②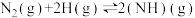

③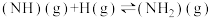

④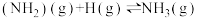

总反应为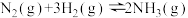

下列说法正确的是
 (Ⅲ)晶面铁原子簇是合成氨工业的一种新型高效催化剂,N2和H2在其表面首先变为活化分子,反应机理为:①
(Ⅲ)晶面铁原子簇是合成氨工业的一种新型高效催化剂,N2和H2在其表面首先变为活化分子,反应机理为:①

②
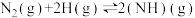

③
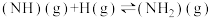

④
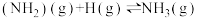

总反应为
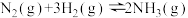

下列说法正确的是
A. (Ⅲ)晶面铁原子簇能够有效降低合成氨反应的活化能和焓变 (Ⅲ)晶面铁原子簇能够有效降低合成氨反应的活化能和焓变 |
B.相同条件下,若1mol氢原子所具有的能量为E1,1 mol氢分子的能量为E2,则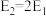 |
| C.反应①和总反应均为放热反应 |
D.总反应的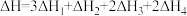 |
您最近一年使用:0次
名校
解题方法
4 .  捕获技术用于去除气流中的
捕获技术用于去除气流中的 或者分离出
或者分离出 作为气体产物,其中
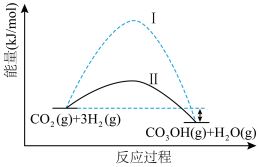
作为气体产物,其中 催化合成甲醇是一种很有前景的方法。如图所示为该反应在无催化剂及有正催化剂时的能量变化(该反应为可逆反应)。
催化合成甲醇是一种很有前景的方法。如图所示为该反应在无催化剂及有正催化剂时的能量变化(该反应为可逆反应)。
(1)温度为523 K时,测得上述反应中生成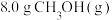 放出的热量为12.3 kJ。反应的热化学方程式为
放出的热量为12.3 kJ。反应的热化学方程式为___________ 。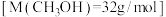
(2)从图可知,有催化剂存在的是过程___________ (填“Ⅰ”或“Ⅱ”)。
(3)一定温度下(各物质均为气态),向体积为2 L的恒容密闭容器中充入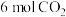 和
和 ,加入合适催化剂进行反应。某时刻测得
,加入合适催化剂进行反应。某时刻测得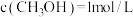 ,此时反应
,此时反应___________ (填“正向移动”、“逆向移动”或“达到平衡)。已知该温度下反应的化学平衡常数值为1/40.
(4)关于 催化合成甲醇的反应,下列说法中合理的是___________(填字母序号)。
催化合成甲醇的反应,下列说法中合理的是___________(填字母序号)。
(5)制备过程中存在副反应: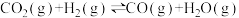
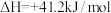 将混合气按进料比
将混合气按进料比 通入反应装置,选择合适催化剂发生反应。不同温度和压强下,
通入反应装置,选择合适催化剂发生反应。不同温度和压强下, 平衡产率和
平衡产率和 平衡转化率分别如图1、图2。
平衡转化率分别如图1、图2。
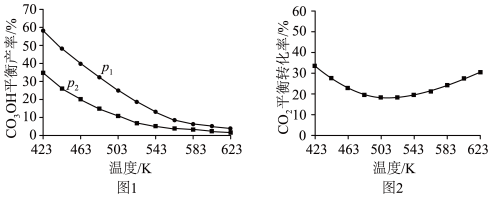
①图1中,压强
___________  (填“>”“=”或“<”),推断的依据是
(填“>”“=”或“<”),推断的依据是___________ 。
②图2中,压强为 ,温度高于503 K后,
,温度高于503 K后, 平衡转化率随温度升高而增大的原因是
平衡转化率随温度升高而增大的原因是___________ 。
 捕获技术用于去除气流中的
捕获技术用于去除气流中的 或者分离出
或者分离出 作为气体产物,其中
作为气体产物,其中 催化合成甲醇是一种很有前景的方法。如图所示为该反应在无催化剂及有正催化剂时的能量变化(该反应为可逆反应)。
催化合成甲醇是一种很有前景的方法。如图所示为该反应在无催化剂及有正催化剂时的能量变化(该反应为可逆反应)。
(1)温度为523 K时,测得上述反应中生成
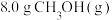 放出的热量为12.3 kJ。反应的热化学方程式为
放出的热量为12.3 kJ。反应的热化学方程式为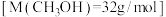
(2)从图可知,有催化剂存在的是过程
(3)一定温度下(各物质均为气态),向体积为2 L的恒容密闭容器中充入
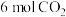 和
和 ,加入合适催化剂进行反应。某时刻测得
,加入合适催化剂进行反应。某时刻测得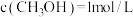 ,此时反应
,此时反应(4)关于
 催化合成甲醇的反应,下列说法中合理的是___________(填字母序号)。
催化合成甲醇的反应,下列说法中合理的是___________(填字母序号)。| A.该反应原子转化率为100% |
B.该反应可用于 的转化,有助于缓解温室效应 的转化,有助于缓解温室效应 |
C.使用催化剂可以降低该反应的 ,从而使反应放出更多热量 ,从而使反应放出更多热量 |
D.降温分离液态甲醇和水,将剩余气体重新通入反应器,可提高 与 与 的利用率 的利用率 |
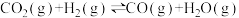
 将混合气按进料比
将混合气按进料比 通入反应装置,选择合适催化剂发生反应。不同温度和压强下,
通入反应装置,选择合适催化剂发生反应。不同温度和压强下, 平衡产率和
平衡产率和 平衡转化率分别如图1、图2。
平衡转化率分别如图1、图2。
①图1中,压强

 (填“>”“=”或“<”),推断的依据是
(填“>”“=”或“<”),推断的依据是②图2中,压强为
 ,温度高于503 K后,
,温度高于503 K后, 平衡转化率随温度升高而增大的原因是
平衡转化率随温度升高而增大的原因是
您最近一年使用:0次
2021-11-15更新
|
181次组卷
|
2卷引用:山西省介休市第十中学2022-2023学年高二上学期 期中考试化学试题
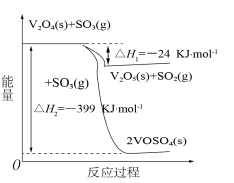
5 . 接触法制硫酸生产中的关键工序是SO2的催化氧化:2SO2(g)+O2(g)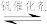 2SO3(g) △H=-196kJ·mol-1。钒催化剂参与反应的能量变化如图所示。下列说法正确的是
2SO3(g) △H=-196kJ·mol-1。钒催化剂参与反应的能量变化如图所示。下列说法正确的是
 2SO3(g) △H=-196kJ·mol-1。钒催化剂参与反应的能量变化如图所示。下列说法正确的是
2SO3(g) △H=-196kJ·mol-1。钒催化剂参与反应的能量变化如图所示。下列说法正确的是
| A.钒催化剂改变了SO2催化氧化的反应热 |
| B.上述条件下加入2molSO2和1molO2发生反应,释放的能量等于196kJ |
| C.1molV2O4(s)的能量比2mol VOSO4(s)的能量多399kJ |
| D.2V2O5(s)+2SO2(g)=2VOSO4(s)+V2O4(s) △H=-351kJ·mol-1 |
您最近一年使用:0次
2021-11-14更新
|
323次组卷
|
3卷引用:山西省吕梁市柳林县2021-2022学年高二上学期期中考试化学试题
6 . 当今,世界多国相继规划了碳达峰、碳中和的时间节点,我国力争于2030年前做到碳达峰,2060年前实现碳中和。因此,研发二氧化碳利用技术,降低空气中二氧化碳的含量成为研究热点。
(1)大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25℃时,相关物质的燃烧热数据如下表:
则25℃时H2(g)和C(石墨,s)生成C6H6(l)的热化学方程式为__________ 。
(2)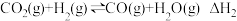
(3)以CO2、H2为原料合成CH3OH的主要反应如下:
I.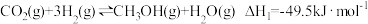
II.
III.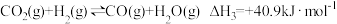
不同压强下,按照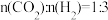 投料,实验测得CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
投料,实验测得CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
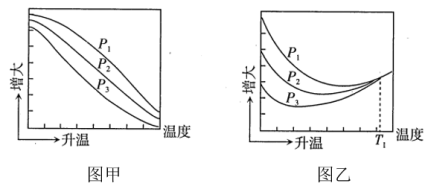
已知:CO2的平衡转化率=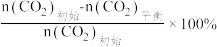
CH3OH的平衡产率=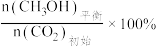
其中纵坐标表示CO2平衡转化率的是图_____ (填“甲”或“乙”);压强P1、P2、P3由大到小的顺序为____ ;图乙中T1温度时,三条曲线几乎交于一点的原因是_______ 。
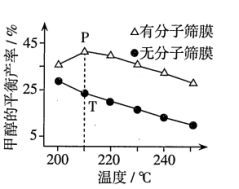
(4)恒压下,按照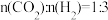 投料发生反应I,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的平衡产率随温度的变化如图所示(分子筛膜具有选择透过性)。P点甲醇的平衡产率高于T点的原因可能是
投料发生反应I,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的平衡产率随温度的变化如图所示(分子筛膜具有选择透过性)。P点甲醇的平衡产率高于T点的原因可能是_________ 。
(1)大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25℃时,相关物质的燃烧热数据如下表:
| 物质 | H2(g) | C(石墨,s) | C6H6(l) |
燃烧热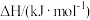 |  |  |  |
(2)
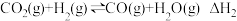
(3)以CO2、H2为原料合成CH3OH的主要反应如下:
I.
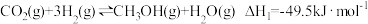
II.

III.
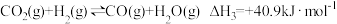
不同压强下,按照
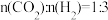 投料,实验测得CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
投料,实验测得CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
已知:CO2的平衡转化率=
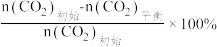
CH3OH的平衡产率=
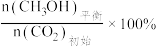
其中纵坐标表示CO2平衡转化率的是图
(4)恒压下,按照
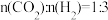 投料发生反应I,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的平衡产率随温度的变化如图所示(分子筛膜具有选择透过性)。P点甲醇的平衡产率高于T点的原因可能是
投料发生反应I,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的平衡产率随温度的变化如图所示(分子筛膜具有选择透过性)。P点甲醇的平衡产率高于T点的原因可能是
您最近一年使用:0次
7 . 碳的单质及化合物在人类生产生活中起着非常重要的作用。请回答下列问题:
(1)已知CH3OH(l)的燃烧热 ,
,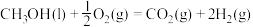
 ,则
,则
______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(2)Cl2(g)和H2O(g)通过灼热的炭层,生成HCl(g)和CO2(g),当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:___________ 。
(3)火箭和导弹表面的薄层是耐高温物质。下列反应可制得耐高温材料,热化学方程式为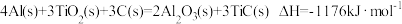 。该反应过程中每转移1mol电子放出的热量为
。该反应过程中每转移1mol电子放出的热量为_________ kJ。
(4)工业上乙烯催化氧化制乙醛的反应原理为: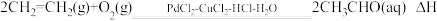 ,该反应原理可以拆解为如下三步反应:
,该反应原理可以拆解为如下三步反应:
I.
II.……
III.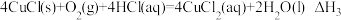
若第II步反应的反应热为 ,且
,且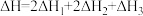 ,则第II步反应的热化学方程式为
,则第II步反应的热化学方程式为__ 。
(5)山西是全国最大的炼焦用煤资源基地,炼焦过程的副产品之一焦炉煤气富含H2、CH4和CO,因此可通过甲烷化反应来提高热值,使绝大部分CO、CO2转化成CH4.甲烷化反应的主要化学原理为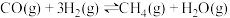 ,已知CO分子中的C与O之间为共价三键。下表所列为常见化学键的键能数据(键能指气态分子中1mol化学键解离成气态原子所吸收的能量):
,已知CO分子中的C与O之间为共价三键。下表所列为常见化学键的键能数据(键能指气态分子中1mol化学键解离成气态原子所吸收的能量):
该反应的
__________  。
。
(1)已知CH3OH(l)的燃烧热
 ,
,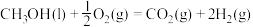
 ,则
,则
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(2)Cl2(g)和H2O(g)通过灼热的炭层,生成HCl(g)和CO2(g),当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:
(3)火箭和导弹表面的薄层是耐高温物质。下列反应可制得耐高温材料,热化学方程式为
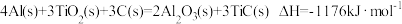 。该反应过程中每转移1mol电子放出的热量为
。该反应过程中每转移1mol电子放出的热量为(4)工业上乙烯催化氧化制乙醛的反应原理为:
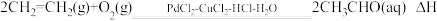 ,该反应原理可以拆解为如下三步反应:
,该反应原理可以拆解为如下三步反应:I.

II.……
III.
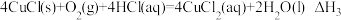
若第II步反应的反应热为
 ,且
,且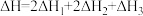 ,则第II步反应的热化学方程式为
,则第II步反应的热化学方程式为(5)山西是全国最大的炼焦用煤资源基地,炼焦过程的副产品之一焦炉煤气富含H2、CH4和CO,因此可通过甲烷化反应来提高热值,使绝大部分CO、CO2转化成CH4.甲烷化反应的主要化学原理为
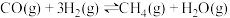 ,已知CO分子中的C与O之间为共价三键。下表所列为常见化学键的键能数据(键能指气态分子中1mol化学键解离成气态原子所吸收的能量):
,已知CO分子中的C与O之间为共价三键。下表所列为常见化学键的键能数据(键能指气态分子中1mol化学键解离成气态原子所吸收的能量):| 化学键 |  |  |  |  |  |  |
键能/( ) ) | 347.7 | 413.4 | 436 | 351 | 1065 | 462.8 |

 。
。
您最近一年使用:0次
10-11高二上·山西临汾·期中
名校
解题方法
8 . 已知热化学反应方程式:Zn(s)+ O2(g)=ZnO(s) ΔH=-351.5kJ·mol-1;Hg(l)+
O2(g)=ZnO(s) ΔH=-351.5kJ·mol-1;Hg(l)+ O2(g)=HgO(s) ΔH=-90.84kJ·mol-1,则热化学反应方程式:Zn(s)+HgO(s)=ZnO(s)+Hg(l)的ΔH为
O2(g)=HgO(s) ΔH=-90.84kJ·mol-1,则热化学反应方程式:Zn(s)+HgO(s)=ZnO(s)+Hg(l)的ΔH为
 O2(g)=ZnO(s) ΔH=-351.5kJ·mol-1;Hg(l)+
O2(g)=ZnO(s) ΔH=-351.5kJ·mol-1;Hg(l)+ O2(g)=HgO(s) ΔH=-90.84kJ·mol-1,则热化学反应方程式:Zn(s)+HgO(s)=ZnO(s)+Hg(l)的ΔH为
O2(g)=HgO(s) ΔH=-90.84kJ·mol-1,则热化学反应方程式:Zn(s)+HgO(s)=ZnO(s)+Hg(l)的ΔH为| A.ΔH=+260.66kJ·mol-1 | B.ΔH=+442.34kJ·mol-1 |
| C.ΔH=-442.34kJ·mol-1 | D.ΔH=-260.66kJ·mol-1 |
您最近一年使用:0次
2021-11-08更新
|
147次组卷
|
27卷引用:2010年山西省临汾一中高二上学期期中考试化学试题
(已下线)2010年山西省临汾一中高二上学期期中考试化学试题(已下线)2011-2012学年江西省兴国县将军中学高二上学期期中考试化学试卷(已下线)2011-2012学年福建省厦门一中高二上学期期中考试化学试卷(已下线)2011-2012学年辽宁省抚顺县高级中学高一下学期期中考试化学试卷(已下线)2012-2013学年浙江省桐乡一中高二下学期期中考试化学试卷2015-2016学年吉林省吉林五十五中高二上学期期中(理)化学试卷甘肃省天水市武山县三校2020-2021学年高二上学期期中联考化学试题 (已下线)必考点01 化学反应的热效应-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版2019选择性必修1)云南省红河县一中2021-2022学年高二上学期期中考试化学试题(已下线)2012-2013学年新疆兵团农二师华山中学高二上学期期末考试化学试卷(已下线)2014届贵州省六校联盟高三第一次联考化学试卷2015-2016北京大学附中宇华教育集团高二12月化学卷2015-2016北京大学附中宇华教育集团高一12月化学卷2015-2016学年陕西省黄陵中学高二上学期期末考试化学试卷2015-2016学年安徽省安庆市怀宁县高河中学高二上期末化学试卷甘肃省武威第五中学2018-2019学年高二上学期期末考试化学试题宁夏青铜峡市高级中学(吴忠中学分校)2019-2020学年高二上学期第一次月考化学试题福建省华安一中、龙海二中2019-2020学年高二上学期第一次联考化学试题甘肃省古浪县第二中学2019-2020学年高二12月基础知识竞赛化学试题【懂做原理题】2020届高三化学选修4二轮专题练——盖斯定律的应用【选择提升24题】黑龙江省绥化地区肇东第四中学2020-2021学年高二上学期期末考试化学试题湖南省常德市石门县第六中学2020-2021学年高二上学期期末考试(合格考)化学试题吉林省大安市第六中学2021-2022学年高二上学期第一次月考化学试题湖南省长沙铁路第一中学2021-2022学年高二上学期第一次阶段性考试化学试题海南省海口嘉勋高级中学2021-2022学年高二上学期10月月考化学试题黑龙江省鸡西市第四中学2022-2023学年高二上学期第一次月考化学试题安徽省芜湖市无为襄安中学2022-2023高二上学期第一次月考化学试题
名校
9 . 利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g) CH3OH(g)△H1
CH3OH(g)△H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H2
CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g) CO(g)+H2O(g)△H3
CO(g)+H2O(g)△H3
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
由此计算△H1=___ kJ·mol-1,已知△H2=-58kJ·mol-1,则△H3=___ kJ·mol-1。
(2)科学家提出制备“合成气反应历程分两步:
反应①:CH4(g)=C(ads)+2H2(g)(慢反应)
反应②:C(ads)+CO2(g)=2CO(g)(快反应)
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图所示:
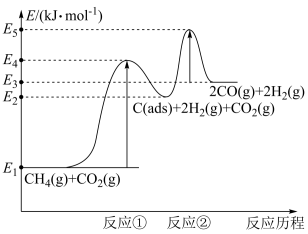
CH4与CO2制备合成气的热化学方程式为__ 。
(3)利用铜基配合物1,10—phenanthroline—Cu催化剂电催化CO2还原制备碳基燃料(包括CO、烷烃和酸等)是减少CO2在大气中累积和实现可再生能源有效利用的关键手段之,其装置原理如图所示。
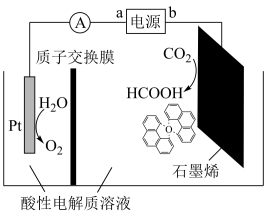
①电池工作过程中,图中Pt电极附近溶液的pH__ (填“变大”或“变小”),阴极的电极反应式为___ 。
②每转移2mol电子,阴极室溶液质量增加___ g。
(4)利用“Na—CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na—CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2 2Na2CO3+C.放电时该电池“吸入CO2,其工作原理如图所示:
2Na2CO3+C.放电时该电池“吸入CO2,其工作原理如图所示:
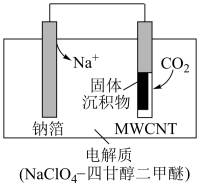
①放电时,正极的电极反应式为___ 。
②若生成的Na2CO3和C全部沉积在电极表面,当转移0.2mol电子时,两极的质量差为___ g。(假设放电前两电极质量相等)
①CO(g)+2H2(g)
 CH3OH(g)△H1
CH3OH(g)△H1②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H2
CH3OH(g)+H2O(g)△H2③CO2(g)+H2(g)
 CO(g)+H2O(g)△H3
CO(g)+H2O(g)△H3回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C≡O | H—O | C—H |
| E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | 413 |
(2)科学家提出制备“合成气反应历程分两步:
反应①:CH4(g)=C(ads)+2H2(g)(慢反应)
反应②:C(ads)+CO2(g)=2CO(g)(快反应)
上述反应中C(ads)为吸附性活性炭,反应历程的能量变化如图所示:

CH4与CO2制备合成气的热化学方程式为
(3)利用铜基配合物1,10—phenanthroline—Cu催化剂电催化CO2还原制备碳基燃料(包括CO、烷烃和酸等)是减少CO2在大气中累积和实现可再生能源有效利用的关键手段之,其装置原理如图所示。

①电池工作过程中,图中Pt电极附近溶液的pH
②每转移2mol电子,阴极室溶液质量增加
(4)利用“Na—CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na—CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2
 2Na2CO3+C.放电时该电池“吸入CO2,其工作原理如图所示:
2Na2CO3+C.放电时该电池“吸入CO2,其工作原理如图所示:
①放电时,正极的电极反应式为
②若生成的Na2CO3和C全部沉积在电极表面,当转移0.2mol电子时,两极的质量差为
您最近一年使用:0次
2021-10-18更新
|
118次组卷
|
2卷引用:山西省运城市2021-2022学年高三上学期期中考试化学试题
2021高三·全国·专题练习
名校
10 . 我国学者结合实验与计算机模拟结果,研究了均相NO-CO的反应历程,该反应经历了I、II、III三个过渡态。图中显示的是反应路径中每一阶段内各驻点的能量相对于此阶段内反应物能量的能量之差。下列说法正确的是
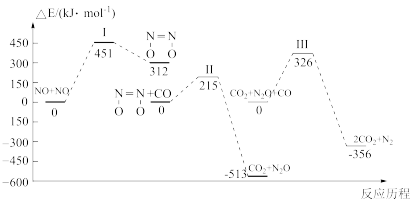

A.N2O比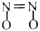 更不容易与CO发生反应 更不容易与CO发生反应 |
| B.整个反应分为三个基元反应阶段,其中第一个反应阶段活化能最大 |
C.2NO(g)+2CO(g) N2(g)+2CO2(g) ∆H>0 N2(g)+2CO2(g) ∆H>0 |
| D.其他条件不变,增大压强或使用催化剂均可以增大反应速率,提高反应物的转化率 |
您最近一年使用:0次
2021-10-13更新
|
158次组卷
|
5卷引用:山西省太原市2021-2022学年高二上学期期中考试化学试题
山西省太原市2021-2022学年高二上学期期中考试化学试题(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)山东省临沂市平邑县第一中学实验部2021-2022学年高二上学期第二次月考化学试题河北省保定市唐县一中2021-2022学年高三上学期第二次月考化学试题



