名校
1 . 第三周期元素的单质及其化合物具有重要用途。在熔融状态下,可用金属钠制备金属钾;MgCl2可制备多种镁产品;铝—空气电池具有较高的比能量,在碱性电解液中总反应为4Al+3O2+4OH-+6H2O=4[Al(OH)4]-。高纯硅广泛用于信息技术领域,高温条件下,将粗硅转化为三氯硅烷(SiHCl3),再经氢气还原得到高纯硅。硫有多种单质,如斜方硫(燃烧热为297kJ·mol–1)、单斜硫等。H2S可除去废水中Hg2+等重金属离子,H2S水溶液在空气中会缓慢氧化生成S而变浑浊。SO2催化氧化是工业制硫酸的重要反应之一,常用V2O5作催化剂。下列化学反应表示正确的是
| A.斜方硫燃烧:S(s,斜方硫)+O2(g)=SO2(g) ∆H=297kJ·mol–1 |
| B.CuSO4溶液中加入小粒金属钠:2Na+Cu2+=Cu+2Na+ |
C.SiHCl3转化为高纯硅:SiHCl3+H2 Si+3HCl Si+3HCl |
| D.铝—空气电池放电时的负极反应:Al+4H2O-3e−=[Al(OH)4]-+4H+ |
您最近一年使用:0次
名校
解题方法
2 . 有效去除大气中的NOx和水体中的氮,并且转化为可利用的资源是重要课题。
(1)在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下: (aq)+2O2(g)=
(aq)+2O2(g)= (aq)+2H+(aq)+H2O(l) ΔH=
(aq)+2H+(aq)+H2O(l) ΔH=_______ kJ·mol-1
(2)近年来,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中的c(OH-)制备纳米Cu2O备受关注,其模拟装置如图甲、乙。_______ (请填“C”或“D”)极相连。
②该电解池的阳极反应式为_______ 。
③该电解池(图乙)中离子交换膜为_______ (请填“阴”或“阳”)离子交换膜。
④理论上,每生产144g纳米Cu2O,需要消耗肼(N2H4)_______ mol。
(3)纳米颗粒在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示。_______ 。
②上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中_______ (填字母)的活化能。
A.*CO+*OH→*CO+*H2O
B.*CO→*OCH
C.*OCH2→*OCH3
D.*OCH3→*CH3OH
(4)磷酸铵镁(MgNH4PO4)沉淀法可去除水体中的氨氮( 和NH3)。实验室中模拟氨氮处理:1 L的模拟氨氮废水(主要含
和NH3)。实验室中模拟氨氮处理:1 L的模拟氨氮废水(主要含 ),置于搅拌器上,设定反应温度为25 ℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30 min后,取液面下2 cm处清液测定氨氮质量浓度。已知:常温下,磷酸铵镁(MgNH4PO4)微溶于水;H3PO4的Ka1=6.9×10-3, Ka2=6.2×10-8 ,Ka3=4.8×10-13。
),置于搅拌器上,设定反应温度为25 ℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30 min后,取液面下2 cm处清液测定氨氮质量浓度。已知:常温下,磷酸铵镁(MgNH4PO4)微溶于水;H3PO4的Ka1=6.9×10-3, Ka2=6.2×10-8 ,Ka3=4.8×10-13。_______ 。
②当反应pH为9.0时,该沉淀法对氨氮的去除率达到最高,当pH继续增至10.0时,氨氮的去除率下降,原因是_______ 。
(1)在微生物作用的条件下,
 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下: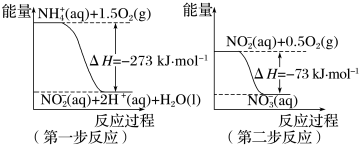
 (aq)+2O2(g)=
(aq)+2O2(g)= (aq)+2H+(aq)+H2O(l) ΔH=
(aq)+2H+(aq)+H2O(l) ΔH=(2)近年来,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中的c(OH-)制备纳米Cu2O备受关注,其模拟装置如图甲、乙。
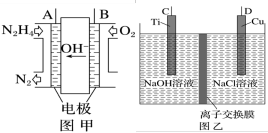
②该电解池的阳极反应式为
③该电解池(图乙)中离子交换膜为
④理论上,每生产144g纳米Cu2O,需要消耗肼(N2H4)
(3)纳米颗粒在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示。
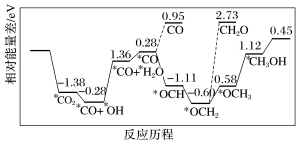
②上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中
A.*CO+*OH→*CO+*H2O
B.*CO→*OCH
C.*OCH2→*OCH3
D.*OCH3→*CH3OH
(4)磷酸铵镁(MgNH4PO4)沉淀法可去除水体中的氨氮(
 和NH3)。实验室中模拟氨氮处理:1 L的模拟氨氮废水(主要含
和NH3)。实验室中模拟氨氮处理:1 L的模拟氨氮废水(主要含 ),置于搅拌器上,设定反应温度为25 ℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30 min后,取液面下2 cm处清液测定氨氮质量浓度。已知:常温下,磷酸铵镁(MgNH4PO4)微溶于水;H3PO4的Ka1=6.9×10-3, Ka2=6.2×10-8 ,Ka3=4.8×10-13。
),置于搅拌器上,设定反应温度为25 ℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30 min后,取液面下2 cm处清液测定氨氮质量浓度。已知:常温下,磷酸铵镁(MgNH4PO4)微溶于水;H3PO4的Ka1=6.9×10-3, Ka2=6.2×10-8 ,Ka3=4.8×10-13。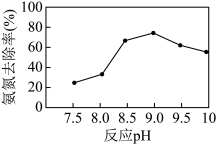
②当反应pH为9.0时,该沉淀法对氨氮的去除率达到最高,当pH继续增至10.0时,氨氮的去除率下降,原因是
您最近一年使用:0次
名校
3 . 尿素[CO(NH2)2]的生产具有重要意义。
(1)尿素的催化合成
已知:2H2(g)+O2(g)=2H2O(l) ΔH1=-286.0 kJ·mol-1
N2(g)+3H2(g)=2NH3(g) ΔH2=-92.2 kJ·mol-1
2NH3(g)+CO2(g)=CO(NH2)2(aq)+H2O(l) ΔH3=-101.5 kJ·mol-1
则反应2CO2+2N2+4H2O=2CO(NH2)2+3O2的 ΔH=___________ kJ·mol-1
(2)尿素的电化学合成
①电催化CO2和 合成尿素的装置如下图所示,生成尿素的电极反应式为
合成尿素的装置如下图所示,生成尿素的电极反应式为___________ 。
已知:CO2在阴极还能被还原为CH4,其生成CH4的趋势比生成CO的趋势更大。但实验数据说明,一定时间内,阴极产物中CO的物质的量大于CH4,可能的原因为___________ 。
(3)尿素的应用
尿素将烟气中氮氧化物还原为N2以达到消除污染的目的。控制其他条件相同,将混有NO、NO2、SO2、N2和O2的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测NO、NO2的脱除率α(α= ×100%)。
×100%)。
①当烟气中有少量SO2时,有利于NO2脱除,其可能的原因是___________ 。
②当烟气中无SO2存在时,且 超过一定数值时,测得α(NO)变为负值,其可能的原因是
超过一定数值时,测得α(NO)变为负值,其可能的原因是___________ 。
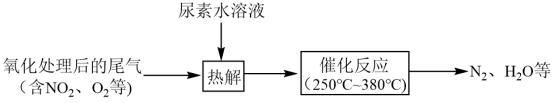
③尿素水溶液热解产生的NH3可去除尾气中的NOx,流程如下:___________ 。
(1)尿素的催化合成
已知:2H2(g)+O2(g)=2H2O(l) ΔH1=-286.0 kJ·mol-1
N2(g)+3H2(g)=2NH3(g) ΔH2=-92.2 kJ·mol-1
2NH3(g)+CO2(g)=CO(NH2)2(aq)+H2O(l) ΔH3=-101.5 kJ·mol-1
则反应2CO2+2N2+4H2O=2CO(NH2)2+3O2的 ΔH=
(2)尿素的电化学合成
①电催化CO2和
 合成尿素的装置如下图所示,生成尿素的电极反应式为
合成尿素的装置如下图所示,生成尿素的电极反应式为
已知:CO2在阴极还能被还原为CH4,其生成CH4的趋势比生成CO的趋势更大。但实验数据说明,一定时间内,阴极产物中CO的物质的量大于CH4,可能的原因为
(3)尿素的应用
尿素将烟气中氮氧化物还原为N2以达到消除污染的目的。控制其他条件相同,将混有NO、NO2、SO2、N2和O2的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测NO、NO2的脱除率α(α=
 ×100%)。
×100%)。①当烟气中有少量SO2时,有利于NO2脱除,其可能的原因是
②当烟气中无SO2存在时,且
 超过一定数值时,测得α(NO)变为负值,其可能的原因是
超过一定数值时,测得α(NO)变为负值,其可能的原因是③尿素水溶液热解产生的NH3可去除尾气中的NOx,流程如下:
您最近一年使用:0次
名校
解题方法
4 . 推动 的综合利用实现碳中和是党中央作出的重大战略决策。
的综合利用实现碳中和是党中央作出的重大战略决策。
Ⅰ. 催化加氢法:以下是
催化加氢法:以下是 催化加氢合成二甲醚发生的两个主要反应:
催化加氢合成二甲醚发生的两个主要反应:
反应Ⅰ:
反应Ⅱ:
(1)反应
___________ 。
(2)在恒压、 和
和 起始量一定的条件下,
起始量一定的条件下, 平衡转化率和平衡时
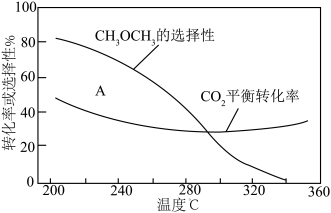
平衡转化率和平衡时 的选择性随温度的变化如图。其中:
的选择性随温度的变化如图。其中: 的选择性
的选择性
 平衡转化率随温度升高而上升的原因是
平衡转化率随温度升高而上升的原因是___________ 。
②220℃时,在催化剂作用下 与
与 反应一段时间后,测得
反应一段时间后,测得 的选择性为:
的选择性为: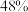 (图中
(图中 点)。不改变反应时间和温度,一定能提高
点)。不改变反应时间和温度,一定能提高 选择性的措施有:
选择性的措施有:___________ 。(答1点即可)
Ⅱ. 催化加氢法:高炉气中捕集
催化加氢法:高炉气中捕集 制
制 的综合利用示意图如图所示。
的综合利用示意图如图所示。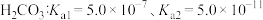 。
。
(3)T℃时,当吸收池中溶液的 时,此时该溶液中
时,此时该溶液中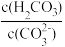 =
=___________ 。
(4)电解池中 电催化还原为
电催化还原为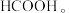
① 在铂电极反应方程式为
在铂电极反应方程式为___________ 。
②铂电极上的副反应除析氢外,没有其它放电过程。若生成 的电解效率
的电解效率 ,当电路中转移
,当电路中转移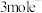 时,阴极室溶液的质量增加
时,阴极室溶液的质量增加___________  。定义:
。定义: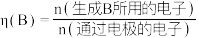
 的综合利用实现碳中和是党中央作出的重大战略决策。
的综合利用实现碳中和是党中央作出的重大战略决策。Ⅰ.
 催化加氢法:以下是
催化加氢法:以下是 催化加氢合成二甲醚发生的两个主要反应:
催化加氢合成二甲醚发生的两个主要反应:反应Ⅰ:

反应Ⅱ:

(1)反应

(2)在恒压、
 和
和 起始量一定的条件下,
起始量一定的条件下, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图。其中:
的选择性随温度的变化如图。其中: 的选择性
的选择性
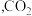 平衡转化率随温度升高而上升的原因是
平衡转化率随温度升高而上升的原因是②220℃时,在催化剂作用下
 与
与 反应一段时间后,测得
反应一段时间后,测得 的选择性为:
的选择性为: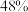 (图中
(图中 点)。不改变反应时间和温度,一定能提高
点)。不改变反应时间和温度,一定能提高 选择性的措施有:
选择性的措施有:Ⅱ.
 催化加氢法:高炉气中捕集
催化加氢法:高炉气中捕集 制
制 的综合利用示意图如图所示。
的综合利用示意图如图所示。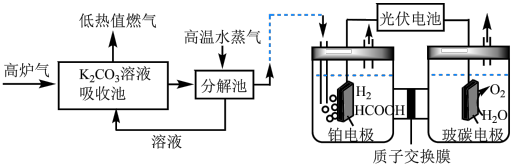
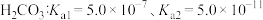 。
。(3)T℃时,当吸收池中溶液的
 时,此时该溶液中
时,此时该溶液中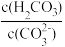 =
=(4)电解池中
 电催化还原为
电催化还原为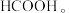
①
 在铂电极反应方程式为
在铂电极反应方程式为②铂电极上的副反应除析氢外,没有其它放电过程。若生成
 的电解效率
的电解效率 ,当电路中转移
,当电路中转移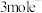 时,阴极室溶液的质量增加
时,阴极室溶液的质量增加 。定义:
。定义:
您最近一年使用:0次
名校
解题方法
5 . 有效去除大气中的NOx和水体中的氮是环境保护的重要课题。
(1)已知:①2CO(g)+O2(g)=2CO2(g);ΔH1=-566.0kJ·mol-1
②N2(g)+2O2(g)=2NO2(g);ΔH2=+64kJ·mol-1
反应:2NO2(g)+4CO(g)=N2(g)+4CO2(g);ΔH3=________ 。
(2)近年研究发现,电催化CO2和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成 ,电解原理如图所示。
,电解原理如图所示。________ 。
(3)磷酸铵镁(MgNH4PO4)沉淀法可去除水体中的氨氮(NH 和NH3)。实验室中模拟氨氮处理:1L的模拟氨氮废水(主要含NH
和NH3)。实验室中模拟氨氮处理:1L的模拟氨氮废水(主要含NH ),置于搅拌器上,设定反应温度为25℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30min后,取液面下2cm处清液测定氨氮质量浓度。
),置于搅拌器上,设定反应温度为25℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30min后,取液面下2cm处清液测定氨氮质量浓度。
①生成磷酸铵镁沉淀的离子反应方程式为________ 。
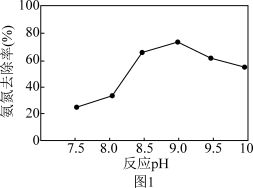
②测得反应pH对氨氮去除率的影响如下图1所示,当pH从7.5增至9.0的过程中,水中氨氮的去除率明显增加,原因是________ 。
①NZVI/BC和(CuPd)/BC复合材料还原硝酸盐的反应机理如下图2所示, 转化为N2或
转化为N2或 的过程可描述为
的过程可描述为________ 。 去除率的影响如上图3,前200min内,pH=9.88时的去除率远低于pH=4.05时,其可能的原因是
去除率的影响如上图3,前200min内,pH=9.88时的去除率远低于pH=4.05时,其可能的原因是________ 。
(1)已知:①2CO(g)+O2(g)=2CO2(g);ΔH1=-566.0kJ·mol-1
②N2(g)+2O2(g)=2NO2(g);ΔH2=+64kJ·mol-1
反应:2NO2(g)+4CO(g)=N2(g)+4CO2(g);ΔH3=
(2)近年研究发现,电催化CO2和含氮物质(
 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成 ,电解原理如图所示。
,电解原理如图所示。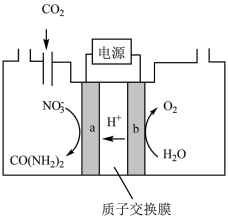
(3)磷酸铵镁(MgNH4PO4)沉淀法可去除水体中的氨氮(NH
 和NH3)。实验室中模拟氨氮处理:1L的模拟氨氮废水(主要含NH
和NH3)。实验室中模拟氨氮处理:1L的模拟氨氮废水(主要含NH ),置于搅拌器上,设定反应温度为25℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30min后,取液面下2cm处清液测定氨氮质量浓度。
),置于搅拌器上,设定反应温度为25℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30min后,取液面下2cm处清液测定氨氮质量浓度。①生成磷酸铵镁沉淀的离子反应方程式为
②测得反应pH对氨氮去除率的影响如下图1所示,当pH从7.5增至9.0的过程中,水中氨氮的去除率明显增加,原因是
①NZVI/BC和(CuPd)/BC复合材料还原硝酸盐的反应机理如下图2所示,
 转化为N2或
转化为N2或 的过程可描述为
的过程可描述为 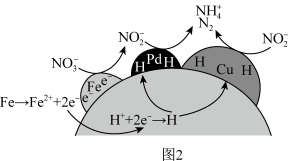
 去除率的影响如上图3,前200min内,pH=9.88时的去除率远低于pH=4.05时,其可能的原因是
去除率的影响如上图3,前200min内,pH=9.88时的去除率远低于pH=4.05时,其可能的原因是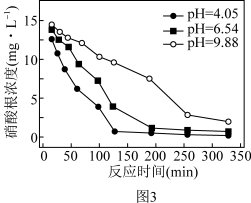
您最近一年使用:0次
名校
6 . 工业及汽车尾气已成为城市空气的主要污染源,研究其反应机理对于环境治理有重要意义。
(1)硝酸厂尾气可以回收制备硝酸。已知:
①2NO(g)+O2(g)=2NO2(g) △H1=-113.0 kJ/mol
②3NO2(g)+H2O(g)=2HNO3(g)+NO(g) △H2=-138.0 kJ/mol
4NO2(g)+O2(g)+2H2O(g)=4HNO3(g) △H=___________ kJ/mol。
(2)液氨催化还原NO是重要的烟气脱硝技术。使用Fe2O3为催化剂,可能的反应过程如图所示。___________ 。
②反应过程图中,虚线方框里的过程可描述为___________ 。
③氨氮比会直接影响该方法的脱硝率。350℃时只改变氨气的投放量,NO的百分含量与氨氮比的关系如图所示。当 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是___________ 。
NO2被Na2CO3溶液吸收生成的三种盐分别是NaNO2、NaNO3和___________ 。(填化学式)
(4)NSR (NOX储存还原)可有效减少氮氧化物排放。工作原理:通过BaO和Ba(NO3)2的相互转化实现NOX的储存和还原,如图所示。___________ 。
(1)硝酸厂尾气可以回收制备硝酸。已知:
①2NO(g)+O2(g)=2NO2(g) △H1=-113.0 kJ/mol
②3NO2(g)+H2O(g)=2HNO3(g)+NO(g) △H2=-138.0 kJ/mol
4NO2(g)+O2(g)+2H2O(g)=4HNO3(g) △H=
(2)液氨催化还原NO是重要的烟气脱硝技术。使用Fe2O3为催化剂,可能的反应过程如图所示。
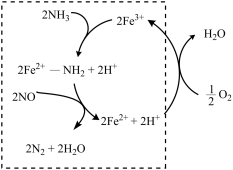
②反应过程图中,虚线方框里的过程可描述为
③氨氮比会直接影响该方法的脱硝率。350℃时只改变氨气的投放量,NO的百分含量与氨氮比的关系如图所示。当
 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是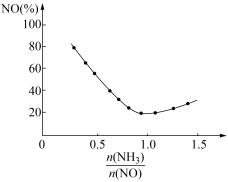
NO2被Na2CO3溶液吸收生成的三种盐分别是NaNO2、NaNO3和
(4)NSR (NOX储存还原)可有效减少氮氧化物排放。工作原理:通过BaO和Ba(NO3)2的相互转化实现NOX的储存和还原,如图所示。
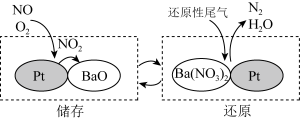
您最近一年使用:0次
名校
解题方法
7 . 在一定条件下CO2催化加氢生成CH3OH,主要发生三个竞争反应:
反应I:
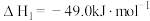
反应Ⅱ:
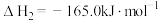
反应ⅡI:
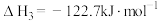
为分析催化剂对反应的选择性,在1L恒容密闭容器中充入一定量的CO2和H2,测得反应进行相同时间后,有关物质的物质的量随温度变化如图所示,下列说法不正确的是
反应I:

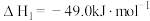
反应Ⅱ:

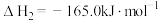
反应ⅡI:

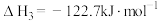
为分析催化剂对反应的选择性,在1L恒容密闭容器中充入一定量的CO2和H2,测得反应进行相同时间后,有关物质的物质的量随温度变化如图所示,下列说法不正确的是

A.  |
| B.其他条件不变,增大H2用量,反应I速率增大,平衡常数增大 |
| C.一定温度下,当容器中的气体压强不再改变时,体系达到平衡 |
| D.温度过高,三种含碳产物的物质的量会迅速降低,可能原因是催化剂活性降低 |
您最近一年使用:0次
名校
解题方法
8 . 过渡金属氧化物离子(以MO+表示)在烃类的选择性氧化等方面应用广泛。MO+与CH4反应的过程如下图所示。不正确 的是
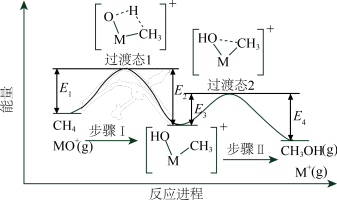
| A.反应速率:步骤I<步骤II |
| B.CH3OH分子中,键角:H—C—H>H—O—C |
| C.若MO+与CH3D反应,生成的氘代甲醇有2种 |
D.CH4(g) + MO+(g)=CH3OH(g) + M+(g)  = E2+E4-E1-E3 = E2+E4-E1-E3 |
您最近一年使用:0次
2024-04-01更新
|
550次组卷
|
5卷引用:江苏省常州市第一中学2023-2024学年高二下学期4月期中考试化学试题
江苏省常州市第一中学2023-2024学年高二下学期4月期中考试化学试题北京市丰台区2023-2024学年高三下学期综合练习(一)化学试题(已下线)通关练08 聚焦反应热、速率及化学平衡-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)化学(天津卷03)-2024年高考化学押题预测卷(已下线)提升练03 反应历程探究与催化原理-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
9 . 异丁烯是一种重要的化工原料,主要用于制备甲基叔丁基醚、丁基橡胶、甲基丙烯腈等。将异丁烷脱氢制备异丁烯,可提高异丁烷的附加值,具有良好的经济与社会效益。回答下列问题。
(1)利用下列燃烧热数据,计算异丁烷直接脱氢生成异丁烯反应的∆H:
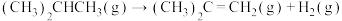 ∆H=
∆H=____________ kJ·mol-1。
(2)在恒温853K、恒压100kPa条件下,初始反应气体组成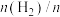 (异丁烷)或
(异丁烷)或 (异丁烷)与平衡时异丁烷的物质的量分数x的关系如下图所示。
(异丁烷)与平衡时异丁烷的物质的量分数x的关系如下图所示。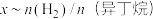 为曲线
为曲线_________ (填“M”或“N”),催化剂易被副反应产生的加聚产物__________ (填写结构简式)影响而失活。
(3)有人提出在恒温恒压条件下加入适量空气,采用异丁烷氧化脱氢的方法制备异丁烯。比较异丁烷直接脱氢制备异丁烯,从平衡产率角度分析该方法的优点是_____________ ,若生产过程中加入的空气过多,产生的主要问题是_____________ 。
(4)有人提出加入适量CO2,采用MgFe2O4催化CO2氧化异丁烷脱氢的方法制备异丁烯。催化过程中,反应物异丁烷、CO2先各自被催化剂上的不同位点吸附。催化剂中电负性较大的金属_____________ (填元素符号)是酸性位点;而电负性较小的金属是碱性位点,吸附________________ (填“异丁烷”或“CO2”)。
(1)利用下列燃烧热数据,计算异丁烷直接脱氢生成异丁烯反应的∆H:
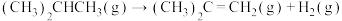 ∆H=
∆H=| 物质 | 异丁烷(g) | 异丁烯(g) | 氢气(g) |
| 燃烧热/(kJ·mol-1) | 2868 | 2700 | 286 |
(2)在恒温853K、恒压100kPa条件下,初始反应气体组成
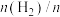 (异丁烷)或
(异丁烷)或 (异丁烷)与平衡时异丁烷的物质的量分数x的关系如下图所示。
(异丁烷)与平衡时异丁烷的物质的量分数x的关系如下图所示。
 为曲线
为曲线(3)有人提出在恒温恒压条件下加入适量空气,采用异丁烷氧化脱氢的方法制备异丁烯。比较异丁烷直接脱氢制备异丁烯,从平衡产率角度分析该方法的优点是
(4)有人提出加入适量CO2,采用MgFe2O4催化CO2氧化异丁烷脱氢的方法制备异丁烯。催化过程中,反应物异丁烷、CO2先各自被催化剂上的不同位点吸附。催化剂中电负性较大的金属
您最近一年使用:0次
2024-03-22更新
|
108次组卷
|
2卷引用:江苏省南京市金陵中学2022-2023学年高二下学期期中考试 化学试卷
10 . 下列实验方案不能达到实验目的的是
| 选项 | A | B | C | D |
| 实验方案 | 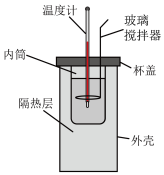 | 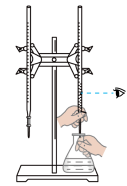 | 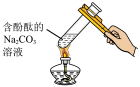 加热后溶液红色加深 | 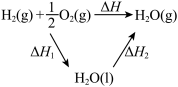 测得ΔH为ΔH1、ΔH2的和 |
| 实验目的 | 用于在实验室测定中和反应的反应热 | 用已知浓度的HCl溶液滴定未知浓度的NaOH溶液 | 验证温度对水解平衡的影响 | 验证ΔH与物质的始末状态有关,与反应过程无关 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



