名校
解题方法
1 . 工业合成氨的反应N2+3H2=2NH3的能量变化如图所示,请回答有关问题:
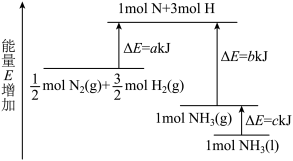
(1)合成1molNH3(l)___________ (填“吸收”或“放出”)___________ kJ的热量。(用字母表示)
(2)已知:拆开1molH—H键、1molN—H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则1molN2(g)完全反应生成NH3(g)产生的能量变化为___________ kJ。
(3)推测反应2NH3(l)=N2(g)+3H2(g)比反应2NH3(g)=N2(g)+3H2(g)___________ (填“吸收”或“放出”)的热量___________ (填“多”或“少”)。

(1)合成1molNH3(l)
(2)已知:拆开1molH—H键、1molN—H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则1molN2(g)完全反应生成NH3(g)产生的能量变化为
(3)推测反应2NH3(l)=N2(g)+3H2(g)比反应2NH3(g)=N2(g)+3H2(g)
您最近一年使用:0次
2021-05-03更新
|
300次组卷
|
8卷引用:山西省朔州市应县第一中学校2019-2020学年高一下学期期中考试化学试题
山西省朔州市应县第一中学校2019-2020学年高一下学期期中考试化学试题江西省南昌市八一中学、洪都中学等七校2020-2021学年高一下学期期中联考化学试题安徽省滁州市定远县育才学校2020-2021学年高一下学期期中考试化学试题江西省赣州市南康区第三中学2020-2021学年高一下学期期中考试化学试题黑龙江省齐齐哈尔市第八中学校2020-2021学年高一下学期期中考试化学试题陕西省渭南市华州区咸林中学2022-2023学年高一下学期期中考试化学试题(已下线)练习3 化学反应热的计算-2020-2021学年【补习教材·寒假作业】高二化学(人教版)云南省昌宁县第一中学2021-2022学年高一 3月月考化学试题
解题方法
2 . 能源危机是当前全球性的问题,“开源节流”是应对能源危机的重要举措。
(1)下列做法有助于能源“开源节流”的是___ (填字母)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源
d.减少资源消耗,增加资源的重复使用和循环再生
(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,氧气充足时燃烧生成二氧化碳,反应中放出的热量如图所示。
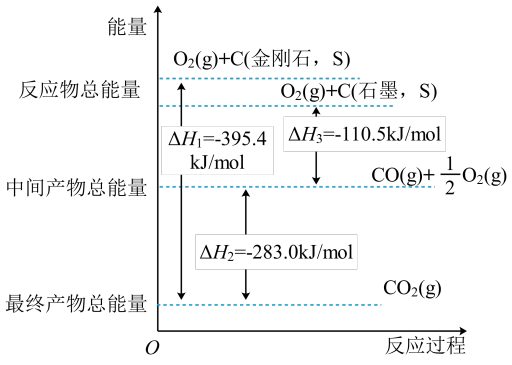
①在通常状况下,___ (填“金刚石”或“石墨”)更稳定;石墨的燃烧热△H为___ 。
②若12g金刚石在24g氧气中燃烧,生成气体36g,则该过程放出的热量为___ 。
(3)已知:N2、O2分子中化学键的键能分别是946mol·L-1、497mol·L-1,N2(g)+O2(g)=2NO(g)△H=+180.0kJ·mol-1,则NO分子中化学键的键能为___ kJ·mol-1。
(4)综合上述有关信息,请写出CO和NO反应生成两种无毒气体的热化学方程式:___ 。
(1)下列做法有助于能源“开源节流”的是
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源
d.减少资源消耗,增加资源的重复使用和循环再生
(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,氧气充足时燃烧生成二氧化碳,反应中放出的热量如图所示。

①在通常状况下,
②若12g金刚石在24g氧气中燃烧,生成气体36g,则该过程放出的热量为
(3)已知:N2、O2分子中化学键的键能分别是946mol·L-1、497mol·L-1,N2(g)+O2(g)=2NO(g)△H=+180.0kJ·mol-1,则NO分子中化学键的键能为
(4)综合上述有关信息,请写出CO和NO反应生成两种无毒气体的热化学方程式:
您最近一年使用:0次
2020-11-24更新
|
367次组卷
|
2卷引用:山西省太原市2020-2021学年高二上学期期中质量监测化学(理)试题
3 . 嫦娥二号卫星采用“长三丙火箭”进行发射,其第三级推进器使用的燃料是液态氢。已知在25℃时,2 g H2(g)与O2(g)完全反应生成H2O(g)时放热241.8KJ。则下列有关判断正确的是
| A.H2(g)的燃烧热是-241.8KJ/mol |
B.25℃时,H2(g)+ O2(g)=H2O(l) ΔH<-241.8KJ/mol O2(g)=H2O(l) ΔH<-241.8KJ/mol |
| C.25℃时,22.4L H2 完全燃烧生成H2O(g)放出的热量为241.8KJ |
D.已知H2O(g)=H2O(l) ΔH=-44KJ/mol,则H2O(l)=H2(g)+ O2(g) ΔH=+241.8KJ/mol O2(g) ΔH=+241.8KJ/mol |
您最近一年使用:0次
解题方法
4 . 研究含氮污染物的治理是环保的一项重要工作。合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5 kJ·mol−1
2C(s)+O2(g)=2CO(g) ΔH=﹣221.0 kJ·mol−1
C(s)+O2(g)=CO2(g) ΔH=﹣393.5 kJ·mol−1
则汽车尾气处理的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=_____ kJ·mol−1,利于该反应自发进行的条件是_______ (选填“高温”或“低温”)。
(2)将0.20mol NO和0.10mol CO充入一个容积恒定为1L的密闭容器中发生反应:2NO(g)+2CO(g) N2(g)+2CO2(g),反应过程中部分物质的浓度变化如图所示:
N2(g)+2CO2(g),反应过程中部分物质的浓度变化如图所示:
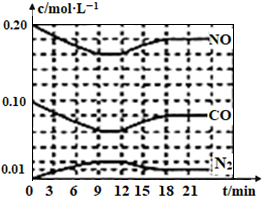
①反应从开始到9min时,用CO2表示该反应的速率是_______ (保留2位有效数字)
②第12min时改变的条件是__________ (填“升温或降温”)。
③第18min时建立新的平衡,此温度下的平衡常数为_________ (列计算式),第24min时,若保持温度不变,再向容器中充入CO和N2各0.060mol,平衡将_____ 移动(填“正向”、“逆向”或“不”)。
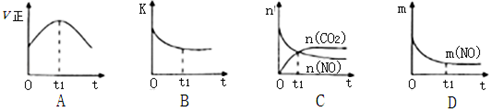
(3)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在t1时刻达到平衡状态的是__ (填序号)。
(如图中v正、K、n、m分别表示正反应速率、平衡常数、物质的量和质量)
(1)已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5 kJ·mol−1
2C(s)+O2(g)=2CO(g) ΔH=﹣221.0 kJ·mol−1
C(s)+O2(g)=CO2(g) ΔH=﹣393.5 kJ·mol−1
则汽车尾气处理的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=
(2)将0.20mol NO和0.10mol CO充入一个容积恒定为1L的密闭容器中发生反应:2NO(g)+2CO(g)
 N2(g)+2CO2(g),反应过程中部分物质的浓度变化如图所示:
N2(g)+2CO2(g),反应过程中部分物质的浓度变化如图所示:
①反应从开始到9min时,用CO2表示该反应的速率是
②第12min时改变的条件是
③第18min时建立新的平衡,此温度下的平衡常数为
(3)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在t1时刻达到平衡状态的是
(如图中v正、K、n、m分别表示正反应速率、平衡常数、物质的量和质量)

您最近一年使用:0次
19-20高三·浙江·阶段练习
解题方法
5 . 氢碘酸和氯水反应的能量关系如图所示。
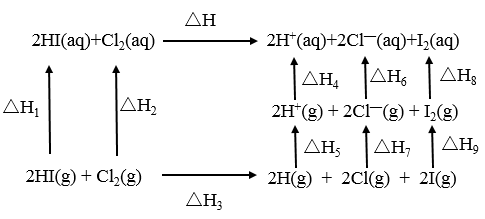
下列说法正确的是

下列说法正确的是
| A.已知HI气体溶于水放热,则ΔH1 <0 |
| B.ΔH = ΔH1 +ΔH2 + ΔH3 +ΔH4 +ΔH5 +ΔH6+ΔH7 +ΔH8 +ΔH9 |
| C.已知ΔH <0,则ΔH3 <0 |
| D.ΔH9 >0 |
您最近一年使用:0次
名校
6 . 戴口罩是防控新型冠状病毒的重要手段,口罩生产的主要原料聚丙烯由丙烯聚合而来。丙烷脱氢是丙烯工业生产的重要途径。反应的热化学方程式为C3H8(g) C3H6(g)+H2(g) △H>0。回答下列问题:
C3H6(g)+H2(g) △H>0。回答下列问题:
(1)从工业生产的角度来看。制备丙烯所用的丙烷可以从下面工业气体中获得的是___ 。
A.液化石油气 B.炼铁高炉尾气 C.水煤气 D.焦炉气
(2)104Pa、105Pa时由一定量丙烷脱氢制丙烯,反应在不同温度下达到平衡,测得丙烷、丙烯的物质的量分数变化关系如图所示。

①104Pa时丙烷及丙烯的物质的量分数随温度变化关系的曲线分别是___ 、___ 。
②丙烷脱氢制丙烯反应在___ (选“高温”或“低温”)时更加容易自发进行。
③起始时充入一定量的丙烷发生反应,计算Q点对应温度下该反应的平衡常数KP=___ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)一种丙烷脱氢制丙烯工艺生产中增加了氧化脱氢部分,O2被引入到脱氢反应体系中,这样做的好处是___ 。
(4)利用CO2的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。其反应机理如图所示。

已知:CO和C3H4、C3H6的燃烧热△H分别为-283•0kJ•mol-1、-2217.8kJ•mol-1、-2049.0kJ•mol-1。
②298K时,该工艺总反应的热化学方程式为___ 。
②该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是___ 。
 C3H6(g)+H2(g) △H>0。回答下列问题:
C3H6(g)+H2(g) △H>0。回答下列问题:(1)从工业生产的角度来看。制备丙烯所用的丙烷可以从下面工业气体中获得的是
A.液化石油气 B.炼铁高炉尾气 C.水煤气 D.焦炉气
(2)104Pa、105Pa时由一定量丙烷脱氢制丙烯,反应在不同温度下达到平衡,测得丙烷、丙烯的物质的量分数变化关系如图所示。

①104Pa时丙烷及丙烯的物质的量分数随温度变化关系的曲线分别是
②丙烷脱氢制丙烯反应在
③起始时充入一定量的丙烷发生反应,计算Q点对应温度下该反应的平衡常数KP=
(3)一种丙烷脱氢制丙烯工艺生产中增加了氧化脱氢部分,O2被引入到脱氢反应体系中,这样做的好处是
(4)利用CO2的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。其反应机理如图所示。

已知:CO和C3H4、C3H6的燃烧热△H分别为-283•0kJ•mol-1、-2217.8kJ•mol-1、-2049.0kJ•mol-1。
②298K时,该工艺总反应的热化学方程式为
②该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是
您最近一年使用:0次
2020-08-28更新
|
544次组卷
|
5卷引用:山西省大同市第一中学2021届高三上学期期中质量检测化学试题
山西省大同市第一中学2021届高三上学期期中质量检测化学试题河南省洛阳市2020届高三第三次统一考试理综化学试题(已下线)专题14 化学反应原理综合-2020年高考真题和模拟题化学分项汇编河南省洛阳市2020届高三三模化学试卷江西省吉安一中2021-2022学年高二上学期第一次段考化学试题
7 . 探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.
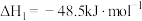
Ⅱ.
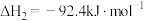
Ⅲ.
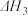
回答下列问题:
(1)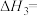
_________  。
。
(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为ɑ mol,CO为b mol,此时H2(g)的浓度为__________ mol﹒L-1(用含a、b、V的代数式表示,下同),反应Ⅲ的平衡常数为___________ 。
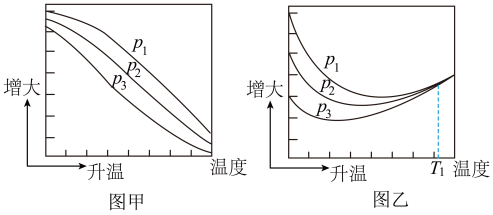
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。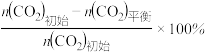
CH3OH的平衡产率=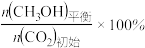
其中纵坐标表示CO2平衡转化率的是图___________ (填“甲”或“乙”);压强p1、p2、p3由大到小的顺序为___________ ;图乙中T1温度时,三条曲线几乎交于一点的原因是___________ 。
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_________ (填标号)。
A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压
Ⅰ.

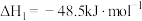
Ⅱ.

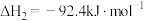
Ⅲ.

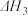
回答下列问题:
(1)
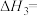
 。
。(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH3OH(g)为ɑ mol,CO为b mol,此时H2(g)的浓度为
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如下图所示。
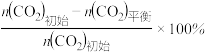
CH3OH的平衡产率=
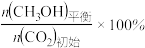
其中纵坐标表示CO2平衡转化率的是图
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为
A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压
您最近一年使用:0次
2020-07-11更新
|
11092次组卷
|
23卷引用:山西省长治市第二中学校2021-2022学年高二上学期期中考试化学试题
山西省长治市第二中学校2021-2022学年高二上学期期中考试化学试题黑龙江省哈尔滨市德强高中2021-2022学年高二上学期期中考试化学试题湖北省武汉市常青联合体2022-2023学年高二上学期期中考试化学试题2020年山东省高考化学试卷(新高考)(已下线)专题09 反应速率、化学平衡-2020年高考真题和模拟题化学分项汇编西藏自治区拉萨市拉萨中学2021届高三第一次月考理综化学试题湖南师范大学附属中学2020-2021学年高二上学期第三次大练习化学试题福建省宁德市2020-2021学年高二上学期期末考试化学试题江苏省扬州中学2020-2021学年高二下学期开学检测化学试题四川省邻水实验学校2021届高三下学期3月开学考试理综化学试题(已下线)重点9 化学反应原理的综合应用-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)重点8 化学反应原理的综合应用-2021年高考化学专练【热点·重点·难点】(已下线)押山东卷第18题 化学反应原理综合题-备战2021年高考化学临考题号押题(山东卷)湖南省长沙市第一中学2020-2021学年高二上学期入学考试化学试题(已下线)专题15 化学反应原理综合-备战2022年高考化学真题及地市好题专项集训【山东专用】(已下线)专题12 化学反应原理综合题—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)押新高考卷17题 化学反应原理综合题-备战2022年高考化学临考题号押题(新高考通版)(已下线)2022年全国甲卷高考真题变式题(非选择题)(已下线)2020年山东卷化学高考真题变式题16-20(已下线)2022年全国乙卷高考变式题(非选择题)(已下线)第20讲 化学平衡常数及转化率的计算(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第10讲 影响化学平衡的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)专题17 原理综合题
10-11高二上·福建福州·期中
名校
解题方法
8 . 在一定温度下,CO和CH4燃烧的热化学方程式分别为
2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890kJ/mol
1molCO和3molCH4组成的混合气体,在相同条件下完全燃烧时,释放的热量为( )
2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890kJ/mol
1molCO和3molCH4组成的混合气体,在相同条件下完全燃烧时,释放的热量为( )
| A.2912kJ | B.2953kJ | C.3236kJ | D.3867kJ |
您最近一年使用:0次
2020-01-23更新
|
780次组卷
|
37卷引用:2015-2016学年山西省右玉一中高一下学期期中考试化学试卷
2015-2016学年山西省右玉一中高一下学期期中考试化学试卷(已下线)2010年福建省福州市八县(市)协作校第一学期期中联考高二理科化学试卷(已下线)2011-2012学年浙江省东阳市南马高中高一下学期期中考试化学试卷(已下线)2013-2014学年浙江省平阳中学高一下学期期中考试化学试卷2014-2015学年福建省泉州一中高二上学期期中考试化学试卷2014-2015学年河北省唐山市开滦第二中学高一下学期期中化学试卷河北省唐山市滦县二中2017-2018学年高二期中考试化学(理)试卷福建省长泰县第一中学2017-2018学年高二上学期期中考试(理)化学试题浙江省温州市求知中学2018-2019学年高二上学期期中考试(选考)化学试题江西省宜春市宜丰县第二中学2019-2020学年高二上学期期中考试化学试题福建省莆田市涵江区莆田第七中学2020-2021学年高二上学期期中考试化学试题(Ⅰ)山西省太原市第五十六中学2021-2022学年高二上学期10月月考化学试题山西省太原市第五十六中学2022-2023学年高二上学期10月联考化学试题(已下线)2010-2011年江苏省扬州中学高一下学期期末考试化学试卷(已下线)2013-2014学年贵州省遵义四中高二上学期期末考试化学试卷(已下线)2015安徽望江中学同步课时练(人教选修4)第一章检测试卷2016-2017学年西藏拉萨中学高二上第一次月考化学试卷2016-2017学年贵州省思南中学高二上半期考试化学卷吉林省辽源市田家炳高级中学2018-2019学年高二9月月考化学试题贵州省遵义市航天高级中学2018-2019学年高二(理)上学期第一次月考化学试题【全国百强校】贵州省遵义航天高级中学2018-2019学年高二上学期第一次月考化学试题黑龙江省齐齐哈尔市第八中学2019-2020学年高二9月月考化学试题山东省新泰二中2019-2020学年高二上学期第一次阶段性考试化学试题吉林省东辽五中2019-2020学年高二上学期9月月考化学试题安徽省滁州市定远县育才学校2019-2020学年高二(实验班)上学期第三次月考化学试题甘肃省古浪县第二中学2019-2020学年高二上学期基础知识竞赛化学试题陕西省宝鸡市渭滨区2019—2020学年高二上学期期末考试化学试题四川省南充市阆中中学2020届高三化学选择题专项训练(9)(已下线)第01章 化学反应与能量(B卷提升篇)——2020-2021学年高二化学选修四同步单元AB卷(人教版)河南省三门峡市第一高级中学2020-2021学年高二上学期9月月考化学试题陕西省延安市第一中学2020-2021学年高二上学期第一次月考化学试题青海省西宁市海湖中学2020-2021学年高二上学期第一阶段测试化学试题宁夏长庆高级中学2020-2021学年高二上学期第一次月考化学试题广东省湛江市雷州市第二中学2020-2021学年高二上学期第一次月考化学试题辽宁省阜新市第二高级中学2020-2021学年高二上学期第二次月考化学试题贵州省贵阳市清镇养正学校2020-2021学年高二上学期第一次月考化学试题1.1.2反应热的测量与计算 课前
解题方法
9 . “二青会”火炬塔中使用的燃料是天然气,主要成分是甲烷,作为一种洁净环保的优质能源,几乎不含硫、粉尘和其他有害物质。
(1)已知:CH4的燃烧热为ΔH=-890kJ•mol-1,CO的燃烧热为ΔH=-283kJ•mol-1
①深海中存在一种甲烷细菌,它们依靠酶使甲烷与O2作用产生的能量存活。常温常压下,甲烷细菌使1mol甲烷生成CO2气体和液态水,放出的能量___ (填“<”“>”或“=”)890kJ。
②写出1molCH4(g)不完全燃烧生成CO(g)和H2O(l)的热化学方程式___ 。
(2)甲烷与CO2可用于制备合成气(主要成分是一氧化碳和氢气):CH4(g)+CO2(g)=2CO(g)+2H2(g),1gCH4(g)参加以上反应可释放15.46kJ的热量,则如图中能表示该反应过程中能量变化的是___ (填字母)。

(3)甲烷转化为CO和H2的反应为:CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH>0
①在一定条件下,CH4的平衡转化率与温度、压强的关系如图所示。则p1___ p2(填“<”“>”或“=”);A、B、C三点处对应的平衡常数(KA、KB、KC)由大到小的顺序为___ 。
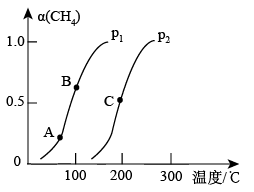
②在恒温恒压的密闭容器中,下列各项能作为判断该反应达到化学平衡状态依据的是___ (填字母)。
a.v(CH4)=v(CO)
b.混合气体的密度不发生变化
c.容器内混合气体的总压强不发生变化
d.一段时间内,用CH4表示的平均反应速率等于零
③将CH4和H2O(g)按等物质的量混合,一定条件下反应达到平衡,CH4的转化率为50%,则反应前与平衡后,混合气体的平均相对分子质量之比为___ 。
(4)甲烷可以合成甲醇来代替日益供应紧张的燃油。工业上用甲烷为原料制备甲醇分为两个阶段:
①制备合成气:CH4(g)+H2O(g)⇌CO(g)+3H2(g)。
②合成甲醇:CO(g)+2H2(g)⇌CH3OH(g)。实验室在恒温(500℃)、恒容(1L)密闭容器中进行模拟合成实验。将1molCO和2molH2通入容器中,10min、40min、50min时分别测得容器中甲醇的浓度为0.60mol•L-1、0.80mol•L-1、0.80mol•L-1。则此条件下该反应开始10min内,H2的平均反应速率为__ ;平衡常数K的数值为___ 。
(1)已知:CH4的燃烧热为ΔH=-890kJ•mol-1,CO的燃烧热为ΔH=-283kJ•mol-1
①深海中存在一种甲烷细菌,它们依靠酶使甲烷与O2作用产生的能量存活。常温常压下,甲烷细菌使1mol甲烷生成CO2气体和液态水,放出的能量
②写出1molCH4(g)不完全燃烧生成CO(g)和H2O(l)的热化学方程式
(2)甲烷与CO2可用于制备合成气(主要成分是一氧化碳和氢气):CH4(g)+CO2(g)=2CO(g)+2H2(g),1gCH4(g)参加以上反应可释放15.46kJ的热量,则如图中能表示该反应过程中能量变化的是

(3)甲烷转化为CO和H2的反应为:CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH>0
①在一定条件下,CH4的平衡转化率与温度、压强的关系如图所示。则p1

②在恒温恒压的密闭容器中,下列各项能作为判断该反应达到化学平衡状态依据的是
a.v(CH4)=v(CO)
b.混合气体的密度不发生变化
c.容器内混合气体的总压强不发生变化
d.一段时间内,用CH4表示的平均反应速率等于零
③将CH4和H2O(g)按等物质的量混合,一定条件下反应达到平衡,CH4的转化率为50%,则反应前与平衡后,混合气体的平均相对分子质量之比为
(4)甲烷可以合成甲醇来代替日益供应紧张的燃油。工业上用甲烷为原料制备甲醇分为两个阶段:
①制备合成气:CH4(g)+H2O(g)⇌CO(g)+3H2(g)。
②合成甲醇:CO(g)+2H2(g)⇌CH3OH(g)。实验室在恒温(500℃)、恒容(1L)密闭容器中进行模拟合成实验。将1molCO和2molH2通入容器中,10min、40min、50min时分别测得容器中甲醇的浓度为0.60mol•L-1、0.80mol•L-1、0.80mol•L-1。则此条件下该反应开始10min内,H2的平均反应速率为
您最近一年使用:0次
解题方法
10 . 全国农村应当在“绿色生态・美丽多彩・低碳节能・循环发展”的理念引导下,更快更好地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设。试回答下列问题:
(1)碳的单质及其部分化合物是人类生产生活的主要能源物质。
①有机物M经过太阳光光照可转化成N,转化过程如图
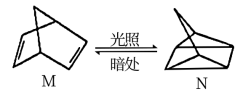
△H=+886kJ/mol,则M、N相比,较稳定的是___ 。
②将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s),△H=-1176kJ/mol,则反应过程中,每转移1mol电子放出的热量为___ 。
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:FeO(s)+CO(g)⇌Fe(s)+CO2(g),△H>0。已知在1100℃时,该反应的平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值__ (填“增大”、“减小”或“不变”)。
②1100℃时测得高炉中,c(CO2)=0.025mol/L,c(CO)=0.1mol/L,则在这种情况下,该反应是否处于化学平衡状态?___ 。(填“是”或“否”),其判断依据是___ 。
(3)目前工业上可用CO2来生产燃料甲醇,有关反应为CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),△H=-50.0kJ/mol。现向容积为1L的密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
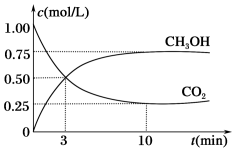
①该反应到达平衡后,H2的转化率α(H2)=____ 。
②下列措施能使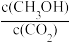 增大的是(填字母)
增大的是(填字母)___ 。
A.升高温度
B.再充入H2
C.再充入CO2
D.将H2O(g)从体系中分离
E.充入He(g),使体系压强增大
③下列各项能作为判断该反应达到化学平衡状态依据的是___ (填字母)。
A.v正(CH3OH)=3v逆(H2)
B.平衡混合物中各组分的含量不再变化
C.CO2和H2的浓度比为1:2
D.混合气体的密度不再变化
(1)碳的单质及其部分化合物是人类生产生活的主要能源物质。
①有机物M经过太阳光光照可转化成N,转化过程如图

△H=+886kJ/mol,则M、N相比,较稳定的是
②将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s),△H=-1176kJ/mol,则反应过程中,每转移1mol电子放出的热量为
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:FeO(s)+CO(g)⇌Fe(s)+CO2(g),△H>0。已知在1100℃时,该反应的平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值
②1100℃时测得高炉中,c(CO2)=0.025mol/L,c(CO)=0.1mol/L,则在这种情况下,该反应是否处于化学平衡状态?
(3)目前工业上可用CO2来生产燃料甲醇,有关反应为CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),△H=-50.0kJ/mol。现向容积为1L的密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。

①该反应到达平衡后,H2的转化率α(H2)=
②下列措施能使
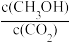 增大的是(填字母)
增大的是(填字母)A.升高温度
B.再充入H2
C.再充入CO2
D.将H2O(g)从体系中分离
E.充入He(g),使体系压强增大
③下列各项能作为判断该反应达到化学平衡状态依据的是
A.v正(CH3OH)=3v逆(H2)
B.平衡混合物中各组分的含量不再变化
C.CO2和H2的浓度比为1:2
D.混合气体的密度不再变化
您最近一年使用:0次



