1 . 工业废气中的硫化氢是一种无色有毒的气体。根据硫化氢的性质,可采取不同的处理方法。
(1)氧化法(克劳斯法),其原理是:
H2S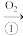 SO2
SO2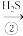 S
S
S(s)+O2(g)=SO2(g) ∆H=-297kJ·mol-1
第②步反应的热化学方程式为___________ 。
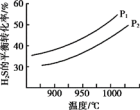
(2)热分解法,其原理是:2H2S(g) S2(?)+2H2(g)。不同温度和压强下,H2S的平衡转化率变化如图。P1
S2(?)+2H2(g)。不同温度和压强下,H2S的平衡转化率变化如图。P1___________ P2(填“>”或“<”),原因是___________ 。
(3)直接电解法,可回收S和H2。

资料:
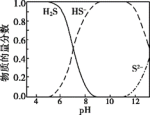
ⅰ.H2S溶液中含硫微粒的物质的量分数随pH变化如图。
ⅱ.(x-1)S+S2− S
S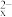 (黄色溶液);S
(黄色溶液);S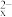 与酸反应生成S。
与酸反应生成S。
①直接电解H2S酸性溶液(pH≈5),容易出现电解反应不能持续进行的情况,结合电极反应式分析其可能的原因___________ 。
②工业上,常用烧碱吸收H2S,将吸收后的溶液(pH=13.2)先进行电解,再用电解后的黄色溶液吸收H2S生成S。反应生成S的离子方程式是___________ 。
(4)间接电解法。先用FeCl3溶液吸收含H2S的工业废气,所得溶液用惰性电极进行电解。
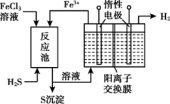
①反应池中发生反应的离子方程式是___________ 。
②该装置实验有两个显著优点:a.H2S的原子利用率100%;b.___________ 。
(5)碱性溶液吸收法。
已知:25℃时,H2S的电离常数Ka1=9.1×10-8、Ka2=1.1×10-12;H2CO3的电离常数Ka1=4.3×10-7、Ka2=5.6×10-11。用Na2CO3溶液吸收含H2S的工业废气,反应的离子方程式是___________ 。
(1)氧化法(克劳斯法),其原理是:
H2S
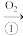 SO2
SO2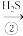 S
S已知:2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) ΔH=-1172kJ·mol-1
S(s)+O2(g)=SO2(g) ∆H=-297kJ·mol-1
第②步反应的热化学方程式为
(2)热分解法,其原理是:2H2S(g)
 S2(?)+2H2(g)。不同温度和压强下,H2S的平衡转化率变化如图。P1
S2(?)+2H2(g)。不同温度和压强下,H2S的平衡转化率变化如图。P1
(3)直接电解法,可回收S和H2。

资料:
ⅰ.H2S溶液中含硫微粒的物质的量分数随pH变化如图。

ⅱ.(x-1)S+S2−
 S
S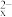 (黄色溶液);S
(黄色溶液);S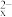 与酸反应生成S。
与酸反应生成S。①直接电解H2S酸性溶液(pH≈5),容易出现电解反应不能持续进行的情况,结合电极反应式分析其可能的原因
②工业上,常用烧碱吸收H2S,将吸收后的溶液(pH=13.2)先进行电解,再用电解后的黄色溶液吸收H2S生成S。反应生成S的离子方程式是
(4)间接电解法。先用FeCl3溶液吸收含H2S的工业废气,所得溶液用惰性电极进行电解。

①反应池中发生反应的离子方程式是
②该装置实验有两个显著优点:a.H2S的原子利用率100%;b.
(5)碱性溶液吸收法。
已知:25℃时,H2S的电离常数Ka1=9.1×10-8、Ka2=1.1×10-12;H2CO3的电离常数Ka1=4.3×10-7、Ka2=5.6×10-11。用Na2CO3溶液吸收含H2S的工业废气,反应的离子方程式是
您最近一年使用:0次
名校
2 . 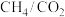 催化重整的反应为
催化重整的反应为
①

其中,积炭是导致催化剂失活的主要原因。产生积炭的反应有:
②
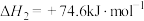
③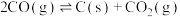
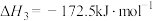
科研人员研究压强对催化剂活性的影响:在1073K时,将恒定组成的 、
、 混合气体,以恒定流速通过反应器,测得数据如下。
混合气体,以恒定流速通过反应器,测得数据如下。

下列分析不正确 的是
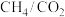 催化重整的反应为
催化重整的反应为①


其中,积炭是导致催化剂失活的主要原因。产生积炭的反应有:
②

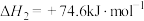
③
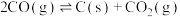
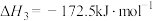
科研人员研究压强对催化剂活性的影响:在1073K时,将恒定组成的
 、
、 混合气体,以恒定流速通过反应器,测得数据如下。
混合气体,以恒定流速通过反应器,测得数据如下。
下列分析
A.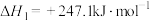 |
| B.压强越大,Ra降低越快,其主要原因是反应①平衡逆向移动 |
C.保持其他条件不变,适当增大投料时 ,可减缓Ra的衰减 ,可减缓Ra的衰减 |
D.研究表明“通入适量 有利于重整反应”,因为 有利于重整反应”,因为 能与C反应并放出热量 能与C反应并放出热量 |
您最近一年使用:0次
2023-11-30更新
|
148次组卷
|
6卷引用:北京市东城区2023届一模考试化学试题
19-20高三上·北京石景山·期末
名校
解题方法
3 . 已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.0 kJ/mol。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下:
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2 kJ/mol
过程Ⅱ:…
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2 kJ/mol
过程Ⅱ:…
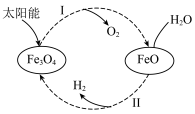
| A.过程Ⅰ中每消耗232 g Fe3O4转移2 mol电子 |
| B.过程Ⅱ的热化学方程式为3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+128.9 kJ/mol |
| C.过程Ⅰ、Ⅱ中能量转化的形式依次是太阳能→化学能→热能 |
| D.铁氧化合物循环制H2具有成本低、产物易分离等优点 |
您最近一年使用:0次
2023-09-19更新
|
359次组卷
|
25卷引用:《2020年新高考政策解读与配套资源》模拟试题10-2020年北京新高考化学模拟试题
(已下线)《2020年新高考政策解读与配套资源》模拟试题10-2020年北京新高考化学模拟试题【区级联考】北京市石景山区2019届高三第一学期期末考试化学试题辽宁省锦州市滨海实验中学2019-2020学年高三上学期期末考试化学试题海南省海南中学2019-2020学年高二上学期期末考试化学试题(已下线)专题九 化学能与热能(提分特训)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训甘肃省天水市甘谷第一中学2019-2020学年高二下学期开学考试化学试题鲁科版(2019)选择性必修1第1章 化学反应与能量转化 第1节综合训练高中必刷题高二选择性必修1第一章 化学反应的热效应 第二节 反应热的计算 第二节综合训练河北省沧州市泊头市第一中学2020-2021学年高二上学期第一次月考化学试题山东省德州市夏津第一中学2020-2021学年高二上学期9月月考化学试题辽源市第五中学2019-2020学年高一下学期第二次月考化学试题湖南省中方一中2020-2021学年高二上学期期中考试化学试题河北省沧州市黄骅中学2020-2021学年高二上学期第三次月考化学试题河南省鹤壁市高级中学2020-2021学年高二上学期尖子生联赛调研二化学试题河北省安平中学2020-2021学年高一下学期第四次月考(期末)化学试题(已下线)模块七 化学反应与能量(模块检测)-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第一单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)贵州省黔西南州赛文高级中学 2021-2022学年高二上学期期中考试化学试题河北省沧州市泊头市第一中学2021-2022学年高二上学期第一次月考化学试题天津市第二中学2022-2023学年高二上学期期中检测化学试题(已下线)第七章 化学反应速率与化学平衡 热点强化12 化学反应历程、机理的分析应用(已下线)题型98 结合反应能量图示或物质循环图示书写热化学方程式山东省烟台市招远第一中学2022-2023学年高一下学期期中考试化学(等级考)试题(已下线)章末综合评价(六)河南省洛阳市宜阳县第一高级中学清北园2023-2024学年高一上学期第七次能力达标测试化学试卷
名校
4 .  资源化利用是解决资源和能源短缺、减少碳排放的一种途径。
资源化利用是解决资源和能源短缺、减少碳排放的一种途径。
I. 制甲醇,过程如下:
制甲醇,过程如下:
i.催化剂活化:
ii. 与
与 在活化后的催化剂表面可逆的发生反应①,其反应历程如图1,同时伴随反应②:
在活化后的催化剂表面可逆的发生反应①,其反应历程如图1,同时伴随反应②:



(1)反应①每生成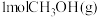 放热
放热 ,写出其热化学方程式:
,写出其热化学方程式:___________ 。
(2) 与
与 混合气体以不同的流速通过反应器,气体流速与
混合气体以不同的流速通过反应器,气体流速与 转化率、
转化率、 选择性的关系如图2。
选择性的关系如图2。
已知: 选择性=n(生成
选择性=n(生成 所用的
所用的 )/n(转化的
)/n(转化的 )。
)。
流速加快可减少产物中 的积累,减少反应
的积累,减少反应___________ (用化学方程式表示)的发生,减少催化剂的失活,提高甲醇选择性。
(3)对于以上 制甲醇的过程,以下描述正确的是
制甲醇的过程,以下描述正确的是___________ (填序号)。
A.反应中经历了 键的形成和断裂
键的形成和断裂
B.加压可以提高 的平衡转化率
的平衡转化率
C.升高温度可以提高甲醇在平衡时的选择性
Ⅱ.一种以甲醇和二氧化碳为原料,利用 和
和 纳米片
纳米片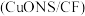 作催化电极,电化学法制备甲酸(甲酸盐)的工作原理如图所示。
作催化电极,电化学法制备甲酸(甲酸盐)的工作原理如图所示。

(4)①b极为直流电源的___________ 极,阴极表面发生的电极反应式为___________ 。
②若有 通过质子交换膜时,生成
通过质子交换膜时,生成 和
和 共
共___________ mol。
 资源化利用是解决资源和能源短缺、减少碳排放的一种途径。
资源化利用是解决资源和能源短缺、减少碳排放的一种途径。I.
 制甲醇,过程如下:
制甲醇,过程如下:i.催化剂活化:

ii.
 与
与 在活化后的催化剂表面可逆的发生反应①,其反应历程如图1,同时伴随反应②:
在活化后的催化剂表面可逆的发生反应①,其反应历程如图1,同时伴随反应②:



(1)反应①每生成
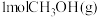 放热
放热 ,写出其热化学方程式:
,写出其热化学方程式:(2)
 与
与 混合气体以不同的流速通过反应器,气体流速与
混合气体以不同的流速通过反应器,气体流速与 转化率、
转化率、 选择性的关系如图2。
选择性的关系如图2。已知:
 选择性=n(生成
选择性=n(生成 所用的
所用的 )/n(转化的
)/n(转化的 )。
)。流速加快可减少产物中
 的积累,减少反应
的积累,减少反应(3)对于以上
 制甲醇的过程,以下描述正确的是
制甲醇的过程,以下描述正确的是A.反应中经历了
 键的形成和断裂
键的形成和断裂B.加压可以提高
 的平衡转化率
的平衡转化率C.升高温度可以提高甲醇在平衡时的选择性
Ⅱ.一种以甲醇和二氧化碳为原料,利用
 和
和 纳米片
纳米片 作催化电极,电化学法制备甲酸(甲酸盐)的工作原理如图所示。
作催化电极,电化学法制备甲酸(甲酸盐)的工作原理如图所示。
(4)①b极为直流电源的
②若有
 通过质子交换膜时,生成
通过质子交换膜时,生成 和
和 共
共
您最近一年使用:0次
2023-05-31更新
|
343次组卷
|
4卷引用:北京市朝阳区2023届高三下学期三模化学试题
5 . 碳酸钠晶体( )失水可得到
)失水可得到 或
或 ,两个化学反应的能量变化示意图如下:
,两个化学反应的能量变化示意图如下:

下列说法不正确 的是
 )失水可得到
)失水可得到 或
或 ,两个化学反应的能量变化示意图如下:
,两个化学反应的能量变化示意图如下:
下列说法
A.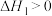 |
B.碳酸钠晶体( )失水是化学变化 )失水是化学变化 |
C.向 中滴加几滴水,温度升高 中滴加几滴水,温度升高 |
D. 失水生成 失水生成 : :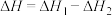 |
您最近一年使用:0次
2023-05-13更新
|
1219次组卷
|
8卷引用:北京市房山区2022-2023学年高三二模化学试题
北京市房山区2022-2023学年高三二模化学试题北京工业大学附属中学2023-2024学年高二上学期期中考试化学试题(已下线)题型13 突破反应热图象(已下线)专题08 化学反应中的能量变化(已下线)第12练 有关反应热的综合考查 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)【知识图鉴】单元讲练测选择性必修1第1单元02基础练河北省石家庄市第一中学2022-2023学年高一下学期7月期末化学试题上海市奉贤中学2023-2024学年高二上学期12月练习化学试题
名校
解题方法
6 . 光解水制氢的关键步骤是水的氧化。我国科学家用仿生催化剂[用 表示]实现在NaHCO3溶液中高效催化水的氧化,该过程物质转化及反应能量变化示意图如下:
表示]实现在NaHCO3溶液中高效催化水的氧化,该过程物质转化及反应能量变化示意图如下:不正确 的是
 表示]实现在NaHCO3溶液中高效催化水的氧化,该过程物质转化及反应能量变化示意图如下:
表示]实现在NaHCO3溶液中高效催化水的氧化,该过程物质转化及反应能量变化示意图如下: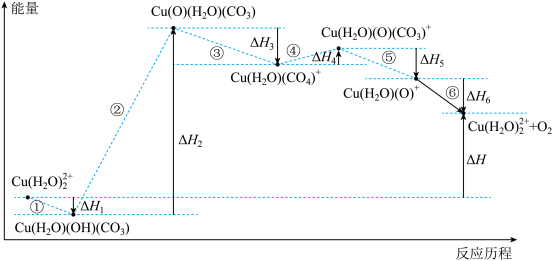
A.步骤①可表示为 |
B.水的氧化反应为: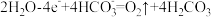 |
C.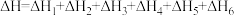 |
| D.催化剂参与反应,降低活化能,加快反应速率 |
您最近一年使用:0次
2023-05-07更新
|
1264次组卷
|
9卷引用:北京市海淀区2022-2023学年高三第二次模拟(下学期期末)考试化学试题
北京市海淀区2022-2023学年高三第二次模拟(下学期期末)考试化学试题福建省厦门第一中学2023届高三下学期模拟考试化学试题北京交通大学附属中学2023-2024学年高三下学期3月月考化学试题湖北省武汉市洪山高级中学2024届高三下学期第 2次模拟考试化学试卷 (已下线)专题08 化学反应中的能量变化(已下线)第12练 有关反应热的综合考查 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题09 化学反应中的热效应与反应机理-2023年高考化学真题题源解密(全国通用)(已下线)考点1 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)选择题16-20
名校
7 . 下列三个化学反应焓变、平衡常数与温度的关系分别如下表所示。下列说法正确的是
| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
①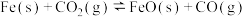  |  | 1.47 | 2.15 |
②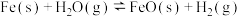  |  | 2.38 | 1.67 |
③  |  | a | b |
A.1173K时,反应①起始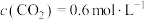 ,平衡时 ,平衡时 约为0.4 约为0.4 |
B.反应②是吸热反应, |
| C.反应③达平衡后,升高温度或缩小反应容器的容积平衡逆向移动 |
D.相同温度下, ; ;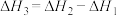 |
您最近一年使用:0次
2023-03-24更新
|
727次组卷
|
7卷引用:北京市丰台区2022-2023学年高三下学期第一次模拟练习化学试题
北京市丰台区2022-2023学年高三下学期第一次模拟练习化学试题(已下线)专题15 化学反应速率和化学平衡海南省海南中学2023届高三下学期第三次模拟考试化学试题北京市第一六一中学2023-2024学年高三上学期12月月考化学试题北京市顺义区第二中学2023-2024学年高三下学期3月月考化学试题湖北省黄冈市重点校2022-2023学年高一下学期期末综合选拔性联考化学试题(已下线)题型13 化学平衡常数的计算及应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
8 . CO2催化加氢制CH4的反应为: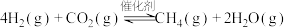 。催化剂上反应过程示意如图1所示。其他条件不变时,CO2的转化率和CH4的选择性(CO2转化为甲烷的量/ CO2转化的总量)随温度变化如图2所示。下列说法不正确的是
。催化剂上反应过程示意如图1所示。其他条件不变时,CO2的转化率和CH4的选择性(CO2转化为甲烷的量/ CO2转化的总量)随温度变化如图2所示。下列说法不正确的是
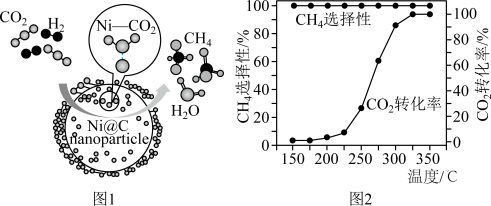
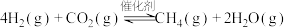 。催化剂上反应过程示意如图1所示。其他条件不变时,CO2的转化率和CH4的选择性(CO2转化为甲烷的量/ CO2转化的总量)随温度变化如图2所示。下列说法不正确的是
。催化剂上反应过程示意如图1所示。其他条件不变时,CO2的转化率和CH4的选择性(CO2转化为甲烷的量/ CO2转化的总量)随温度变化如图2所示。下列说法不正确的是
A.催化剂改变了 中O—C—O键的键角 中O—C—O键的键角 |
| B.150℃到350℃时,基本没有发生副反应 |
C. 催化加氢制 催化加氢制 是一个吸热反应 是一个吸热反应 |
D.结合下列热化学方程式,可以通过盖斯定律计算 加氢制 加氢制 的反应热 的反应热 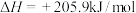 、 、  |
您最近一年使用:0次
2023-03-17更新
|
521次组卷
|
2卷引用:北京市石景山区2022-2023学年高三下学期质量监控(零模)化学试题
名校
9 . 我国提出 2060 年前实现碳中和,为有效降低大气 CO2中的含量,以 CO2为原料制备甲烷、戊烷、甲醇等能源物质具有较好的发展前景。CO2在固体催化剂表面加氢合成甲烷过程中发生如下反应:
Ⅰ.主反应:CO2(g)+4H2(g) CH4(g)+2H2O(g) ∆H1=-156.9 kJ·mol-l
CH4(g)+2H2O(g) ∆H1=-156.9 kJ·mol-l
Ⅱ.副反应:CO2(g)+H2(g) CO(g)+H2O(g) ∆H2=+41.1 kJ·mol-l
CO(g)+H2O(g) ∆H2=+41.1 kJ·mol-l
(1)已知:Ⅲ.2H2(g)+O2(g)=2H2O(g) ∆H3=-395.6 kJ·mol-l
Ⅳ.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ∆H4=__________ 。
(2)CO2加氢合成甲烷时,通常控制温度为 500 °C 左右,其可能的原因为_______。
(3)500 °C 时,向 1 L 恒容密闭容器中充入 4 mol CO2和 12 mol H2,初始压强为 p,20 min 时主、副反应都达到平衡状态,测得 c(H2O)=5 mol·L-1,体系压强为3/4 p, 则 0~ 20 min 内 v(CH4)=________ ,平衡时 CH4选择性= ___________ (CH4选择性= × 100%, 计算保留三位有效数字)。
× 100%, 计算保留三位有效数字)。
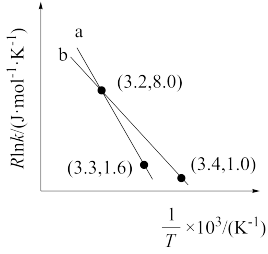
(4)以 CO2催化加氢合成的甲醇为原料,在催化剂作用下可以制取丙烯,反应的化学方程式为 3CH3OH(g) C3H6(g)+3H2O(g)。该反应的 Arrhenius 经验公式的实验数据如图中曲线 a 所示,已知 Arhenius 经验公式
C3H6(g)+3H2O(g)。该反应的 Arrhenius 经验公式的实验数据如图中曲线 a 所示,已知 Arhenius 经验公式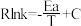 ,(Ea为活化能,k 为速率常数,R 和 C 为常数)。当改变外界条件时,实验数据如图中的曲线 b 所示,则实验可能改变的外界条件是
,(Ea为活化能,k 为速率常数,R 和 C 为常数)。当改变外界条件时,实验数据如图中的曲线 b 所示,则实验可能改变的外界条件是 __________ 。
Ⅰ.主反应:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ∆H1=-156.9 kJ·mol-l
CH4(g)+2H2O(g) ∆H1=-156.9 kJ·mol-lⅡ.副反应:CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2=+41.1 kJ·mol-l
CO(g)+H2O(g) ∆H2=+41.1 kJ·mol-l(1)已知:Ⅲ.2H2(g)+O2(g)=2H2O(g) ∆H3=-395.6 kJ·mol-l
Ⅳ.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ∆H4=
(2)CO2加氢合成甲烷时,通常控制温度为 500 °C 左右,其可能的原因为_______。
| A.反应速率快 | B.平衡转化率高 |
| C.催化剂活性高 | D.主反应催化剂选择性好 |
 × 100%, 计算保留三位有效数字)。
× 100%, 计算保留三位有效数字)。(4)以 CO2催化加氢合成的甲醇为原料,在催化剂作用下可以制取丙烯,反应的化学方程式为 3CH3OH(g)
 C3H6(g)+3H2O(g)。该反应的 Arrhenius 经验公式的实验数据如图中曲线 a 所示,已知 Arhenius 经验公式
C3H6(g)+3H2O(g)。该反应的 Arrhenius 经验公式的实验数据如图中曲线 a 所示,已知 Arhenius 经验公式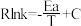 ,(Ea为活化能,k 为速率常数,R 和 C 为常数)。当改变外界条件时,实验数据如图中的曲线 b 所示,则实验可能改变的外界条件是
,(Ea为活化能,k 为速率常数,R 和 C 为常数)。当改变外界条件时,实验数据如图中的曲线 b 所示,则实验可能改变的外界条件是 
您最近一年使用:0次
名校
解题方法
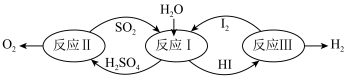
10 . 氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:
(1)已知:






反应I的热化学方程式:_______ 。
(2)反应I所得产物的溶液在碘过量时会自发分成两层。分离两层溶液的实验操作是_______ 。
(3)研究发现,通过电解方法实现反应I,既可减少碘的加入量,也可减少溶液后续纯化过程的能耗。写出通过电解法实现反应I时,阳极的电极反应式:_______ 。
(4)碘硫循环过程中反应I所制备出的HI浓度较低,必须对HI溶液进行浓缩。电解电渗析浓缩HI溶液的原理如下图所示,初始时阳极液和阴极液相同,溶液组成均为n(HI):n(H2O):n(I2)=1:6.8:2。
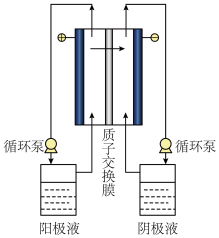
①电渗析过程中,阳极液中I2的浓度会_______ (填“增大”或“减小”)。
②结合化学用语,解释阴极区进行HI浓缩的原理_______ 。
(5)某科研小组采用双极膜电渗析法制备高浓度氢碘酸,工作原理如下图所示。

已知:双极膜在直流电场作用下可将水解离,在双极膜的两侧分别得到H+和OH-。
①X极是_______ (填“阳极”或“阴极”)。
②电解后,_______ 室获得较浓的氢碘酸(填“a”、“b”或“c”)。

(1)已知:






反应I的热化学方程式:
(2)反应I所得产物的溶液在碘过量时会自发分成两层。分离两层溶液的实验操作是
(3)研究发现,通过电解方法实现反应I,既可减少碘的加入量,也可减少溶液后续纯化过程的能耗。写出通过电解法实现反应I时,阳极的电极反应式:
(4)碘硫循环过程中反应I所制备出的HI浓度较低,必须对HI溶液进行浓缩。电解电渗析浓缩HI溶液的原理如下图所示,初始时阳极液和阴极液相同,溶液组成均为n(HI):n(H2O):n(I2)=1:6.8:2。

①电渗析过程中,阳极液中I2的浓度会
②结合化学用语,解释阴极区进行HI浓缩的原理
(5)某科研小组采用双极膜电渗析法制备高浓度氢碘酸,工作原理如下图所示。

已知:双极膜在直流电场作用下可将水解离,在双极膜的两侧分别得到H+和OH-。
①X极是
②电解后,
您最近一年使用:0次
2023-01-11更新
|
360次组卷
|
3卷引用:北京市通州区2022-2023学年高三上学期摸底考试化学试卷



