1 . 下列三个化学反应焓变、平衡常数与温度的关系分别如下表所示。下列说法正确的是
| 化学反应 | 平衡常数 | 温度 | |
 | 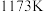 | ||
①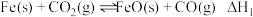 |  | 1.47 | 2.15 |
②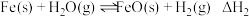 |  | 2.38 | 1.67 |
③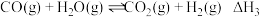 |  | a | b |
| A.反应②是吸热反应 |
| B.反应③达平衡后,升高温度平衡正向移动 |
C.相同温度下,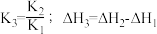 |
D.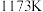 时,若反应①起始 时,若反应①起始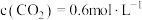 ,平衡时 ,平衡时 约为 约为 |
您最近一年使用:0次
名校
解题方法
2 .  相关转化的研究,对解决环境、能源问题意义重大。
相关转化的研究,对解决环境、能源问题意义重大。
(1) 催化加氢制取汽油,
催化加氢制取汽油, 转化过程示意图如图:
转化过程示意图如图:
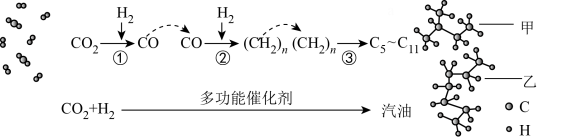
下列说法不正确的是___________ 。
a.反应①的产物中含有水 b.图中甲与乙互为同系物
c.反应②中只有碳碳键形成 d.汽油主要是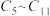 的烃类混合物
的烃类混合物
(2) 与
与 经催化重整可制得合成气:
经催化重整可制得合成气:

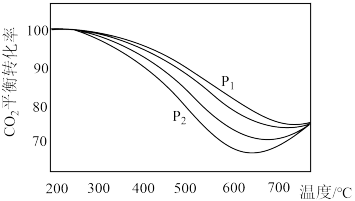
已知: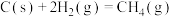
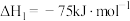
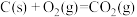



该催化重整反应的
___________  。
。
(3) 与
与 反应制取中醇
反应制取中醇 。
。
已知 与
与 反应生成
反应生成 气体和水蒸气放出
气体和水蒸气放出 的热量。
的热量。
写出 与
与 制取
制取 的热化学方程式
的热化学方程式___________ 。
(4)制取化工原料草酸铝 。
。
利用 电池,能有效地将
电池,能有效地将 转化成草酸铝,工作原理如图所示。
转化成草酸铝,工作原理如图所示。
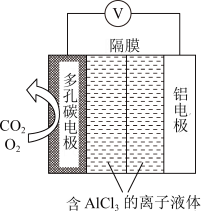
①电池的负极反应式是:___________ 。
②电池的正极反应式: (草酸根)。
(草酸根)。
正极反应过程中, 起催化作用,催化过程可表示为:
起催化作用,催化过程可表示为:
I.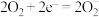
Ⅱ.
写出Ⅱ的离子方程式:___________ 。
 相关转化的研究,对解决环境、能源问题意义重大。
相关转化的研究,对解决环境、能源问题意义重大。(1)
 催化加氢制取汽油,
催化加氢制取汽油, 转化过程示意图如图:
转化过程示意图如图:
下列说法不正确的是
a.反应①的产物中含有水 b.图中甲与乙互为同系物
c.反应②中只有碳碳键形成 d.汽油主要是
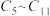 的烃类混合物
的烃类混合物(2)
 与
与 经催化重整可制得合成气:
经催化重整可制得合成气:

已知:
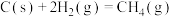
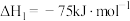
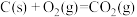



该催化重整反应的

 。
。(3)
 与
与 反应制取中醇
反应制取中醇 。
。已知
 与
与 反应生成
反应生成 气体和水蒸气放出
气体和水蒸气放出 的热量。
的热量。写出
 与
与 制取
制取 的热化学方程式
的热化学方程式(4)制取化工原料草酸铝
 。
。利用
 电池,能有效地将
电池,能有效地将 转化成草酸铝,工作原理如图所示。
转化成草酸铝,工作原理如图所示。
①电池的负极反应式是:
②电池的正极反应式:
 (草酸根)。
(草酸根)。正极反应过程中,
 起催化作用,催化过程可表示为:
起催化作用,催化过程可表示为:I.
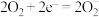
Ⅱ.

写出Ⅱ的离子方程式:
您最近一年使用:0次
名校
3 . 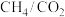 催化重整的反应为
催化重整的反应为
①

其中,积炭是导致催化剂失活的主要原因。产生积炭的反应有:
②
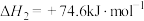
③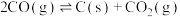
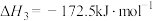
科研人员研究压强对催化剂活性的影响:在1073K时,将恒定组成的 、
、 混合气体,以恒定流速通过反应器,测得数据如下。
混合气体,以恒定流速通过反应器,测得数据如下。

下列分析不正确 的是
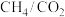 催化重整的反应为
催化重整的反应为①


其中,积炭是导致催化剂失活的主要原因。产生积炭的反应有:
②

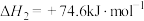
③
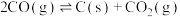
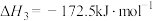
科研人员研究压强对催化剂活性的影响:在1073K时,将恒定组成的
 、
、 混合气体,以恒定流速通过反应器,测得数据如下。
混合气体,以恒定流速通过反应器,测得数据如下。
下列分析
A.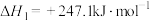 |
| B.压强越大,Ra降低越快,其主要原因是反应①平衡逆向移动 |
C.保持其他条件不变,适当增大投料时 ,可减缓Ra的衰减 ,可减缓Ra的衰减 |
D.研究表明“通入适量 有利于重整反应”,因为 有利于重整反应”,因为 能与C反应并放出热量 能与C反应并放出热量 |
您最近一年使用:0次
2023-11-30更新
|
148次组卷
|
6卷引用:北京市第一○一中学2023-2024学年高三下学期开学考试化学试题
名校
解题方法
4 . 有催化剂的条件下,将 和
和 混合加热可制备
混合加热可制备 。主要的反应有:
。主要的反应有:
Ⅰ.
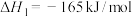
Ⅱ.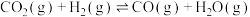

Ⅲ.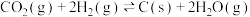
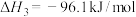
(1) 、
、 、
、 的沸点由高到低的顺序是
的沸点由高到低的顺序是__________ 。
(2)由燃烧热求 。已知
。已知 (g)和CO(g)的燃烧热分别为-285.8kJ/mol、-283kJ/mol。
(g)和CO(g)的燃烧热分别为-285.8kJ/mol、-283kJ/mol。
①要计算 至少还需要一个过程的热效应(该热效应记为
至少还需要一个过程的热效应(该热效应记为 ),则此过程的热化学方程式是
),则此过程的热化学方程式是___________ 。
②
____________ (用含有 的代数式表示)。
的代数式表示)。
(3) 的电子式是
的电子式是__________ ,其中C=O键的键能是799kJ/mol, 中O—H键的键能是463kJ/mol。则,H—H键的键能与C—H的键能相差
中O—H键的键能是463kJ/mol。则,H—H键的键能与C—H的键能相差__________ kJ/mol。
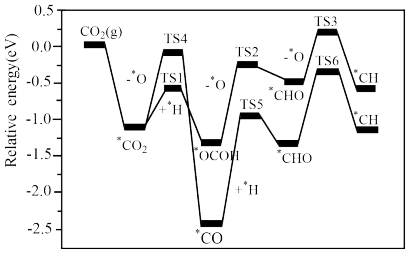
(4) 甲烷化反应的机理大体可归结为两种,如图表示了两种途径每步反应的能量变化(TSx代表过渡态,*表示吸附在催化剂表面的物料),其中速率较快的途径中的决速步的化学方程式是
甲烷化反应的机理大体可归结为两种,如图表示了两种途径每步反应的能量变化(TSx代表过渡态,*表示吸附在催化剂表面的物料),其中速率较快的途径中的决速步的化学方程式是___________________ 。
(5)将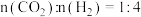 混合气持续以一定的流速通过含催化剂的恒容反应器,测定
混合气持续以一定的流速通过含催化剂的恒容反应器,测定 的转化率和
的转化率和 的选择性随温度的变化关系如图所示。温度高于500℃后,
的选择性随温度的变化关系如图所示。温度高于500℃后, 的转化率几乎保持不变但
的转化率几乎保持不变但 的选择性下降的可能原因是
的选择性下降的可能原因是________________________ 。

(6)不同压强下,保持相同的投料比,测定反应体系中 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如图所示。
的平衡产率随温度的变化关系如图所示。
 时曲线出现拐点的温度高于
时曲线出现拐点的温度高于 时的,原因是
时的,原因是___________________________ 。
 和
和 混合加热可制备
混合加热可制备 。主要的反应有:
。主要的反应有:Ⅰ.

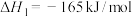
Ⅱ.
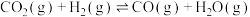

Ⅲ.
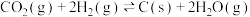
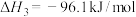
(1)
 、
、 、
、 的沸点由高到低的顺序是
的沸点由高到低的顺序是(2)由燃烧热求
 。已知
。已知 (g)和CO(g)的燃烧热分别为-285.8kJ/mol、-283kJ/mol。
(g)和CO(g)的燃烧热分别为-285.8kJ/mol、-283kJ/mol。①要计算
 至少还需要一个过程的热效应(该热效应记为
至少还需要一个过程的热效应(该热效应记为 ),则此过程的热化学方程式是
),则此过程的热化学方程式是②

 的代数式表示)。
的代数式表示)。(3)
 的电子式是
的电子式是 中O—H键的键能是463kJ/mol。则,H—H键的键能与C—H的键能相差
中O—H键的键能是463kJ/mol。则,H—H键的键能与C—H的键能相差(4)
 甲烷化反应的机理大体可归结为两种,如图表示了两种途径每步反应的能量变化(TSx代表过渡态,*表示吸附在催化剂表面的物料),其中速率较快的途径中的决速步的化学方程式是
甲烷化反应的机理大体可归结为两种,如图表示了两种途径每步反应的能量变化(TSx代表过渡态,*表示吸附在催化剂表面的物料),其中速率较快的途径中的决速步的化学方程式是
(5)将
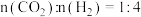 混合气持续以一定的流速通过含催化剂的恒容反应器,测定
混合气持续以一定的流速通过含催化剂的恒容反应器,测定 的转化率和
的转化率和 的选择性随温度的变化关系如图所示。温度高于500℃后,
的选择性随温度的变化关系如图所示。温度高于500℃后, 的转化率几乎保持不变但
的转化率几乎保持不变但 的选择性下降的可能原因是
的选择性下降的可能原因是
(6)不同压强下,保持相同的投料比,测定反应体系中
 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如图所示。
的平衡产率随温度的变化关系如图所示。
 时曲线出现拐点的温度高于
时曲线出现拐点的温度高于 时的,原因是
时的,原因是
您最近一年使用:0次
名校
5 . 中国科学家在淀粉人工光合成方面取得重大突破性进展,该实验方法首先将CO2催化还原为CH3OH。已知CO2催化加氢的主要反应有:
① CO2(g) + 3H2(g) CH3OH(g) + H2O(g) ΔH1=- 49.4 kJ/mol
CH3OH(g) + H2O(g) ΔH1=- 49.4 kJ/mol
② CO2(g) + H2(g) CO(g) + H2O(g) ΔH2=+ 41.2 kJ/mol
CO(g) + H2O(g) ΔH2=+ 41.2 kJ/mol
其他条件不变时,在相同时间内温度对CO2催化加氢的影响如下图。下列说法不正确 的是
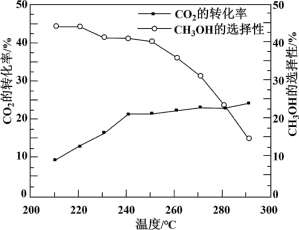
【注】CH3OH的选择性=
① CO2(g) + 3H2(g)
 CH3OH(g) + H2O(g) ΔH1=- 49.4 kJ/mol
CH3OH(g) + H2O(g) ΔH1=- 49.4 kJ/mol② CO2(g) + H2(g)
 CO(g) + H2O(g) ΔH2=+ 41.2 kJ/mol
CO(g) + H2O(g) ΔH2=+ 41.2 kJ/mol其他条件不变时,在相同时间内温度对CO2催化加氢的影响如下图。下列说法

【注】CH3OH的选择性=

A.CO(g) + 2H2(g) CH3OH(g) ΔH=- 90.6 kJ/mol CH3OH(g) ΔH=- 90.6 kJ/mol |
| B.使用催化剂,能降低反应的活化能,增大活化分子百分数 |
| C.其他条件不变,增大压强,有利于反应向生成CH3OH的方向进行 |
| D.220~240 ℃,升高温度,对反应②速率的影响比对反应①的小 |
您最近一年使用:0次
2023-02-16更新
|
613次组卷
|
13卷引用:北京市第二十中学2022-2023学年高三下学期开学检测化学试题
北京市第二十中学2022-2023学年高三下学期开学检测化学试题北京师范大学附属实验中学2023-2024学年高二下学期开学检测化学试题北京市西城区2021~2022学年高三上学期期末考试化学试题北京市第一六一中学2022-2023学年高三上学期10月月考化学试题北京市北京师范大学附属中学2022-2023学年高二上学期期中考试化学试题北京一零一中学2022-2023学年高三上学期统练六化学试题北京市一0一中学2022-2023学年高二下学期期中考试化学试题 北京市回民学校2023-2024学年高三上学期统练二化学试题北京市第十五中学2023-2024学年高二上学期期中考试化学试题北京市育才学校2023-2024学年高一上学期化学期中试题新疆阿克苏地区等2地新疆生产建设兵团第一师第二高级中学等2校2022-2023学年高三下学期2月月考化学试题福建省南平第一中学2023-2024学年高三上学期10月月考化学试题广东省广州市实验外语学校2023-2024学年高二上学期11月期中考试化学试题
名校
6 . 2022北京冬奥会采用氢气作为火炬燃料,选择氢能汽车作为赛事交通服务用车,充分体现了绿色奥运的理念。已知:
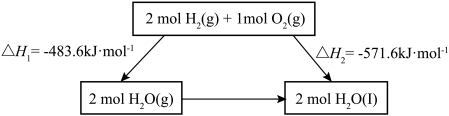
下列说法不正确 的是

下列说法
| A.氢气既可以通过燃烧反应提供热能,也可以设计成燃料电池提供电能 |
B. 的过程中, 的过程中, , , |
C.断裂2mol 和1mol 和1mol 中化学键所需能量大于断裂2mol 中化学键所需能量大于断裂2mol 中化学键所需能量 中化学键所需能量 |
D.化学反应的 ,只与反应体系的始态和终态有关,与反应途径无关 ,只与反应体系的始态和终态有关,与反应途径无关 |
您最近一年使用:0次
2022-11-04更新
|
616次组卷
|
9卷引用:北京市第五中学2023-2024学年高二上学期开学考化学试卷
名校
解题方法
7 . 烟气脱硫脱硝技术是环境科学研究的热点。某小组模拟 氧化结合
氧化结合 溶液吸收法同时脱除
溶液吸收法同时脱除 和NO的过程示意图如下。
和NO的过程示意图如下。

(1)气体反应器中的主要反应原理及相关数据如下表。
①根据已知求解:

_______ 。
②其他条件不变时,高于150℃,在相同时间 内 和NO的转化率均随温度升高而降低,原因是
和NO的转化率均随温度升高而降低,原因是_______ 。
③其他条件不变, 和NO初始的物质的量浓度相等时,经检测装置1分析,在
和NO初始的物质的量浓度相等时,经检测装置1分析,在相同时间 内, 和NO的转化率随
和NO的转化率随 的浓度的变化如图。结合数据分析NO的转化率高于
的浓度的变化如图。结合数据分析NO的转化率高于 的原因
的原因_______ 。

(2)其他条件不变, 和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内,
和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内, 与NO的物质的量之比对
与NO的物质的量之比对 和NO脱除率的影响如下图。
和NO脱除率的影响如下图。

① 溶液显碱性,用化学平衡原理解释:
溶液显碱性,用化学平衡原理解释:_______ 。
② 的浓度很低时,
的浓度很低时, 的脱除率超过97%,原因是
的脱除率超过97%,原因是_______ 。
③在吸收器中, 与
与 反应生成
反应生成 和
和 的离子方程式是
的离子方程式是_______ 。
④在吸收器中,随着吸收过程的进行,部分 被转化为
被转化为 ,反应中
,反应中 和
和 的物质的量之比为1:1,该反应的离子方程式是
的物质的量之比为1:1,该反应的离子方程式是_______ 。
 氧化结合
氧化结合 溶液吸收法同时脱除
溶液吸收法同时脱除 和NO的过程示意图如下。
和NO的过程示意图如下。
(1)气体反应器中的主要反应原理及相关数据如下表。
| 反应 | 平衡常数(25℃) | 活化能/(kJ/mol) |
反应a: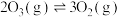  |  | 24.6 |
反应b: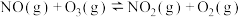  | 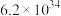 | 3.17 |
反应c:  | 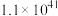 | 58.17 |
①根据已知求解:


②其他条件不变时,高于150℃,在
 和NO的转化率均随温度升高而降低,原因是
和NO的转化率均随温度升高而降低,原因是③其他条件不变,
 和NO初始的物质的量浓度相等时,经检测装置1分析,在
和NO初始的物质的量浓度相等时,经检测装置1分析,在 和NO的转化率随
和NO的转化率随 的浓度的变化如图。结合数据分析NO的转化率高于
的浓度的变化如图。结合数据分析NO的转化率高于 的原因
的原因
(2)其他条件不变,
 和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内,
和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内, 与NO的物质的量之比对
与NO的物质的量之比对 和NO脱除率的影响如下图。
和NO脱除率的影响如下图。
①
 溶液显碱性,用化学平衡原理解释:
溶液显碱性,用化学平衡原理解释:②
 的浓度很低时,
的浓度很低时, 的脱除率超过97%,原因是
的脱除率超过97%,原因是③在吸收器中,
 与
与 反应生成
反应生成 和
和 的离子方程式是
的离子方程式是④在吸收器中,随着吸收过程的进行,部分
 被转化为
被转化为 ,反应中
,反应中 和
和 的物质的量之比为1:1,该反应的离子方程式是
的物质的量之比为1:1,该反应的离子方程式是
您最近一年使用:0次
解题方法
8 . 铂(Pt)是一种贵金属,广泛用于化工领域。从某废催化剂(主要含有Pt、C、Al2O3、MgO)中回收Pt的一种工艺流程如图所示。

(1)I中焙烧时,C与空气中的O2生成了CO和CO2,发生的反应如下:
C(s)+O2(g)=CO2(g) △H1=-393.5kJ·mol-1;
2C(s)+O2(g)=2CO(g) △H2=-221kJ·mol-1;
2CO(g)+O2(g)=2CO2(g) △H3=____ kJ·mol-1。
(2)实验人员采用三种不同的浸出液分别研究II中Pt的浸出率。所用的浸出液分别是HCl-H2SO4-NaClO3、HCl-NaClO3和HCl-H2O2。
①将下列浸出反应的离子方程式补充完整:____ 。
3Pt+ Cl-+
Cl-+ ClO
ClO +
+ _____=3[PtCl6]2-+
_____=3[PtCl6]2-+ H2O
H2O
②当NaClO3或H2O2作为氧化剂浸出等量Pt时,n(NaClO3):n(H2O2)=____ 。
③c(H+)相同、浸出时间相同时,三种浸出液对Pt的浸出率如表。
[注:c(NaClO3)按照②中的物质的量关系换算成c(H2O2)计]。
a.以HCl-NaClO3为例,说明当其中氧化剂浓度大于0.2mol·L-1时,Pt的浸出率降低的原因:随着c(NaClO3)增大,其氧化性增强,部分ClO 被
被_____ 还原而消耗。
b.氧化剂浓度均为0.2mol·L-1时,甲中Pt的浸出率最低的可能原因:由于三种浸出液中的c(H+)均相同,_____ 。
(3)III中萃取剂(R3N)的萃取机理如下(O表示有机体系,A表示水溶液体系)。
i.R3N(O)+H+(A)+Cl-(A) R3NHCl(O)
R3NHCl(O)
ii.2R3NHCl(O)+[PtCl6]2-(A) (R3NH2)[PtCl6](O)+2Cl-(A)
(R3NH2)[PtCl6](O)+2Cl-(A)
①分离操作x是____ 。
②IV中向含Pt的有机物中加入NaOH溶液可使[PtCl6]2-进入水溶液体系,反应的离子方程式是_____ 。

(1)I中焙烧时,C与空气中的O2生成了CO和CO2,发生的反应如下:
C(s)+O2(g)=CO2(g) △H1=-393.5kJ·mol-1;
2C(s)+O2(g)=2CO(g) △H2=-221kJ·mol-1;
2CO(g)+O2(g)=2CO2(g) △H3=
(2)实验人员采用三种不同的浸出液分别研究II中Pt的浸出率。所用的浸出液分别是HCl-H2SO4-NaClO3、HCl-NaClO3和HCl-H2O2。
①将下列浸出反应的离子方程式补充完整:
3Pt+
 Cl-+
Cl-+ ClO
ClO +
+ _____=3[PtCl6]2-+
_____=3[PtCl6]2-+ H2O
H2O②当NaClO3或H2O2作为氧化剂浸出等量Pt时,n(NaClO3):n(H2O2)=
③c(H+)相同、浸出时间相同时,三种浸出液对Pt的浸出率如表。
[注:c(NaClO3)按照②中的物质的量关系换算成c(H2O2)计]。
| 氧化剂浓度/mol·L-1 | 0.1 | 0.2 | 0.3 | 0.4 | |
| 甲 | HCl-H2SO4-NaClO3对Pt的浸出率/% | 72.7 | 78.2 | 77.5 | 75.4 |
| 乙 | HCl-NaClO3对Pt的浸出率/% | 79.6 | 85.3 | 82.1 | 81.6 |
| 丙 | HCl-H2O2对Pt的浸出率/% | 80.0 | 85.6 | 83.2 | 82.5 |
a.以HCl-NaClO3为例,说明当其中氧化剂浓度大于0.2mol·L-1时,Pt的浸出率降低的原因:随着c(NaClO3)增大,其氧化性增强,部分ClO
 被
被b.氧化剂浓度均为0.2mol·L-1时,甲中Pt的浸出率最低的可能原因:由于三种浸出液中的c(H+)均相同,
(3)III中萃取剂(R3N)的萃取机理如下(O表示有机体系,A表示水溶液体系)。
i.R3N(O)+H+(A)+Cl-(A)
 R3NHCl(O)
R3NHCl(O)ii.2R3NHCl(O)+[PtCl6]2-(A)
 (R3NH2)[PtCl6](O)+2Cl-(A)
(R3NH2)[PtCl6](O)+2Cl-(A)①分离操作x是
②IV中向含Pt的有机物中加入NaOH溶液可使[PtCl6]2-进入水溶液体系,反应的离子方程式是
您最近一年使用:0次
名校
9 . 我国科学家实现了在铜催化剂条件下将DMF[(CH3)2NCHO]转化为三甲胺[N(CH3)3]。计算机模拟单个DMF分子在铜催化剂表面的反应历程如图所示,下列说法正确的是
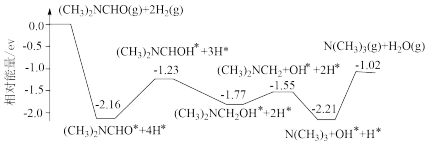

| A.该历程中最小能垒的化学方程式为 (CH3)2NCH2OH*=(CH3)2NCH2+OH* |
| B.该历程中最大能垒(活化能)为2.16eV |
| C.该反应热化学方程式为(CH3)2NCHO(g)+2H2(g)=N(CH3)3(g)+H2O(g) ΔH=-1.02ev•mol-1 |
| D.增大压强或升高温度均能加快反应速率,并增大DMF平衡转化率 |
您最近一年使用:0次
2022-08-24更新
|
780次组卷
|
29卷引用:北京市第二十中学2022-2023学年高三下学期开学检测化学试题
北京市第二十中学2022-2023学年高三下学期开学检测化学试题河北省张家口市宣化一中2020-2021学年高二下学期期初考试化学试题山东省威海市2020届高三年级高考模拟考(二模)化学试题(已下线)专题07 化学反应中的能量变化-2020年高考真题和模拟题化学分项汇编浙江省杭州第二中学2021届高三上学期期中考试化学试题(已下线)解密08 化学反应与能量(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密08 化学反应与能量(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)浙江省绍兴市第一中学2020-2021学年高三1月高考适应性考试化学试题(已下线)押全国卷理综第13题 反应机理图分析、能垒图分析等创新题型及阿伏伽德罗常数-备战2021年高考化学临考题号押题(课标全国卷)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)湖南省长沙市雅礼中学2021-2022学年高三上学期月考卷(三)化学试题辽宁省大连市第一中学 2021-2022学年高三上学期期中联考化学试题河南省顶尖名校联盟2021-2022学年高二下学期联赛考试化学试题(已下线)卷04 小题素养卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)2022年湖南卷高考真题变式题(11-14)(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)山西省运城市教育发展联盟2021-2022学年高二上学期11月期中检测化学试题辽宁省大连市普兰店区第一中学2022届高三上学期期中联考化学试题湖南省邵阳市第二中学2022届高三下学期全真模拟考试化学试题湖南省株洲市第二中学2022-2023学年高二上学期期中考试化学试题湖南省株洲南方中学2022-2023学年高二上学期期中考试化学试题(已下线)第七章 化学反应速率与化学平衡 热点强化12 化学反应历程、机理的分析应用(已下线)查补易混易错04 化学反应原理部分-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)山东省青岛第二中学2021-2022学年高二上学期期中考试化学试题福建省南安市华侨中学2023-2024学年高二上学期10月月考化学试题福建省德化一中、永安一中、漳平一中三校协作2023-2024学年高二上学期12月联考化学试题(已下线)广西“贵百河”2023-2024学年高二上学期12月份联考化学试题山东省德州市实验中学2023-2024学年高二上学期期中考试 化学试题
名校
解题方法
10 . 烟气脱硫脱硝技术是环境科学研究的热点。某小组模拟 氧化结合
氧化结合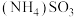 溶液吸收法同时脱除
溶液吸收法同时脱除 和NO的过程示意图如下。
和NO的过程示意图如下。
①已知: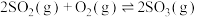
 ,则
,则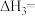
_______ 。
②其他条件不变时,高于150℃,在相同时间内 和NO的转化率均随温度升高而降低,原因是
和NO的转化率均随温度升高而降低,原因是_______ 。
③其他条件不变, 和NO初始的物质的量浓度相等时,经检测装置1分析,在相同时间内,
和NO初始的物质的量浓度相等时,经检测装置1分析,在相同时间内, 和NO的转化率随
和NO的转化率随 的浓度的变化如图。结合数据分析NO的转化率高于
的浓度的变化如图。结合数据分析NO的转化率高于 的原因
的原因_______ 。 和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内,
和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内, 与NO的物质的量之比对
与NO的物质的量之比对 和NO脱除率的影响如图。
和NO脱除率的影响如图。 溶液显碱性,用化学平衡原理解释:
溶液显碱性,用化学平衡原理解释:_______ 。
② 的浓度很低时,
的浓度很低时, 的脱除率超过97%,原因是
的脱除率超过97%,原因是_______ 。
③在吸收器中, 与
与 反应生成
反应生成 和
和 的离子方程式是
的离子方程式是_______ 。
④在吸收器中,随着吸收过程的进行,部分 被转化为
被转化为 ,反应中
,反应中 和
和 的物质的量之比为1:1,该反应的离子方程式是
的物质的量之比为1:1,该反应的离子方程式是_______ 。
 氧化结合
氧化结合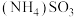 溶液吸收法同时脱除
溶液吸收法同时脱除 和NO的过程示意图如下。
和NO的过程示意图如下。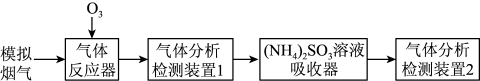
| 反应 | 平衡常数(25℃) | 活化能/(kJ/mol) |
反应a: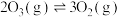 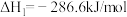 |  | 24.6 |
反应b: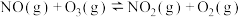 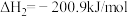 | 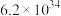 | 3.17 |
反应c:  | 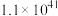 | 58.17 |
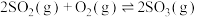
 ,则
,则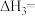
②其他条件不变时,高于150℃,在相同时间内
 和NO的转化率均随温度升高而降低,原因是
和NO的转化率均随温度升高而降低,原因是③其他条件不变,
 和NO初始的物质的量浓度相等时,经检测装置1分析,在相同时间内,
和NO初始的物质的量浓度相等时,经检测装置1分析,在相同时间内, 和NO的转化率随
和NO的转化率随 的浓度的变化如图。结合数据分析NO的转化率高于
的浓度的变化如图。结合数据分析NO的转化率高于 的原因
的原因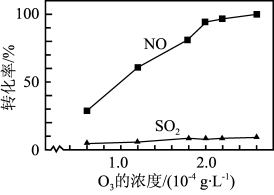
 和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内,
和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内, 与NO的物质的量之比对
与NO的物质的量之比对 和NO脱除率的影响如图。
和NO脱除率的影响如图。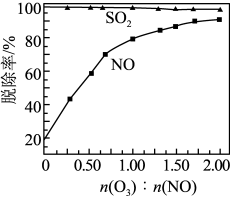
 溶液显碱性,用化学平衡原理解释:
溶液显碱性,用化学平衡原理解释:②
 的浓度很低时,
的浓度很低时, 的脱除率超过97%,原因是
的脱除率超过97%,原因是③在吸收器中,
 与
与 反应生成
反应生成 和
和 的离子方程式是
的离子方程式是④在吸收器中,随着吸收过程的进行,部分
 被转化为
被转化为 ,反应中
,反应中 和
和 的物质的量之比为1:1,该反应的离子方程式是
的物质的量之比为1:1,该反应的离子方程式是
您最近一年使用:0次
2022-04-10更新
|
763次组卷
|
6卷引用:北京一零一中2023-2024学年高三上学期第一次月考(开学考)化学试卷



