1 . 工业废气中的硫化氢是一种无色有毒的气体。根据硫化氢的性质,可采取不同的处理方法。
(1)氧化法(克劳斯法),其原理是:
H2S SO2
SO2 S
S
S(s)+O2(g)=SO2(g) ∆H=-297kJ·mol-1
第②步反应的热化学方程式为___________ 。
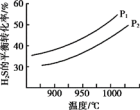
(2)热分解法,其原理是:2H2S(g) S2(?)+2H2(g)。不同温度和压强下,H2S的平衡转化率变化如图。P1
S2(?)+2H2(g)。不同温度和压强下,H2S的平衡转化率变化如图。P1___________ P2(填“>”或“<”),原因是___________ 。
(3)直接电解法,可回收S和H2。

资料:
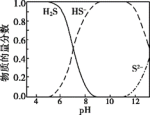
ⅰ.H2S溶液中含硫微粒的物质的量分数随pH变化如图。
ⅱ.(x-1)S+S2− S
S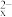 (黄色溶液);S
(黄色溶液);S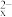 与酸反应生成S。
与酸反应生成S。
①直接电解H2S酸性溶液(pH≈5),容易出现电解反应不能持续进行的情况,结合电极反应式分析其可能的原因___________ 。
②工业上,常用烧碱吸收H2S,将吸收后的溶液(pH=13.2)先进行电解,再用电解后的黄色溶液吸收H2S生成S。反应生成S的离子方程式是___________ 。
(4)间接电解法。先用FeCl3溶液吸收含H2S的工业废气,所得溶液用惰性电极进行电解。
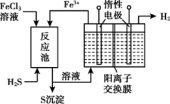
①反应池中发生反应的离子方程式是___________ 。
②该装置实验有两个显著优点:a.H2S的原子利用率100%;b.___________ 。
(5)碱性溶液吸收法。
已知:25℃时,H2S的电离常数Ka1=9.1×10-8、Ka2=1.1×10-12;H2CO3的电离常数Ka1=4.3×10-7、Ka2=5.6×10-11。用Na2CO3溶液吸收含H2S的工业废气,反应的离子方程式是___________ 。
(1)氧化法(克劳斯法),其原理是:
H2S
 SO2
SO2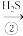 S
S已知:2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) ΔH=-1172kJ·mol-1
S(s)+O2(g)=SO2(g) ∆H=-297kJ·mol-1
第②步反应的热化学方程式为
(2)热分解法,其原理是:2H2S(g)
 S2(?)+2H2(g)。不同温度和压强下,H2S的平衡转化率变化如图。P1
S2(?)+2H2(g)。不同温度和压强下,H2S的平衡转化率变化如图。P1
(3)直接电解法,可回收S和H2。

资料:
ⅰ.H2S溶液中含硫微粒的物质的量分数随pH变化如图。

ⅱ.(x-1)S+S2−
 S
S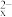 (黄色溶液);S
(黄色溶液);S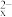 与酸反应生成S。
与酸反应生成S。①直接电解H2S酸性溶液(pH≈5),容易出现电解反应不能持续进行的情况,结合电极反应式分析其可能的原因
②工业上,常用烧碱吸收H2S,将吸收后的溶液(pH=13.2)先进行电解,再用电解后的黄色溶液吸收H2S生成S。反应生成S的离子方程式是
(4)间接电解法。先用FeCl3溶液吸收含H2S的工业废气,所得溶液用惰性电极进行电解。

①反应池中发生反应的离子方程式是
②该装置实验有两个显著优点:a.H2S的原子利用率100%;b.
(5)碱性溶液吸收法。
已知:25℃时,H2S的电离常数Ka1=9.1×10-8、Ka2=1.1×10-12;H2CO3的电离常数Ka1=4.3×10-7、Ka2=5.6×10-11。用Na2CO3溶液吸收含H2S的工业废气,反应的离子方程式是
您最近一年使用:0次
名校
2 . 已知Fe2O2(s)+ C(s)=
C(s)=  CO2(g)+2Fe(s) △H=+234.1kJ·mol-1,C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1,则2Fe(s)+
CO2(g)+2Fe(s) △H=+234.1kJ·mol-1,C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1,则2Fe(s)+ O2(g)=Fe2O3(s)的△H是
O2(g)=Fe2O3(s)的△H是
 C(s)=
C(s)=  CO2(g)+2Fe(s) △H=+234.1kJ·mol-1,C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1,则2Fe(s)+
CO2(g)+2Fe(s) △H=+234.1kJ·mol-1,C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1,则2Fe(s)+ O2(g)=Fe2O3(s)的△H是
O2(g)=Fe2O3(s)的△H是| A.-824.4kJ·mol-1 | B.-627.6kJ·mol-1 |
| C.-744.7kJ·mol-1 | D.-169.4kJ·mol-1 |
您最近一年使用:0次
2024-03-18更新
|
376次组卷
|
4卷引用:北京市中国人民大学附属中学2023-2024学年高一下学期期中考试化学试题
名校
解题方法
3 .  相关转化的研究,对解决环境、能源问题意义重大。
相关转化的研究,对解决环境、能源问题意义重大。
(1) 催化加氢制取汽油,
催化加氢制取汽油, 转化过程示意图如图:
转化过程示意图如图:
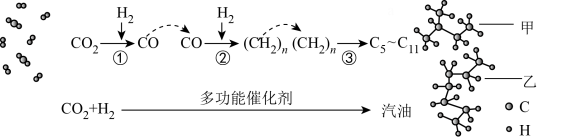
下列说法不正确的是___________ 。
a.反应①的产物中含有水 b.图中甲与乙互为同系物
c.反应②中只有碳碳键形成 d.汽油主要是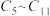 的烃类混合物
的烃类混合物
(2) 与
与 经催化重整可制得合成气:
经催化重整可制得合成气:

已知: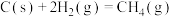
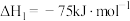
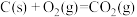



该催化重整反应的
___________  。
。
(3) 与
与 反应制取中醇
反应制取中醇 。
。
已知 与
与 反应生成
反应生成 气体和水蒸气放出
气体和水蒸气放出 的热量。
的热量。
写出 与
与 制取
制取 的热化学方程式
的热化学方程式___________ 。
(4)制取化工原料草酸铝 。
。
利用 电池,能有效地将
电池,能有效地将 转化成草酸铝,工作原理如图所示。
转化成草酸铝,工作原理如图所示。
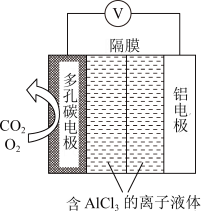
①电池的负极反应式是:___________ 。
②电池的正极反应式: (草酸根)。
(草酸根)。
正极反应过程中, 起催化作用,催化过程可表示为:
起催化作用,催化过程可表示为:
I.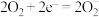
Ⅱ.
写出Ⅱ的离子方程式:___________ 。
 相关转化的研究,对解决环境、能源问题意义重大。
相关转化的研究,对解决环境、能源问题意义重大。(1)
 催化加氢制取汽油,
催化加氢制取汽油, 转化过程示意图如图:
转化过程示意图如图:
下列说法不正确的是
a.反应①的产物中含有水 b.图中甲与乙互为同系物
c.反应②中只有碳碳键形成 d.汽油主要是
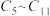 的烃类混合物
的烃类混合物(2)
 与
与 经催化重整可制得合成气:
经催化重整可制得合成气:

已知:
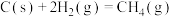
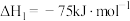
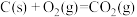



该催化重整反应的

 。
。(3)
 与
与 反应制取中醇
反应制取中醇 。
。已知
 与
与 反应生成
反应生成 气体和水蒸气放出
气体和水蒸气放出 的热量。
的热量。写出
 与
与 制取
制取 的热化学方程式
的热化学方程式(4)制取化工原料草酸铝
 。
。利用
 电池,能有效地将
电池,能有效地将 转化成草酸铝,工作原理如图所示。
转化成草酸铝,工作原理如图所示。
①电池的负极反应式是:
②电池的正极反应式:
 (草酸根)。
(草酸根)。正极反应过程中,
 起催化作用,催化过程可表示为:
起催化作用,催化过程可表示为:I.
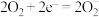
Ⅱ.

写出Ⅱ的离子方程式:
您最近一年使用:0次
名校
解题方法
4 . TiCl4是由钛精矿(主要成分为TiO2)制备钛(Ti)的重要中间产物,制备纯TiCl4的流程示意图如下:

资料:TiCl4及所含杂质氯化物的性质
(1)氯化过程: 与
与 难以直接反应,加碳生成CO和
难以直接反应,加碳生成CO和 可使反应得以进行。
可使反应得以进行。
已知:
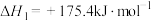


①沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的热化学方程式___________ 。
②氯化过程中CO和CO2可以相互转化,根据如图判断:CO2生成CO反应的
___________ 0(填“>”“<”或“=”)。
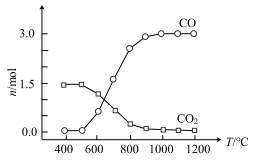
③氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤渣中含有___________ 。
(2)结构决定物质的性质,请从结构角度解释下列事实的原因。
已知TiCl4分子为正四面体结构。
①TiCl4的沸点高于SiCl4___________ 。
②MgCl2熔点远高于AlCl3___________ 。
(3)根据物质沸点不同可以进行分离提纯。
精制过程:粗TiCl4经两步蒸馏得纯TiCl4。示意图如下:
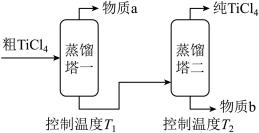
物质a是___________ ,T2应控制在___________ 。

资料:TiCl4及所含杂质氯化物的性质
| 化合物 |  | TiCl4 |  |  |  |
| 沸点/℃ | 58 | 136 | 181(升华) | 316 | 1412 |
| 熔点/℃ | -69 | -25 | 193 | 304 | 714 |
| 在TiCl4的溶解性 | 互溶 | - | 微溶 | 难溶 |
(1)氯化过程:
 与
与 难以直接反应,加碳生成CO和
难以直接反应,加碳生成CO和 可使反应得以进行。
可使反应得以进行。已知:

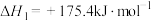


①沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的热化学方程式
②氯化过程中CO和CO2可以相互转化,根据如图判断:CO2生成CO反应的


③氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤渣中含有
(2)结构决定物质的性质,请从结构角度解释下列事实的原因。
已知TiCl4分子为正四面体结构。
①TiCl4的沸点高于SiCl4
②MgCl2熔点远高于AlCl3
(3)根据物质沸点不同可以进行分离提纯。
精制过程:粗TiCl4经两步蒸馏得纯TiCl4。示意图如下:

物质a是
您最近一年使用:0次
5 .  和
和 是两种造成温室效应的主要气体,高温下可发生干重整反应进行综合利用,反应过程的能量变化如图所示:
是两种造成温室效应的主要气体,高温下可发生干重整反应进行综合利用,反应过程的能量变化如图所示:
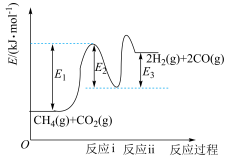
(1)干重整主反应的热化学方程式为_____ (用 、
、 、
、 表示反应热),反应速率由反应决定
表示反应热),反应速率由反应决定_____ (填“ⅰ”或“ⅱ”)。
(2)反应器中还同时存在副反应: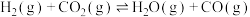
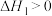
①下图表示投料比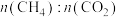 为
为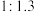 时,不同温度下的反应结果,下列说法中正确的是
时,不同温度下的反应结果,下列说法中正确的是_____ 。(填字母)
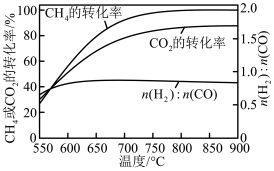
A.加压有利于增大 和
和 反应的速率但不利于提高二者的平衡转化率
反应的速率但不利于提高二者的平衡转化率
B.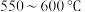 ,升温更有利于主反应,主反应先达到平衡
,升温更有利于主反应,主反应先达到平衡
C.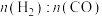 始终低于
始终低于 ,与副反应有关
,与副反应有关
②体系中会发生积炭反应
 ,为研究其热效应,还需要利用反应
,为研究其热效应,还需要利用反应_____ 的 。
。
③添加一定量的载氧剂 ,可避免积炭反应发生,增大
,可避免积炭反应发生,增大 的值,推测可能发生的反应,写出化学反应方程式
的值,推测可能发生的反应,写出化学反应方程式_____ 。
(3)文献中指出 和
和 可以发生反应生成
可以发生反应生成 和
和 ,且反应进行程度较大,但干重整反应器中进行程度小。结合键能数据,从平衡角度阐明理由
,且反应进行程度较大,但干重整反应器中进行程度小。结合键能数据,从平衡角度阐明理由_____ 。
 和
和 是两种造成温室效应的主要气体,高温下可发生干重整反应进行综合利用,反应过程的能量变化如图所示:
是两种造成温室效应的主要气体,高温下可发生干重整反应进行综合利用,反应过程的能量变化如图所示:
(1)干重整主反应的热化学方程式为
 、
、 、
、 表示反应热),反应速率由反应决定
表示反应热),反应速率由反应决定(2)反应器中还同时存在副反应:
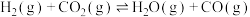
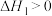
①下图表示投料比
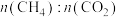 为
为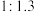 时,不同温度下的反应结果,下列说法中正确的是
时,不同温度下的反应结果,下列说法中正确的是
A.加压有利于增大
 和
和 反应的速率但不利于提高二者的平衡转化率
反应的速率但不利于提高二者的平衡转化率B.
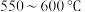 ,升温更有利于主反应,主反应先达到平衡
,升温更有利于主反应,主反应先达到平衡C.
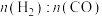 始终低于
始终低于 ,与副反应有关
,与副反应有关②体系中会发生积炭反应

 ,为研究其热效应,还需要利用反应
,为研究其热效应,还需要利用反应 。
。③添加一定量的载氧剂
 ,可避免积炭反应发生,增大
,可避免积炭反应发生,增大 的值,推测可能发生的反应,写出化学反应方程式
的值,推测可能发生的反应,写出化学反应方程式(3)文献中指出
 和
和 可以发生反应生成
可以发生反应生成 和
和 ,且反应进行程度较大,但干重整反应器中进行程度小。结合键能数据,从平衡角度阐明理由
,且反应进行程度较大,但干重整反应器中进行程度小。结合键能数据,从平衡角度阐明理由| 化学键 | 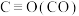 |  |  |  |
键能 | 1072 | 436 | 413 | 464 |
您最近一年使用:0次
6 . 氯苯是工业废水中的常见污染物,将其降解或资源化转化在能源利用、环境保护等方面意义重大。通常,废水中氯苯的处理过程为:

资料:25℃、101kPa时,氯苯、邻苯二酚燃烧反应的热化学方程式如下:
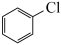 (l)
(l)
 (s)
(s)
(1)25℃、101kPa时,在催化剂作用下,氯苯与 、
、 反应生成邻苯二酚和
反应生成邻苯二酚和 的热化学方程式为
的热化学方程式为___________ 。
(2)可用于检验转化ii后是否有邻苯二酚剩余的试剂为___________ 。
(3)传统处理工艺常用空气将废水中的氯苯吹出,所得空气、氯苯的混合气体通过催化剂表面完成转化i,所得产物在实验条件下均为气态。其他条件不变时,增大通入废水的空气流速,废水中氯苯去除率提高;但i中氯苯的转化率降低。氯苯转化率降低的可能原因是___________ (填字母)。
a.单位时间内通过催化剂表面的混合气体变少
b.混合气体在催化剂表面反应的时间变短
c.i中转化反应的化学平衡常数变小
(4)我国科研人员开发了一种电化学装置(如图),可在更温和的条件下实现转化i、ii。
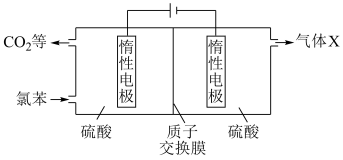
①阳极区发生的电极反应为:___________ 。(补充不完整的反应)

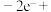 □___________=
□___________= +□___________+□___________
+□___________+□___________


②资料:电解效率
一定时间内,阴极共得到44.8L气体X(标准状况), 。若阳极区
。若阳极区 (
( )=5%,所有邻苯二酚完全转化为
)=5%,所有邻苯二酚完全转化为 ,则
,则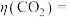
___________ 。
③一段时间后,阴极区溶液pH保持不变,结合化学用语解释其原因:___________ 。

资料:25℃、101kPa时,氯苯、邻苯二酚燃烧反应的热化学方程式如下:
 (l)
(l)
 (s)
(s)
(1)25℃、101kPa时,在催化剂作用下,氯苯与
 、
、 反应生成邻苯二酚和
反应生成邻苯二酚和 的热化学方程式为
的热化学方程式为(2)可用于检验转化ii后是否有邻苯二酚剩余的试剂为
(3)传统处理工艺常用空气将废水中的氯苯吹出,所得空气、氯苯的混合气体通过催化剂表面完成转化i,所得产物在实验条件下均为气态。其他条件不变时,增大通入废水的空气流速,废水中氯苯去除率提高;但i中氯苯的转化率降低。氯苯转化率降低的可能原因是
a.单位时间内通过催化剂表面的混合气体变少
b.混合气体在催化剂表面反应的时间变短
c.i中转化反应的化学平衡常数变小
(4)我国科研人员开发了一种电化学装置(如图),可在更温和的条件下实现转化i、ii。

①阳极区发生的电极反应为:

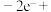 □___________=
□___________= +□___________+□___________
+□___________+□___________

②资料:电解效率

一定时间内,阴极共得到44.8L气体X(标准状况),
 。若阳极区
。若阳极区 (
( )=5%,所有邻苯二酚完全转化为
)=5%,所有邻苯二酚完全转化为 ,则
,则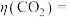
③一段时间后,阴极区溶液pH保持不变,结合化学用语解释其原因:
您最近一年使用:0次
名校
解题方法
7 .  与ICl的反应机理如下:
与ICl的反应机理如下:
反应①: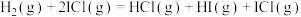 ;
;
反应②: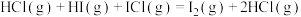 ,
,
其能量曲线如下图所示。不正确 的是
 与ICl的反应机理如下:
与ICl的反应机理如下:反应①:
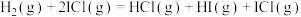 ;
;反应②:
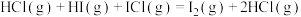 ,
,其能量曲线如下图所示。

A.反应①的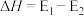 |
| B.反应①②均是放热反应 |
C. 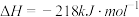 |
| D.该反应的反应速率主要取决于②的快慢 |
您最近一年使用:0次
2024-01-20更新
|
187次组卷
|
3卷引用:北京市顺义区2023-2024学年高二上学期期末考试化学试题
解题方法
8 . 甲醇是一种重要的化工原料,具有广阔的开发和应用前景。工业上使用水煤气(CO与H2的混合气体)转化成甲醇(CH3OH)。
(1)已知一定条件下,发生反应: ,
,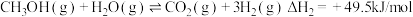 ,该条件下,水煤气转化成甲醇的热化学方程式是
,该条件下,水煤气转化成甲醇的热化学方程式是________ 。
(2)在体积可变的恒压密闭容器中投入0.5 mol CO和0.75 mol H2,不同条件下发生上述反应。实验测得平衡时CH3OH的物质的量(n)随温度(T)、压强(p)的变化如图1所示。
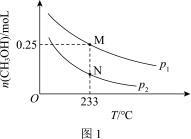
①p1____ p2(填“<”或“>”)。
②M点对应的平衡混合气体的体积为1 L,则233 ℃时,该反应的平衡常数K=_______ ,H2的转化率为______ (保留1位小数)。
③下列叙述能说明上述反应在p1条件下达到化学平衡状态的是_______ (填字母)。
a.单位时间内消耗1 mol CO的同时生成1 mol CH3OH
b.CH3OH的体积分数不再改变
c.密闭容器的体积不再改变
(3)工业上可利用甲醇羰基化法进一步制取甲酸甲酯: 。在容积不变的密闭容器中,投入等物质的量的CH3OH和CO,相同时间内CO的转化率随温度变化如图2所示(不考虑其他副反应)。
。在容积不变的密闭容器中,投入等物质的量的CH3OH和CO,相同时间内CO的转化率随温度变化如图2所示(不考虑其他副反应)。
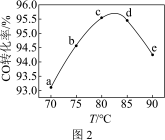
①b、c、d三点中,尚未达到化学平衡状态的点是________ 。
②该反应是_______ (填“放热”或“吸热”)反应。
③曲线ac段和de段的变化趋势不同。试从反应速率和平衡角度说明理由:________ 。
(1)已知一定条件下,发生反应:
 ,
,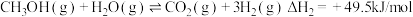 ,该条件下,水煤气转化成甲醇的热化学方程式是
,该条件下,水煤气转化成甲醇的热化学方程式是(2)在体积可变的恒压密闭容器中投入0.5 mol CO和0.75 mol H2,不同条件下发生上述反应。实验测得平衡时CH3OH的物质的量(n)随温度(T)、压强(p)的变化如图1所示。

①p1
②M点对应的平衡混合气体的体积为1 L,则233 ℃时,该反应的平衡常数K=
③下列叙述能说明上述反应在p1条件下达到化学平衡状态的是
a.单位时间内消耗1 mol CO的同时生成1 mol CH3OH
b.CH3OH的体积分数不再改变
c.密闭容器的体积不再改变
(3)工业上可利用甲醇羰基化法进一步制取甲酸甲酯:
 。在容积不变的密闭容器中,投入等物质的量的CH3OH和CO,相同时间内CO的转化率随温度变化如图2所示(不考虑其他副反应)。
。在容积不变的密闭容器中,投入等物质的量的CH3OH和CO,相同时间内CO的转化率随温度变化如图2所示(不考虑其他副反应)。
①b、c、d三点中,尚未达到化学平衡状态的点是
②该反应是
③曲线ac段和de段的变化趋势不同。试从反应速率和平衡角度说明理由:
您最近一年使用:0次
名校
9 . 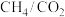 催化重整的反应为
催化重整的反应为
①

其中,积炭是导致催化剂失活的主要原因。产生积炭的反应有:
②
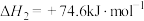
③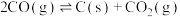
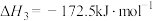
科研人员研究压强对催化剂活性的影响:在1073K时,将恒定组成的 、
、 混合气体,以恒定流速通过反应器,测得数据如下。
混合气体,以恒定流速通过反应器,测得数据如下。

下列分析不正确 的是
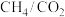 催化重整的反应为
催化重整的反应为①


其中,积炭是导致催化剂失活的主要原因。产生积炭的反应有:
②

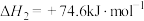
③
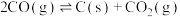
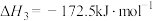
科研人员研究压强对催化剂活性的影响:在1073K时,将恒定组成的
 、
、 混合气体,以恒定流速通过反应器,测得数据如下。
混合气体,以恒定流速通过反应器,测得数据如下。
下列分析
A.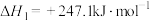 |
| B.压强越大,Ra降低越快,其主要原因是反应①平衡逆向移动 |
C.保持其他条件不变,适当增大投料时 ,可减缓Ra的衰减 ,可减缓Ra的衰减 |
D.研究表明“通入适量 有利于重整反应”,因为 有利于重整反应”,因为 能与C反应并放出热量 能与C反应并放出热量 |
您最近一年使用:0次
2023-11-30更新
|
148次组卷
|
6卷引用:北京市第一○一中学2023-2024学年高三下学期开学考试化学试题
名校
解题方法
10 . 光解水制氢的关键步骤是水的氧化。我国科学家用仿生催化剂[用 表示]实现在NaHCO3溶液中高效催化水的氧化,该过程物质转化及反应能量变化示意图如下:
表示]实现在NaHCO3溶液中高效催化水的氧化,该过程物质转化及反应能量变化示意图如下:不正确 的是
 表示]实现在NaHCO3溶液中高效催化水的氧化,该过程物质转化及反应能量变化示意图如下:
表示]实现在NaHCO3溶液中高效催化水的氧化,该过程物质转化及反应能量变化示意图如下: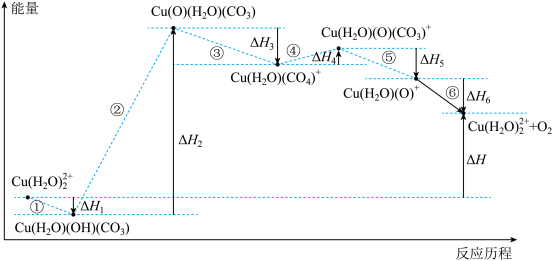
A.步骤①可表示为 |
B.水的氧化反应为: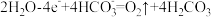 |
C.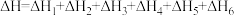 |
| D.催化剂参与反应,降低活化能,加快反应速率 |
您最近一年使用:0次
2023-05-07更新
|
1265次组卷
|
9卷引用:北京交通大学附属中学2023-2024学年高三下学期3月月考化学试题
北京交通大学附属中学2023-2024学年高三下学期3月月考化学试题北京市海淀区2022-2023学年高三第二次模拟(下学期期末)考试化学试题湖北省武汉市洪山高级中学2024届高三下学期第 2次模拟考试化学试卷 (已下线)专题08 化学反应中的能量变化(已下线)第12练 有关反应热的综合考查 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)福建省厦门第一中学2023届高三下学期模拟考试化学试题(已下线)专题09 化学反应中的热效应与反应机理-2023年高考化学真题题源解密(全国通用)(已下线)考点1 化学反应的热效应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)选择题16-20



