1 . C、CO、CH4、C2H5OH是常用燃料,1 g上述物质分别完全燃烧生成CO2(g)和H2O(l)时,放出的热量依次为32.8 kJ、10.1 kJ、55.6 kJ、29.7 kJ。相同物质的量的这4种燃料完全燃烧,放出热量最多的是
| A.C | B. CO | C. CH4 | D.C2H5OH |
您最近半年使用:0次
2 . 已知:H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6 kJ·mol-1
2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1
H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1
下列说法正确的是
2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1
H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1
下列说法正确的是
A.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照条件和点燃条件下的 不同 不同 |
| B.CH3OH(l)的燃烧热为1452 kJ·mol-1 |
C. H2SO4(aq)+ H2SO4(aq)+ Ba(OH)2(aq)= Ba(OH)2(aq)= BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 |
| D.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 |
您最近半年使用:0次
2021-04-24更新
|
265次组卷
|
3卷引用:江苏省沭阳县2020-2021学年高二下学期中调研测试化学试题
江苏省沭阳县2020-2021学年高二下学期中调研测试化学试题(已下线)第二节 燃烧热 能源(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)贵州省黔西南布依族苗族自治州2022-2023学年高二上学期期末考试化学试题
名校
3 . 25℃、 下,碳、氢气、甲烷和葡萄糖(C6H12O6)的燃烧热依次是
下,碳、氢气、甲烷和葡萄糖(C6H12O6)的燃烧热依次是 、
、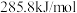 、
、 、
、 ,则下列热化学方程式正确的是
,则下列热化学方程式正确的是
 下,碳、氢气、甲烷和葡萄糖(C6H12O6)的燃烧热依次是
下,碳、氢气、甲烷和葡萄糖(C6H12O6)的燃烧热依次是 、
、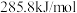 、
、 、
、 ,则下列热化学方程式正确的是
,则下列热化学方程式正确的是A. |
B. |
C. |
D. |
您最近半年使用:0次
4 . 已知25℃、101kPa下,1mol水蒸发为水蒸气需要吸热44.0kJ
①H+(aq)+OH-(aq)=H2O(l)△H1=-57.3kJ•mol-1
②2CH3OH(l)+3O2(g)=4H2O(g)+2CO2(g)△H2=-1277.0kJ•mol-1
下列有关说法错误的是
①H+(aq)+OH-(aq)=H2O(l)△H1=-57.3kJ•mol-1
②2CH3OH(l)+3O2(g)=4H2O(g)+2CO2(g)△H2=-1277.0kJ•mol-1
下列有关说法错误的是
| A.若反应②中CH3OH变为气态,则该反应的反应热△H>△H2 |
| B.CH3OH(l)的燃烧热△H=-726.5kJ•mol-1 |
| C.CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l)△H>﹣57.3kJ•mol-1 |
| D.液态水变为水蒸气过程中需要克服分子间作用力 |
您最近半年使用:0次
2021-04-13更新
|
629次组卷
|
6卷引用:河北省秦皇岛市2021届普通高中学业水平选择性考试第二次模拟演练化学试题
河北省秦皇岛市2021届普通高中学业水平选择性考试第二次模拟演练化学试题(已下线)押山东卷第07题 化学反应与能量-备战2021年高考化学临考题号押题(山东卷)(已下线)第17讲 化学能与热能(精讲)-2022年一轮复习讲练测河南省商城县观庙高级中学2021-2022学年高二上学期12月月考化学试题(已下线)第03讲 盖斯定律(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)江西省九校2022-2023学年高二下学期开学联考化学试题
名校
解题方法
5 . 煤的气化和天然气净化过程中会产生H2S,将其吸收与转化是环境保护和资源利用的有效措施。回答下列问题:
(1)利用足量纯碱溶液可吸收低浓度H2S,生成的含硫物质主要是___________ (填化学式。H2S的Ka1=1.3×10-7,Ka2=7.1×10-15;H2CO3的Ka1=4.4×10-7,Ka2=4.7×10-11)。
(2)电解氧化法处理H2S的原理是:在氧化反应器中,利用Fe3+氧化H2S;在电解反应器中实现Fe3+的再生,并副产氢气,总反应为H2S(g) S(s)+H2(g) △H1,相关物质的燃烧热数据如下表:
S(s)+H2(g) △H1,相关物质的燃烧热数据如下表:
则△H1=___________ kJ·mol-1。
(3)H2S高温裂解转化为H2和硫蒸气S2 反应方程式:2H2S(g) 2H2(g)+S2(g) 。维持体系压强为100 kPa,反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图所示。
2H2(g)+S2(g) 。维持体系压强为100 kPa,反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图所示。

①H2S高温裂解反应的△H___________ 0(填“>”或“<”)。曲线c代表的物质是___________ (填化学式)
②反应温度为1300℃时,H2S的平衡转化率为___________ ,反应的平衡常数Kp=___________ (计算结果保留1位小数)。
(1)利用足量纯碱溶液可吸收低浓度H2S,生成的含硫物质主要是
(2)电解氧化法处理H2S的原理是:在氧化反应器中,利用Fe3+氧化H2S;在电解反应器中实现Fe3+的再生,并副产氢气,总反应为H2S(g)
 S(s)+H2(g) △H1,相关物质的燃烧热数据如下表:
S(s)+H2(g) △H1,相关物质的燃烧热数据如下表:| 物质 | H2S(g) | S(s) | H2(g) |
| 燃烧热AH/(kJ·mol-1) | -562.0 | -296.8 | -258.8 |
(3)H2S高温裂解转化为H2和硫蒸气S2 反应方程式:2H2S(g)
 2H2(g)+S2(g) 。维持体系压强为100 kPa,反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图所示。
2H2(g)+S2(g) 。维持体系压强为100 kPa,反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图所示。
①H2S高温裂解反应的△H
②反应温度为1300℃时,H2S的平衡转化率为
您最近半年使用:0次
6 . 火电厂利用燃煤发电,煤燃烧中的热化学方程式有:
C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
CO(g)+ O2(g)=CO2(g) ΔH2=-283 kJ/mol
O2(g)=CO2(g) ΔH2=-283 kJ/mol
C(s)+ O2(g)=CO(g) ΔH3=?
O2(g)=CO(g) ΔH3=?
下列有关说法中不正确的是
C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
CO(g)+
 O2(g)=CO2(g) ΔH2=-283 kJ/mol
O2(g)=CO2(g) ΔH2=-283 kJ/molC(s)+
 O2(g)=CO(g) ΔH3=?
O2(g)=CO(g) ΔH3=?下列有关说法中不正确的是
| A.CO的燃烧热为283 kJ/mol |
| B.二氧化碳分解为一氧化碳和氧气的反应是吸热反应 |
| C.ΔH3=ΔH2-ΔH1=110.5 kJ/mol |
| D.ΔH3=ΔH1-ΔH2=-110.5 kJ/mol |
您最近半年使用:0次
2021-03-17更新
|
161次组卷
|
2卷引用:云南省文山州砚山县第三高级中学2020-2021学年高二1月月考化学试题
11-12高二上·福建福州·阶段练习
名校
解题方法
7 . 分析表中的四个热化学方程式,判断氢气和丙烷的标准燃烧热分别是
| “嫦娥一号”发射火箭燃料 | 液氢(H2) | ①2H2(g)+O2(g)=2H2O(l)ΔH=-571.6kJ∙mol-1 ②2H2(l)+O2(l)=2H2O(g) ΔH=-482.6kJ∙mol-1 |
| 北京奥运会“祥云”火炬燃料 | 丙烷(C3H8) | ③C3H8(l)+5O2(g)=3CO2(g)+4H2O(g) ΔH=-2013.8kJ∙mol-1 ④C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2221.5kJ∙mol-1 |
| A.-571.6kJ∙mol-1,-2221.5kJ∙mol-1 | B.-285.5kJ∙mol-1,-2013.8kJ∙mol-1 |
| C.-285.8kJ∙mol-1,-2221.5kJ∙mol-1 | D.-241.3kJ∙mol-1,-2013.8kJ∙mol-1 |
您最近半年使用:0次
2021-03-17更新
|
540次组卷
|
20卷引用:2011-2012年福建省福州市罗源一中高二上学期第一次月考化学试卷
(已下线)2011-2012年福建省福州市罗源一中高二上学期第一次月考化学试卷(已下线)2014届甘肃省天水市秦安县高三上学期期末检测化学试卷(已下线)2013-2014福建安溪一中、惠安一中、养正中学下学期期中高二化学(已下线)2015安徽望江中学同步课时练(人教选修4)第一章检测试卷(已下线)2014-2015学年云南省玉溪市第一中学高二上学期期中考试化学试卷2015-2016学年山东省淄博市淄川一中等三校高二上期末联考化学试卷2015-2016学年云南省昆明三中高二下期中化学试卷2016-2017学年陕西省西安中学高二上10月月考化学试卷贵州省遵义市航天高级中学2018-2019学年高二(理)上学期第一次月考化学试题【全国百强校】贵州省遵义航天高级中学2018-2019学年高二上学期第一次月考化学试题四川省成都七中实验学校2018-2019学年高二上学期10月月考化学试题吉林省东辽五中2019-2020学年高二上学期9月月考化学试题江西省赣州市赣县第三中学2020-2021学年高二上学期9月入学考试化学试题(重点班)吉林省辽源市田家炳高级中学校2020-2021学年高二上学期第一次月考化学试题安徽省六安市舒城育才学校2020-2021学年高二上学期期末考试化学试题(已下线)1.2 燃烧热 能源-2021-2022学年高二化学课后培优练(人教版选修4)陕西省泾阳县2020-2021学年高二上学期期中考试化学试题(已下线)1.1.2 热化学方程式 燃烧热(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)河北省衡水市武强中学2021-2022学年高二下学期期中考试化学试题(已下线)第一章 化学反应的热效应(A卷·知识通关练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修1)
解题方法
8 . 航天燃料从液态变为固态,是一项技术突破。铍是高效率的火箭材料,燃烧时放出巨大的能量,每千克的铍完全燃烧放出的热量为62700kJ。则铍燃烧的热化学方程式正确的是
A.Be+ O2=BeO ΔH=-564.3kJ·mol-1 O2=BeO ΔH=-564.3kJ·mol-1 |
B.Be(s)+ O2(g)=BeO(s) ΔH=+564.3kJ·mol-1 O2(g)=BeO(s) ΔH=+564.3kJ·mol-1 |
C.Be(s)+ O2(g)=BeO(s) ΔH=-564.3kJ·mol-1 O2(g)=BeO(s) ΔH=-564.3kJ·mol-1 |
D.Be(s)+ O2(g)=BeO(g) ΔH=-564.3kJ O2(g)=BeO(g) ΔH=-564.3kJ |
您最近半年使用:0次
解题方法
9 . 已知下列热化学方程式:
①H2(g)+ O2(g)=H2O(l) ΔH=-285kJ·mol-1
O2(g)=H2O(l) ΔH=-285kJ·mol-1
②H2(g)+ O2(g)=H2O(g) ΔH=-241kJ·mol-1
O2(g)=H2O(g) ΔH=-241kJ·mol-1
③C(s)+ O2(g)=CO(g) ΔH=-110kJ·mol-1
O2(g)=CO(g) ΔH=-110kJ·mol-1
④C(s)+O2(g)=CO2(g) ΔH=-393kJ·mol-1,
回答下列问题:
(1)H2的燃烧热为___ kJ·mol-1;C的燃烧热为___ kJ·mol-1。
(2)燃烧10gH2生成液态水,放出的热量为___ kJ。
(3)写出表示CO燃烧热的热化学方程式___ 。
①H2(g)+
 O2(g)=H2O(l) ΔH=-285kJ·mol-1
O2(g)=H2O(l) ΔH=-285kJ·mol-1②H2(g)+
 O2(g)=H2O(g) ΔH=-241kJ·mol-1
O2(g)=H2O(g) ΔH=-241kJ·mol-1③C(s)+
 O2(g)=CO(g) ΔH=-110kJ·mol-1
O2(g)=CO(g) ΔH=-110kJ·mol-1④C(s)+O2(g)=CO2(g) ΔH=-393kJ·mol-1,
回答下列问题:
(1)H2的燃烧热为
(2)燃烧10gH2生成液态水,放出的热量为
(3)写出表示CO燃烧热的热化学方程式
您最近半年使用:0次
名校
解题方法
10 . 下列化学用语的有关表达不正确的是
①甲烷的球棍模型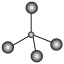
②苯乙烯(C8H8)的比例模型可以表示为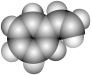
③-CH3与-OH、NH 具有相同质子数
具有相同质子数
④因氢气的燃烧热为c kJ·mol-1,故水电解的热化学方程式为2H2O (l)=2H2(g)+O2(g) △H=+c kJ·mol-1
⑤因CuSO4·5H2O(s)=CuSO4(s)+5H2O(1) △H= +b kJ·mol-1,故1 mol CuSO4(s)溶于水时,放出的热量为b kJ
①甲烷的球棍模型

②苯乙烯(C8H8)的比例模型可以表示为

③-CH3与-OH、NH
 具有相同质子数
具有相同质子数④因氢气的燃烧热为c kJ·mol-1,故水电解的热化学方程式为2H2O (l)=2H2(g)+O2(g) △H=+c kJ·mol-1
⑤因CuSO4·5H2O(s)=CuSO4(s)+5H2O(1) △H= +b kJ·mol-1,故1 mol CuSO4(s)溶于水时,放出的热量为b kJ
| A.②③④⑤ | B.①④⑤ | C.①③⑤ | D.②④⑤ |
您最近半年使用:0次
2021-02-05更新
|
394次组卷
|
3卷引用:江西师范大学附属中学2020-2021学年高二上学期期末考试化学试题
江西师范大学附属中学2020-2021学年高二上学期期末考试化学试题(已下线)专题08 化学反应与能量-备战2021届高考化学二轮复习题型专练江西省师范大学附属中学2021-2022学年高二上学期期末化学试题



