1 . 完成下列问题
(1)已知1mol石墨转化为1mol金刚石要吸收能量,则石墨比金刚石_______ (填“ 稳定”或“不稳定”)。
(2)工业合成氨中氢气的重要来源是水煤气,主要发生两个反应,它们的能量变化如图所示。

从宏观角度分析两个反应中反应物和生成物之间的能量关系_______ 。
(3)25℃和101 kPa下, H2(g) +Cl2(g) =2HCl (g)能量变化如图,根据图示回答下列问题:
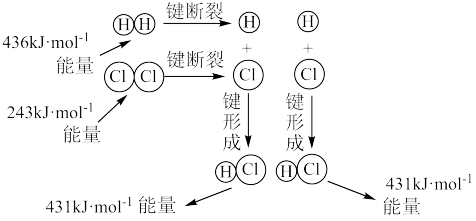
图示中,431kJ·mol -1表示的含义是_______ ; 反应H2(g) +Cl2(g) = 2HC1(g)的焓变 ΔH=_______ 。
(4)已知:①H2O(g)=H2(g)+ O2(g) ΔH= +241. 8kJ/mol;
O2(g) ΔH= +241. 8kJ/mol;
②H2O(g)=H2O(1) ΔH =-44. 0kJ/mol;
③C(s)+ O2(g) =CO(g) ΔH =-110. 5kJ/mol;
O2(g) =CO(g) ΔH =-110. 5kJ/mol;
④C(s)+ O2(g)=CO2(g) ΔH = -393.5kJ/mol。
请回答:碳的燃烧热是_______ ; 10gH2完全燃烧生成液态水,放出的热量为_______ ;写出CO燃烧热的热化学方程式_______ 。
(5)50mL 0. 50mol·L-1盐酸与50mL 0. 55mol·L-1NaOH溶液在如图所示的装置中进行中和反应,通过实验可测定中和反应过程中放出的热量。回答下列问题:
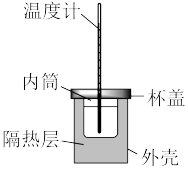
①实验装置上看,尚缺少一种玻璃仪器,该仪器的名称是_______ 。
②实验中,NaOH 溶液过量的目的是_______ 。
③若操作时忘记盖上杯盖,测得的中和反应热的数值_______ (填“偏大”“偏小”或“无影响”,下同)。用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和反应热的数值会_______ 。
(1)已知1mol石墨转化为1mol金刚石要吸收能量,则石墨比金刚石
(2)工业合成氨中氢气的重要来源是水煤气,主要发生两个反应,它们的能量变化如图所示。

从宏观角度分析两个反应中反应物和生成物之间的能量关系
(3)25℃和101 kPa下, H2(g) +Cl2(g) =2HCl (g)能量变化如图,根据图示回答下列问题:

图示中,431kJ·mol -1表示的含义是
(4)已知:①H2O(g)=H2(g)+
 O2(g) ΔH= +241. 8kJ/mol;
O2(g) ΔH= +241. 8kJ/mol; ②H2O(g)=H2O(1) ΔH =-44. 0kJ/mol;
③C(s)+
 O2(g) =CO(g) ΔH =-110. 5kJ/mol;
O2(g) =CO(g) ΔH =-110. 5kJ/mol;④C(s)+ O2(g)=CO2(g) ΔH = -393.5kJ/mol。
请回答:碳的燃烧热是
(5)50mL 0. 50mol·L-1盐酸与50mL 0. 55mol·L-1NaOH溶液在如图所示的装置中进行中和反应,通过实验可测定中和反应过程中放出的热量。回答下列问题:

①实验装置上看,尚缺少一种玻璃仪器,该仪器的名称是
②实验中,NaOH 溶液过量的目的是
③若操作时忘记盖上杯盖,测得的中和反应热的数值
您最近一年使用:0次
2 . 化学创造了丰富的物质世界,指导着我们的生产、生活,下列有关说法错误的是
| A.“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高 |
| B.钙钛矿太阳能光伏电池和锂离子电池的能量转化形式不同 |
| C.合成氨工业的反应温度控制在400~500℃,目的是使化学平衡向正反应方向移动 |
D. 实现“ 实现“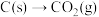 ”、“ ”、“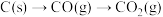 ”两种转化时放出的能量一样多 ”两种转化时放出的能量一样多 |
您最近一年使用:0次
3 . 甲醇是重要的化工原料,工业上可利用 生产甲醇,同时可降低温室气体二氧化碳的排放。
生产甲醇,同时可降低温室气体二氧化碳的排放。
已知:①
 kJ·mol
kJ·mol
②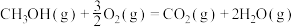
 kJ·mol
kJ·mol
③

(1)
_______ kJ·mol ,反应③在
,反应③在_______ (填“高温”、“低温”或“任何温度”)下能自发进行。
(2)下列措施中,能提高 平衡转化率的是_______(填标号)。
平衡转化率的是_______(填标号)。
(3)在一密闭容器中加入1 mol  和3 mol
和3 mol  ,在一定条件下进行反应③,测得
,在一定条件下进行反应③,测得 的平衡转化率与温度、压强的关系如图所示。
的平衡转化率与温度、压强的关系如图所示。
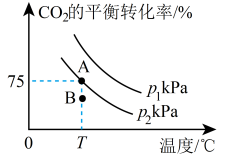
①压强
_______ (填“>”、“=”或“<”,下同) ,理由是
,理由是_______ 。
②当压强为 时,B点
时,B点
_______  。
。
③T℃、 kPa下,
kPa下, 的平衡体积分数为
的平衡体积分数为_______ %,该条件下反应③的压强平衡常数
_______  (以分压表示,分压=总压×物质的量分数)。在此平衡下,再将0.25 mol
(以分压表示,分压=总压×物质的量分数)。在此平衡下,再将0.25 mol  和0.25 mol
和0.25 mol  充入反应容器,平衡向
充入反应容器,平衡向_______ (填“正反应”或“逆反应”)方向移动。
 生产甲醇,同时可降低温室气体二氧化碳的排放。
生产甲醇,同时可降低温室气体二氧化碳的排放。已知:①

 kJ·mol
kJ·mol
②
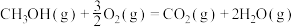
 kJ·mol
kJ·mol
③


(1)

 ,反应③在
,反应③在(2)下列措施中,能提高
 平衡转化率的是_______(填标号)。
平衡转化率的是_______(填标号)。| A.压缩容器体积 | B.将 液化分离出来 液化分离出来 |
C.恒容下充入 | D.使用高效催化剂 |
 和3 mol
和3 mol  ,在一定条件下进行反应③,测得
,在一定条件下进行反应③,测得 的平衡转化率与温度、压强的关系如图所示。
的平衡转化率与温度、压强的关系如图所示。
①压强

 ,理由是
,理由是②当压强为
 时,B点
时,B点
 。
。③T℃、
 kPa下,
kPa下, 的平衡体积分数为
的平衡体积分数为
 (以分压表示,分压=总压×物质的量分数)。在此平衡下,再将0.25 mol
(以分压表示,分压=总压×物质的量分数)。在此平衡下,再将0.25 mol  和0.25 mol
和0.25 mol  充入反应容器,平衡向
充入反应容器,平衡向
您最近一年使用:0次
解题方法
4 . 氮及其化合物在科研及生产中均有重要的应用。回答下列问题:
(1)NH3与O2在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:
反应i:4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) ΔH1= -905kJ·mol-1
反应ii:4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g) ΔH2= -1268kJ·mol-1
该条件下N2被O2生成NO的热化学方程式为_______ 。
(2)已知:N2O4(g)⇌2NO2(g) ΔH>0,将0.04mol N2O4气体充入1L的恒容密闭容器中,控制反应温度为T1,c(N2O4)随t(时间)变化曲线如图。
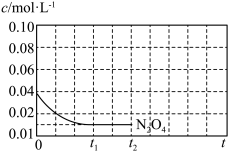
①下列可以作为反应达到平衡的判据是_______ 。
A.容器内压强不变 B.v正(N2O4)=2v逆(NO2) C.K不变
D.混合气体的密度不变 E.混合气体的颜色不变
②t1时刻反应达到平衡,若t1=15min,计算0~15 min内的平均反应速率v(NO2)=_______ ,此时反应的平衡常数K=_______ 。
③反应温度T1时,画出0~t2时段,c(NO2)随t变化曲线。保持其他条件不变,改变反应温度为T2(T2>T1),再次画出0~t2时段,c(NO2)随t变化趋势的曲线_______ 。
(3)升高温度,绝大多数的化学反应速率增大,但是NO氧化反应2NO(g)+O2(g)⇌2NO2(g) ΔH< 0,该反应的速率却随温度的升高而减小。查阅资料得知NO氧化反应的反应历程分两步,每步反应的速率方程中k正和k逆随温度的升高都增大。
I. 2NO(g)⇌N2O2(g)(快) ΔH1<0;速率方程为v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2)
II. N2O2(g)+O2(g)⇌2NO2(g)(慢) ΔH2<0;速率方程为v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2)
①根据速率方程分析,决定NO氧化反应速率的步骤是_______ (填“I”或“II”),升高温度该反应速率减小的原因是_______ 。
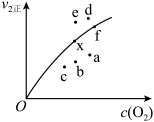
②一定温度下,反应达到平衡状态,由实验数据得到v2正~c(O2)的关系可用如图表示。当x点升高到某一温度时,反应重新达到平衡,则变为相应的点为_______ (填字母)。
(1)NH3与O2在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:
反应i:4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) ΔH1= -905kJ·mol-1
反应ii:4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g) ΔH2= -1268kJ·mol-1
该条件下N2被O2生成NO的热化学方程式为
(2)已知:N2O4(g)⇌2NO2(g) ΔH>0,将0.04mol N2O4气体充入1L的恒容密闭容器中,控制反应温度为T1,c(N2O4)随t(时间)变化曲线如图。

①下列可以作为反应达到平衡的判据是
A.容器内压强不变 B.v正(N2O4)=2v逆(NO2) C.K不变
D.混合气体的密度不变 E.混合气体的颜色不变
②t1时刻反应达到平衡,若t1=15min,计算0~15 min内的平均反应速率v(NO2)=
③反应温度T1时,画出0~t2时段,c(NO2)随t变化曲线。保持其他条件不变,改变反应温度为T2(T2>T1),再次画出0~t2时段,c(NO2)随t变化趋势的曲线
(3)升高温度,绝大多数的化学反应速率增大,但是NO氧化反应2NO(g)+O2(g)⇌2NO2(g) ΔH< 0,该反应的速率却随温度的升高而减小。查阅资料得知NO氧化反应的反应历程分两步,每步反应的速率方程中k正和k逆随温度的升高都增大。
I. 2NO(g)⇌N2O2(g)(快) ΔH1<0;速率方程为v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2)
II. N2O2(g)+O2(g)⇌2NO2(g)(慢) ΔH2<0;速率方程为v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2)
①根据速率方程分析,决定NO氧化反应速率的步骤是
②一定温度下,反应达到平衡状态,由实验数据得到v2正~c(O2)的关系可用如图表示。当x点升高到某一温度时,反应重新达到平衡,则变为相应的点为

您最近一年使用:0次
名校
解题方法
5 . 我国提出争取在2030年前实现碳达峰,2060年前实现碳中和。 的相关转化对解决环境问题、能源问题等有重要的意义。
的相关转化对解决环境问题、能源问题等有重要的意义。
Ⅰ.已知:①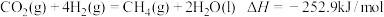
②
(1)

_______  。
。
Ⅱ.目前工业上有一种方法可以利用 生产燃料甲醇,发生的反应为:
生产燃料甲醇,发生的反应为: 。在800℃时,向体积为1L的密闭容器中,充入
。在800℃时,向体积为1L的密闭容器中,充入 和
和 ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。 的平均反应速率为
的平均反应速率为_______  。
。
(3)反应达到平衡时,该反应的平衡常数
_______ ; 的转化率为
的转化率为_______ 。
(4)若在上述平衡体系中再充入 和
和 (保持温度不变),则此平衡将
(保持温度不变),则此平衡将_______ 移动(填“向正反应方向”、“不”、“向逆反应方向”)。
(5)若将温度升高到1000℃,测得反应平衡常数为1,则该反应的
_______ 0(填“>”或“<”)。
 的相关转化对解决环境问题、能源问题等有重要的意义。
的相关转化对解决环境问题、能源问题等有重要的意义。Ⅰ.已知:①
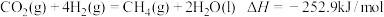
②

(1)


 。
。Ⅱ.目前工业上有一种方法可以利用
 生产燃料甲醇,发生的反应为:
生产燃料甲醇,发生的反应为: 。在800℃时,向体积为1L的密闭容器中,充入
。在800℃时,向体积为1L的密闭容器中,充入 和
和 ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。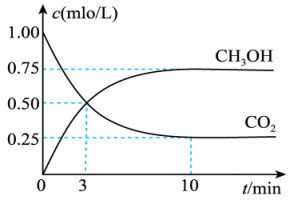
 的平均反应速率为
的平均反应速率为 。
。(3)反应达到平衡时,该反应的平衡常数

 的转化率为
的转化率为(4)若在上述平衡体系中再充入
 和
和 (保持温度不变),则此平衡将
(保持温度不变),则此平衡将(5)若将温度升高到1000℃,测得反应平衡常数为1,则该反应的

您最近一年使用:0次
2023-02-01更新
|
218次组卷
|
2卷引用:贵州省凯里市第一中学2022-2023学年高二上学期期末考试化学试题
名校
解题方法
6 . 化学反应是人类获得能量的重要途径。请结合所学知识解决以下问题。
I.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
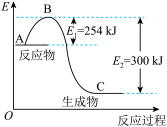
(1)如图是 和
和 反应生成
反应生成 的过程中能量变化示意图,请写出
的过程中能量变化示意图,请写出 和
和 反应的热化学方程式
反应的热化学方程式_______ 。
(2)用 催化还原NO,还可以消除氮氧化物的污染。已知:
催化还原NO,还可以消除氮氧化物的污染。已知:
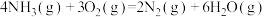
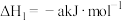 ①
①
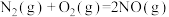
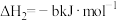 ②
②
若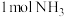 还原NO至
还原NO至 ,则该反应过程中的反应热
,则该反应过程中的反应热
____ kJ/mol(用含a、b的式子表示)。
II.某科研单位利用电化学原理用来制备硫酸,装置如图所示。电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。
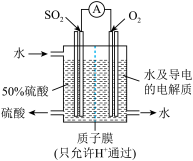
(3)通入 的电极为
的电极为_______ 极,其电极反应式为_______ 。
(4)电解质溶液中的 通过质子膜
通过质子膜_______ 移动(填“向左”、“向右”或“不”)。
III.用石墨棒作电极,在 、
、 、
、 、
、 等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
(5)当阴极放出 ,阳极放出
,阳极放出 时,电解质是
时,电解质是_______ (写化学式,下同)。
(6)当阴极放出 ,阳极放出
,阳极放出 时,电解质是
时,电解质是_______ 。
(7)通过电子的物质的量与阴极析出的金属的物质的量、阳极放出的气体的物质的量之比为4∶2∶1时,电解质是_______ 。
I.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)如图是
 和
和 反应生成
反应生成 的过程中能量变化示意图,请写出
的过程中能量变化示意图,请写出 和
和 反应的热化学方程式
反应的热化学方程式
(2)用
 催化还原NO,还可以消除氮氧化物的污染。已知:
催化还原NO,还可以消除氮氧化物的污染。已知: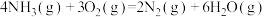
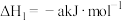 ①
①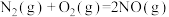
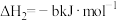 ②
②若
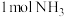 还原NO至
还原NO至 ,则该反应过程中的反应热
,则该反应过程中的反应热
II.某科研单位利用电化学原理用来制备硫酸,装置如图所示。电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。

(3)通入
 的电极为
的电极为(4)电解质溶液中的
 通过质子膜
通过质子膜III.用石墨棒作电极,在
 、
、 、
、 、
、 等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:
等离子中选出适当离子组成电解质,电解其溶液,写出符合条件的一种电解质的化学式:(5)当阴极放出
 ,阳极放出
,阳极放出 时,电解质是
时,电解质是(6)当阴极放出
 ,阳极放出
,阳极放出 时,电解质是
时,电解质是(7)通过电子的物质的量与阴极析出的金属的物质的量、阳极放出的气体的物质的量之比为4∶2∶1时,电解质是
您最近一年使用:0次
名校
7 . 我国科学家研究表明 甲基苄溴(
甲基苄溴( ,Ph代表苯基)在NaOH水溶液中水解的反应历程如图所示,下列说法正确的是
,Ph代表苯基)在NaOH水溶液中水解的反应历程如图所示,下列说法正确的是

 甲基苄溴(
甲基苄溴( ,Ph代表苯基)在NaOH水溶液中水解的反应历程如图所示,下列说法正确的是
,Ph代表苯基)在NaOH水溶液中水解的反应历程如图所示,下列说法正确的是
| A.TS1和TS2均为中间产物 |
| B.第二步反应的速率小于第一步反应的速率 |
| C.该水解反应分两步进行且两步反应均为吸热反应 |
D.总反应为 |
您最近一年使用:0次
名校
8 . HCl气体被氧气氧化的能量关系如图,下列叙述正确的是


A.该反应 、 、 |
B.该反应的浓度平衡常数 |
C.用E表示键能,则该反应 |
D.反应 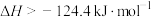 |
您最近一年使用:0次
2023-01-11更新
|
331次组卷
|
3卷引用:甘肃省庆阳市2022-2023学年高二上学期期末考试化学试题
解题方法
9 . CO2的捕获和转化可减少CO2排放并实现资源的利用。在催化剂作用下,消耗CH4和CO2,生成合成气(H2、CO),主要发生反应i,可能发生副反应ii、iii:
i.CH4(g)+CO2(g) 2CO(g)+2H2(g)
2CO(g)+2H2(g)  H1
H1
ii.CH4(g)=C(s)+2H2(g) H2=+75.0kJ•mol-1
H2=+75.0kJ•mol-1
iii.2CO(g)=CO2(g)+C(s) H3=-172.0kJ•mol-1
H3=-172.0kJ•mol-1
(1)
 H1=
H1=_____ 。
(2)反应i为可逆反应。从化学平衡的角度分析,利于生成合成气的条件是______ 。
(3)经研究发现,添加碱性助剂(如CaO)可以促进CO2的吸附与活化。反应过程如图1。反应I完成后,以N2为载气,将恒定组成、恒定流速的N2、CH4混合气通入盛有足量CaCO3的反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2。反应过程中始终未检测到CO2,催化剂表面有积炭。
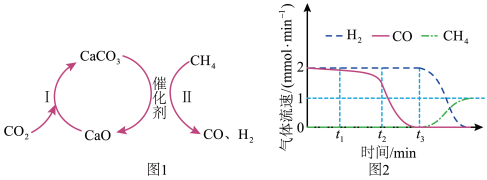
①反应II的化学方程式为_____ 。
②t1~t3,n(H2)>n(CO),且生成H2的速率不变,可能发生的副反应是_____ (填序号“ii”或“iii”)。
③t3时,生成CO的速率为0,是因为反应II不再发生,可能的原因是_____ 。
i.CH4(g)+CO2(g)
 2CO(g)+2H2(g)
2CO(g)+2H2(g)  H1
H1ii.CH4(g)=C(s)+2H2(g)
 H2=+75.0kJ•mol-1
H2=+75.0kJ•mol-1iii.2CO(g)=CO2(g)+C(s)
 H3=-172.0kJ•mol-1
H3=-172.0kJ•mol-1(1)
 H1=
H1=(2)反应i为可逆反应。从化学平衡的角度分析,利于生成合成气的条件是
| A.高温高压 | B.高温低压 | C.低温高压 | D.低温低压 |

①反应II的化学方程式为
②t1~t3,n(H2)>n(CO),且生成H2的速率不变,可能发生的副反应是
③t3时,生成CO的速率为0,是因为反应II不再发生,可能的原因是
您最近一年使用:0次
名校
解题方法
10 . 油气开采、石油化工、煤化工等行业的废气中均含有硫化氢,需要将其回收处理并加以利用。
Ⅰ.高温热分解法: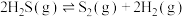
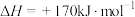
(1)该反应的化学平衡常数表达式为_______ 。
(2)升高温度,该反应的化学平衡常数_______ (填“变大”“变小”或“不变”)。
(3)工业上,通常在等温、等压条件下将 与Ar的混合气体通入反应器,发生
与Ar的混合气体通入反应器,发生 热分解反应,达到平衡状态后,若继续向反应器中通入Ar,
热分解反应,达到平衡状态后,若继续向反应器中通入Ar, 的平衡转化率会
的平衡转化率会_______ (填“增大”“减小”或“不变”),利用平衡常数与浓度商的关系说明理由:_______ 。
Ⅱ.克劳斯法:
已知: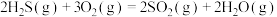
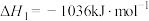

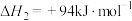
(4)用克劳斯法处理 ,若生成1mol
,若生成1mol ,放出热量
,放出热量_______ kJ。
(5)用克劳斯法处理 时,研究人员对反应条件对
时,研究人员对反应条件对 产率的影响进行了如下研究。
产率的影响进行了如下研究。
①其他条件相同时,相同时间内, 产率随温度的变化如图1所示。由图1可见,随着温度升高,
产率随温度的变化如图1所示。由图1可见,随着温度升高, 产率先增大后减小,原因是
产率先增大后减小,原因是_______ 。

②其他条件相同时,相同时间内, 产率随
产率随 值的变化如图2所示。
值的变化如图2所示。 值过高不利于提高
值过高不利于提高 产率,可能的原因是
产率,可能的原因是_______ 。

Ⅰ.高温热分解法:
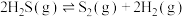
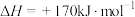
(1)该反应的化学平衡常数表达式为
(2)升高温度,该反应的化学平衡常数
(3)工业上,通常在等温、等压条件下将
 与Ar的混合气体通入反应器,发生
与Ar的混合气体通入反应器,发生 热分解反应,达到平衡状态后,若继续向反应器中通入Ar,
热分解反应,达到平衡状态后,若继续向反应器中通入Ar, 的平衡转化率会
的平衡转化率会Ⅱ.克劳斯法:

已知:
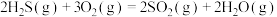
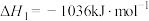

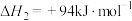
(4)用克劳斯法处理
 ,若生成1mol
,若生成1mol ,放出热量
,放出热量(5)用克劳斯法处理
 时,研究人员对反应条件对
时,研究人员对反应条件对 产率的影响进行了如下研究。
产率的影响进行了如下研究。①其他条件相同时,相同时间内,
 产率随温度的变化如图1所示。由图1可见,随着温度升高,
产率随温度的变化如图1所示。由图1可见,随着温度升高, 产率先增大后减小,原因是
产率先增大后减小,原因是
②其他条件相同时,相同时间内,
 产率随
产率随 值的变化如图2所示。
值的变化如图2所示。 值过高不利于提高
值过高不利于提高 产率,可能的原因是
产率,可能的原因是
您最近一年使用:0次
2023-01-06更新
|
792次组卷
|
6卷引用:北京海淀区2022-2023学年高二上学期期末考试化学试题



