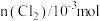1 . 某团队报道了高温富水环境下,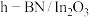 催化丙烷氧化脱氢原理,涉及反应如下:
催化丙烷氧化脱氢原理,涉及反应如下:
i.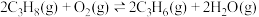

ii.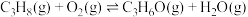

回答下列问题:
(1)上述反应过程中涉及的C、N、O元素可以组成多种配体,如CO、 、
、 等,CO、
等,CO、 的配位原子是C,而
的配位原子是C,而 的配位原子是N,简述其原因
的配位原子是N,简述其原因___________ 。
(2)已知:丙烷、丙烯的燃烧热分别为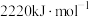 、
、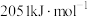 。18g液态水变为
。18g液态水变为 吸收热量44kJ。则
吸收热量44kJ。则
___________  。下列关于反应i自发性判断正确的是
。下列关于反应i自发性判断正确的是___________ (填标号)。
A.任何温度都能自发进行 B.任何温度都不能自发进行
C.在较高温度下能自发进行 D.在较低温度下能自发进行
(3)已知反应i速率方程为 (k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。
(k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。
①一定温度下,反应速率与浓度( )关系如下表所示:
)关系如下表所示:
根据数据计算,α+β+γ+δ=___________ 。
②速率常数与温度、活化能关系式为 (R、C为常数,T为温度,
(R、C为常数,T为温度, 为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与
为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与 关系如图:
关系如图:___________ (填“Cat1”或“Cat2”)。
(4)在密闭容器中充入 和
和 ,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示:
,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示:___________ 。
② 下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)在熔融碳酸钠中,丙烷-空气燃料电池的放电效率高。该燃料电池放电时,负极的电极反应式为___________ 。
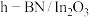 催化丙烷氧化脱氢原理,涉及反应如下:
催化丙烷氧化脱氢原理,涉及反应如下:i.
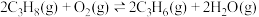

ii.
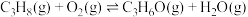

回答下列问题:
(1)上述反应过程中涉及的C、N、O元素可以组成多种配体,如CO、
 、
、 等,CO、
等,CO、 的配位原子是C,而
的配位原子是C,而 的配位原子是N,简述其原因
的配位原子是N,简述其原因(2)已知:丙烷、丙烯的燃烧热分别为
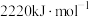 、
、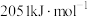 。18g液态水变为
。18g液态水变为 吸收热量44kJ。则
吸收热量44kJ。则
 。下列关于反应i自发性判断正确的是
。下列关于反应i自发性判断正确的是A.任何温度都能自发进行 B.任何温度都不能自发进行
C.在较高温度下能自发进行 D.在较低温度下能自发进行
(3)已知反应i速率方程为
 (k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。
(k为速率常数只与温度、催化剂有关;α、β、γ、δ为反应级数,可以为正数、负数或分数)。①一定温度下,反应速率与浓度(
 )关系如下表所示:
)关系如下表所示:| 序号 |  | 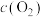 | 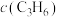 | 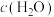 | v |
| Ⅰ | 0.1 | 0.1 | 0.1 | 0.1 | k |
| Ⅱ | 0.2 | 0.1 | 0.1 | 0.1 | 4k |
| Ⅲ | 0.2 | 0.4 | 0.1 | 0.1 | 8k |
| Ⅳ | 0.4 | 0.1 | 0.2 | 0.1 | 8k |
| Ⅴ | 0.4 | 0.4 | 0.1 | 0.2 | 16k |
②速率常数与温度、活化能关系式为
 (R、C为常数,T为温度,
(R、C为常数,T为温度, 为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与
为活化能且不随温度变化而变化)。在不同催化剂Cat1、Cat2作用下,Ink与 关系如图:
关系如图: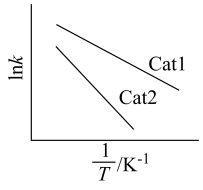
(4)在密闭容器中充入
 和
和 ,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示:
,仅发生上述反应i和ii,测得丙烷的平衡转化率与温度、压强关系如图所示: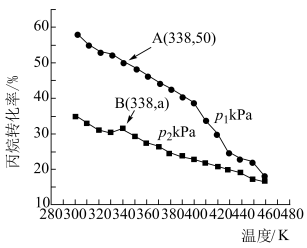
②
 下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
下,A点丙烯的选择性为80%(选择性等于丙烯的物质的量与丙烷转化的总物质的量之比)。B点时,反应ii的压强平衡常数
(5)在熔融碳酸钠中,丙烷-空气燃料电池的放电效率高。该燃料电池放电时,负极的电极反应式为
您最近一年使用:0次
2 . 苯基甲基乙炔( )可用作医药中间体,制备帕瑞昔布钠。一定条件下,苯基甲基乙炔可与HCl发生催化加成,反应过程如下:
)可用作医药中间体,制备帕瑞昔布钠。一定条件下,苯基甲基乙炔可与HCl发生催化加成,反应过程如下:

已知: ,下列说法正确的是
,下列说法正确的是
 )可用作医药中间体,制备帕瑞昔布钠。一定条件下,苯基甲基乙炔可与HCl发生催化加成,反应过程如下:
)可用作医药中间体,制备帕瑞昔布钠。一定条件下,苯基甲基乙炔可与HCl发生催化加成,反应过程如下:
已知:
 ,下列说法正确的是
,下列说法正确的是A. 中最多4个碳原子共线 中最多4个碳原子共线 |
B.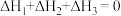 |
| C.产物Ⅱ比产物I稳定,两者互为立体异构体 |
| D.反应I的活化能大于反应Ⅱ |
您最近一年使用:0次
名校
解题方法
3 . 碘及碘的化合物在生产、生活中有广泛应用。在KI溶液中滴加少量 溶液发生有关反应如下:
溶液发生有关反应如下:
①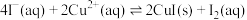
 ;
;
②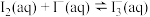 (棕黄色)
(棕黄色)  。
。
回答下列问题:
(1)在碘水中加入 ,萃取、分液得到紫红色液体和水层(M)。
,萃取、分液得到紫红色液体和水层(M)。
①由此可知, 的溶解度:四氯化碳>水,从结构角度分析其原因:
的溶解度:四氯化碳>水,从结构角度分析其原因:___________ ;
②检验M中是否有 的试剂是
的试剂是___________ 。
(2)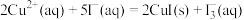

___________ 。
(3)一定温度下,在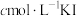 溶液中加入适量的
溶液中加入适量的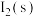 ,只发生反应
,只发生反应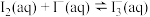
 。测得
。测得 与温度(T)关系如图所示。
与温度(T)关系如图所示。
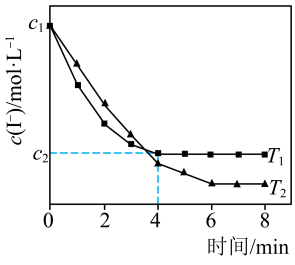
①
___________ (填“>”“<”或“=”)0。
② 温度下,0~4min时间段内
温度下,0~4min时间段内 平均速率
平均速率 为
为___________  。
。
(4)某温度下,起始在反应器中加入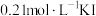 溶液和
溶液和 固体(忽略溶液体积变化),发生上述①②反应。测得
固体(忽略溶液体积变化),发生上述①②反应。测得 、
、 、
、 的平衡浓度与起始
的平衡浓度与起始 关系如图所示。
关系如图所示。
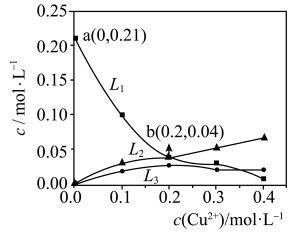
①起始 时,
时, 的平衡转化率为
的平衡转化率为___________ 。
②该温度下,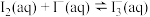 的平衡常数K=
的平衡常数K=___________ 。
(5) 的氧化性比
的氧化性比 的强,但是KI和
的强,但是KI和 发生复分解反应,不发生氧化还原反应,其原因是
发生复分解反应,不发生氧化还原反应,其原因是___________ 。
 溶液发生有关反应如下:
溶液发生有关反应如下:①
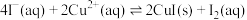
 ;
;②
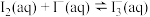 (棕黄色)
(棕黄色)  。
。回答下列问题:
(1)在碘水中加入
 ,萃取、分液得到紫红色液体和水层(M)。
,萃取、分液得到紫红色液体和水层(M)。①由此可知,
 的溶解度:四氯化碳>水,从结构角度分析其原因:
的溶解度:四氯化碳>水,从结构角度分析其原因:②检验M中是否有
 的试剂是
的试剂是(2)
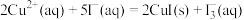

(3)一定温度下,在
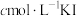 溶液中加入适量的
溶液中加入适量的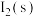 ,只发生反应
,只发生反应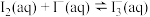
 。测得
。测得 与温度(T)关系如图所示。
与温度(T)关系如图所示。
①

②
 温度下,0~4min时间段内
温度下,0~4min时间段内 平均速率
平均速率 为
为 。
。(4)某温度下,起始在反应器中加入
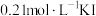 溶液和
溶液和 固体(忽略溶液体积变化),发生上述①②反应。测得
固体(忽略溶液体积变化),发生上述①②反应。测得 、
、 、
、 的平衡浓度与起始
的平衡浓度与起始 关系如图所示。
关系如图所示。
①起始
 时,
时, 的平衡转化率为
的平衡转化率为②该温度下,
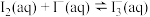 的平衡常数K=
的平衡常数K=(5)
 的氧化性比
的氧化性比 的强,但是KI和
的强,但是KI和 发生复分解反应,不发生氧化还原反应,其原因是
发生复分解反应,不发生氧化还原反应,其原因是
您最近一年使用:0次
解题方法
4 . 下列实验方案达不到相应实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A | 分别测定稀NaOH溶液和稀氨水与稀盐酸发生中和反应的反应热 | 确定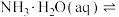 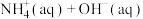 的 的 |
| B | 将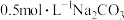 溶液逐渐升温,用pH传感器测量溶液的pH 溶液逐渐升温,用pH传感器测量溶液的pH | 探究温度对 水解平衡的影响 水解平衡的影响 |
| C | 常温下,向两支盛有5mL  溶液的试管中分别加入5mL 溶液的试管中分别加入5mL 硫酸、5mL 硫酸、5mL 硫酸 硫酸 | 探究浓度对反应速率的影响 |
| D | 将5mL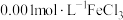 溶液和5mL 溶液和5mL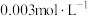 KSCN溶液混合后,再加入KCl固体 KSCN溶液混合后,再加入KCl固体 | 探究浓度对化学平衡: 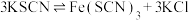 的影响 的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-07更新
|
42次组卷
|
2卷引用:河南省焦作市2023-2024学年高二上学期1月期末化学试题
5 . 近年来,随着聚酯工业的快速发展,Cl2的需求量和HCl的产出量也随之迅速增长。Deacon发明了直接氧化法(称作Deacon反应):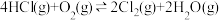 。
。
用O2将HCl转化为Cl2,可提高效益,减少污染。
回答下列问题:
(1)传统上Deacon反应可通过如图所示的催化剂循环实现。

Deacon反应的△H=_______ (用△H1和△H2表示)
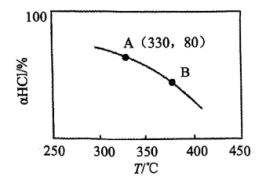
(2)在恒温、体积为1L的刚性密闭容器中发生Deacon反应,HCl、O2初始投料分别为4mol、1mol。实验测得HCl平衡转化率(α(HCl))随温度变化的曲线如图。
①下列说法能说明Deacon反应在此条件下到达平衡状态的有________ 。
A.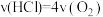 B.H2O的质量分数不变
B.H2O的质量分数不变
C. 不变 D.
不变 D. 不变
不变
②Deacon反应的△H________ 0(填“>”、“=”或“<”,下同),A、B两点的平衡常数K(A)与K(B)的大小关系是K(A)________ K(B)。
③Deacon反应在A点的平衡常数K=________ 。
④保持温度及投料比不变,提高HCl的平衡转化率的方法有________ 。(写出2种)
⑤若HCl、O2初始投料分别为5mol、1mol,画出相应α(HCl)-T曲线的示意图__________ 。
(3)一定条件下测得反应过程中n(Cl2)的数据如下:
2.0~6.0min内以HCl的物质的量变化表示的反应速率为_______ mol·min-1。
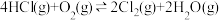 。
。用O2将HCl转化为Cl2,可提高效益,减少污染。
回答下列问题:
(1)传统上Deacon反应可通过如图所示的催化剂循环实现。

Deacon反应的△H=
(2)在恒温、体积为1L的刚性密闭容器中发生Deacon反应,HCl、O2初始投料分别为4mol、1mol。实验测得HCl平衡转化率(α(HCl))随温度变化的曲线如图。

①下列说法能说明Deacon反应在此条件下到达平衡状态的有
A.
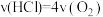 B.H2O的质量分数不变
B.H2O的质量分数不变C.
 不变 D.
不变 D. 不变
不变②Deacon反应的△H
③Deacon反应在A点的平衡常数K=
④保持温度及投料比不变,提高HCl的平衡转化率的方法有
⑤若HCl、O2初始投料分别为5mol、1mol,画出相应α(HCl)-T曲线的示意图
(3)一定条件下测得反应过程中n(Cl2)的数据如下:
| 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| 0 | 1.8 | 3.7 | 5.4 | 7.2 |
您最近一年使用:0次
名校
解题方法
6 . 不同的化学反应具有不同的反应热,人们可以通过多种方法获得反应热的数据,通常用实验进行测定,也可以进行理论推算。
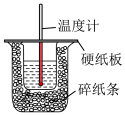
(1)在科学研究中,科学家常用量热计来测量反应热。我校某化学兴趣小组的同学欲测定中和热。用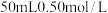 盐酸与
盐酸与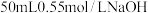 溶液在如图所示的简化装置中进行中和反应。则:
溶液在如图所示的简化装置中进行中和反应。则:
①从实验装置上看,图中尚缺少的一种仪器是______ 。
②大烧杯上如不盖硬纸板,求得的中和热数值_________ (填“偏大”“偏小”或“无影响”)。
③如果用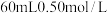 盐酸与
盐酸与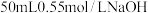 溶液进行反应,与上述实验相比,所求中和热
溶液进行反应,与上述实验相比,所求中和热_____ (填“相等”或“不相等”)。
(2) 与
与 在
在 催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用
催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用 作催化剂时该反应的过程示意图如图所示:
作催化剂时该反应的过程示意图如图所示:
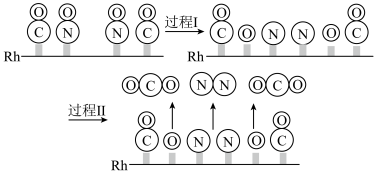
①过程Ⅰ为________ (填“吸热”或“放热”)过程。
②已知过程Ⅰ的焓变为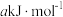 ,过程Ⅱ的焓变为
,过程Ⅱ的焓变为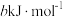 ,则该反应的热化学方程式为
,则该反应的热化学方程式为_______ 。
(3)已知: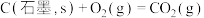
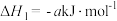
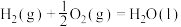
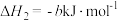
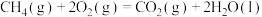
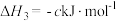
计算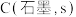 与
与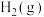 反应生成
反应生成 的
的 为
为______  (用含
(用含 的式子表示)。
的式子表示)。
(4)标准状况下, 在
在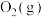 中完全燃烧生成
中完全燃烧生成 和
和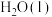 ,放出
,放出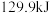 热量,请写出表示
热量,请写出表示 燃烧热的热化学方程式:
燃烧热的热化学方程式:_______ 。

(1)在科学研究中,科学家常用量热计来测量反应热。我校某化学兴趣小组的同学欲测定中和热。用
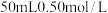 盐酸与
盐酸与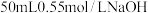 溶液在如图所示的简化装置中进行中和反应。则:
溶液在如图所示的简化装置中进行中和反应。则:①从实验装置上看,图中尚缺少的一种仪器是
②大烧杯上如不盖硬纸板,求得的中和热数值
③如果用
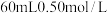 盐酸与
盐酸与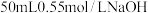 溶液进行反应,与上述实验相比,所求中和热
溶液进行反应,与上述实验相比,所求中和热(2)
 与
与 在
在 催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用
催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用 作催化剂时该反应的过程示意图如图所示:
作催化剂时该反应的过程示意图如图所示:
①过程Ⅰ为
②已知过程Ⅰ的焓变为
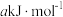 ,过程Ⅱ的焓变为
,过程Ⅱ的焓变为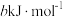 ,则该反应的热化学方程式为
,则该反应的热化学方程式为(3)已知:
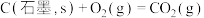
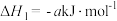
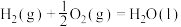
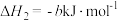
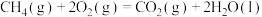
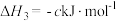
计算
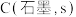 与
与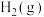 反应生成
反应生成 的
的 为
为 (用含
(用含 的式子表示)。
的式子表示)。(4)标准状况下,
 在
在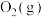 中完全燃烧生成
中完全燃烧生成 和
和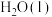 ,放出
,放出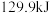 热量,请写出表示
热量,请写出表示 燃烧热的热化学方程式:
燃烧热的热化学方程式:
您最近一年使用:0次
7 . 在载人航天器中,可以利用 和
和 的反应,将航天员呼出的
的反应,将航天员呼出的 转化为
转化为 等,发生的反应为
等,发生的反应为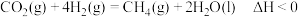 ,下列说法正确的是
,下列说法正确的是
 和
和 的反应,将航天员呼出的
的反应,将航天员呼出的 转化为
转化为 等,发生的反应为
等,发生的反应为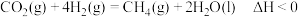 ,下列说法正确的是
,下列说法正确的是| A.该反应的反应物键能总和大于生成物键能总和 |
B.加入合适的催化剂, 的值将减小 的值将减小 |
C.每断裂 键,同时形成 键,同时形成 键 键 |
D.对于反应 与 与 的值相同 的值相同 |
您最近一年使用:0次
2024-02-13更新
|
108次组卷
|
2卷引用:贵州省黔东南州2023-2024学年高二上学期 期末化学试题
名校
8 . 一定温度下,在恒容密闭容器中充入乙烯和环丙烷,发生反应:

下列叙述错误的是

下列叙述错误的是
| A.其他条件不变,增大乙烯浓度,能提高正反应速率 |
| B.当压强不变时,反应达到平衡状态 |
C.其他条件不变,增大光照强度, 会增大 会增大 |
| D.平衡后加入催化剂,平衡不移动 |
您最近一年使用:0次
2024-02-08更新
|
85次组卷
|
2卷引用:河南省南阳市六校2023-2024学年高二上学期1月期末联考化学试题
9 . 合成甲醇的绿色新途径是利用含有 的工业废气为碳源,涉及的主要反应如下:
的工业废气为碳源,涉及的主要反应如下:
I.

Ⅱ.
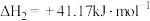
Ⅲ.___________
(1)已知 ,写出反应Ⅲ的热化学方程式:
,写出反应Ⅲ的热化学方程式:___________ ; 、
、 与
与 分别为反应I、Ⅱ、Ⅲ的平衡常数,其关系为
分别为反应I、Ⅱ、Ⅲ的平衡常数,其关系为
___________ 。
(2)在恒温恒容下反应物投料比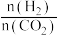 对
对 平衡转化率
平衡转化率 的影响如图A所示,相同时间内甲醇产率
的影响如图A所示,相同时间内甲醇产率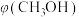 随反应温度的变化如图B所示。
随反应温度的变化如图B所示。
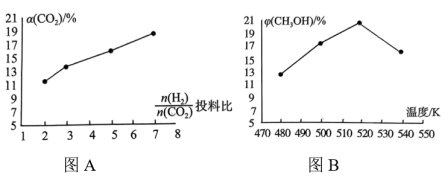
图A中随着投料比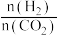 的增大,
的增大, 增大的原因是
增大的原因是___________ 。根据图B分析甲醇产率呈如图所示变化的原因是___________ 。
(3)研发低温下优良的催化剂是目前二氧化碳加氢合成甲醇研究对象之一,通过相关实验获得两种催化剂X、Y对反应I的催化效能曲线如图所示,已知Arrhenius经验公式为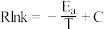 (
( 为速率常数,
为速率常数, 为活化能,R和C为常数)。
为活化能,R和C为常数)。
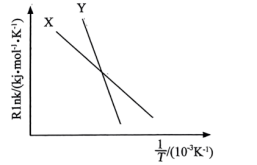
其中催化效能较高的是___________ (填“X”或“Y”)。
(4)将 与
与 按投料比
按投料比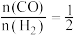 充入密闭容器中,在温度为
充入密闭容器中,在温度为 、压强为
、压强为 时只发生反应Ⅲ,测得平衡时混合气体中
时只发生反应Ⅲ,测得平衡时混合气体中 的物质的量分数为50%,则
的物质的量分数为50%,则 的转化率为
的转化率为___________ ;压强平衡常数
___________ (用平衡分压代替平衡浓度,平衡分压=总压×体积分数,用含 的代数式表示)。
的代数式表示)。
 的工业废气为碳源,涉及的主要反应如下:
的工业废气为碳源,涉及的主要反应如下:I.


Ⅱ.

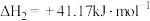
Ⅲ.___________

(1)已知
 ,写出反应Ⅲ的热化学方程式:
,写出反应Ⅲ的热化学方程式: 、
、 与
与 分别为反应I、Ⅱ、Ⅲ的平衡常数,其关系为
分别为反应I、Ⅱ、Ⅲ的平衡常数,其关系为
(2)在恒温恒容下反应物投料比
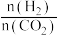 对
对 平衡转化率
平衡转化率 的影响如图A所示,相同时间内甲醇产率
的影响如图A所示,相同时间内甲醇产率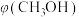 随反应温度的变化如图B所示。
随反应温度的变化如图B所示。
图A中随着投料比
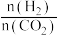 的增大,
的增大, 增大的原因是
增大的原因是(3)研发低温下优良的催化剂是目前二氧化碳加氢合成甲醇研究对象之一,通过相关实验获得两种催化剂X、Y对反应I的催化效能曲线如图所示,已知Arrhenius经验公式为
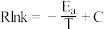 (
( 为速率常数,
为速率常数, 为活化能,R和C为常数)。
为活化能,R和C为常数)。
其中催化效能较高的是
(4)将
 与
与 按投料比
按投料比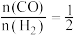 充入密闭容器中,在温度为
充入密闭容器中,在温度为 、压强为
、压强为 时只发生反应Ⅲ,测得平衡时混合气体中
时只发生反应Ⅲ,测得平衡时混合气体中 的物质的量分数为50%,则
的物质的量分数为50%,则 的转化率为
的转化率为
 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-02-02更新
|
114次组卷
|
2卷引用:山东省济南市2023-2024学年高二上学期1月期末化学试题
名校
解题方法
10 . 磷及其化合物应用广泛,磷元素有白磷、红磷、黑磷等单质。
(1)一定条件下,红磷在氯气中燃烧的产物有两种( 和
和 ),反应过程中的能量变化关系如图所示。回答下列问题:
),反应过程中的能量变化关系如图所示。回答下列问题:
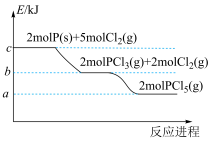
写出固态红磷在一定量的 中完全燃烧生成气态物质(
中完全燃烧生成气态物质( )的热化学方程式:
)的热化学方程式:____________________________ 。( 用图中字母表示)
用图中字母表示)
(2)白磷( )在
)在 中燃烧有如下转化关系。
中燃烧有如下转化关系。
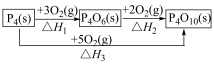
其中
_____________ (用含 和
和 的代数式表示)。
的代数式表示)。
(3)已知: (s,白磷)
(s,白磷) (s,黑磷)
(s,黑磷)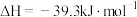 ;
;
 (s,白磷)
(s,白磷) (s,红磷)
(s,红磷)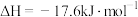 ;
;
由此推知,其中最稳定的磷单质是__________ (填“白磷”、“黑磷”或“红磷”)。
(1)一定条件下,红磷在氯气中燃烧的产物有两种(
 和
和 ),反应过程中的能量变化关系如图所示。回答下列问题:
),反应过程中的能量变化关系如图所示。回答下列问题:
写出固态红磷在一定量的
 中完全燃烧生成气态物质(
中完全燃烧生成气态物质( )的热化学方程式:
)的热化学方程式: 用图中字母表示)
用图中字母表示)(2)白磷(
 )在
)在 中燃烧有如下转化关系。
中燃烧有如下转化关系。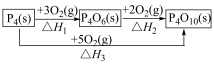
其中

 和
和 的代数式表示)。
的代数式表示)。(3)已知:
 (s,白磷)
(s,白磷) (s,黑磷)
(s,黑磷)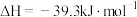 ;
; (s,白磷)
(s,白磷) (s,红磷)
(s,红磷)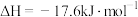 ;
;由此推知,其中最稳定的磷单质是
您最近一年使用:0次